超高强海工钢EH890 在模拟海洋环境下的腐蚀行为研究
车马俊,马新元,杜晓洁,李恒坤,徐震霖
(1.安徽工业大学材料科学与工程学院,安徽 马鞍山 243002;2.南京钢铁股份有限公司,江苏 南京 210035;3.江苏省高端钢铁材料重点实验室,江苏 南京 210035)
0 前 言
在中国工程院2020 年发布的«面向2035 的新材料强国战略研究》中,高性能海工钢被列为先进基础材料领域的重点发展方向,开发高强高耐蚀海洋平台用钢具有极大的科研价值和战略意义。
传统的海洋工程用钢多为Ni-Cr-Mo 高强钢,代表产品为美国的HY 系列钢,日本的NS 系列钢、英国的HLES80/100 钢和法国的QT(N)钢,因添加了较高含量的Ni、Cr、Mo 等合金元素,随着强度的提高,船体钢的碳当量和裂纹敏感性也随之大幅增加。为同步提高强度和可焊性,美国又陆续研制了HSLA 系列铜时效硬化钢和ULCB 系列超低碳贝氏体钢[1-3]。然而国内在高性能海工钢领域仍存在较大的差距,受海洋环境的影响,钢在服役过程中极易被Cl-侵蚀产生腐蚀,严重影响使用寿命。张大征[4]对海洋平台用690 MPa 级中锰钢组织性能及海水腐蚀行为进行了研究,结果表明在高浓度的Cl-环境中,Cl-促进了γ-FeOOH 的形成,降低了钢的耐腐蚀性。张振等[5]采用电化学试验方法,对比研究了D36、F460 和F690 钢在模拟海水中的电化学腐蚀行为,结果表明在NaCl 溶液中长时间浸泡后,材料表面腐蚀产物膜厚度依次降低,整体上呈现均匀腐蚀特征,耐腐蚀性能降低。通过在低合金高强钢中加入一定量的Cu,可以显著提高材料的耐蚀性能,Cu 在试样表面偏聚并形成稳定的CuFeO2氧化物,在腐蚀初期促进形成更加致密的保护膜层,从而提高耐蚀性[6,7]。
对海工钢最主要的需求与技术挑战来自于减轻整体重量和增加安全性。一方面,通过超高强韧实现结构减重,有利于装备制造与运输;另一方面,钢铁材料需要兼备耐蚀性能,不但可延长其寿命周期,还可减少维护费用。然而,开发高强与高耐蚀性兼备的海工钢是极具挑战的[8-10]。项目组通过在钢中加入一定量的Cu 和Ni 元素,利用时效过程大量纳米富Cu 相的析出强化基体,成功开发屈服强度高于890 MPa 的超高强海工钢。同时,Cu 和Ni 在腐蚀过程中形成的具有保护性的膜层提高了钢的耐蚀性。本工作对比分析了EH890 和EH460 在3.5%NaCl 溶液中腐蚀行为,通过动电位极化曲线与电化学阻抗谱测量,结合X 射线衍射(XRD)、扫描电镜(SEM)、X 射线光电子能谱(XPS)等分析手段,对腐蚀形貌与腐蚀产物进行了细致讨论,为超高强度海工钢在海洋环境中的应用提供了参考。
1 试 验
1.1 试 材
试材为调质态EH890 和EH460 钢,化学成分如表1 所示。将材料通过线切割加工成尺寸为10 mm×10 mm×2 mm 的样品,用于浸泡和电化学试验。试验开始前,所有试样均经水磨砂纸逐级打磨至1 500 号,并用去离子水清洗,酒精擦拭,烘干,置于干燥皿中备用。

表1 试验钢化学成分(质量分数) %Table 1 Chemical composition of test steels (mass fraction) %
1.2 电化学试验
电化学试验在CHR-7601 型电化学工作站进行,采用三电极体系,同时控制室温(25±1) ℃,铂片为辅助电极,饱和甘汞电极为参比电极,工作电极是在3.5%NaCl 溶液中浸泡1 h 的待测样。在EIS 测试前,开路电位测量600 s 直到达到稳定值,作为EIS 测试的初始值。EIS 测试频率为1.0×(105~10-2) Hz,电压振幅为10 mV,使用ZSimpWin 软件对EIS 进行数据分析。动电位极化曲线测试初始电位为-2 V,最终电位为1.5 V,扫描速率为10 mV/s。为保证试验结果的再现性,每个测试都进行至少3 次。
1.3 腐蚀产物形貌与物相分析
室温下将EH460 和EH890 置于3.5%NaCl 溶液中浸泡7 d。使用Tescan MIRA3 XMU 型场发射扫描电子显微镜(SEM)对浸泡后试样表面形貌进行微观分析,用Ultima IV X 射线衍射仪(XRD)对浸泡后试样表面腐蚀产物进行物相分析,2θ范围20°~80°,辐射Cu 靶,电压为40 kV,电流为40 mA,扫描速率为5 (°)/min。采用带有Al Kα射线源的X 射线光电子能谱(XPS)分析钝化膜的成分,用C 的标准峰校准(C1s,284.8 eV),使用Avantage 商业软件对XPS 数据进行拟合和分析。
2 结果与讨论
2.1 动电位极化曲线
图1 为EH460 和EH890 钢在3.5%NaCl 溶液中的动电位极化曲线。从极化曲线来看,2 种材料在极化过程中均形成了稳定的钝化区,这表明在电化学腐蚀初期,试样表面可以形成钝化膜提高腐蚀抗力;EH890 钢自腐蚀电位略高,说明其在3.5%NaCl 溶液中腐蚀倾向更小。根据塔菲尔外推法拟合动电位极化曲线,拟合出的电化学参数见表2。其中Ecorr表示腐蚀电位,Jcorr表示腐蚀电流密度,Rp表示腐蚀金属电极的极化电阻,βa表示阳极极化曲线的塔菲尔斜率,βc表示阴极极化曲线的塔菲尔斜率。极化电阻与腐蚀电流密度Jcorr具有反比关系,如式(1)所示,极化电阻数值越大,腐蚀电流密度密度Jcorr数值会越小,即在相同的试验条件下,可以根据极化电阻的数值来比较腐蚀速度的快慢。对于一个具体的腐蚀过程B是常数,可根据阳极和阴极极化曲线的塔菲尔斜率来计算,βa、βc和B存在的换算关系如式(2)所示[11]。

图1 EH460 和EH890 在3.5%NaCl 中的动电位极化曲线Fig.1 Potentiodynamic polarization curves of EH460 and EH890 test steels in 3.5%NaCl

表2 EH460 和EH890 在3.5%NaCl 中的极化曲线拟合结果Table 2 Polarization curve fitting results of EH890 and EH460 test steels in 3.5%NaCl
对极化曲线的电化学拟合参数进行分析可知,EH460 钢的腐蚀电流密度为6.11×10-6A/cm2,极化电阻为5.40×103Ω·cm2,而EH890 的电流密度是4.94×10-6A/cm2,极化电阻是5.50×103Ω·cm2,腐蚀电流密度降低了20%,说明在3.5%NaCl 溶液的腐蚀环境中,EH890 钢的腐蚀速率较慢,拥有更好的耐蚀性。EH890钢的腐蚀电位高于EH460 钢,腐蚀电位正移,说明其表面形成的钝化膜对基体更具有保护作用。EH890 中含有一定量的Cu 和Ni,在腐蚀初期,Ni 以NiFe2O4存在于钝化膜层中,促进了EH890 钢的腐蚀电位正移,同时Cu 在钢材表面发生沉积,增加了锈层的致密度,抑制了阳极的溶解[12-14]。
2.2 电化学阻抗谱
图2 为2 种材料在3.5%NaCl 溶液中的Nyquist 谱和Bode 谱,其中点状为试验数据,实线为拟合数据。
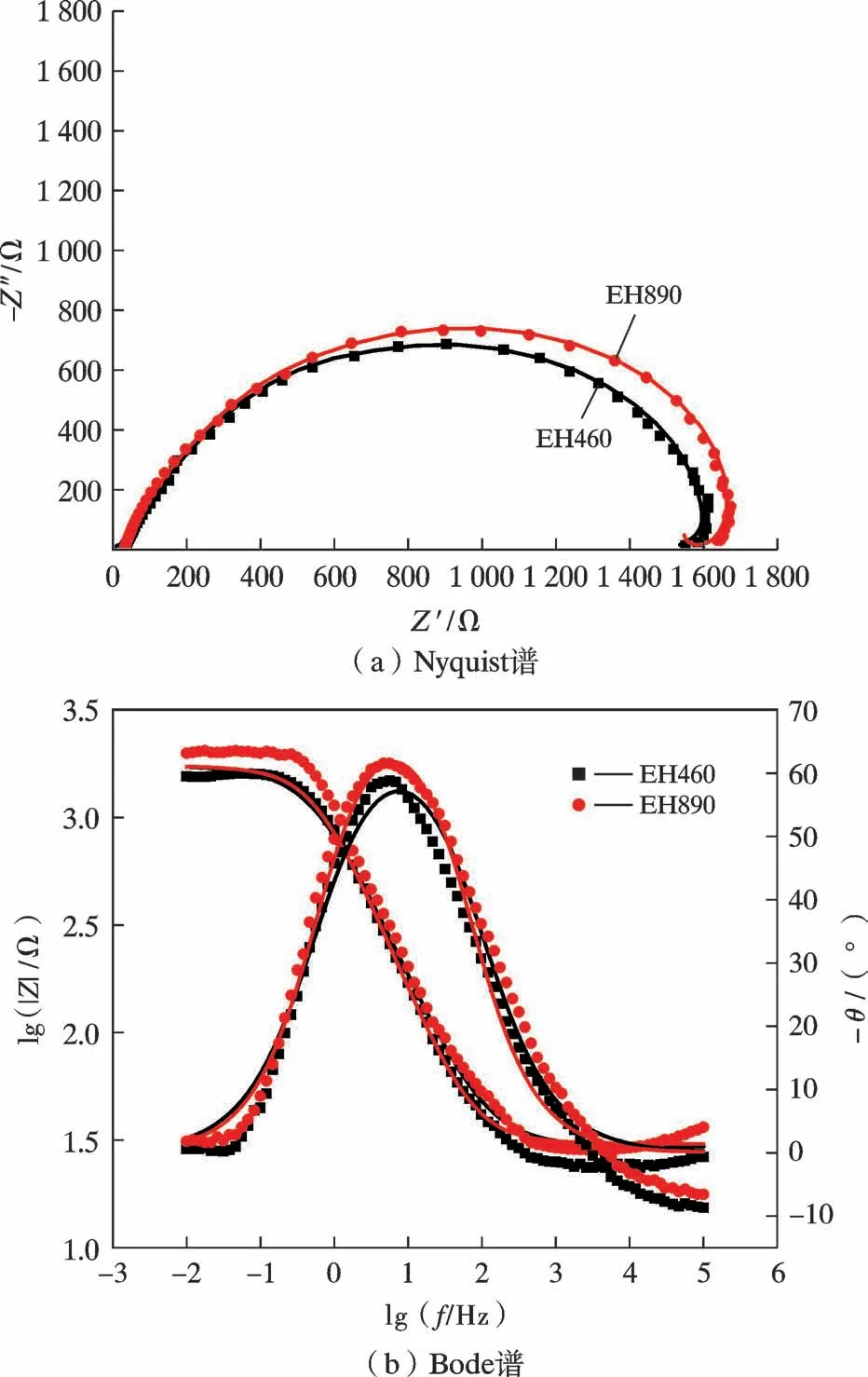
图2 EH460 和EH890 在3.5%NaCl 中的电化学阻抗谱Fig.2 Electrochemical impedance spectroscopy of EH460 and EH890 in 3.5%NaCl
2 种材料的Nyquist 谱形状类似,显示出半圆形电容回路,表明其腐蚀特性基本相同,腐蚀过程主要受电荷转移控制,一般认为,Nyquist 谱的圆弧半径(R)越大,说明电荷转移难度越大,钝化膜保护作用更好[15]。由图可知,EH890 钢容抗弧半径较大,表明EH890 钢电荷转移阻力更大,具有更好的耐蚀性。Bode 图中固定频率为0.1 Hz 处的阻抗绝对值|Z|通常与极化电阻有关,它反映了材料在溶液中的耐腐蚀性[16]。从图2b 可以得出,EH890 钢的|Z|值在0.1 Hz 时高于EH460 钢,这一事实表明在3.5%NaCl 溶液中,EH890 钢比EH460钢更耐腐蚀。此外,EH460 钢的相位角不大于60°,而EH890 钢的相位角不大于65°,但总体上高于EH460 钢,较大的相位角也在一定程度上表明其耐腐蚀性更高[17]。
根据图3 等效电路模型对电化学阻抗谱进行拟合,恒相位元件(Qdl)与电阻(Rt)并联,电阻(Rsol)与它们串联。其中Rsol表示溶液阻力,可通过将高频渐近线外推到Nyquist 谱中的实轴来估计,Rsol值越大,表明导电能力越弱;Qdl是工作电极与电解质之间电容(双电层电容),在进行电化学阻抗谱测量时,电极表面进行双电层周期性的充、放电过程和电极反应速度周期性的变化过程,大小受样品的电极表面积和电极表面粗糙度影响[18];Rt是钝化膜与基体间电荷转移电阻,Rt值越大,表明电极表面上的电荷转移过程越慢,钝化膜保护效果越好。
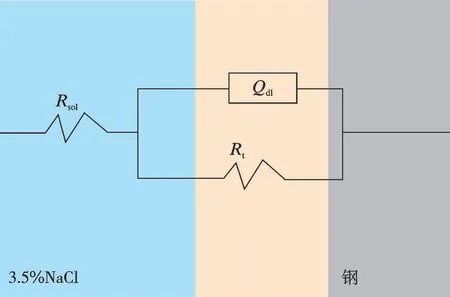
图3 等效电路Fig.3 Equivalent circuit diagram
表3 列出了EH890 钢和EH460 钢在3.5%NaCl 溶液中的交流阻抗拟合参数。如表3 所示,EH890 钢的溶液电阻Rsol更大,说明EH890 钢的溶液导电能力较弱,Qdl值低于EH460 钢,证明了EH890 钢表面粗糙度更小,更不易被腐蚀。就电荷转移电阻(Rt)而言,EH890 钢的Rt值为1.712×103Ω·cm2,EH460 钢的Rt值为1.034×103Ω·cm2,EH890 钢的电荷转移电阻是EH460 钢的1.6 倍,进一步证明了EH890 钢比EH460钢具有更好的耐腐蚀性能。

表3 E4H60 和EH890 在3.5%NaCl 溶液中的交流阻抗拟合结果Table 3 Fitting results of AC impedance of EH460 and EH890 in 3.5%NaCl solution
2.3 腐蚀形貌
为进一步研究EH460 钢和EH890 钢在模拟海水中的耐腐蚀性能,对在3.5%NaCl 溶液中浸泡7 d 后的2 种试样的锈层进行SEM 扫描,其腐蚀形貌见图4。

图4 EH460 和EH890 在3.5%NaCl 溶液中浸泡7 d 后腐蚀形貌Fig.4 Corrosion morphology of EH460 and EH890 after immersion in 3.5%NaCl solution for 7 d
由图可知,2 种材料在3.5%NaCl 溶液中浸泡后,随 着腐蚀的发生,腐蚀产物为团絮状,并不断聚集长大。EH460 腐蚀类型为不均匀腐蚀,并伴有裂纹的产生;而EH890 呈现均匀腐蚀特征,铬、镍、铜等合金元素的添加促进了致密锈层的形成,从而有效提高了EH890 钢在含氯离子环境中的耐腐蚀性能[5,19]。这一结果表明,与EH460 钢相比,EH890 钢具有更好的耐腐蚀性。
2.4 锈层物相
图5 是EH460 和EH890 2 种钢在3.5%NaCl 溶液中浸泡7 d 后表面锈层的XRD 谱。结果表明,2 种材料锈层的相组成基本相同,主要为α-FeOOH、γ-FeOOH和Fe3O4。通常在腐蚀过程中,Fe 基体首先被腐蚀成Fe2+,生成FeO 和Fe(OH)2,然后继续腐蚀成Fe3+,形成α-FeOOH 和γ-FeOOH 等[20-22]。由于腐蚀产物吉布斯自由能的差异,不稳定的γ-FeOOH 相会随着腐蚀时间的延长,逐渐转变为更为稳定致密的α-FeOOH 相,α-FeOOH相不导电,对基体具有较好的保护作用,很多学者将腐蚀产物的保护作用归因于α-FeOOH 的存在[23-25]。因此α-FeOOH 相比例越大,耐腐蚀性越好,而且较稳定的氧化物Fe3O4的出现,也会使锈层不断变厚,对氯离子的穿透有一定的阻滞作用,具有一定的保护性。

图5 H460 和EH890 在3.5%NaCl 溶液中浸泡7 d 后表面锈层的XRD 谱Fig.5 XRD phase analysis of surface rust layer of EH460 and EH890 after soaking for 7 d
经3.5%NaCl 溶液中浸泡7 d 后,选取试样表面未产生腐蚀区进行XPS 分析测试。图6 为EH460 和EH890 在3.5%NaCl 溶液中浸泡7 d 后锈层中的O1s、Fe2p3/2、Ni2p3/2和Cu2p3/2的XPS 分析结果。

图6 EH460 和EH890 在3.5%NaCl 溶液中浸泡7 d 后所形成锈层的XPS 谱Fig.6 XPS spectra of rust layer formed by soaking EH460 and EH890 in 3.5%NaCl solution for 7 d
在分析XPS 图谱之前,通过将结合能的峰位置与C1s 峰的结合能标准值(284.8 eV)对比来校准,XPS 分峰拟合时,相关拟合参数参考相关文献,同一种化合物的半高宽(FWHM)相同;同一种化合物的峰值位置不完全相同,但差值不大于0.3 eV[26,27]。O1s 第1 个峰为生成M-O 金属氧化物所对应的O2-;第2 个峰为生成M-(OH)n金属氢氧化物所对应的OH-,由XPS 分析结果可知,O2-主要以Fe 的氧化物形式存在,而与OH-相关的氢氧化物,对应于FeOOH 和Cu(OH)2的形成。如图6b 和6d 显示了在锈层上的Fe2p 光谱,Fe2p 光谱被认定为3 个组成峰,分别对应于Fe3O4、NiFe2O4和FeOOH。稳定的氧化物Fe3O4能增加锈层厚度阻碍Cl-的穿透,NiFe2O4的存在也是EH890 钢的腐蚀电位正移、耐腐蚀性较好的原因。值得注意的是,在EH890 钢的锈层表面检测到了Cu 与Ni 元素,如图6e,6f 所示。EH890 钢的Ni2p 图谱由2 个组成峰构成,对应于NiFe2O4和NiO;Cu2p 图谱由Cu(OH)2和CuFeO22 个组成峰构成。据报道[28]CuFeO2会在锈层中富集,提高锈层致密性,从而使其腐蚀的阴极和阳极过程均受到抑制,这说明锈层中的CuFeO2的含量越高,耐腐蚀性越好。XPS 谱的测试结果进一步证明了EH890 拥有比EH460 钢更优异的耐腐蚀性能。
3 结 论
(1)在3.5%NaCl 溶液中,同EH460 钢相比,EH890钢的腐蚀电流密度降低了20%,电荷转移电阻Rt提高了1.6 倍,EH890 具有更好的耐腐蚀性。
(2)在3.5%NaCl 溶液中浸泡7 d 后,EH890 试样表面呈均匀腐蚀特征,而EH460 试样则表现为不均匀腐蚀,并且局部发生龟裂。
(3)在EH890 锈层中生成的CuFeO2和NiFe2O4,提高了腐蚀初期锈层的致密性,抑制了腐蚀的进程,从而提高了EH890 在3.5%NaCl 溶液中耐腐蚀性。

