UHPLC-MS/MS法测定盐酸普萘洛尔缓释片中基因毒性杂质N-亚硝基普萘洛尔
黄海伟,袁松,张娜,张龙浩,刘阳,张庆生
(中国食品药品检定研究院,国家药品监督管理局化学药品质量研究与评价重点实验室,北京 102629)
盐酸普萘洛尔化学名称为1-异丙基-3-(1-萘氧基)-2-丙醇盐酸盐(见图1A),盐酸普萘洛尔为非选择性竞争抑制β受体阻滞剂[1],临床上常用于高血压、心律失常和心绞痛的治疗[2-3]。2022年3月加拿大卫生部(Health Canada)发布通告,辉瑞制药公司自愿召回60、80、120、160 mg 4种规格共29批次盐酸普萘洛尔缓释胶囊,此次召回是因为在这些批次中检测出超过每天允许摄入量的N-亚硝基普萘洛尔(见图1B)[4-5]。
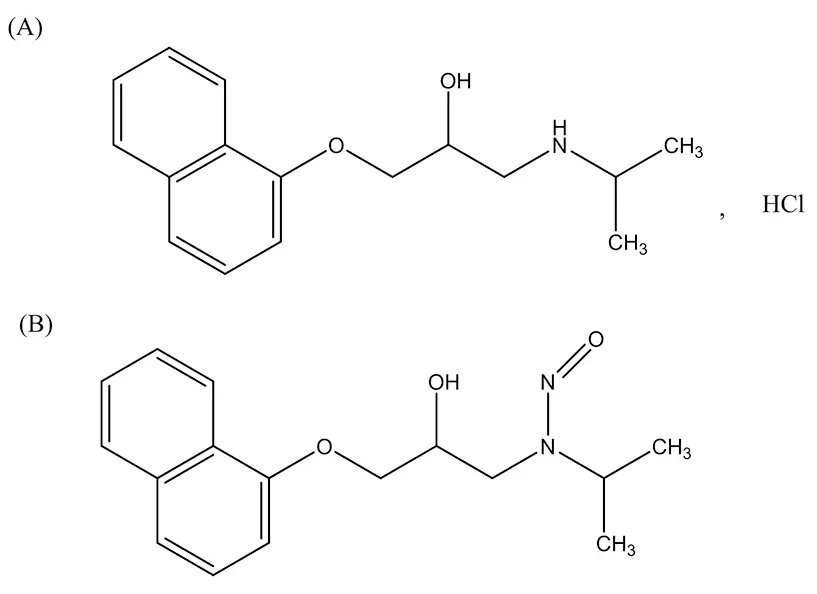
图1 盐酸普萘洛尔(A)及N-亚硝酸普萘洛尔(B)的结构式
N-亚硝基类化合物具有直接或间接的致癌作用,长期小剂量接触或单次较大剂量接触都可能致癌[6-8],亚硝胺类化合物是由于药物生产过程中发生了某些副反应而产生。自2018年缬沙坦中N-二甲基亚硝胺(NDMA)检出以来,又有N-二乙基亚硝胺(NDEA)、N-亚硝基-N-甲基-4-氨基丁酸(NMBA)等杂质陆续在药品中检出,国家药品监督管理局、美国食品药品监督管理局(FDA)以及欧洲药品管理局(EMA)都发布了有关药品中遗传毒性杂质控制策略、检测方法以及限度要求等指导原则,多个药品因N-亚硝基类化合物超出每日允许摄入量被召回[9-11]。已报道的N-亚硝基类化合物主要分为两类,一类与药物本身结构无关,在药品生产过程中由残留溶剂等引入,例如NDMA、NDEA等;一类则直接与药物本身相关,通常是原料药中的仲胺结构与微量残留的亚硝酸盐反应生成相应的杂质[12-14]。N-亚硝基普萘洛尔属于上述的第二类杂质,只在普萘洛尔相关制剂中被发现。目前尚无该基因毒性杂质检测及限度的相关报道,本文拟采用超高效液相色谱-串联质谱(UHPLC-MS/MS)建立盐酸普萘洛尔缓释片中N-亚硝基普萘洛尔的检测方法,为盐酸普萘洛尔中遗传毒性杂质检查和质量控制提供参考依据。
1 材料
1.1 仪器Agilent 1290-6470液相色谱-串联三重四级杆质谱仪(美国Agilent公司),配备电喷雾离子源(ESI)和Masshunter数据处理系统;XP205DR型电子分析天平(瑞士Mettler公司),Milli-Q超纯水纯化系统(美国Millipore公司)。
1.2 药物与试剂甲醇(质谱级,美国Fisher Scientific公司),乙腈(质谱级,美国Sigma-Aldrich公司),甲酸(质谱级,德国Merck公司),甲酸铵(质谱级,美国Fisher Scientific公司),水为超纯水,N-亚硝基普萘洛尔对照品(批号:PN20220312,PERIDA公司,纯度96.8%),盐酸普萘洛尔缓释片(市场采购)。
2 方法与结果
2.1 溶液制备
2.1.1 标准曲线对照品溶液制备精密称取N-亚硝基普萘洛尔对照品10.43 mg,置100 mL量瓶中,加甲醇使溶解并稀释至刻度,摇匀,作为对照品储备液。精密量取对照品储备液0.1 mL,置100 mL量瓶中,用甲醇稀释至刻度,摇匀,精密量取1.0、2.0、5.0、7.0、10.0、10.0 mL上述溶液分别置100、100、100、100、100、50 mL量瓶中,用甲醇稀释至刻度,摇匀,作为浓度分别约为1.0、2.0、5.0、7.0、10.0、20.0 ng·mL-1的系列线性溶液。
2.1.2 供试品溶液制备取本品10片,精密称定,研细,混匀,精密称取约相当于盐酸普萘洛尔20 mg的细粉,置15 mL离心管中,精密加入甲醇5 mL,涡旋3 min,滤过,取续滤液作为供试品溶液。
2.2 色谱及质谱条件
2.2.1 色谱条件采用Waters ACQUITY UPLC CSHTMC18(150 mm×3.0 mm,1.7 μm)色谱柱;以10 mmol·L-1甲酸铵的水溶液(含0.1%甲酸)作为流动相A,乙腈溶液(含0.1%甲酸)作为流动相B,梯度洗脱:0.0~5.0 min, 50%B;5.0~7.0 min, 50%B→70%B;7.0~9.0 min, 70%B;9.0~9.0 min, 70%B→50%B;9.0~13.0 min, 50%B;流速为0.5 mL·min-1,柱温为50 ℃,进样器温度为5 ℃,进样体积为10 μL。
2.2.2 质谱条件采用电喷雾离子源(electrospray Ionization Source,ESI),正离子检测模式,干燥气温度为300 ℃,干燥气流量为6 L·min-1,喷雾电压为35 psi,鞘气温度为350 ℃,鞘气流量为10 L·min-1,毛细管电压为4 500 V。采集方式为多反应监测(Multiple reaction monitor,MRM)模式,以m/z289.2→72.2作为定量离子对,碎裂电压为78 V,碰撞电压为12 V,以m/z289.2→145.1作为定性离子对,碎裂电压为78 V,碰撞电压为12 V。
2.3 方法学考察
2.3.1 专属性试验取甲醇作为空白溶剂和“2.1.1”项下1 ng·mL-1的对照品溶液,分别进样,记录色谱图(见图2),在所建立的色谱和质谱条件下,N-亚硝基普萘洛尔的保留时间为6.74 min,峰型良好,空白溶剂对检测无干扰。
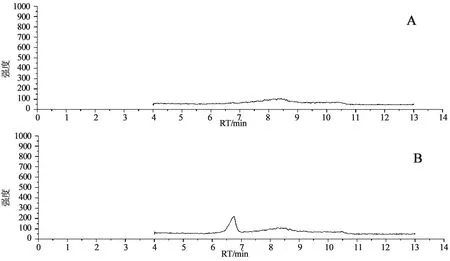
A.甲醇溶液;B.对照品溶液
2.3.2 检测限与定量限试验取“2.1.1”项下1 ng·mL-1的线性溶液,以甲醇为稀释剂逐步稀释,分别在信噪比(S/N)为10∶1和3∶1时作为定量限和检测限,测得N-亚硝基普萘洛尔的定量限和检测限分别为0.3、0.09 ng·mL-1。
2.3.3 线性关系考察精密量取“2.1.1”项下系列线性溶液,进样检测,记录色谱图。以N-亚硝基普萘洛尔峰面积Y为纵坐标,以质量浓度X(ng·mL-1)为横坐标进行线性回归,得N-亚硝基普萘洛尔的线性回归方程为Y=2 563.38X-161.38(r=0.999 9),结果表明在1.01~20.19 ng·mL-1浓度范围内,N-亚硝基普萘洛尔峰面积与质量浓度之间呈良好的线性关系。
2.3.4 精密度和重复性试验取“2.1.1”项下5.0 ng·mL-1的线性溶液连续进样6次,得N-亚硝基普萘洛尔峰面积的RSD为1.13%,结果表明系统精密度良好。取盐酸普萘洛尔缓释片,按“2.1.2”项下方法平行制备6份供试品溶液,进样检测,按标准曲线法计算N-亚硝基普萘洛尔含量,计算得6份供试品溶液中N-亚硝基普萘洛尔含量的RSD为3.58%。结果表明方法具有良好的重复性。
2.3.5 稳定性试验取“2.1.1”项下5.0 ng·mL-1的线性溶液,放置于进样盘,分别在0、8 h进样检测,结果N-亚硝基普萘洛尔峰面积的相对偏差为2.96%,结果表明5 ℃条件下对照品溶液在8 h内稳定;取“2.3.4”项下1份重复性试验供试溶液,放置于进样盘,分别在0、2、5、7 h进样检测。结果N-亚硝基普萘洛尔峰面积的RSD(n=4)为2.66%,结果表明5 ℃条件下供试品溶液在7 h内稳定。
2.3.6 提取效率试验取盐酸普萘洛尔缓释片,按“2.1.2”项下方法平行制备2份供试品溶液,其中1份涡旋3 min,另一份涡旋10 min,进样检测,按标准曲线法计算N-亚硝基普萘洛尔含量,计算得2份供试品溶液中N-亚硝基普萘洛尔含量相对标对偏差为3.77%。结果表明涡旋3 min可提取完全。
2.3.7 回收率试验取盐酸普萘洛尔缓释片,精密称定,研细,混匀,精密称取细粉约57 mg(约相当于盐酸普萘洛尔20 mg),置15 mL离心管中,精密加入“2.1.1”项下10 ng·mL-1(高浓度)、5 ng·mL-1(中浓度)、2 ng·mL-1(低浓度)的线性溶液5 mL,涡旋3 min,滤过,取续滤液作为回收率溶液,每个浓度点平行制备3份,进样检测,结果见表1,低、中、高浓度点的回收率分别为98.4%(RSD2.7%,n=3)、101.6%(RSD1.1%,n=3)、103.2%(RSD1.5%,n=3),结果表明回收率良好。

表1 加样回收率结果
2.4 样品测定按“2.1”项下制备盐酸普萘洛尔缓释片供试品溶液,照“2.2”项下条件进样检测,记录色谱图,以峰面积按标准曲线法计算供试品溶液中N-亚硝基普萘洛尔的含量,测得盐酸普萘洛尔缓释片中N-亚硝基普萘洛尔含量为1.8 μg·g-1。
3 讨论
由于盐酸普萘洛尔供试品溶液浓度较高,普萘洛尔峰与N-亚硝基普萘洛尔峰需要达到较大的分离度,才能将普萘洛尔峰切入废液不至于干扰杂质的检测,所以首先对不同类型的色谱柱进行了考察,最终选用Waters ACQUITY UPLC CSHTMC18色谱柱,N-亚硝基普萘洛尔峰型良好,且可与普萘洛尔峰完全分离,但两者洗脱时间较长,为提高实验效率在此基础上对色谱条件进行优化,增加有机相比例以缩短分析时间;不同流动相系统对色谱保留和杂质的质谱响应影响非常大,对流动相系统进行了考察,当采用乙腈为流动相时体系,N-亚硝基普萘洛尔出峰较快,且质谱响应增强,可满足分析的分离度要求。前期的试验显示N-亚硝基普萘洛尔在甲醇中易溶,在乙腈中微溶,以甲醇-水作为溶剂为较优选择,但缓释片加极少量水后即成凝胶状无法进样检测,为保证提取完全和样品检测的准确性,选择了以甲醇作为溶剂,以甲醇作为溶剂时,存在一定的溶剂效应,N-亚硝基普萘洛尔峰前沿,峰形变宽,灵敏度降低,为此,采用较大内径的色谱柱,并增加进样体积至10 μL,即可满足N-亚硝基普萘洛尔检测灵敏度的要求。
目前未见N-亚硝基普萘洛尔的毒理学数据,暂无明确控制限度,提示药品研发生产、相关科研机构应对杂质进行深入的毒理研究以建立合理的控制限度,保障用药安全。
4 结论
本研究建立了盐酸普萘洛尔缓释片中N-亚硝基普萘洛尔的UHPLC-MS/MS检测方法,并进行了相关方法学验证,结果表明,所建立的方法具有良好的专属性、灵敏度和准确度,可准确测定盐酸普萘洛尔缓释片中潜在的N-亚硝基普萘洛尔的含量,有助于盐酸普萘洛尔缓释片的市场监管,保障药品质量安全。

