射血分数保留型心力衰竭患者血浆纤维蛋白原水平与易损期预后的预测价值研究
马 聪,徐志伟,高彦琳,成 威(安徽省第二人民医院心血管内科,合肥 230000)
射血分数保留的心力衰竭(heart failure with preserved ejection fraction,HFpEF)占所有心力衰竭患者的一半左右[1],主要临床表现为急性肺水肿,甚至晕厥或休克等,需立即送医治疗,且预后较差,部分患者短期内易复发,入院率及死亡率均较高[2]。有研究提出[3],心力衰竭患者出院后三个月内,病情不稳定,死亡及再住院风险均较高,将该时期定义为易损期。老年人本身存在凝血-纤溶系统失衡、增龄性血流动力学异常及神经内分泌系统激活,极易并发血栓栓塞事件,有研究报道[4],这可能与患者存在血栓前高凝状态相关,而纤维蛋白原(fibrinogen,FIB)是反映血栓前高凝状态的敏感指标之一。心力衰竭患者体内的IL-6,IL-1 等促炎细胞因子分泌增加,从而刺激肝脏合成更多的FIB,高浓度的FIB 对凝血系统、血小板聚集、血液流变学及血管内皮细胞均产生较大影响,患者全血黏度增高,血液流动性降低,血小板膜糖蛋白复合物与血小板结合,导致血液系统持续微血栓状态[5]。已有大量研究证实[6],心力衰竭患者有较差的长期预后,但对单独评价HFpEF 患者易损期预后的研究较少。本研究就FIB 水平对HFpEF 患者易损期预后的影响进行探讨,以期为临床研究提供理论依据。
1 材料与方法
1.1 研究对象 前瞻性研究,选取2019 年2月~2022 年3 月于安徽省第二人民医院诊治的HFpEF 患者102 例为研究对象。纳入标准:①年龄≥18 岁;②HFpEF 的诊治依据《中国心力衰竭诊断和治疗指南2018》[7];③符合NYHA 心功能分级[8]≥Ⅲ级。排除标准:①并发肥厚性心肌病、限制性心肌病、先天性心脏病及心肌炎;②并发免疫系统疾病、恶性肿瘤、肝肾衰竭等疾病者;③需行透析或血滤治疗的终末期患者。本研究已经我院伦理委员会批准,受试者自愿签署同意书。
1.2 仪器与试剂 AU5800 全自动生化分析仪及LH7500全自动血液分析仪(贝克曼库尔特有限公司(美国);高速离心机(广州吉迪仪器有限公司);一次性抗凝真空采血管(江苏康健医疗用品有限公司);PHILIPS+EPIQ 7C彩色超声诊断仪[飞利浦公司(荷兰)]。
1.3 方法 记录患者的性别、体重指数(body mass index,BMI)、年龄;冠心病、糖尿病、高血脂、高血压;超声心动图:左心室射血分数(left ventricular ejection fraction,LVEF)、左心室舒张末期内径(left ventricular end diastolic dimension,LVEDD)、左心室收缩末期内径(left ventricular end-systolic dimension,LVESD);入院24 h 内的生化指标:血红蛋白、空腹血糖、白细胞、清蛋白、总胆固醇、血肌酐、糖化血红蛋白、N 段B 型钠尿肽前体(N-segment B-type natriuretic peptide precursor,NT-proBNP)、肌酸激酶(creatine kinase,CK)、低密度脂蛋白- 胆固醇(low density lipoprotein cholesterin,LDL-C)、心肌肌钙蛋白I(cardiac troporlin I,cTnI)和FIB,其中入选患者均于晨起基础状态下取静脉血,采用酶联免疫吸附法进行FIB 检测,检测仪为贝克曼DXI800 全自动血凝分析仪(美国贝克曼公司);治疗方法:利尿剂、血管紧张素转换酶抑制剂(angiotensin converting enzyme inhibitor,ACEI)/血管紧张素受体阻断剂(angiotensin receptor blocker,ARB)、醛固酮受体拮抗剂、β受体阻滞剂、洋地黄类药物、他汀类药物。
患者出院后二周内进行门诊随访,然后分别于1 个月、3 个月,由心内科医生对出院患者进行电话随访。终点事件为复合终点(因心力衰竭再入院或全因死亡)。
1.4 统计学分析 采用SPSS22.0 进行数据分析。计量资料以均数±标准差(±s)表示,使用t检验;计数资料以频数表示,使用卡方检验。使用受试者工作特征(receiver operating characteristic,ROC)曲线评价FIB 对HFpEF 患者易损期复合终点预测的最佳临界值,并据此进行分组,比较两组的一般资料及实验室指标。使用Spearman 相关性分析FIB 与各指标的相关性。采用Kaplan-Meier 法和LOG-rank 检验分析FIB 水平对患者复合终点事件发生风险的影响。筛选影响患者预后情况的指标,将FIB 纳入和剔除分别构建HFpEF 患者易损期预后的预测模型,并利用ROC 对模型进行评价,使用Bootstrap 重复取样的方法对模型进行内部验证。P<0.05 为差异有统计学意义。
2 结果
2.1 FIB 对HFpEF 患者易损期复合终点预测的ROC 曲线 以血浆中FIB 水平为检测变量,以分组为状态变量,定状态变量值为1,建立ROC 曲线,见图1。以曲线最左上方的点(Youden 指数最大)为最佳临界值。结果发现,血浆FIB 检测HFpEF患者易损期终点事件的ROC 曲线下面积(area under curve,AUC)为0.876,敏感度和特异度分别为86.9%,78.3%,最佳分界值为3.19 g/L。以此最佳分界值将入选患者分为两组:FIB<3.19 g/L 为A组(n=52),FIB ≥3.19 g/L 为B 组(n=50)。

图1 FIB 对HFpEF 患者易损期复合终点预测的ROC 曲线
2.2 两组患者的一般资料及实验室指标比较 见表1。比较A 组和B 组患者的一般资料、实验室指标、超声心动图指标及药物治疗方法,结果发现,与A 组相比,B 组患者的NYHA 分级Ⅲ~Ⅳ占比,β受体阻滞剂治疗占比和醛固酮受体拮抗剂占比均明显升高,空腹血糖、LDL-C,血肌酐、NTproBNP,cTnI 和CK 水平均明显升高,血红蛋白和清蛋白水平均明显降低,差异具有统计学意义(均P<0.05)。
表1 两组患者的一般资料及实验室指标比较[n(%),±s]
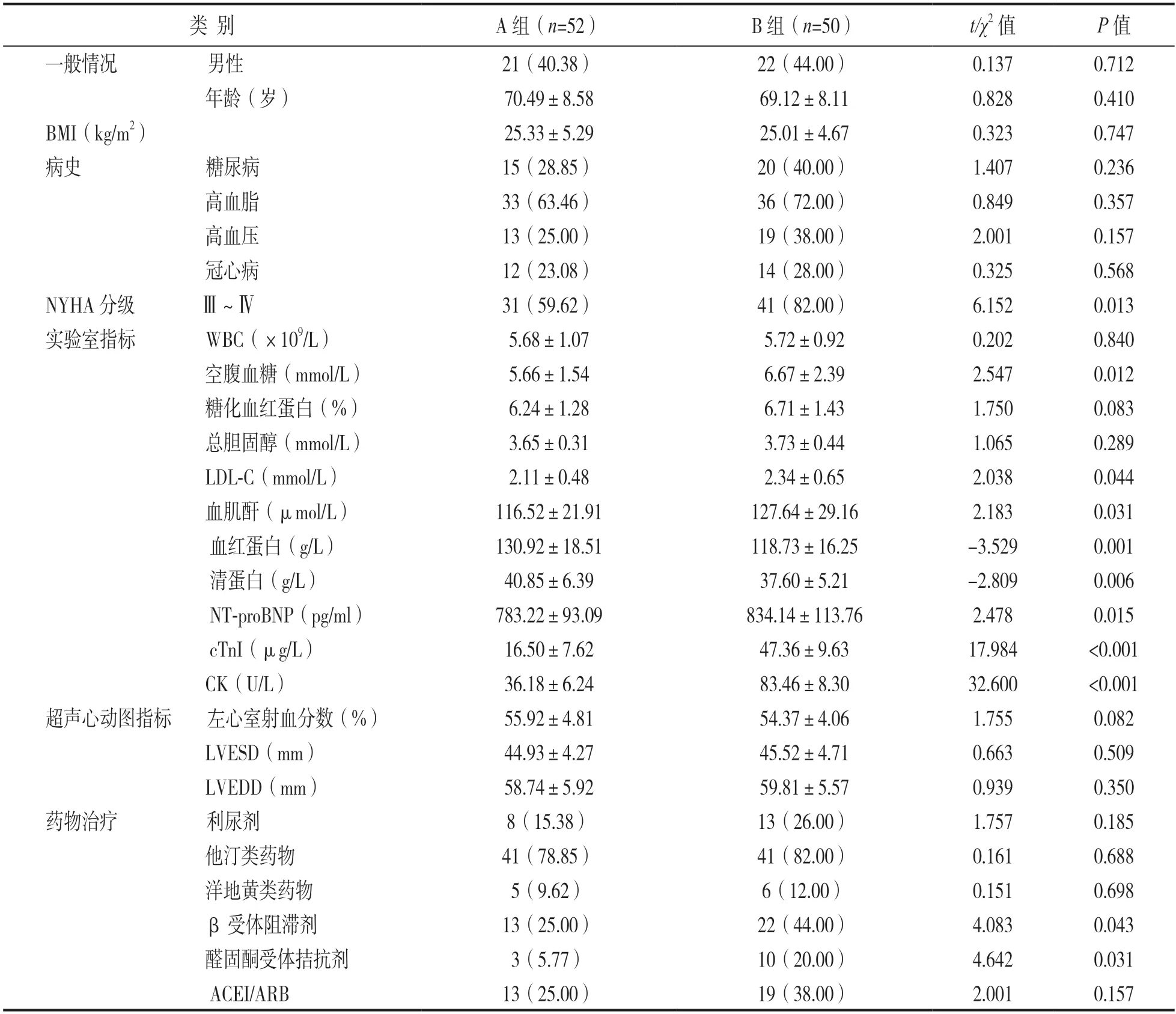
表1 两组患者的一般资料及实验室指标比较[n(%),±s]
类 别A 组(n=52)B 组(n=50)t/χ2 值P 值一般情况 男性21(40.38)22(44.00)0.1370.712年龄(岁)70.49±8.5869.12±8.110.8280.410 BMI(kg/m2)25.33±5.2925.01±4.670.3230.747病史 糖尿病15(28.85)20(40.00)1.4070.236高血脂33(63.46)36(72.00)0.8490.357高血压13(25.00)19(38.00)2.0010.157冠心病12(23.08)14(28.00)0.3250.568 NYHA 分级 Ⅲ~Ⅳ31(59.62)41(82.00)6.1520.013实验室指标 WBC(×109/L)5.68±1.075.72±0.920.2020.840空腹血糖(mmol/L)5.66±1.546.67±2.392.5470.012糖化血红蛋白(%)6.24±1.286.71±1.431.7500.083总胆固醇(mmol/L)3.65±0.313.73±0.441.0650.289 LDL-C(mmol/L)2.11±0.482.34±0.652.0380.044血肌酐(μmol/L)116.52±21.91127.64±29.162.1830.031血红蛋白(g/L)130.92±18.51118.73±16.25-3.5290.001清蛋白(g/L)40.85±6.3937.60±5.21-2.8090.006 NT-proBNP(pg/ml)783.22±93.09834.14±113.762.4780.015 cTnI(μg/L)16.50±7.6247.36±9.6317.984<0.001 CK(U/L)36.18±6.2483.46±8.3032.600<0.001超声心动图指标 左心室射血分数(%)55.92±4.8154.37±4.061.7550.082 LVESD(mm)44.93±4.2745.52±4.710.6630.509 LVEDD(mm)58.74±5.9259.81±5.570.9390.350药物治疗 利尿剂8(15.38)13(26.00)1.7570.185他汀类药物41(78.85)41(82.00)0.1610.688洋地黄类药物5(9.62)6(12.00)0.1510.698 β 受体阻滞剂13(25.00)22(44.00)4.0830.043醛固酮受体拮抗剂3(5.77)10(20.00)4.6420.031 ACEI/ARB13(25.00)19(38.00)2.0010.157
2.3 FIB 水平与血清及心肌损伤标志物的相关性分析 采用Spearman 相关性分析上述P<0.05 的血清及心肌损伤标志物与FIB 水平的相关性,结果见图2。血红蛋白、清蛋白与FIB 水平呈明显负相关(r=-0.831,-0.805,P=0.004,0.008);空腹血糖、LDL-C,血肌酐、NT-proBNP,cTnI 及CK 与FIB水平呈明显正相关(r=0.784,0.732,0.016,0.759,0.861,0.883,P=0.010,0.023,0.016,0.014,0.002,0.002)。

图2 两组患者易损期生存分析
2.4 两组患者易损期生存分析 见图2。随访三个月内,复合终点共发生23 例,其中全因死亡6 例,心力衰竭再入院17 例。A 组复合事件发生率(7 例,13.46%)及心力衰竭再入院率(4 例,7.69%)均明显低于B 组[16 例(32.00%),13 例(26.00%)]。使用Kaplan-Meier 法分析二组患者不同FIB 水平与易损期内复合终点事件、因心力衰竭再住院风险及全因死亡率的相关性,Log-Rank 检验发现,分别比较复合终点事件及因心力衰竭再入院风险,差异有统计学意义(P<0.05)。而两组的全因死亡率差异无统计学意义(P>0.05)。
2.5 影响HFpEF 患者易损期预后不良的单因素COX 比例风险回归 见表2。以易损期因心力衰竭再入院或全因死亡为结局事件,将102 例患者分为预后良好组和预后不良组,比较两组的一般资料、实验室指标、超声心动图指标及药物治疗方法,结果发现,两组的NYHA 分级Ⅲ~Ⅳ,WBC,空腹血糖、LDL-C,血肌酐、血红蛋白、清蛋白、NTproBNP,cTnI,醛固酮受体拮抗剂、CK,FIB 和β 受体阻滞剂差异均有统计学意义(均P<0.05)。
表2 影响HFpEF 患者易损期预后不良的单因素COX 比例风险回归[n(%),±s]
类 别预后良好组(n=78)预后不良组(n=24)χ2/t 值P 值一般情况 男性32(41.03)11(45.83)0.174 0.677年龄(岁)69.27±7.9172.28±8.261.614 0.110 BMI(kg/m2)24.96±4.8125.11±5.090.132 0.895病史 糖尿病24(30.77)11(45.83)1.848 0.174高血脂52(66.67)17(70.83)0.146 0.703高血压21(26.92)10(41.67)1.886 0.170冠心病25(32.05)12(50.00)2.558 0.110 NYHA 分级 Ⅲ~Ⅳ52(66.67)22(91.67)5.760 0.016实验室指标 WBC(×109/L)5.50±0.885.93±0.942.060 0.042空腹血糖(mmol/L)5.86±1.456.70±2.512.055 0.043糖化血红蛋白(%)6.39±1.306.87±1.521.519 0.132总胆固醇(mmol/L)3.57±0.443.62±0.560.455 0.650 LDL-C(mmol/L)2.08±0.632.40±0.712.111 0.037血肌酐(μmol/L)108.92±20.47130.38±31.662.087 0.039血红蛋白(g/L)128.51±16.54114.36±14.95-3.745<0.001清蛋白(g/L)41.25±6.1036.82±4.93-3.243 0.002 NT-proBNP(pg/ml)768.12±102.13842.14±121.762.965 0.004 cTnI(μg/L)15.35±7.2251.43±9.6719.686<0.001 CK(U/L)41.28±7.5679.19±9.4320.228<0.001 FIB(g/L)2.79±0.753.46±0.933.610<0.001超声心动图指标 左心室射血分数(%)56.20±8.1955.08±6.920.606 0.546 LVESD(mm)42.19±6.3844.93±7.611.756 0.082 LVEDD(mm)57.52±7.4158.43±8.060.515 0.607药物治疗 利尿剂15(19.23)6(25.00)0.374 0.541他汀类药物62(79.49)20(83.33)0.172 0.678洋地黄类药物9(11.54)2(8.33)0.196 0.658 β 受体阻滞剂22(28.21)13(54.17)5.488 0.019醛固酮受体拮抗剂7(8.97)6(25.00)4.348 0.037 ACEI/ARB15(19.23)7(29.17)1.071 0.301
2.6 影响HFpEF 患者易损期预后不良的COX 比例风险回归 见图3。将表2 中P<0.05 的指标纳入COX 比例风险回归模型,因变量为HFpEF 患者易损期预后情况(预后良好=0,预后不良=1)。结果发现,NYHA 分级Ⅲ~Ⅳ,NT-proBNP,cTnI,CK 和FIB 是影响HFpEF 患者易损期预后不良的危险因素,血红蛋白、清蛋白是保护因素。
2.7 ROC 预测模型评价 通过ROC 评价上述模型的诊断效能,模型1 AUC 为0.882(95%CI:0.810~0.937),灵敏度和特异度分别为84.6%,87.9%。模型2 AUC 为0.771(95%CI:0.735~856),灵敏度和特异度分别为74.7%,75.3%,提示模型1 诊断效能更佳。
2.8 两个模型的内部验证校准图 见图4。内部验证显示,校准图中标准曲线与预测曲线吻合较好,提示预测的HFpEF 患者易损期预后不良情况与实际结果较好一致性较好。

图4 两模型的内部验证校准图
3 讨论
依据左心室射血分数(LVEF)水平,临床通常将心力衰竭分为射血分数保留的心力衰竭(HFpEF)、射血分数中间型的心力衰竭(HFmrEF)及射血分数减低的心力衰竭(HFrEF)。近年来,临床医生对HFrEF 及HFmrEF 的诊断和治疗已取得较大成果,然而对于HFpEF 的了解还很少[9],HFpEF 患者院外管理仍存在大量空白。出院后三个月内,由于该时期心力衰竭患者血流动力学不稳定、心室收缩功能降低;加之患者入院时存在充血症状及下肢水肿、呼吸困难等体征,肝脏、肾脏等器官也可能存在不同程度损害,住院期间未能彻底纠正这些损害,使得出院后充血加重,导致患者在该时期极易发生再入院或死亡,因此,临床将该时期称为“心力衰竭易损期”。鉴于易损期内较高的再入院率及死亡率,寻找可反映HFpEF 患者易损期预后情况的有效标志物,探索其与患者一般临床指标及预后的关系,对改善易损期预后具有重要意义。
FIB 是一种由肝脏合成的急性时相反应蛋白,是血浆中含量最高的凝血因子[10]。FIB 作用于血管壁,直接参与血栓形成,随着血浆FIB 含量增加,心肌病变程度加重,越容易引发心血管疾病。已有研究发现FIB 是心肌梗死等心脑血管疾病的独立预测因素[11]。本研究发现,FIB 与空腹血糖,LDL-C,血肌酐,NT-proBNP,cTnI 及CK 呈明显正相关。血肌酐,NT-proBNP,CK 和cTnI 作为常用的心肌损伤标志物,可反映心脏衰竭程度,三者含量明显升高可提示患者心肌受损严重[12]。以往也有研究报道[13-14],心肌损伤指标与FIB 可协同加快心血管疾病进展。HFpEF 患者空腹血糖水平增高可能是由于机体处于应激状态,其体内应激相关激素分泌增多,导致糖异生增强,血小板活性增加,使患者体内处于高血小板状态,在FIB 协同作用下,极易形成微血栓,从而导致患者出院后发生心血管事件风险增加[15]。脂代谢紊乱可导致心力衰竭进展,近年来已有研究证实[16],LDL-C 与心力衰竭密切相关。LDL-C 是重要的内皮损伤因素,可上调巨噬细胞集落刺激因子和单核细胞趋化蛋白-1 基因表达,从而促进炎症反应,诱导微血栓形成。此外,本研究发现,血红蛋白、清蛋白与FIB 水平呈明显负相关。血红蛋白是反映贫血状况的指标,其含量减少,引起贫血,导致血流加速,心脏负荷加重,心肌肥厚,FIB 含量增加,进一步引起心肌细胞损伤[17]。清蛋白水平减少,稀释患者血液,血浆胶体渗透压降低,血管内液体转移至组织间,引起负重,FIB 水平增加,引起心力衰竭症状加重。以上均反映FIB 水平升高患者本身生化指标也会发生异常,导致病情加重。
已有研究报道[18],FIB 水平升高与心肌梗死等心血管疾病远期预后有关。本研究生存曲线结果显示,FIB 水平对HFpEF 患者易损期复合终点事件及因心力衰竭再入院风险有明显影响。分析原因可能是:①HFpEF 患者心排出量减少,激活交感-肾上腺系统,刺激机体释放更多的儿茶酚胺,通过α肾上腺素受体激活血小板,影响纤溶活性;②心力衰竭时交感-肾上腺系统被激活,血管紧张素Ⅱ刺激血小板聚集,阻碍纤溶酶原的作用,造成微血栓形成,导致预后不良;③发生心力衰竭时组织缺血缺氧,血管内皮细胞受损,暴露内皮下胶原蛋白,激活内源性凝血途径,进一步造成机体高凝状态及微血栓形成,从而增加心力衰竭再入院风险[19]。为进一步探究FIB 对HFpEF 患者预后不良的预测价值,本研究分别建立2 个模型,模型1 纳入FIB,模型2 未纳入FIB,评价结果显示,模型1 有更高的预测价值。通过ROC 曲线及内部数据验证显示,2 个模型的预测价值均较好。此外,本研究结果显示,NYHA 分级Ⅲ~Ⅳ,NT-proBNP,cTnI,CK均是影响HFpEF 患者易损期预后不良的危险因素,血红蛋白、清蛋白是保护因素。与WANG 等[20-21],的研究结果一致。
综上所述,FIB 与血红蛋白、清蛋白呈明显负相关;与空腹血糖、LDL-C,血肌酐、NT-proBNP,cTnI 及CK 呈明显正相关。FIB 是HFpEF 患者易损期预后不良的独立预测因子。本研究为一项单中心研究,病例数较少。不仅只有FIB 会影响HFpEF患者易损期全因死亡或再入院,其他凝血纤溶相关指标也会对预后产生不同程度的影响,并可能影响对FIB 研究结果的分析。因此,后续本课题组会增加样本量,纳入其他相关凝血纤溶相关指标,分析各相关指标间的关系。
- 现代检验医学杂志的其它文章
- 急性肺栓塞患者血清ADAM15和MMP-2表达水平及其与疾病严重程度的相关性研究
- 肺炎支原体感染诱发哮喘患儿血清中miR-424-5p和CX3CL1表达水平及与预后预测价值研究
- ALKBH5调控GEFT的m6A修饰对胆管癌转移及EMT的实验研究
- LncRNA NNT-AS1通过调控miR-582-5p/NCKAP1轴激活Hippo-YAP/TAZ信号通路促进膀胱癌细胞增殖、迁移、侵袭和干细胞干性影响
- 血浆外泌体miR-4306表达水平联合CT征象对单发非实性肺结节良恶性鉴别的价值研究
- 白细胞介素-1β基因(rs16944)单核苷酸多态性与骨髓增生异常综合征易感性及临床特征的相关性研究

