过敏性鼻炎患者IgE、miR-487b和EOS水平分析及其与VAS评分的相关性*
马荧雪,缪陶林,庄强尔
无锡市儿童医院耳鼻咽喉科,江苏无锡 214000
过敏性鼻炎(AR)是易感机体接触过敏原后受到免疫球蛋白IgE介导并造成Ⅰ型变态反应的表现之一,该过程由多种免疫细胞和细胞因子参与[1-2]。AR患儿主要的临床表现包括鼻通气性差、有明显痒感、出现大量清水样涕及阵发性喷嚏,多数患儿病程较长且呈季节性发病,一定程度上会影响患儿的生活质量[3-4]。有学者围绕AR的发病机制进行分析发现嗜酸细胞(EOS)的水平异常增加是其主要病理表现[5]。微小RNA-487b(miR-487b)被认定可以实现对蛋白质的转录调控进而影响机体的炎症反应,并对巨噬细胞产生负调控作用,提示miR-487b可能参与AR的发生过程[6]。另外,研究发现患儿出现明显过敏反应的主要机制为IgE介导的Ⅰ型变态反应,针对该指标的临床检测也成为目前常用的诊断方式,检测血清特异性IgE水平并观察患儿阳性反应变化情况,可明确患儿过敏源并开展针对性地治疗,对改善患儿临床症状、提高生活质量具有积极作用[7]。因此本研究对AR患儿IgE、miR-487b和EOS水平进行分析,探讨其与患儿疼痛程度的相关性,现将研究结果报道如下。
1 资料与方法
1.1一般资料 将2020年1月至2022年6月在本院门诊确诊为AR的共98例患儿纳入研究作为AR患儿组。另外,选取同期在本院接受体检的健康儿童66例作为对照组。AR患儿组中,男56例,女42例;年龄4~12岁,平均(8.16±2.14)岁;病程3个月至3年,平均(6.25±1.01)个月。健康对照组中,男39例,女27例;年龄3~12岁,平均(7.81±2.22)岁。两组基线资料包括性别、年龄等数据比较,差异无统计学意义(P>0.05),具有可比性。AR患儿组纳入标准:(1)患儿临床症状表现及诊断结果均符合AR诊断标准[8];(2)临床资料完整;(3)患儿及家属临床依从性好,可配合完成本研究相关调查工作直至研究结束。排除标准:(1)合并鼻息肉/鼻腔内肿瘤患儿;(2)患儿在本院就诊前6个月内接受过免疫治疗、抗过敏药物治疗、激素治疗等;(3)合并其他过敏症状;(4)具有鼻腔相关手术史;(5)合并肝、肾等严重器质性功能障碍病变。
1.2方法
1.2.1IgE检测 取所有研究对象空腹状态下肘静脉血5 mL并收集于促凝管中,30 min后行离心机离心操作,参数设定为3 500 r/min,离心半径10 cm,持续离心15 min后取上清液(血浆)作为待测标本。应用UniCAP 100E全自动体外免疫诊断仪(瑞典Phadia AB公司)及配套试剂盒检测特异性IgE水平。
1.2.2以PCR法检测血浆miR-487b的表达 取1.2.1中分离的血浆标本置于-20 ℃低温冰箱保存待测。应用实时荧光定量PCR(qPCR)测定研究对象血浆中miR-487b的表达水平。按照试剂盒说明书严格完成操作,首先提取研究对象血样中血浆总RNA,经异丙醇沉淀浓缩后应用75%乙醇完成洗涤并干燥,之后加入100 μL DEPC水,对所得RNA纯度及完整度进行检测并明确;按照逆转录试剂盒说明书完成cDNA逆转录,之后置于-20 ℃保存备用。qPCR反应(反应体系20 μL):上下游引物各1 μL,双蒸水6 μL,每一样本设定3个平行检测孔。上下游引物、内参基因引物由上海恒斐生物科技有限公司设计并合成,miR-487b的检测以U6为内参。引物序见表1。反应条件:预变性 95 ℃ 8 min;在90 ℃环境下持续变性20 s,之后60 ℃环境下完成退火并持续40 s,在72 ℃环境下延伸25 s,共持续40个循环。采用2-ΔΔCt法计算血浆中miR-487b相对表达水平。

表1 qPCR引物序列
1.2.3以全自动血液细胞分析仪检测EOS水平 采用空腹状态下取得的抗凝静脉血标本进行EOS检测,使用的检测仪器为迈瑞BC5150全自动血液细胞分析仪。
1.2.4以视觉模拟量表(VAS)评分评估患儿疼痛程度 AR患儿均根据自身临床症状填写VAS评分(其得分可采用cm作为计量单位,使用0~10 cm来表示):以VAS评分<5.3 cm为轻度,≥5.3 cm为中重度[9]。
1.3观察指标 (1)对比两组各指标水平;(2)对比不同严重程度AR患儿各指标水平;(3)分析各指标单一检测及三项联合检测模式对AR的诊断效能;(4)分析各指标与AR患儿VAS评分的相关性。

2 结 果
2.1比较两组IgE、miR-487b和EOS水平 AR患儿组IgE、EOS水平均明显高于对照组(P<0.05);AR患儿组miR-487b表达水平明显低于对照组(P<0.05),见表2。
表2 两组IgE、miR-487b和EOS表达情况对比
2.2比较不同严重程度AR患儿IgE、miR-487b和EOS水平 根据AR患儿病情严重程度进行评估并建立亚组,分别为轻度AR组(51例)和中重度AR组(47例),对比两组各指标水平,结果显示,随着AR患儿病情严重程度的增加,其IgE、EOS水平呈升高的趋势,其miR-487b表达呈下降趋势(均P<0.05),见表3。
表3 不同严重程度AR患儿IgE、miR-487b和EOS表达情况对比
2.3分析IgE、miR-487b和EOS单一检测及三项联合检测模式对AR的诊断效能 ROC曲线分析显示,IgE、miR-487b和EOS单一检测的曲线下面积均较低,三项联合检测的曲线下面积明显高于单一指标检测(AUC=0.908,P<0.05),见表4、图1。
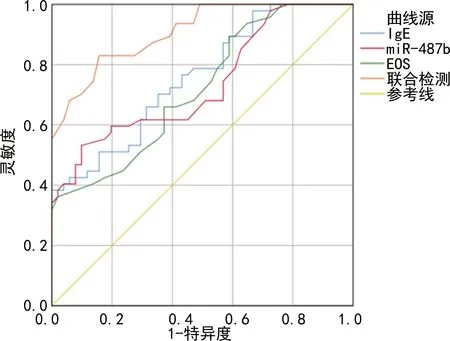
图1 IgE、miR-487b、EOS单项及联合检测对AR的诊断价值分析
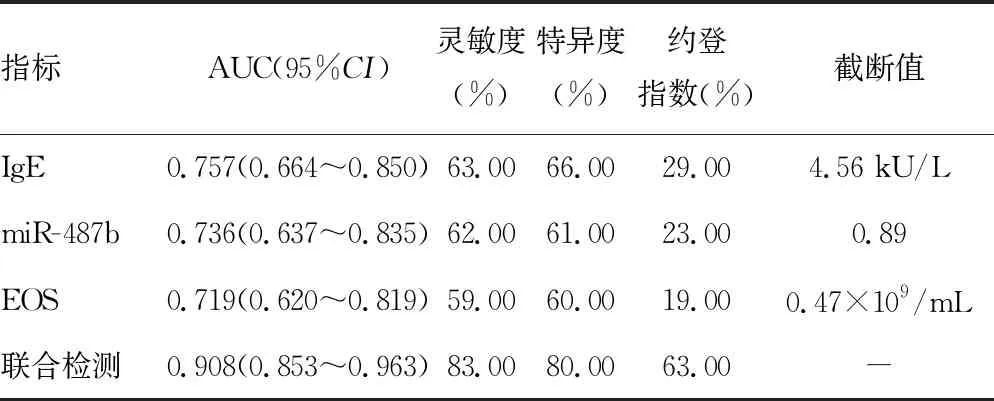
表4 IgE、miR-487b、EOS单项及联合检测对AR的诊断价值分析
2.4IgE、miR-487b和EOS与AR患儿VAS评分的相关性 Pearson相关分析显示,IgE、EOS与VAS评分呈正相关(r=0.581、0.594,P<0.05),miR-487b水平与VAS评分呈负相关(r=-0.587,P<0.05),见图2~4。
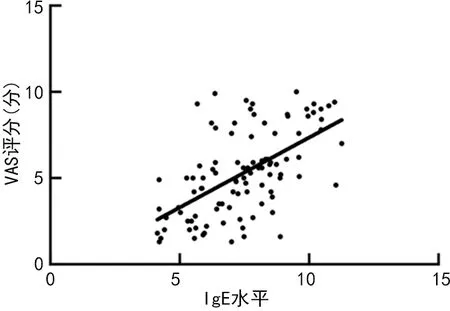
图2 IgE与VAS评分的相关性
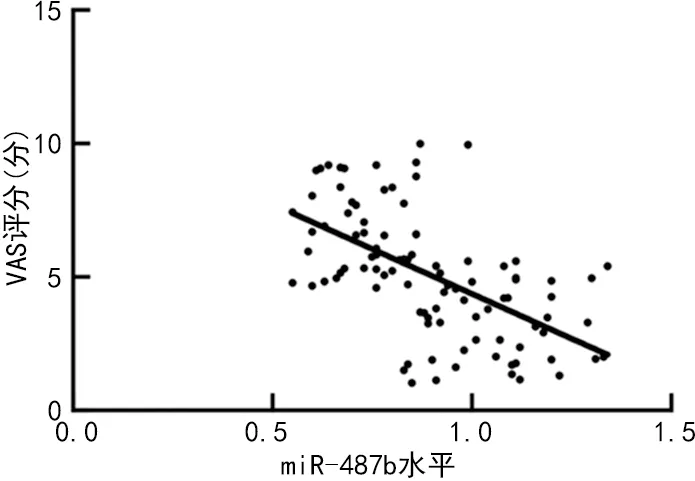
图3 miR-487b与VAS评分的相关性
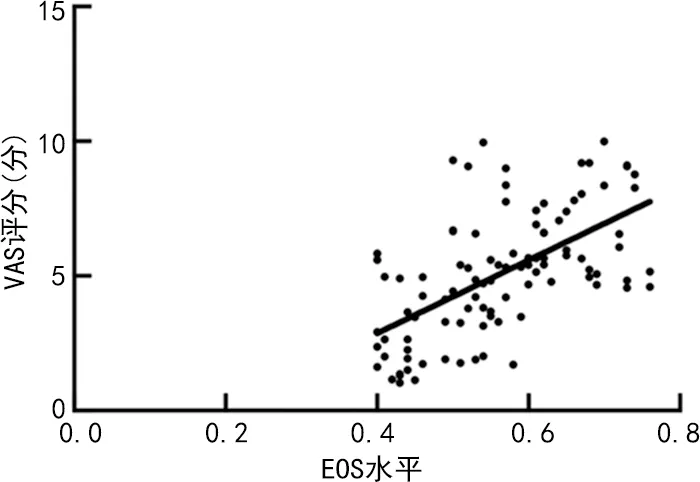
图4 EOS表达与VAS评分的相关性
3 讨 论
AR是临床耳鼻喉科常见的一类病症,随着人们居住环境污染程度的加剧,AR发病率也呈现逐年递增态势[10]。AR患儿发病若不给予科学合理的干预治疗方案,随着病情进展很可能会引发哮喘、分泌性中耳炎等病症。现阶段临床针对AR发病因素进行了探讨,多数学者认为是抗原进入易过敏个体内引起相关炎症介质的大量释放加剧了炎症反应[11]。
本研究针对AR患儿及健康受试者进行对比研究,发现AR患儿IgE水平较健康儿童明显增高,而且随着病情程度的增加,该指标水平呈升高趋势,原因可能是与AR发病机制有关。既往研究已证实AR发病主要是机体内IgE介导的、以EOS浸润为主的慢性炎症。受AR患儿自身过敏体质影响,当机体吸入变应原后所产生的特异性IgE与自身鼻黏膜肥大细胞和嗜碱性粒细胞处聚集的IgE受体进行结合,当患儿再次吸入变应原时,与靶细胞表面的IgE结合后释放大量炎症介质介质进而引发AR[12]。
本研究结果显示,AR患儿EOS水平较健康儿童明显升高,而且随着病情程度的加剧,患儿EOS水平更高,分析原因可能是EOS在机体内的作用机制有关。EOS属于一类具有免疫监视的效应细胞,EOS的活化会到导致炎症介质释放并加剧各类炎症反应。EOS可导致鼻黏膜受损,增加鼻黏膜的敏感性。相关研究显示[13],EOS活化不仅会造成机体发生过敏性疾病的风险增加,一定程度上也会影响患者的病情发展程度。本研究结果与既往研究结果基本一致,分析原因可能是AR发作过程中上皮细胞、成纤维细胞等所释放的炎症因子促使EOS分化并趋化迁移至鼻黏膜。同时嗜酸性粒细胞、上皮细胞和肥大细胞可以分泌多种炎症因子,使鼻黏膜组织中EOS呈现高表达。EOS活化后的产物可合成大量毒性物质,进而引发呼吸道黏膜上皮损伤,加重局部的炎症反应[14]。既往关于一项AR发病机制的研究指出,EOS的异常表达可导致小血管壁损伤并加剧局部通透性,进而造成组织水肿及血浆外渗,加重鼻部症状,与本研究结果基本一致[15]。
既往有学者研究发现miR-487b可抑制炎症介质进而减轻心力衰竭患儿机体炎症反应程度[16]。而一项动物实验结果发现,AR模型小鼠miR上调可以抑制炎症介质表达,进而起到抑制AR的效用,提示miR-487b是治疗AR的潜在治疗靶点[17]。本研究结果显示,miR-487b在AR患儿人群呈现低表达,而且随着患儿病情程度的加剧呈现下降趋势,提示miR-487b对AR病情的发生发展具有一定参与作用,而出现这一差异的原因可能是miR-487b在患儿机体中起到抑制炎症反应的效用。miR-487b是14q32miRNA簇成员之一,临床研究显示该miRNA在机体炎症状态下可实现对基因转录的有效抑制,进而对炎症相关因子起到抑制作用;miR-487b在人体内可靶向控制IL-33,miR-487b表达上调可实现对炎症因子的抑制效用,并提示miR-487b可能是AR的相关有效检测指标。
另外,本研究建立ROC曲线进行分析发现,IgE、miR-487b、EOS三项指标对诊断AR病情程度均有一定效用,但三者联合检测诊断效能更高,提示后续临床可通过上述三项指标明确患儿病情发展程度并针对性给予有效治疗。AR的过敏原主要以吸入性过敏原(以户尘螨和粉尘螨为主)为主。VAS评分能较好地反映AR患儿的疾病严重程度。采用Pearson相关系数分析发现,IgE、EOS水平与VAS评分呈正相关,miR-487b表达与VAS评分呈负相关,也进一步提示上述三项指标可有效反映出患儿临床症状严重程度。
综上所述,IgE、miR-487b和EOS对AR患儿的诊断效能较高,而且三项指标联合检测的效能更高。IgE、miR-487b和EOS水平与AR患儿疼痛程度密切相关,提示临床可密切观察AR患儿IgE、miR-487b和EOS水平并完善相应诊疗方案,减轻患儿临床不良症状,促进患儿快速康复。但本研究也存在一定不足,如样品量较少且整个研究时间较短,可能会使研究结果出现偏倚性,后续研究中会继续扩大样本量及样本范围,深入分析相关机制来提高研究的科学性和结论的准确性。

