乳腺癌放疗患者疾病不确定感、癌因疲乏与心理控制源相关性分析
李红玉,王 静,张金珠
(郑州大学附属肿瘤医院 河南省肿瘤医院 河南郑州450000)
乳腺癌是女性常见恶性肿瘤,放疗是乳腺癌主要治疗措施之一[1]。在乳腺癌放疗的治疗过程中,患者需要面对治疗方案、治疗效果、生活质量等方面的未知和不确定性,产生不安和焦虑[2]。乳腺癌放疗患者治疗过程漫长而复杂,患者需要承受较大的精神压力,由于疾病不确定感、睡眠质量下降也可能导致疲乏感[3]。此外治疗期间,患者的身体运动量下降,身体适应能力下降,身体疲劳感增加,可能会出现癌因性疲乏。癌因性疲乏是一种身体和情绪上的疲乏感,与日常疲劳感不同,它不会因为休息或睡眠而缓解,严重影响患者的生活质量[3]。乳腺癌放疗患者需要认真对待疾病不确定感、癌因性疲乏问题,积极采取措施进行缓解,提高生活质量,同时也要保持乐观的心态[4]。心理控制源是指个体通过自我努力和控制来应对不确定性和压力的能力[5]。乳腺癌放疗会对患者的身体和心理造成一定的负担,患者需要通过积极的心理控制源来应对这些负面影响。本研究通过探究乳腺癌放疗患者疾病不确定感、癌因疲乏及心理控制源的相关性,旨在更加高效的帮助患者减轻癌因性疲乏,减轻疾病不确定感,以提高患者的生活质量,促进患者康复,缩短住院时间,减轻经济负担。现报告如下。
1 对象与方法
1.1 研究对象 选取2020年8月1日~2022年8月31日在我院就诊的100例乳腺癌放疗患者为研究对象,患者年龄30~73(53.8±9.7)岁;受教育程度:高中及以下38例,大专30例,本科及以上32例;婚姻状况:未婚20例,已婚72例,离异3例,丧偶5例;肿瘤TNM分期:Ⅱ期49例,Ⅲ期29例,Ⅳ期22例;放疗次数2~16(8.9±2.1)次。纳入标准:①经病理诊断为乳腺癌[6]者;②年龄≥18岁者;③为女性患者,术后接受放疗者。排除标准:①存在认知功能障碍或合并精神疾病者;②合并其他恶心肿瘤患者;③有严重的听力及语言沟通障碍者;④合并严重脏器功能障碍者;⑤依从性较差不能配合完成研究者。本研究经医院医学伦理委员会审核批准,由患者及家属签署知情同意书。
1.2 方法
1.2.1 一般资料调查 患者入院时接受基本资料及病理信息调查,采用医院自制的调查问卷,基本资料包括性别、年龄、受教育程度、婚姻状况、肿瘤TNM分期、放疗次数。
1.2.2 心理控制源 采用多维度健康状况心理控制源量表(MHLC)[7]对患者心理控制源水平进行评估,该量表由18个项目构成,具体分为机遇量表(机遇型)、权威人士量表(他控型)、内控性(内控型)量表3 个子量表;每个项目采用6级评分法,根据说明将每个量表的原始分转换成0~100分,得分越高表示心理控制源状况越好,Cronbach′s α为0.86。MHLC评分<61分为中低水平, MHLC评分≥61分为高水平,本组患者中低水平61例作为对照组,高水平39例作为研究组。
1.2.3 疾病不确定感 采用Mishel疾病不确定感自评量表(MUIS)[8]对患者的疾病不确定感进行评估,该量表包括对疾病预后不可预测性、不明确性、复杂性、信息缺乏性4个维度,共24个条目,每个条目按1~5级进行评分,1~5分表示影响程度由非常不同意到非常同意,总分为32~160分,得分越高表示疾病不确定感越严重,Cronbach′s α为0.89。
1.2.4 癌因性疲乏 采用改良版Piper疲乏量表(RPFS)[9]对患者疲乏程度进行评估,该量表包括4个维度,共22个条目,每维度10分,0分表示没有疲劳、1~3分表示轻度疲劳、4~6 分表示中度疲劳、7~10 分表示重度疲劳,最终量表得分越高表示疲乏程度越严重,Cronbach′s α为0.90。
1.3 调查方法 由医护人员向患者发放调查问卷,由患者独立填写完成后现场收回,本次共计发放100份问卷,回收100份,回收率为100%。
2 结果
2.1 100例乳腺癌放疗患者MHLC评分与常模比较 见表1。

表1 100例乳腺癌放疗患者MHLC评分与常模比较(分,
2.2 两组MUIS评分比较 见表2。

表2 两组MUIS评分比较(分,
2.3 两组RPFS评分比较 见表3。

表3 两组RPFS评分比较(分,
2.4 乳腺癌患者疾病不确定感、癌因性疲乏与心理控制源相关性分析 见表4。
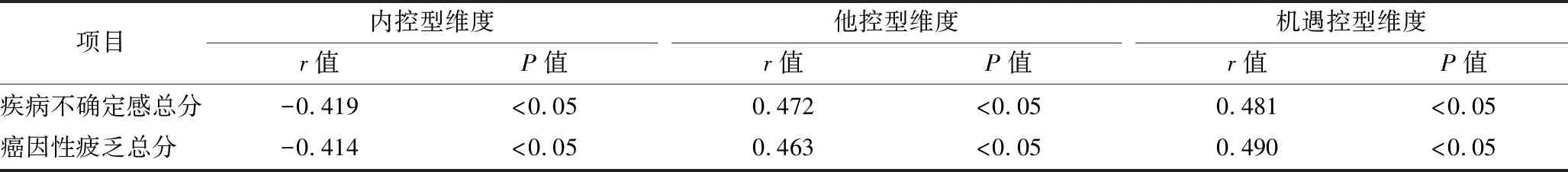
表4 乳腺癌患者疾病不确定感、癌因性疲乏与心理控制源相关性分析
3 讨论
心理控制源是指个体感知控制环境和自我命运的能力和信念。有研究发现,心理控制源水平较高的患者具有更强的心理适应能力和更少的情绪问题,能够更好地应对疾病不确定性带来的压力,乳腺癌患者心理控制源水平与患者的心理健康、生活质量密切相关[10]。心理控制源包括两个方面:内部控制源和外部控制源。内部控制源是指个体相信自己的行为和决策能够影响环境和结果;而外部控制源则是指个体相信外部因素(如运气、命运等)决定了环境和结果。有研究发现,内部控制源水平较高的患者在面对疾病不确定性时表现出更强的主动性和积极性,更容易采取有效的应对措施,而外部控制源水平较高的患者则更容易感到无助和失望。
本研究100例乳腺癌放疗患者MHLC中他控型、机遇控型评分均高于常模(P<0.05),而内控型评分低于常模(P<0.05),提示乳腺癌放疗患者心理控制源偏外部控制,缺乏足够的自信。放疗治疗过程中,可能会面临疾病的不确定性,如疾病是否会复发、治疗效果如何等,这种不确定性会引起患者的恐惧和焦虑;同时,患者可能会因为手术或放疗等治疗方式而导致身体外貌的改变,如乳房变形、脱发等,这些改变会影响患者的自信心和自尊心,社交活动减少,社交支持缺失。此外,患者可能会出现乳房肿胀、疼痛、皮肤干燥、瘙痒等不适症状及放疗的副作用,这些症状会引起患者的不适感和痛苦,从而影响患者的情绪和心理状态。因此,对乳腺癌放疗患者,提高其内部控制源水平、鼓励其采取积极主动的应对措施,有助于降低其疾病不确定感和缓解负性情绪。同时,心理干预和支持也可以帮助患者提高其心理控制源水平,从而增强其应对疾病的能力和信心。
本文研究表明,100例乳腺癌放疗患者MUIS、RPSF总分与MHLC中内控型维度评分呈负相关(P<0.05),与他控型、机遇控型评分呈正相关(P<0.05),说明患者的疾病不确定感与心理控制源存在负相关。也就是说,疾病不确定感越高,患者的心理控制源越低,即患者越难以应对自己的疾病和治疗过程,心理状态越容易受到影响。治疗过程中的不确定性和恐惧感会影响患者对治疗的信任,而医疗专业人员的支持和关怀则能够帮助患者增强对治疗的信任感和控制感。乳腺癌放疗患者的心理控制源还包括社会支持和情感调节。社会支持可以减轻患者的焦虑和抑郁,而情感调节则可以帮助患者更好地应对治疗过程中的情绪波动。
乳腺癌放疗患者在治疗过程中可能会经历疲乏感,是一种身体和心理疲劳的表现。有研究表明,乳腺癌放疗患者的疲乏感可能与多种因素相关,包括癌症本身、治疗副作用、心理因素等。在心理因素方面,心理控制源是指一个人的内在信念和期望,即一个人相信自己能够控制环境中的事物,并且相信自己的努力可以产生积极的结果。相反,缺乏心理控制源的人可能认为自己无法控制环境中的事物,他们的努力可能不会产生积极的结果,它们可以影响个体的行为和情感反应。有研究发现,缺乏心理控制源的患者更容易出现疲乏感,因为他们可能会感到无助和无力。具有心理控制源的患者则更有可能采取积极的行动来应对疲乏感,从而缓解疲乏症状。乳腺癌放疗患者的心理控制源可能与其疲乏感有关。具体而言,具有心理控制源的患者可能更容易应对疲乏感,而缺乏心理控制源的患者则可能更容易出现疲乏感。因此,在治疗和管理癌因性疲乏的过程中,应考虑心理因素,并提供相关的支持和治疗。如心理治疗、认知行为疗法、冥想等技术,可以帮助乳腺癌放疗患者减轻心理压力,提高心理控制源水平,减轻癌因性疲乏的症状。
总之,乳腺癌放疗患者的心理控制源是一个复杂的问题,需要医疗专业人员、社会支持和患者本身的努力来共同解决。这些因素的积极作用可以帮助患者更好地应对治疗过程中的心理挑战。

