EGFR在胶质瘤中的表达及其与胶质瘤诊断和预后的分析
刘志轩 姜 蕊
湖北省钟祥市中医院脑病科 431900
中枢神经系统(CNS)恶性肿瘤是预后最差的癌症之一,早在1985年,Westermark B等人发现,表皮生长因子受体(Epidermal Growth Factor Receptor,EGFR)基因和胶质瘤密切相关[1]。研究表明EGFR促进胶质瘤增长并影响人的生存率[2-4],然而,EGFR对人胶质肿瘤预后的影响却少有报道,本文利用肿瘤数据库TCGA 数据库,结合R语言,验证EGFR是否在胶质瘤中高表达,并评估其能否对胶质瘤的患者预后产生影响,为后续EGFR相关分子筛选、明星通路的阐明以及胶质瘤和EGFR相关靶点分子的筛选奠定前期基础。
1 资料与方法
1.1 临床资料的获取 从癌基因组数据库(TCGA,https://portal.gdc.cancer.gov/)获取 GBMLGG(胶质瘤)项目中 level 3 HTSeq-FPKM格式的RNAseq数据,将 FPKM (fregments per kilobase per million) 格式的RNAseq数据转换成了TPM (transcripts per million reads) 格式,进而进行log2转化。根据分子:EGFR[ENSG00000146648],以0%~50% VS 50%~100%进行分组(EGFR低表达组、EGFR高表达组)、利用软件:R(3.6.3版本)进行统计分析与表格生成[5]。P<0.05表示两组抑或多组之间的亚组间存在统计学差异。
1.2 EGFR在胶质瘤中的表达情况 调取数据:UCSC XENA (https://xenabrowser.net/datapages/)经Toil流程(Vivian J等,2017)[6]统一处理的TCGA和GTEx的TPM格式的RNAseq数据。提取TCGA的GBMLGG(胶质瘤)和GTEx中对应的正常组织数据,进而分为临床变量: 胶质瘤组 VS 正常组。接着将数据按照TPM格式的RNAseq数据进行log2转化方法进行转化。 在R软件中利用ggplot2包可视化分子: EGFR[ENSG00000146648] 在两组中的表达情况。
1.3 ROC曲线分析 利用R(3.6.3版本)中R包: pROC包[1.17.0.1版本](用于分析)、ggplot2包[3.3.3版本] (用于可视化)处理数据。数据:UCSC XENA (https://xenabrowser.net/datapages/)经Toil流程(Vivian J 等,2017)[6]统一处理的TCGA和GTEx的TPM格式的RNAseq数据。提取TCGA的GBMLGG(胶质瘤)和GTEx中对应的正常组织数据,进而分为临床变量: 胶质瘤组 VS 正常组。以横坐标为假阳性率(FPR),纵坐标为真阳性率(TPR) 预测分子:EGFR[ENSG00000146648]在鉴定肿瘤中的作用。数据转化方法为:TPM格式的RNAseq数据进行log2转化。
1.4 KM生存分析 从癌基因组数据库(TCGA,https://portal.gdc.cancer.gov/ )获取 GBMLGG(胶质瘤)项目中 level 3 HTSeq-FPKM格式的RNAseq数据,将FPKM格式的RNAseq数据转换成了TPM格式,进而进行log2转化。根据分子:EGFR[ENSG00000146648],以0%~50% VS 50%~100%进行分组,然后利用R包:survminer包[0.4.9版本](用于可视化)、survival包[3.2-10版本] (用于生存资料的统计分析),利用软件:R(3.6.3版本)进行统计分析与可视化。
2 结果
2.1 TCGA数据库中患者临床数据特征 从 TCGA数据库中纳入696例患者临床信息,男398例,女298例,其中男性相对女性EGFR表达增高(P<0.05)。同时我们也发现相对年轻的患者EGFR的表达也存在增高现象(P<0.05);相比较前两者,EGFR在胶质瘤亚型中表达差异不显著(P=0.127)。相比较EGFR的低表达,EGFR的高表达增加死亡率(17.5% VS 21.6%),同时降低生存率(32.5%VS 28.4% )。见表1。

表1 高/低表达EGFR组临床资料对比
2.2 EGFR在胶质瘤中的表达情况 从TCGA数据库中纳入1 157例正常组和689例胶质肿瘤组患者,从统计描述表中可以看到,正常组的中位数(上下四分位数)为2.10(1.59~2.57),胶质瘤组的中位数(上下四分位数)为5.68(4.69~6.57),见表2。正态性检验结果显示,样本不满足正态性检验(P<0.05), Mann-WhitneyU检验(Wilcoxon rank sum test)结果显示,胶质瘤组高于正常组,两组的差值中位数为3.573(3.466~3.682),差异具有统计学意义(P<0.001)。
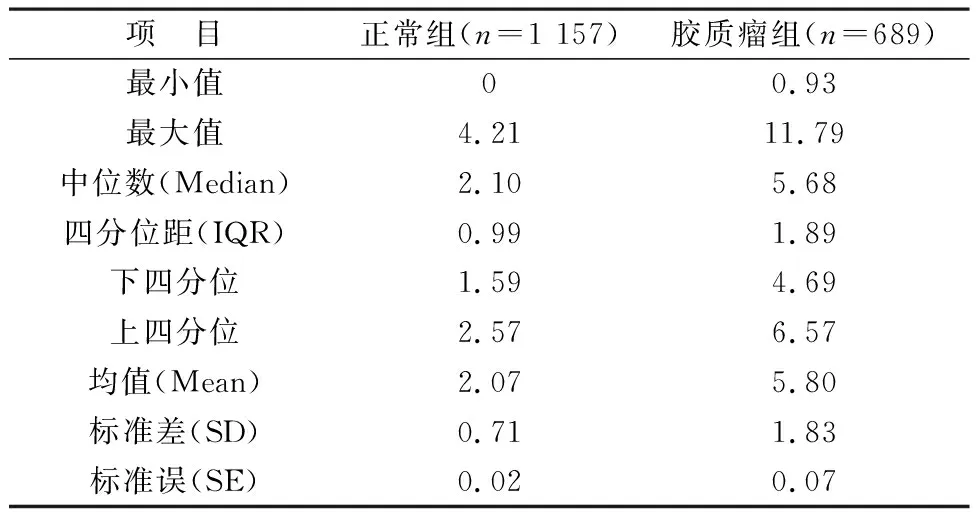
表2 正常组和胶质瘤组EGFR表达情况统计学数据
2.3 EGFR分子诊断胶质瘤的能力 从图1可见,EGFR在诊断胶质瘤能力方面,变量EGFR在诊断胶质瘤的临床特异性和敏感度有较高准确性(AUC=0.979,95%CI= 0.971~0.986)。

图1 EGFR在预测胶质瘤的ROC曲线ROC曲线下的面积值在0.5和1之间。AUC越接近于1,说明诊断效果越好。AUC在 0.5~0.7时有较低准确性,AUC在0.7~0.9时有一定准确性,AUC在0.9以上时有较高准确性
2.4 EGFR在胶质瘤患者预后生存中的能力 经survminer包计算得到各组的中位生存时间,其中EGFR低表达组的中位生存时间为63.8(46.7~95.8)个月;EGFR高表达组的中位生存时间为41.7(32.5~51.2)个月。从统计检验表可得:Log-rank检验结果提示,不同EGFR表达分组的生存时间分布差异具有统计学意义(P=0.014);Cox回归结果提示,不同EGFR表达分组的生存时间分布的差异具有统计学意义(P=0.014)。以上结果提示EGFR高表达组预后更差。见图2。

图2 EGFR高/低表达在胶质瘤患者预后生存中的KM曲线图
3 讨论
胶质瘤是临床中常见的原发性CNS恶性肿瘤,为了指导临床实际运用,临床上常用世界卫生组织(WHO)分类系统和 Kernoban 分类系统。上述分类系统在评估神经胶质瘤的恶性程度上具有优势,但是判断神经胶质瘤患者的预后上存在明显短板。因此引入分子病理学分级进而指导神经胶质瘤治疗具有很强的现实意义。本文基于前期临床实践和对肿瘤相关数据的挖掘,肯定了EGFR在胶质瘤中高表达,并且EGFR表达量对胶质瘤患者临床预后存在显著影响。
临床资料表中发现EGFR存在年龄和性别差异,EGFR在男性胶质瘤患者中表达增多,本次试验的结果和Quinn T Ostrom等人在NEURO-ONCOLOGY杂志上发表了关于在男性胶质瘤患者中高表达的结论一致[7],然而目前对男性患者EGFR的生物来源尚不清楚,最近一篇论文论述了关于男性Y染色中SOX2部位活化,刺激血管生成素样4蛋白 (ANGPTL4)表达,增加EGFR磷酸化水平,继而激活磷酸肌醇3-激酶(PI3K)/AKT和细胞外信号调节激酶(ERK)促进4E-BP1磷酸化进而级联诱导干细胞增殖的报道[3],综上虽然临床资料显示EGFR具有男性化倾向,但具体生物机制尚待研究。此外,在临床资料中我们还发现年龄对EGFR的表达存在影响,在资料中可见EGFR表达高峰主要集中在年龄≤60岁的人群中,而年龄>60岁无论EGFR表达高/低均较前者明显减少,这一结果可能和胶质瘤病情严重,患者普遍生存率低有关。另外一项关于胶质瘤的研究报告称,EGFR水平高低、OS与年龄分组(≥40岁,<40岁)存在相关性[8]。本文结果显示,低表达与高表达EGFR分组在组织学类型方面无统计学差异(P=0.127),本次临床基线资料中也发现EGFR表达高低和胶质瘤生存率相关。
表2结果表明EGFR在神经胶质瘤中明显表达,提示胶质瘤中的某种细胞抑或组织经由某种机制高表达EGFR。有学者系统阐述了胶质母细胞通过活化EGFRv Ⅲ达到EGFR级联放大的作用,并通过激活RAS/MAPK/ERK、PI3K/AKT、JAK/STAT、phospholipase C(PLC)/PKC等通路进一步刺激肿瘤生长,抵抗化疗药物进而达到肿瘤恶性增殖的目的[2]。同时,该结果和之前临床基线资料中胶质母细胞中EGFR高表达占比高的结果相一致。
在预测正常组和胶质瘤结局上,图1 EGFR的ROC曲线下面积为0.979,显示出良好的预测能力。目前关于EGRF对胶质瘤的生物学预测功能得到极大的关注和试验认证[9-11]。另外一项研究报道了T1加权动态对比增强MRI可作为EGFRv Ⅲ状态的无创生物标志物,用于胶质瘤的诊断[12]。图2展示了EGFR在预测胶质瘤预后的良好效果,结果显示:EGFR低表达组的中位生存时间为63.8(46.7~95.8)个月,EGFR高表达组的中位生存时间为41.7(32.5~51.2)个月。EGFR高表达明显缩短患者生存期,提示EGFR能作为胶质瘤的预后因素。
本研究也存在一定的局限性:(1)研究数据来自TCGA数据库,没有EGRF相关的临床或者动物研究验证;(2)对EGRF相关基因和通路机制未做进一步阐明和揭示。本研究利用生物信息技术对EGFR和胶质瘤相关性进行研究,展示了EGFR对胶质瘤患者具有良好的预测及预后预测功能,为将来EGFR相关制剂运用于临床,为胶质瘤患者的早诊断,预后评估提供理论线索。

