腹腔镜胃癌手术后发生肺部并发症的危险因素分析
方文姗
胃癌在我国所有恶性肿瘤中死亡率排名第3,发病率排名第2,对我国人民的健康产生了严重的威胁。胃癌的治疗方案中手术是主要治疗方式,腹腔镜手术因为其创伤较小、术后恢复较快等优势在临床应用广泛。在腹腔镜胃癌手术后常见肺部并发症,严重时甚至可导致患者死亡。本文采用本院收治的120 例实施腹腔镜手术的胃癌为研究样本,通过统计分析的方法对腹腔镜胃癌手术后患者发生肺部并发症的危险因素进行研究,为预防术后并发症提供参考,结果报告如下。
1 资料与方法
1.1 一般资料 研究对象来自于本院外科2017 年1 月~2021 年12 月实施腹腔镜胃癌手术的120 例患者,其中男84 例,女36 例;年龄29~89 岁,平均年龄65.4 岁。手术方式:全腹腔镜手术方式79 例,其中远端胃切除61 例,全胃切除18 例;腹腔镜辅助手术方式41 例,其中全胃切除11 例,远端胃切除30 例。根据患者术后是否发生肺部并发症分为A 组(发生并发症,25 例)及B 组(未发生并发症,95 例)。纳入患者均为仅采用腹腔镜胃癌手术的原发性胃癌患者,具有齐全的病理和临床资料,手术医生在腹腔镜手术方面具有丰富的经验。
1.2 诊断标准 术后肺部并发症指的是在腹腔镜胃癌手术后肺部发生的异常症状,因资料原因,本研究的术后肺部并发症指的是肺炎、急性呼吸窘迫综合征和胸腔积液,其诊断标准为:①腹腔镜胃癌手术后,肺部CT 或者胸片与手术前新增改变明显,出现肺部炎性浸润、积液等症状;②腹腔镜胃癌手术后,患者有咳痰、发热、呼吸困难等肺部症状。
1.3 方法 收集患者一般资料和临床病理资料,包括基本资料,身高、体重、体质量指数(BMI)、年龄、是否吸烟史、是否有肺部的基础疾病史;术前营养指标,包括术前血红蛋白、白蛋白水平;手术过程中的指标,包括采用全腔镜手术或腔镜辅助手术、全胃切除或远端胃切除、手术时间、建立二氧化氮(NO2)气腹时间、气管插管时间、术中出血量;手术后的相关指标,包括原发肿瘤情况、淋巴结转移情况、有无远端转移及是否发生术后腹部相关并发症、是否留置胃管。通过对上述指标进行对比分析,从而研究腹腔镜胃癌手术后发生肺部并发症的危险因素。
1.4 统计学方法 采用SPSS22.0 统计学软件进行统计分析。计量资料以均数±标准差()表示,采用t检验;计数资料以率(%)表示,采用χ2检验;等级计数资料采用秩和检验;通过Logistic 回归分析腹腔镜胃癌手术后发生肺部并发症的危险因素。P<0.05 表示差异具有统计学意义。
2 结果
2.1 两组患者单因素计量资料检验结果比较 两组年龄、身高、体重、BMI、术前血红蛋白、术前白蛋白、气腹时间、气腹时间比例比较,差异无统计学意义(P>0.05)。A 组手术时间、气管插管时间长于B 组,术中出血量多于B 组,差异具有统计学意义(P<0.05)。见表1。
表1 两组患者单因素计量资料检验结果比较()
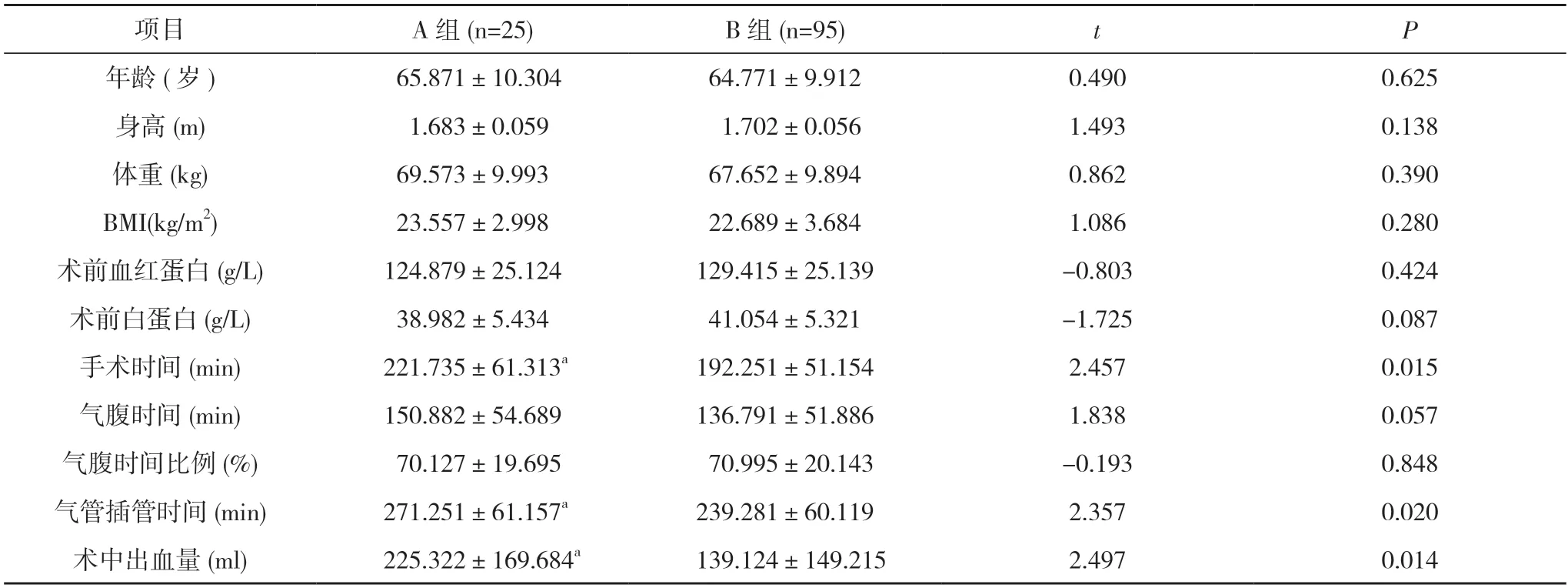
表1 两组患者单因素计量资料检验结果比较()
注:与B 组比较,aP<0.05
2.2 两组患者单因素计数资料检验结果比较 两组性别、吸烟史、手术方式及术后T 分期、N 分期、M 分期比较,差异无统计学意义(P>0.05);A 组肺部基础病史、全胃切除、术后留置胃管、术后发生腹部并发症占比分别为48.0%(12/25)、36.0%(9/25)、68.0%(17/25)、36.0%(9/25),均高于B 组的26.3%(25/95)、16.8%(16/95)、33.7%(35/95)、3.2%(3/95),差异具有统计学意义(P<0.05)。见表2。
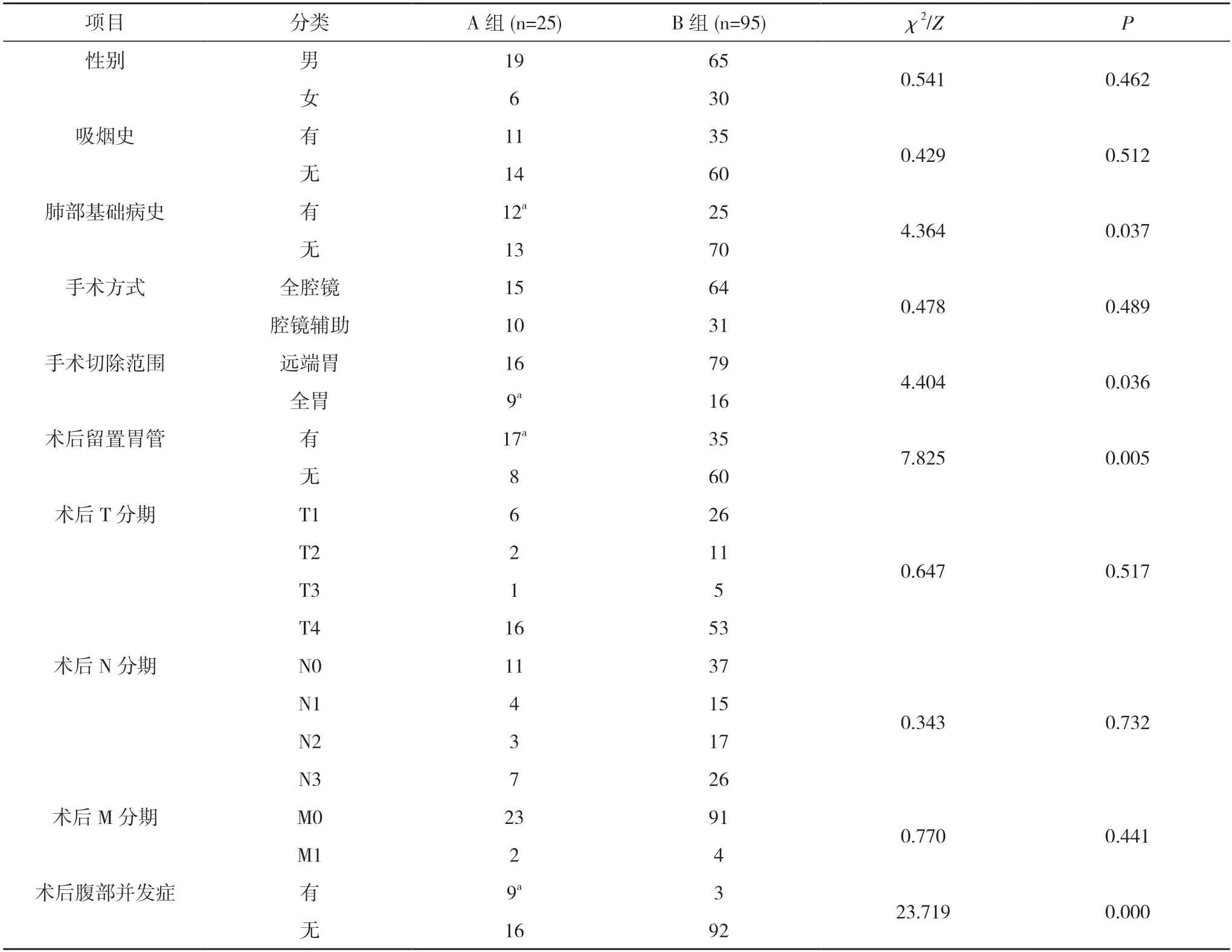
表2 两组患者单因素计数资料检验结果比较(n)
2.3 两组远端胃切除、全胃切除患者的手术方式比较 两组远端胃切除、全胃切除患者的手术方式比较,差异均无统计学意义(P>0.05)。见表3,表4。

表3 两组远端胃切除患者的手术方式比较[n(%)]

表4 两组全胃切除患者的手术方式比较[n(%)]
2.4 多因素Logistic 回归分析 Logistic 回归分析显示,术后发生腹部并发症、肺部基础病史、术后留置胃管为腹腔镜胃癌手术后发生肺部并发症的独立危险因素(P<0.05)。见表5。
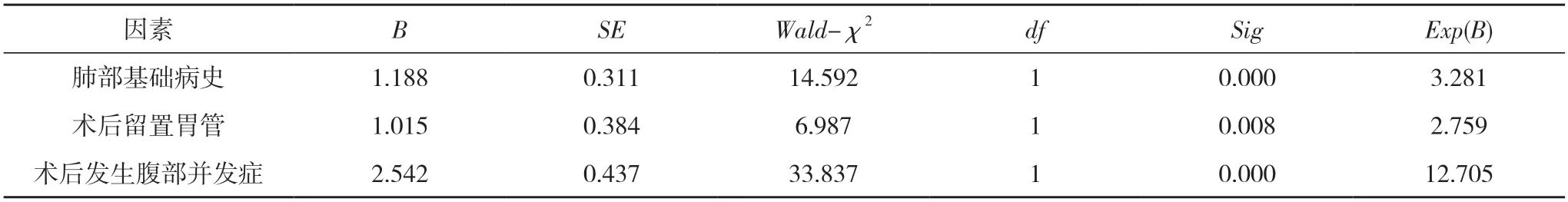
表5 多因素Logistic 回归分析
3 讨论
3.1 年龄 年龄与身体各器官机能关系密切,因此对于患者术后的恢复影响很大[1-3]。有学者研究了4000 多例外科手术患者的恢复情况,发现年龄≥60 岁的患者在手术后发生肺部并发症的几率为6.7%,要高于<60 岁患者的5.2%[4]。因为老年人的呼吸功能退化明显,相关的肺部机能,例如呼吸肌力、功能残气量、顺应性等都会随着年龄的增长而下降,增加了患者术后引发肺部并发症的风险[5]。但对本次选取的样本进行研究得出的结果显示,年龄对腹腔镜胃癌手术后肺部并发症的影响并不明显,与本次选用的样本年龄分布跨度大有关。
3.2 体重 体重是否标准与身高相关,因此单独研究体重因素意义不大,重点需要关注患者的BMI。BMI的计算比较简单,即体重(kg)与身高平方(m2)的比值,可以直接反映出一个人的肥胖程度,比值越大肥胖程度越高[6,7]。肥胖本身就会导致身体出现多种疾病,并且在患者术后恢复过程中会因为肥胖致使身体耗氧量增加,肺部功能受到影响,增加了术后肺部并发症的发生风险[8,9]。但是本次研究中,BMI 的分析结果无统计学差异。主要是因为数据分布原因,本次选择的样本平均BMI 为24 kg/m2左右,按照世界卫生组织(WHO)的肥胖分类,属于正常和超重范畴。另外,体重均为入院时测量数据,而不是手术前测量数据,在入院后因为饮食习惯的调整和心理状态的变化都会对体重有所影响,对本次研究结果也会产生影响。
3.3 吸烟史 本次研究受到样本收集的限制,未能搜集到患者比较详细的吸烟史,对于吸烟患者的烟龄、吸烟量、是否已经戒烟等数据均未掌握,只统计了是否有吸烟史,所以本次研究的数据分析结果无统计学差异。吸烟对肺部的影响很大,烟气中含有的有害物质,例如尼古丁和焦油对气道黏膜、气管上皮柱状纤毛影响很大,可促进气道分泌物增加,降低清除能力,甚至可以直接损伤肺实质,造成人体免疫力下降,引发肺内感染,这些都会增加腹腔镜胃癌手术后发生肺部并发症的风险[10]。有研究文献显示,如果患者吸烟指数>400,会大幅提高术后肺部并发症的发生几率[11]。吸烟指数为吸烟年数与每天吸烟支数的乘积,也就是和烟龄与吸烟量有关,而本次研究未能详细掌握患者的吸烟详细数据,致使研究结果出现差异。
3.4 肺部基础病史 如果患者有肺部基础病史,会对其肺部的基础功能造成一定的影响,例如肺部的顺应性、通气和弥散等功能会降低,而且手术中的一些操作还可能导致肺功能障碍加重,对术后恢复造成影响,使肺部并发症的发生几率增加[12]。本次研究中,有肺部基础病史的患者在手术前肺部基础病都已经痊愈,结果显示,A 组肺部基础病史占比高于B 组,差异有统计学意义(P<0.05),说明肺部基础病史与腹腔镜胃癌手术后发生肺部并发症有明显的正向相关性。同时对肺部基础病史做了Logistic 回归分析,结果表明肺部基础病史是腹腔镜胃癌手术后发生肺部并发症的独立危险因素(P<0.05)。分析其原因:①肺部基础病史会导致患者肺部机能降低,一般会有轻微缺氧和二氧化碳(CO2)蓄积症状,一般情况下机体会代偿性的增加通气量,但在手术时需要吸入麻醉类药物,这样会抑制患者的通气反应,容易引起低氧血症;②手术结束后一般不能立即拔管,需要复苏观察,这样也会导致肺部感染的几率增加,引起并发症。
3.5 手术方式及切除范围 随着医学技术的发展,在胃癌手术中采用腹腔镜手术方式患者的越来越多,虽然腹腔镜手术难度更高、操作时间更长,但在吻合、止血方面腹腔镜手术更具优势,而且对患者的创伤更小,更利于患者的康复[13]。在本次研究中,胃癌手术无论是采取全腔镜手术还是腔镜辅助手术,与肺部发生并发症并无统计学差异,也就是说采用腹腔镜手术与发生肺部并发症无直接关系。但是手术切除范围却与术后发生肺部并发症有密切关系,研究结果显示,A 组全胃切除占比高于B 组,差异具有统计学意义(P<0.05)。分析造成这种结果的原因:无论是全胃切除还是胃远端切除,手术时间均较长,出血较多,且两种切除范围都会比较靠近膈肌,对膈肌造成刺激,从而对患者的通气功能造成一定的影响,尤其是全胃切除手术后,空肠和食管的吻合口具有较大的张力,造成吻合困难,容易发生瘘,甚至会破入胸腔造成全身的炎症反应[14,15]。
3.6 术前营养情况 胃癌患者在饮食和吸收方面存在一定的功能障碍,大多数都会造成营养不良,对术后恢复造成一定的影响。主要的营养指标包括白蛋白和血红蛋白。白蛋白的功能非常广,最主要的作用是维持血浆胶体渗透压,如果患者术前血液中白蛋白含量低,会导致组织液渗出于胸腔内,对肺组织造成压迫,影响呼吸功能。而血红蛋白不足会影响血液氧和CO2的运输功能,造成低氧血症,增加肺部并发症的发生几率。本研究结果显示,两组术前血红蛋白、术前白蛋白、气腹时间、气腹时间比例比较,差异无统计学意义(P>0.05)。说明术前营养情况对术后肺部并发症无影响。主要是因为手术后对患者采取营养支持治疗对其所需营养进行了及时的补充,因此对本次研究结果未造成影响。
3.7 术中危险因素 腹腔镜胃癌手术中有3 个危险因素,分别为术中出血量、手术时间和气管插管时间。本次研究结果中,A 组手术时间、气管插管时间长于B 组,术中出血量多于B 组,差异具有统计学意义(P<0.05)。从手术时间角度分析,腹腔镜胃癌手术,无论是远端胃切除,还是全胃切除,都是靠近膈肌进行的,长时间的手术会加强对膈肌的刺激和伤害,所以发生肺部并发症的几率就会增高。另外长时间的手术会增加单肺通气时间,从而产生会对身体造成伤害的氧自由基。气管插管时间越长,肺部受到感染的几率就会增加,从而提高术后肺部并发症的发生几率[16,17]。术中出血量增加会导致组织缺氧,一旦有效的血液循环减少就要及时进行输血,而输血治疗也会导致患者的免疫力下降,提高术后肺部发生并发症的几率[18-22]。
3.8 术后留置胃管 本次研究结果显示,A 组术后留置胃管占比高于B 组,差异具有统计学意义(P<0.05),说明术后留置胃管与腹腔镜胃癌手术后发生肺部并发症具有非常密切的关系。而且Logistic 回归分析显示,术后留置胃管为腹腔镜胃癌手术后发生肺部并发症的独立危险因素(P<0.05)。腹腔镜胃癌手术后留置胃管对患者的恢复确实会造成很多不利影响,例如吞咽时胃管与咽喉会不断摩擦,对患者的黏膜、气道都会造成一定影响,同时还容易导致患者恶心呕吐,从而引起误吸;另外,胃管壁会粘附痰液,容易滋生细菌从而导致肺部感染[23-25]。
3.9 术后发生腹部并发症 本次研究结果显示,A 组术后发生腹部并发症占比高于B 组,差异具有统计学意义(P<0.05)。说明术后发生腹部并发症与腹腔镜胃癌手术后发生肺部并发症具有非常密切的关系。Logistic 回归分析显示,术后发生腹部并发症为腹腔镜胃癌手术后发生肺部并发症的独立危险因素(P<0.05)。腹腔镜胃癌手术后一旦发生腹部并发症,会大大提高其腹腔感染的几率,从而引起瘘、出血等症状,对膈肌造成一定的刺激,引起肺部感染;而且一旦患者发生腹部并发症,会增加身体消耗,导致低蛋白血症或贫血现象,间接增加了肺部发生并发症的几率[26,27]。
综上所述,手术时间、气管插管时间、术中出血量、胃部切除范围、肺部基础病史及术后留置胃管和发生腹部并发症这7 个危险因素会明显提高腹腔镜胃癌手术后肺部并发症的发生几率,其中肺部基础病史、术后留置胃管和发生腹部并发症为腹腔镜胃癌手术后发生肺部并发症的独立危险因素,全腔镜手术与腔镜辅助方式手术对手术范围无明显影响。但由于受到搜集数据的限制,指标的选取和数据的深度挖掘不足,导致研究结果可能出现一定偏差,需要今后在工作中进一步研究。

