高稳定性壳聚糖凝胶堵剂的制备与成胶性能评价*
杨 洋,贺小萱,时 娟,张 浩
(1.成都理工大学能源学院,四川成都 610059;2.陕西省油气田特种增产技术重点实验室(西安石油大学),陕西西安 710065;3.新疆油田公司实验检测研究院,新疆克拉玛依 830023)
0 前言
聚丙烯酰胺类凝胶堵剂在油田调剖堵水[1]、井筒堵漏[2-3]、修井暂堵[4]等领域应用广泛。然而,由于聚丙烯酰胺类聚合物在高温条件下易发生水解、无规断裂等热降解作用,加之无机盐电荷屏蔽、双电层压缩等作用影响,聚丙烯酰胺类凝胶堵剂的抗温抗盐性能不足[5-6]。此外,聚丙烯酰胺类聚合物自身的柔性链结构使其分子链在强剪切作用下易发生断裂,在经过地面设备、管线、炮眼、地层的剪切后成胶强度显著降低,抗剪切性能不足[7]。上述问题造成聚丙烯酰胺类聚合物在高温、高盐、强剪切条件下难以形成高强度凝胶并维持稳定,限制了凝胶堵剂的油藏适应范围。
目前,将丙烯酰胺类聚合物进行功能化改性以及多组分复配是提高其凝胶强度及稳定性的主要方法。通过引入含有大空间位阻功能基团的单体,聚合物链的刚性可得到有效提升,聚合物凝胶的抗温、抗盐、抗剪切性能显著提高[8-9]。此外,黏土矿物、无机纳米颗粒等材料与丙烯酰胺类聚合物复配后,可通过物理填充、物理交联等作用提高聚合物凝胶强度及稳定性[10-11]。但是,上述技术措施并未从本质上改变丙烯酰胺类聚合物柔性链的结构特征,聚合物的抗温、抗盐、抗剪切性能仍不能完全满足现场施工需求。
壳聚糖是一种生物多糖聚合物,由β-(1,4)-2-氨基-2-脱氧-d-吡喃葡萄糖和2-乙酰氨基-2-脱氧-d-吡喃葡萄糖单元组成,其分子链刚性较强,抗温、抗盐、抗剪切性能好于丙烯酰胺类聚合物[12]。此外,相比传统无机交联的纤维素、胍胶、黄原胶等多糖聚合物凝胶体系,壳聚糖分子链上大量的胺基为实现有机交联提供了可能。有机交联形成的共价键相比无机交联形成的离子键更加稳定,有助于提高凝胶的稳定性。因此,本研究旨在研制一种抗温、抗盐、抗剪切的壳聚糖凝胶堵剂,并探明其成胶机理与成胶行为。
1 实验部分
1.1 材料与仪器
氯化钠(NaCl)、N,N'-亚甲基双丙烯酰胺(MBA)、壳聚糖(CTS,脱乙酰度为95%)、醋酸、氢氧化钠,分析纯,上海阿拉丁生化科技有限公司;部分水解聚丙烯酰胺(HPAM),相对分子质量2×107,水解度20%~22%,江苏富淼科技股份有限公司。
FE28数字pH计,瑞士梅特勒托利多公司;西林瓶,广州康明玻璃制品有限公司;MARS III流变仪,德国哈克公司;VERTEX 70v 傅立叶红外光谱仪(FTIR),德国布鲁克公司;Quanta扫描电镜(SEM),美国FEI 公司;STA6000 热重分析仪(TG-DTG),美国珀金埃尔默仪器有限公司;SX-0708吴茵搅拌器,青岛森欣机电设备有限公司。
1.2 实验方法
(1)凝胶基液的制备
将一定质量的CTS 粉末缓慢加入2.0%的醋酸水溶液中,同时保持溶液机械搅拌(300 r/min);待CTS完全溶解后,向溶液中加入MBA粉末,完全溶解后得到凝胶基液。采用1 mol/L 的醋酸和氢氧化钠溶液调控凝胶基液的pH值。所有凝胶基液均在室温下制备。
(2)成胶时间和成胶强度的测定
将西林瓶作为容器封装凝胶基液后放入一定温度的烘箱进行成胶实验,采用Sydansk 等[13]提出的目测代码法评价凝胶的成胶时间。凝胶目测代码如表1 所示,将凝胶基液从初始状态转变为强度C级的时间记录为成胶时间。
由于本文研究的凝胶体系成胶后目测的代码强度均为I级,为进一步量化凝胶强度,采用流变仪的平板测试模块测量凝胶的弹性模量。在1 Hz 的频率条件下进行应变扫描,确定线性黏弹区间,随后保持应变1.0%及1.0 Hz 的频率进行黏弹性测试。整个测试过程为300 s,测试过程中弹性模量值几乎恒定,取该稳定弹性模量值量化凝胶体系的成胶强度。
(3)成胶机理分析
采用FTIR、SEM、TG-DTG 分析CTS 凝胶体系的成胶机理。采用衰减全反射法(ATR 法)对冻干样品粉末进行FTIR 测试。红外光谱波数范围400~4000 cm-1,分辨率4 cm-1。将样品置于液氮环境下冷冻及真空干燥,对冻干样品进行脆断和喷金处理,采用扫描电镜观察其微观结构。在氮气气氛下,温度从30 ℃加热至630 ℃,升温速率为10 ℃/min,用热重分析仪自动记录冻干粉末样品的热重损失数据。
2 结果与讨论
2.1 CTS-MBA凝胶成胶机理
CTS-MBA凝胶体系(2.0%CTS、0.6%MBA)成胶前后的微观形貌如图1 所示。CTS-MBA 凝胶体系成胶前呈不规则的网状结构,成胶后呈现出明显的三维立体蜂巢结构,说明CTS 与MBA 之间发生了交联反应,改变了凝胶体系的微观形貌。
从红外光谱图(图2)可见,CTS-MBA凝胶体系的红外特征峰与CTS、MBA的红外特征峰基本叠加吻合。值得注意的是,在1675 cm-1及1621 cm-1处,CTS的红外光谱中未观察到明显的特征峰,而MBA及CTS-MBA的红外光谱中均可观察到明显的特征峰。其中,在MBA的红外光谱中,1621 cm-1处的透过率相对高于1675 cm-1处;而在CTS-MBA 的红外光谱中,两处特征峰的透过率相对大小发生变化,1675 cm-1处的透过率高于1621 cm-1处。考虑到1675 cm-1处特征峰来源于C=O 的伸缩振动,而1621 cm-1处特征峰来源于C=C的伸缩振动,可推测C=C键数量在交联反应后减少。
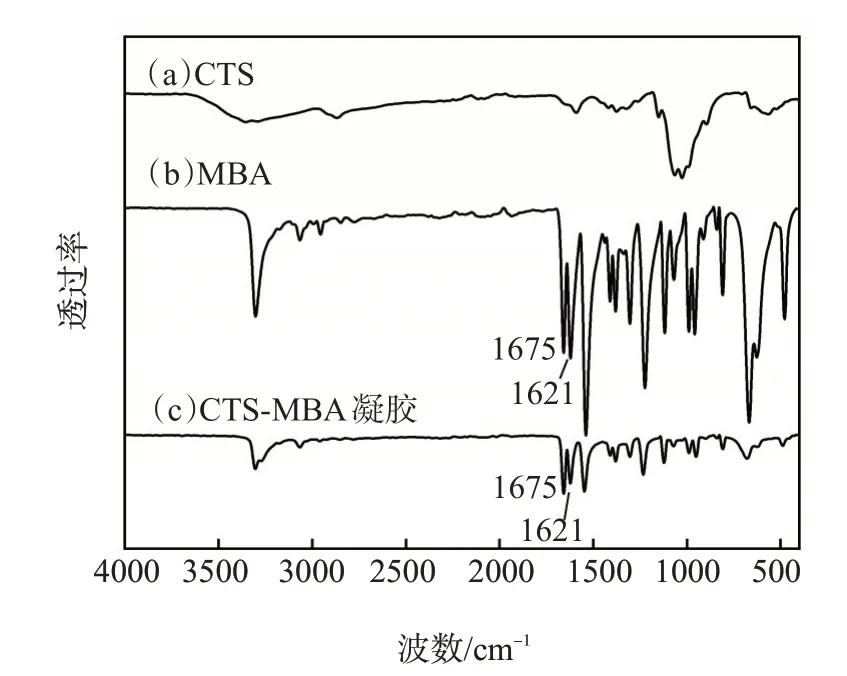
图2 CTS-MBA凝胶与反应物的红外光谱图
由CTS 与CTS-MBA 凝胶的TG-DTG 曲线(图3)可以看出,CTS的失重主要分为两个阶段。在温度从30 ℃升高到100 ℃的过程中发生约12%的质量损失,可能源于结晶水的挥发;随后在100~250 ℃的升温过程中无明显质量损失;当温度高于250 ℃,质量损失持续增加直至630 ℃,其中在302.8℃的失重速率最大。CTS-MBA凝胶的失重同样分为两个阶段。200 ℃以下的失重可能与结晶水及醋酸的挥发有关;温度高于200 ℃后的失重可能与分子结构的热分解有关,其中在272.8 ℃的失重速率最大。由此可见,相对于CTS,CTS-MBA 的热稳定性有所降低,主要原因可能与MBA 分子结构稳定性相较含有大量环状刚性结构的CTS 略差有关。凝胶中的MBA 结构单元降低了分解温度,但同时也证明CTS 与MBA 发生了交联反应,进而改变了分子网络的热性质。根据以上分析,推测凝胶的成胶机理如图4 所示。CTS 的—NH2基团与MBA 的α,β-不饱和羰基发生迈克加成反应,MBA以共价键交联CTS 分子链,最终形成凝胶三维网络结构。
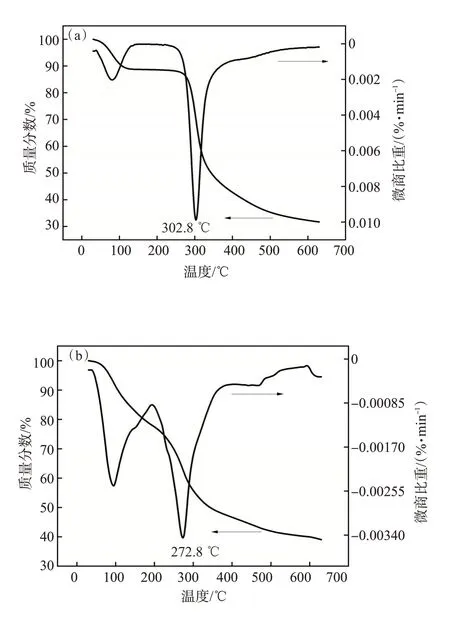
图3 CTS(a)与CTS-MBA凝胶(b)的TG-DTG曲线

图4 CTS-MBA凝胶体系交联反应方程式
2.2 CTS凝胶体系制备条件优化
2.2.1 CTS加量对凝胶体系成胶性能的影响
采用30 g/L 氯化钠盐水配制CTS 凝胶基液,交联剂MBA 的质量分数保持0.6%不变,pH 值为4.2,评价不同CTS加量下凝胶体系的成胶性能,成胶实验均在120 ℃条件下进行,结果如图5 所示。凝胶体系强度随CTS加量的增大而逐渐升高,这一变化规律与聚丙烯酰胺类聚合物凝胶的成胶特性类似。随着CTS加量的增大,溶液中CTS分子数量增加,为交联反应提供了更多的交联位点,进而形成了更大的交联密度及凝胶强度。此外,CTS加量越大,成胶时间越短,这是由于更多的交联位点加快了CTS与MBA的交联反应速度。当CTS质量分数从1.5%增至2.0%时,凝胶强度的增幅较大;当CTS加量从2.0%增至3.5%时,凝胶强度增幅较低。因此,考虑到经济成本,CTS 的加量2.0%可作为优化值进行后续研究。

图5 CTS加量对凝胶成胶性能的影响
2.2.2 交联剂加量对凝胶体系成胶性能的影响
采用30 g/L 氯化钠盐水配制CTS 凝胶基液,在CTS加量为2.0%、pH值为4.2、成胶温度为120 ℃的条件下,交联剂MBA 加量对凝胶体系成胶性能的影响如图6所示。随着MBA加量的增大,凝胶强度增加。当MBA 加量(0.2%)较低时,凝胶强度仅为84 Pa;当MBA 加量(0.6%)较高时,凝胶强度为166 Pa。MBA 加量从0.6%增至1.0%时,凝胶强度仅从166 Pa增至170 Pa。因此,选取0.6%为MBA的优化加量进行后续研究。此外,MBA加量越大,MBA与CTS上—NH2基团反应的几率越大,成胶时间越短。

图6 MBA加量对凝胶成胶性能的影响
2.2.3 pH值对凝胶体系成胶性能的影响
CTS 需要在酸性条件下才能发生溶解,酸加量的变化会直接造成溶液pH 值的变化,因此需要明确pH 值对凝胶体系成胶性能的影响。采用30 g/L氯化钠盐水配制CTS 凝胶基液,在CTS 加量为2.0%、MBA加量为0.6%、成胶温度为120 ℃的条件下,pH 值对凝胶体系成胶性能的影响如图7 所示。由图7 可见,pH 值为3.2 时无法成胶,随着pH 值从3.9 增至5.6,凝胶强度由78 Pa 逐渐增至176 Pa,成胶时间从20 h缩短至4 h。pH值对CTS凝胶体系的成胶行为产生了较大影响,这与其他生物聚合物凝胶体系类似。Kolnes等[14]发现黄原胶/Cr3+凝胶体系的成胶时间随着pH 值的降低而延迟,六水离子Cr(H2O)63+随着pH 值的增加转化为高活性氢氧化物Cr(OH)(H2O)52+和Cr(OH)2(H2O)4+,在较高的pH值下成胶时间缩短。然而,上述pH 对凝胶成胶性能影响的解释不适用于CTS 凝胶体系。对实验现象的一种可能解释为:随着醋酸浓度的增加,CTS的质子化程度越来越高,意味着随着pH值的降低,越来越多的—NH2基团转化为NH3+,MBA的反应位点减少。因此,在较低的pH值下,交联反应速度变慢且凝胶强度变低。pH值低于4.2时凝胶强度急剧降低。综合不同pH值下凝胶体系的成胶行为,CTS凝胶体系的pH值适用范围为4.2~5.6。

图7 pH值对凝胶成胶性能的影响
2.2.4 矿化度对凝胶体系成胶性能的影响
在CTS 加量为2.0%、MBA 加量为0.6%、pH 值为4.2、成胶温度为120 ℃的条件下,矿化度对凝胶体系成胶性能的影响如图8所示。随着矿化度的增加,凝胶体系的成胶时间逐渐缩短。当矿化度从3 g/L 增至50 g/L 时,成胶时间由19 h 缩短到6 h。此外,随着矿化度的增加,凝胶强度由76 Pa 增至172 Pa。矿化度对凝胶体系成胶性能的影响可能与电荷屏蔽作用有关。不同矿化度的盐水由氯化钠和去离子水配制而成,盐水中含有大量Cl-。Cl-与NH3+之间发生电荷屏蔽效应,CTS分子线团收缩,增加了MBA 分子与CTS 上α,β-不饱和羰基反应的机会,交联反应速率及交联密度提升,从而缩短了成胶时间。
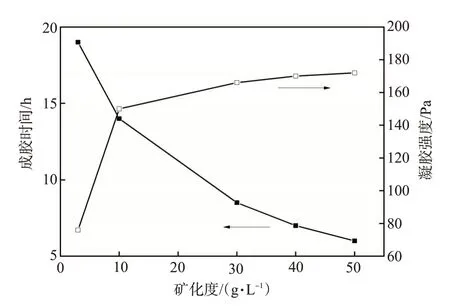
图8 矿化度对凝胶成胶性能的影响
2.2.5 温度对凝胶体系成胶性能的影响
在CTS 加量为2.0%、MBA 加量为0.6%的条件下,温度对凝胶体系成胶性能的影响如图9 所示。在不同的矿化度及pH 值条件下,凝胶强度随着温度的升高均有所增加,说明高温促进了交联反应的进行。为了进一步分析温度对凝胶体系成胶时间的影响,采用阿伦尼乌斯模型对数据进行拟合(图10)。阿伦尼乌斯模型如下:

图9 在不同矿化度和pH条件下温度对凝胶强度的影响

图10 在不同矿化度和pH条件下温度对凝胶成胶时间的影响
其中,tG—凝胶时间,h;M—时间常数,h;Ea—活化能,kJ/mol;R—通用气体常数,kJ/(mol·K);T—溶质温度,K。
通过实验数据拟合,得到模型(2)、(3)、(4):
根据拟合模型对比分析可知,当矿化度为30 g/L、pH 值为4.2 时,CTS 与MBA 的交联反应活化能为79.9 kJ/mol。当pH值从4.2增至5.2时,活化能降至73.1 kJ/mol,这意味着在较高的pH 条件下,CTS 和MBA 更容易发生交联反应,这与2.2.3 节的结果一致。同样,当矿化度从30 g/L增至50 g/L时,活化能从79.9 kJ/mol 降至78.3 kJ/mol,这也与2.2.4 节中无机盐可以促进凝胶成胶的结果一致。
2.3 剪切作用对凝胶体系成胶性能的影响
采用吴茵搅拌器对凝胶基液进行高速(6000 r/min)剪切,剪切不同时间后测量基液的黏度,根据黏度损失百分比量化凝胶基液的剪切降解率D,计算方法如式(5)所示。
其中,μ0—凝胶基液的初始黏度;μ—剪切后凝胶基液的黏度。
由图11可见,1%CTS与1%HPAM的剪切降解率随剪切时间的增加而增加。剪切30 min 后,HPAM 的降解率达到88.6%,而CTS 的仅为9.68%。相比HPAM的柔性链结构,CTS的刚性链结构赋予了凝胶体系较强的抗剪切性能。在矿化度为30 g/L、pH=4.2、CTS 加量为2.0%、MBA 加量为0.6%时,将高速剪切不同时间后的基液(具有不同的剪切降解率)放入烘箱,CTS-MBA凝胶体系的成胶性能如图12 所示。当剪切降解率由0 增至9.68%时,成胶时间略有增加,凝胶强度从166 Pa降至162 Pa,强度下降率仅为2.4%,整体变化不显著。CTS-MBA 体系良好的抗剪切性有助于准确控制和预测凝胶体系注入井筒或地层后的成胶时间。

图11 CTS与HPAM的剪切降解率随剪切时间的变化

图12 剪切降解对凝胶性能的影响
2.4 长期稳定性
2.0% CTS 和0.6% MBA 组成的凝胶体系具有良好的热稳定性,可以在120 ℃、矿化度为30 g/L、pH=4.2 的高温高盐条件下保持I 级强度90 d,且无脱水现象。Al-Muntasheri 等[15]的研究表明,聚丙烯酰胺-聚乙烯亚胺(PAM-PEI)凝胶体系在PAM含量不低于7.0%时才能在120 ℃下稳定2 周以上,相比之下CTS-MBA 凝胶体系中CTS 的用量较低,有助于降低药剂成本。
3 结论
CTS 与MBA 可通过迈克加成反应形成共价键交联,随着CTS或MBA浓度的增大,凝胶体系成胶强度增加,成胶时间减少。矿化度或pH 值的增加会降低CTS-MBA 体系交联反应的活化能,成胶时间缩短,凝胶强度增加。凝胶的抗剪切性较好,凝胶基液在6000 r/min下剪切30 min后的成胶强度下降率仅为2.4%。凝胶具有良好的热稳定性,2.0%CTS和0.6%MBA组成的凝胶体系的性能在120 ℃老化90 d后依然保持稳定。

