桂枝甘草汤传统汤剂与配方颗粒成分比较*
施钧瀚,姚静,王艳丽,张耀,曹英杰,,4,桂新景,王青晓,岳佑凇,路露,张璐,李学林,刘瑞新
(1.河南中医药大学第一附属医院药学部,郑州 450000;2.河南中医药大学药学院制剂教研室,郑州 450008;3.河南中医药大学呼吸疾病中医药防治省部共建协同创新中心,郑州 450046;4.河南省中药临床药学中医药重点实验室,郑州 450000;5.河南省中药临床应用、评价与转化工程研究中心,河南省中药安全评价与风险防控工程研究中心,郑州 450000;6.河南省药品医疗器械检验院,郑州 450000)
中药配方颗粒(dispensing granule of Chinese medicine,DGCM)改进了传统汤剂(traditional decoction,TD)绝大多数弊端,是对传统汤剂的一次突破[1-2]。但其试点20多年以来一直发展缓慢,究其原因就是DGCM与传统汤剂的等效性问题[2-3]。近年来,研究人员对二者进行了对比研究[4-7],但这些研究并不能解除人们对配方颗粒疗效的担忧[8-9]。此外,对于DGCM的研究主要集中在实验室条件下的成分对比[10-12],研究者采用同批次饮片自制配方颗粒与其所制传统汤剂进行比较,或选用由配方颗粒厂家提供的配方颗粒及同来源饮片(同批次),这种方法虽然可以比较制备工艺不同所致差异,但不能完全重现患者在医院就诊后,依据医师处方所得的传统汤剂和配方颗粒的一致性,在饮片质量等级和制备工艺的双重影响下,传统汤剂与配方颗粒在真实世界存在很大差异。本实验在真实世界条件下采集制备传统汤剂与DGCM样品,对比研究其化学成分是否相同。
桂枝甘草汤(Guizhi Gancao decoction,GGD)出自《伤寒论》[11],处方组成为:桂枝(去皮)四两(12 g),甘草(炙)二两(6 g)。该方为温阳益气、治疗心悸基本方,临床常作为药对使用,又因为该处方药味较少,便于研究,同时兼顾研究单煎合煎是否相同,并且处方化学成分具有代表性,甘草中指标性成分甘草苷和甘草酸铵为水溶性成分,桂枝中指标性成分桂皮醛具有挥发性,另外还含有活性成分肉桂酸,因此笔者在本实验以GGD为研究对象,通过高效液相色谱(HPLC)特征图谱方法,比较传统汤剂与DGCM化学成分差异,以期为传统汤剂改革及配方颗粒合理应用提供参考。
1 仪器与试药
1.1仪器 Waterse 2695高效液相色谱仪、EmPower色谱工作站(美国沃特世公司);CP225 D电子分析天平(德国Sartorius)。
1.2试药 乙腈、甲醇、磷酸为色谱纯(西格玛公司);超纯水(采用MilliPoreQ,18.2 MQ·cm制备);其他试剂均为分析纯。
桂枝(产地:广西,批号:1801181,180401,180721)、炙甘草(产地:内蒙古,批号:180309,180804,190314)饮片购买于多家中医院(河南中医药大学第一附属医院、河南中医药大学第三附属医院、郑州市中医院),经河南中医药大学第一附属医院陈天朝主任药师鉴定,桂枝基原为樟科植物肉桂CinnamomumcassiaPresl.;甘草基原为豆科植物光果甘草GlycyrrhizaglabraL.。9批桂枝配方颗粒(A厂3批,每克颗粒相当于饮片12 g,批号:1601628,1607633,1605608;B厂3批,每克颗粒相当于饮片12 g,批号:1609001,1612024,1602031;C厂3批,每克颗粒相当于饮片21 g,批号:16030081,16032685,16030402),9批炙甘草配方颗粒(A厂3批,每克颗粒相当于饮片3 g,批号:1601622,1605616,1608636;B厂3批,每克颗粒相当于饮片3 g,批号:16080116,161003w,1511001s;C厂3批,每克颗粒相当于饮片7 g,批号:16010013,16101025,16120502);甘草苷对照品(批号:111610-201607)、肉桂酸对照品(批号:110786-201604)、桂皮醛对照品(批号:110710-201821)、甘草酸铵对照品(批号:110731-201720)均购自中国食品药品检定研究院。
2 方法与结果
2.1色谱条件 色谱柱:Agilent Zorbax SB-Aq(250 mm×4.6 mm,5 μm);流动相为乙腈-0.1 mol·L-1磷酸溶液,梯度洗脱程序见表1[12];流量1.0 mL·min-1;检测波长254 nm;柱温25 ℃;进样量10 μL。
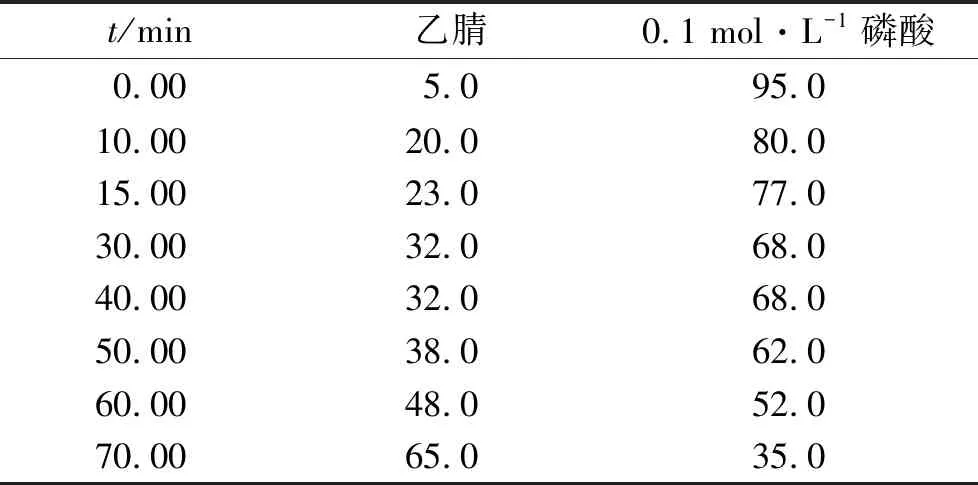
表1 梯度洗脱程序
2.2样品的制备
2.2.1传统汤剂样品 取桂枝12 g、炙甘草6 g,加10倍量水(180 mL)浸泡30 min,加热至沸腾,并保持微沸状态20 min,趁热滤过,放冷,药渣加8倍量水(144 mL),再煎煮20 min,趁热滤过,放冷,合并2次滤液[13],置250 mL量瓶,加水至刻度,备用(取不同批次饮片同法制备3份样品)。
2.2.2A、B、C厂DGCM 样品 取相当于桂枝饮片12 g、炙甘草饮片6 g的配方颗粒(按照厂家标示浓缩比折算),置250 mL量瓶,加热水使溶解,放冷,加水定容至刻度,混匀,即得。取A、B、C厂配方颗粒各3批,分别同法制备样品。
2.3供试品溶液的制备 取“2.2”项下传统汤剂及A、B、C厂DGCM 各25 mL,分别置50 mL量瓶,加甲醇至刻度,摇匀,静置,取上清液过孔径0.45 μm微孔滤膜,即得。传统汤剂 3批与3个厂家各3批配方颗粒分别标记为传统汤剂1、传统汤剂2、传统汤剂3、A1、A2、A3、B1、B2、B3、C1、C2、C3。
2.4对照品溶液的制备 分别精密称取甘草苷、甘草酸铵、桂皮醛、肉桂酸对照品,加甲醇溶解,分别制成甘草苷1.126 4 mg·mL-1、甘草酸铵1.216 8 mg·mL-1、桂皮醛1.306 4 mg·mL-1、肉桂酸1.224 0 mg·mL-1储备液,再分别精密量取储备液0.5 mL,置10 mL量瓶,加甲醇至刻度,制成甘草苷56.32 μg·mL-1、甘草酸铵60.84 μg·mL-1、桂皮醛65.32 μg·mL-1、肉桂酸61.2 μg·mL-1的混合对照品溶液。
2.5 阴性供试品溶液的制备
2.5.1缺桂枝阴性(即甘草饮片)供试品溶液 原方去桂枝,按传统汤剂样品溶液制备方法制备缺桂枝阴性样品溶液,并按“2.3”项方法制备缺桂枝阴性供试品溶液。
2.5.2缺甘草阴性(即桂枝饮片)供试品溶液 原方去甘草,按传统汤剂样品溶液的制备方法制备缺甘草阴性样品溶液,并按“2.3”项方法制备缺甘草阴性供试品溶液。
2.6方法学验证
2.6.1专属性考察 分别取“2.2”项混合对照品溶液、供试品溶液、阴性样品溶液,按“2.1”项色谱条件,分别进样并记录色谱图。样品中甘草苷、甘草酸铵、桂皮醛、肉桂酸的色谱峰与对照品一致且无干扰,该方法专属性良好。
2.6.2重复性实验 精密吸取传统汤剂1供试品溶液,按“2.1”项色谱条件连续进样6次测定,记录色谱图。结果各主要共有特征峰的相对保留时间无明显变化,RSD在0.1%~0.2%;相对峰面积RSD集中在0.5%~2.8%;甘草苷、甘草酸铵、桂皮醛、肉桂酸峰面积的RSD分别为2.2%,0.5%,2.5%,1.0%,保留时间的RSD分别为0.1%,0.1%,0.2%,0.1%,结果表明仪器精密度良好。
2.6.3稳定性实验 精密吸取传统汤剂1供试品溶液,分别于0,2,4,8,12,16,24 h按“2.1”项色谱条件进样分析,结果各主要共有特征峰的相对保留时间无明显变化,RSD在0.1%~0.6%;相对峰面积RSD集中在0.5%~4.6%;甘草苷、甘草酸铵、桂皮醛、肉桂酸峰面积的RSD分别为2.9%,0.5%,3.1%,1.1%,保留时间的RSD分别为0.1%,0.1%,0.2%,0.1%,结果表明供试品溶液24 h内稳定。
2.6.4线性关系考察 取甘草苷、甘草酸铵、桂皮醛、肉桂酸对照品溶液,分别配制成0.554 4,0.600 8,0.655 6,0.612 4 mg·mL-1溶液,精密量取以上溶液0.1,0.2,0.5,1,1.5,2 mL,分别置10 mL量瓶,加甲醇定容,摇匀,即得不同浓度对照品溶液,按“2.1”项色谱条件进样10 μL,以峰面积积分值为纵坐标(Y)、进样量为横坐标(X),进行线性回归,绘制标准曲线,计算 4个成分的线性回归方程及线性范围,结果见表2。
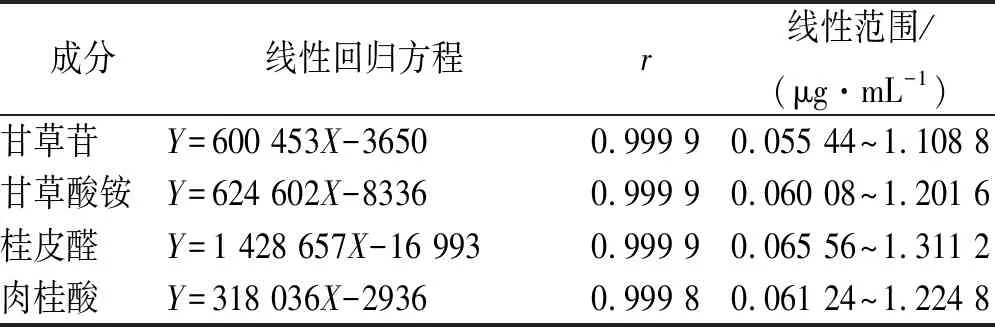
表2 各成分线性回归方程及线性范围
2.6.5加样回收率实验 精密量取已知各指标成分含量的同一批传统汤剂样品6份,每份12.5 mL。分别精密加入1.126 4 mg·mL-1甘草苷溶液0.5 mL、1.216 8 mg·mL-1甘草酸铵溶液2.5 mL、1.306 4 mg·mL-1桂皮醛溶液2.5 mL、1.224 0 mg·mL-1肉桂酸溶液2 mL,加甲醇至25 mL,按照“2.3”项方法制备供试品溶液,按“2.1”项色谱条件进样测定,计算回收率,结果甘草苷、甘草酸铵、桂皮醛、肉桂酸平均加样回收率分别为100.9%,100.1%,99.3%,100.1%;RSD分别为1.9%,1.5%,1.5%,0.8%,见表3。
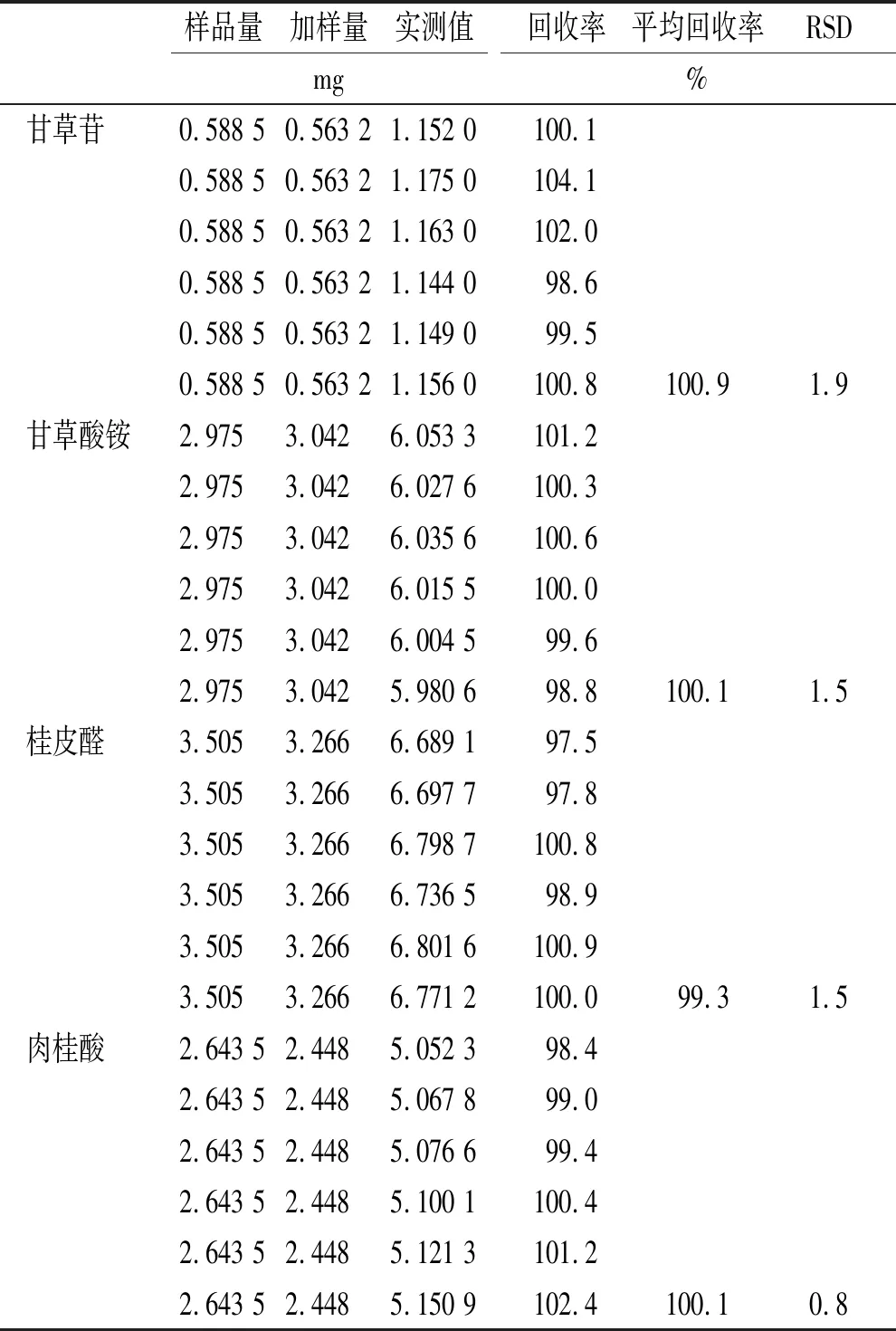
表3 桂枝甘草汤加样回收率实验结果
2.7特征图谱的建立及图谱采集
2.7.1特征图谱的建立 分别取桂枝、甘草饮片3批,按照“2.2.1”项下方法制成汤剂,按“2.3”项下方法制备供试品溶液,在“2.1”项下色谱条件进行测定,参照文献[12]建立GGD特征图谱,确定肉桂酸为参比峰,并确定25个共有峰作为标准汤剂共有峰。
2.7.2传统汤剂与DGCM特征图谱的采集 分别精密吸取“2.3”项各供试品溶液10 μL,注入液相色谱仪,按照“2.1”项所建立的色谱条件进样测定,记录GGD 传统汤剂和3个厂家DGCM的HPLC特征图谱。结果见图1。
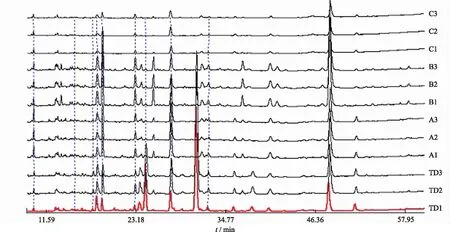
图1 桂枝甘草汤不同样品匹配色谱图(254 nm)
2.7.3主要色谱峰的鉴定与归属 分别精密吸取“2.3”“ 2.4”“ 2.5”项对照品溶液、传统汤剂供试品溶液和阴性供试品溶液10 μL,注入液相色谱仪,按照“2.1”项所建立的色谱条件进样测定,记录HPLC图谱。结果见图2。
由对照品及阴性供试品对比可知,1,3,4,5,6,7,11,12,17,18号峰为桂枝中成分;2,8,10,13,14,19,20,22,23,24,25号峰为炙甘草中成分;9,15,16,21号峰桂枝甘草中均有。通过峰面积大小对比,9,16,21号峰以桂枝中为主,峰面积约为炙甘草中的10倍,15号峰峰面积两者相差不大,应为两者共有峰。另外,10号峰为甘草苷,17号峰为肉桂酸,18号峰为桂皮醛,24号峰为甘草酸铵。
2.8特征图谱比较
2.8.1传统汤剂、DGCM特征图谱相关性 采用《中药色谱指纹图谱相似度评价系统2004A版》评价桂枝甘草汤传统汤剂、3个厂家DGCM的特征图谱相关参数,设定参照图谱,将色谱峰自动匹配,生成对照图谱(R,平均值法),并进行谱峰差异性评价和整体相似性评价。相似度评价结果表明,传统汤剂与DGCM相似度较低(相似度<0.4),A、B、C厂家DGCM之间相似度较高(相似度>0.8)。见表4。
2.8.2化学成分种类和数目比较 通过比较特征图谱峰数,传统汤剂中12,21号峰在3厂家DGCM中均检测不到;在C厂家DGCM中检测不到11,13号峰,在A厂家DGCM中18号峰峰面积较小,而B、C厂家DGCM中检测不到18号峰。通过比较特征图谱峰面积发现,共有峰色谱峰峰面积不同,与传统汤剂相比有高有低。综上所述,DGCM与传统汤剂在化学成分种类与数目上存在一定差异,传统汤剂共有色谱峰25个,3家DGCM能检出峰数目分别为23个(A厂)、22个(B厂)、20个(C厂)。另外,B厂家颗粒比传统汤剂有明显多出的色谱峰,原因有2种可能,一种是B厂家所用的原料饮片基原不同,另一种是B厂家所用的加工工艺不同。
2.8.3共有峰峰面积比较 将3批传统汤剂色谱图中各共有峰总峰面积均值定为1,采用归一化法求得其他供试品共有峰总峰面积相对值,结果见图3。结果显示,与传统汤剂比较,A厂家配方颗粒图谱有7个峰峰面积明显较高(P<0.05),8个峰峰面积相当,10个明显较低(有2个测不到峰面积);B厂家配方颗粒图谱中有6个峰峰面积明显较高,8个峰峰面积相当,11个较低(有3个测不到峰面积);C厂家配方颗粒图谱中有3个峰峰面积相当,其余均明显较低(有5个测不到峰面积)。以3批传统汤剂色谱图中所有共有峰总峰面积的均值定为1,采用归一化法求得其他供试品共有峰总峰面积的相对值。结果显示4类供试品(传统汤剂及A、B、C厂DGCM)中各成分含量的相对总和比值分别为1,0.64,0.47,0.14,说明DGCM中各成分含量总和均低于传统汤剂。
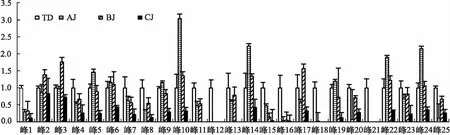
图3 不同GGD样品共有峰峰面积
2.8.4已知成分含量比较 采用外标一点法计算甘草苷、甘草酸铵、桂皮醛、肉桂酸含量。运用t检验评价A、B、C厂DGCM供试品中含量与传统汤剂供试品的差异,以传统汤剂中各指标成分含量平均值为1,采用归一化法求得其他供试品中各指标成分含量相对值,结果见图4。由图4可知,不同供试品中甘草苷含量:A厂>B厂(P<0.01)≈传统汤剂(P>0.05)>C厂(P<0.05);甘草酸铵含量:A厂>B厂(P<0.01)≈传统汤剂(P>0.05)>C厂(P<0.01);肉桂酸含量:B厂>传统汤剂(P<0.01)≈A厂(P>0.05)>C厂(P<0.05);3个厂家配方颗粒中桂皮醛含量极低,远低于传统汤剂(P<0.01)。
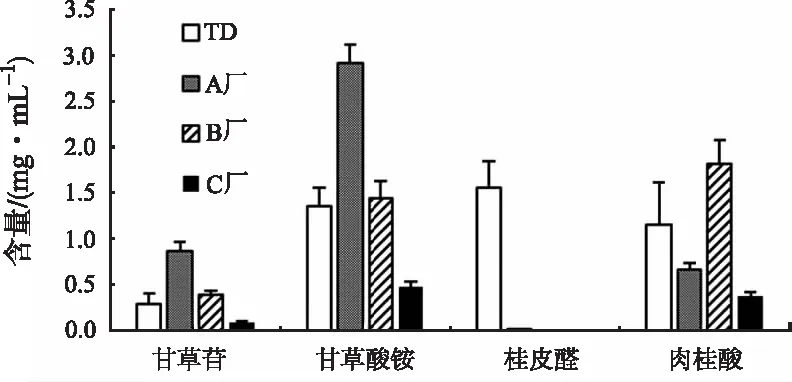
图4 GGD不同样品中甘草苷、甘草酸铵、肉桂酸、桂皮醛含量
3 讨论
3.1样品来源的选择与确定 笔者在本实验以临床常用经典药对GGD为研究载体,所用饮片和配方颗粒均从医疗机构购买,选择临床医疗实际中真实存在的两类汤剂形式——由医疗机构购得的饮片制备的传统汤剂与由医疗机构购得的配方颗粒制备的配方颗粒汤剂——作为对比对象,而对该两类对比对象的制备原料——饮片批次不做统一要求,目的是反映患者的真实用药情况。基于课题组之前对当归补血汤[13]的研究经验,笔者在后期实验设计中,有意按照“科研结合临床、科研结合实际”原则,以“黑箱”方法和“整体观”思想为指导,以问题为导向、以结果为导向,大胆抛开各类“过程”的复杂影响,化繁为简,直接对真实世界中带有自身固有特征的两类对象进行对比,试图发现共性问题和规律,使结论更能反映临床实际,更能指导临床合理使用配方颗粒。
3.2色谱条件的选择 色谱条件采用文献[12]方法,该方法经反复验证,稳定可靠。本实验样品及供试品处理方法略有不同,供试品浓度比之前研究中供试品浓度高,样品中峰面积更为突出,因而所选共有峰仅有3个较小的峰不同,其余共有峰均相同。
3.3指标性成分的确定 桂枝中含有化学成分苯丙素、木脂素、简单芳香小分子等化合物,也含少量萜类、黄酮类、苷类等化合物。其中挥发油类主要成分为桂皮醛,具有良好的抗肿瘤、抗炎、血管保护、抗过敏等作用[14-15]。另外,桂枝中还含有肉桂酸,具有抗炎、发汗等功效,桂皮醛具有解热镇痛、抗菌等作用[15]。《中华人民共和国药典》2020年版把桂皮醛作为桂枝药材的指标性成分进行含量控制[16]。甘草苷、甘草酸铵是甘草中主要活性成分,具有保肝、抗炎、镇痛、抗肿瘤、抗病毒、抗炎、杀菌等作用[17-21],因此选桂皮醛、肉桂酸、甘草苷、甘草酸铵为含量测定指标。
3.4指标性成分含量分析比较 通过对比传统汤剂和3个厂家DGCM指标性成分的含量测定结果发现,对于化学成分甘草苷、甘草酸铵,与传统汤剂相比,A厂家配方颗粒含量高,B厂配方颗粒无差异,而C厂配方颗粒含量低;对于肉桂酸,A厂配方颗粒无差异,B厂配方颗粒含量高,而C厂配方颗粒含量低;对于桂皮醛,3厂配方颗粒中含量均低,几乎检测不到。
复方煎煮过程中,会导致一些成分含量发生变化,甚至产生新成分[22]。3个厂家配方颗粒中桂皮醛含量极低,而肉桂酸含量相对较高,因为桂皮醛为挥发性成分,并且不稳定,易氧化成肉桂酸,因此推测可能桂枝配方颗粒制备或存放过程中,桂皮醛因具有挥发性和还原性,可能挥发或者氧化而几乎全部损失了。
另外,B厂家DGCM中有明显多出的色谱峰,本实验主要研究传统汤剂与DGCM的差异,并不能确定是原料基原不同还是加工工艺不同所致,这也从另一方面说明统一配方颗粒行业标准的必要性。此外,笔者在本实验对传统汤剂的选择仅为郑州市3家医院,一定程度上只代表本地域内传统汤剂与DGCM差异,后期将进一步扩大传统汤剂样本选择范围,以期得到更具普遍意义的结论。
3.5特征图谱的分析比较 特征图谱技术能全面反映中药饮片或制剂内在化学特征,具有“整体性”和“模糊性”特点,适用于评价DGCM质量[23]。笔者在本实验通过比较GGD 传统汤剂与3个厂家DGCM特征图谱,结果发现3个厂家DGCM与传统汤剂相比,化学成分种类和含量均有一定差异,传统汤剂化学成分种类较多,DGCM中化学成分而有升有降,其中C厂家各指标成分含量及峰面积相对均较小。并对其相关性进行分析,结果3个厂家配方颗粒剂与传统汤剂的相似度<0.4,3个厂家配方颗粒之间相似度>0.8。
综上所述,患者实际使用的传统汤剂与DGCM相比,其化学成分含量存在差异。原因可能与中药饮片、制备工艺等不同所致。由此可见,国家统一配方颗质量标准确有必要,否则会影响临床使用效果[24]。这也进一步提示,临床用药时应以传统汤剂为参考标准,结合各类汤剂的成分特点、药性特点及疾病特点等全面权衡,合理确定给药剂量。笔者在本实验仅从体外化学成分层面对其进行对比,其入血成分及相应药理作用的对比,课题组后续将进行深入探讨,以获取更全面的二者差异规律。

