药物共晶领域中国专利分析*
冀威文,张宝喜,龚利香,张丽,胡堃,杨世颖,吕扬
(北京协和医学院&中国医学科学院药物研究所,晶型药物研究北京市重点实验室,北京 100050)
药物共晶是药物活性成分(active pharmaceutical ingredient,API)和共晶形成物(cocrystal former,CCF)以氢键或其他非共价键结合形成的固态晶体[1],《中华人民共和国药典》2020年版晶型指导原则将共晶药物纳入晶型物质范畴。共晶药物不仅能提高原料药的溶解度[2]、渗透性[3]、生物利用度[4]、稳定性[5]以及机械加工性能[6],而且作为新型药物联用方式[7],很大程度上可以提高药物联用价值,成为新药开发的研究思路,进而通过专利对新药研究成果进行有力的技术保护。
国内外共晶领域经历了长期探索[8],共晶体最早于1783年在从尿素水溶液中结晶出氯化钠(NaCl)时被发现,但直到十九世纪中叶才被分离和分析[9-11];DESIRAJU[12]在1995年引入超分子合成子概念;直到2004年,“药物相组成的晶体工程”的概念才出现[13]。国内学者在吕扬、杜冠华等专家的组织下于2009年出版我国首部《晶型药物》学术专著,2019年出版《晶型药物》第2版,上述两本专著均提到共晶概念[1]。2011年,美国食品药品管理局(FDA)颁布《行业指南:药物共晶的监管分类》[14],2015年版《中华人民共和国药典》首次收载“9015药品晶型研究及晶型质量控制指导原则”[15],2020年版《中华人民共和国药典》四部通则9015新增“共晶物”内容,均明确了共晶属晶型药物范畴[16]。2021年,国家食品药品监督管理局药品审评中心 (Center For Drug Evaluation,CDE)发布《化学仿制药晶型研究技术指导原则(试行)》[17]。近年来,药物共晶研究越来越引起我国企业及药物学家的重视[18-20]。
随着药物共晶技术的发展以及其在药物研究中优势的体现,近年来药物共晶专利申请量呈上升趋势,国内专利申请量增长迅速。专利是对新药研发成果及新产品最有力的技术保护手段[21],专利文献可以提供科学技术发展的发明创造印记,对专利进行分析可以获得技术发展新动态,预测技术发展新趋势。笔者在本文归纳分析我国药物共晶领域近20年的专利申请情况,从专利申请时间与数量、专利申请单位类别、专利法律状态、专利申请保护类型、涉及的API及CCF类别、专利记载的技术效果等方面,阐述我国药物共晶相关知识产权保护现状与趋势,以期为制药领域科技工作者把握我国药物共晶研究现状与未来发展方向提供基础参考,也为促进共晶药物的专利布局规划提供启示。
1 专利检索和筛查方法及结果分析
笔者在国家知识产权局专利检索及分析系统中进行查询,以“((共晶OR cocrystal OR eutectic))) AND (IPC=((C07 OR A61)))”为检索式进行检索,其中C07与A61分别表示有机化学与药物领域的专利分类号。检索截止日期为2022年10月15日。经过人工筛选,剔除材料、炸药、电池、导体及光学元件等无关的共晶专利信息,得到符合筛选要求的专利1064项。在上述专利中,一部分是直接以药物或先导物的共晶物、共晶物制备方法、共晶物制药用途为主题的发明专利,将其归为药物共晶专利,共629项;另一部分专利未直接保护共晶物本身,而是在保护新化合物的基础上,将共晶作为一种新的扩展保护形式,与专利中常出现的药学上可接受的盐、晶型、溶剂化物、立体异构体、前药、代谢产物等被并列提及,这部分专利定义为化合物扩展保护专利,共435项。
鉴于发明专利申请自申请日起(有优先权的,自优先权日起)满18个月公开,同时数据库更新存在一定程度时滞,因此截止本文数据检索日,尚有2021—2022年提出的部分专利申请未被数据库收录,导致本文2021—2022年期间的专利申请数据统计不完全,但对药物共晶领域近20年的现状趋势分析影响不大,后文对此不再赘述。
1.1药物共晶相关的中国专利申请概况分析 结果见图1。FDA先后于2013和2016年分别发布了关于药物共晶监管分类的指导原则及其修订版,最终于2018年2月发布《工业指南:药物共晶的监管分类》最终版。2006年,我国出现首个涉及共晶的化合物扩展保护专利,2007年我国首次有国外申请人申请的药物共晶专利。从2008年开始,国内申请人提交的药物共晶专利以迅猛的速度发展。
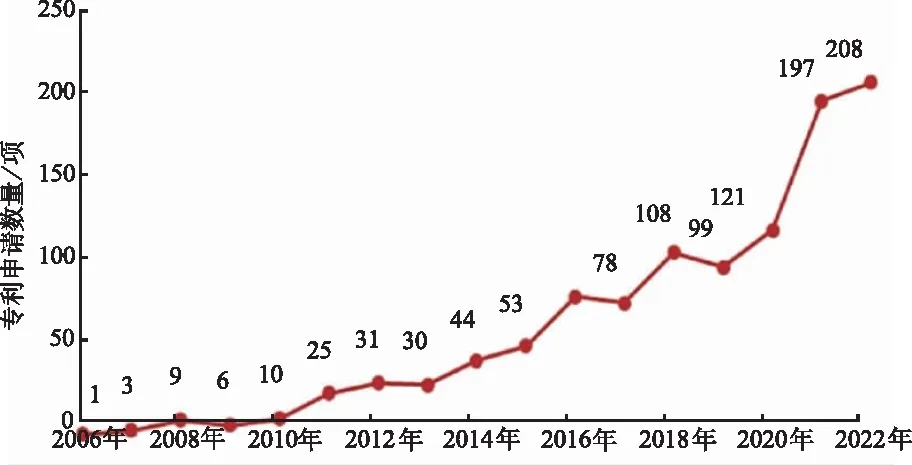
图1 药物共晶专利年度申请趋势
1.1.1专利申请的时间分布 结果见图2。2006—2010年共晶技术领域专利申请量较低,申请数量不足10项,均以化合物扩展保护专利为主,之后随着该领域研究技术的进步与研究热度的发展,申请量逐年增加,并呈现出持续上升的趋势。2011—2014年,专利申请主要以共晶专利为主,化合物扩展保护专利占比较小,2015年后,化合物扩展保护专利的申请数量明显提高;2021和2022年两类专利的申请量都维持在较高水平。这体现出药物共晶领域的研究成果增多,专利申请人保护共晶专利的意识增强。
分析药物共晶专利申请人的分布情况(图2 b)可知,该领域专利申请中,国内申请人的专利申请总量803项,国外申请人的专利申请总量302项。2014年开始,国内专利数量稳步增长,显示我国制药领域对药物共晶的关注度持续增加。
从药物共晶专利和化合物扩展保护专利的申请人分布情况(图2c、2d)可以看出,2011年之前国内外申请人相对较少,此后国内药物共晶专利申请占据了中国相关专利总申请量的主体部分,进入了快速发展期。但就化合物扩展保护专利而言,申请数量的波动也显示出国内专利申请策略存在很大进步空间。有策略地申请药物共晶专利,将其作为继药物结构保护之后的二次知识产权专利保护,可以从固体物质层面对化学药物的专利保护期限进行延长[1]。由于部分专利申请尚未公开或部分国外申请尚未申请进入中国等原因,共晶专利的实际申请量均存在高于目前统计数据的可能。
鉴于化合物扩展保护专利的申请文本中,未涉及具体共晶物的技术特征和技术效果,仅仅是本领域对共晶的认识提高与关注度增加的一种体现,故后续的专利分析中,均以629项药物共晶专利作为分析基础。
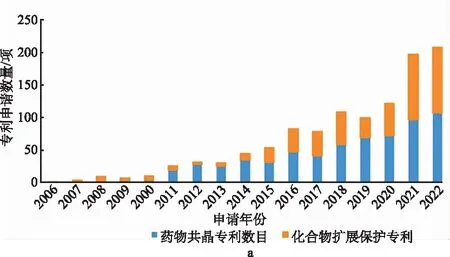
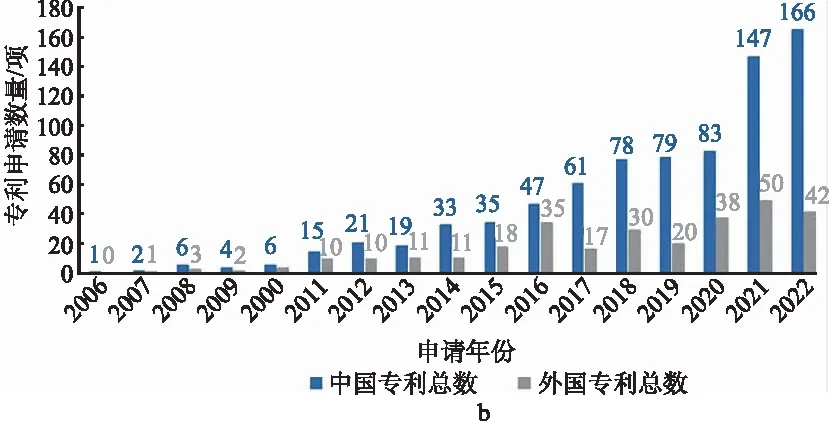
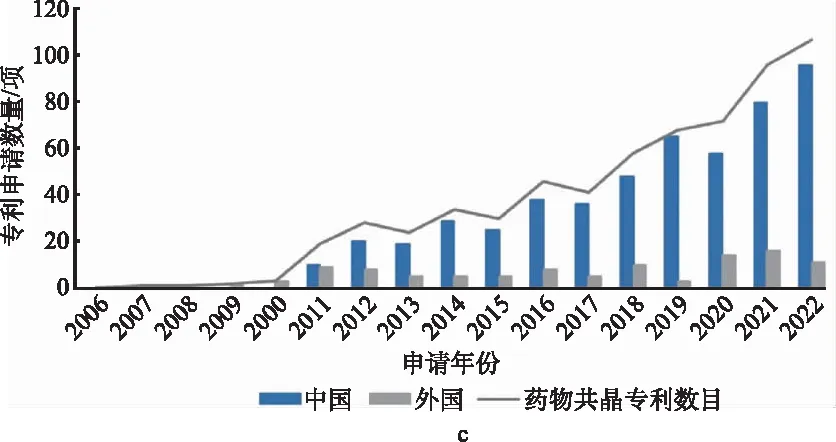
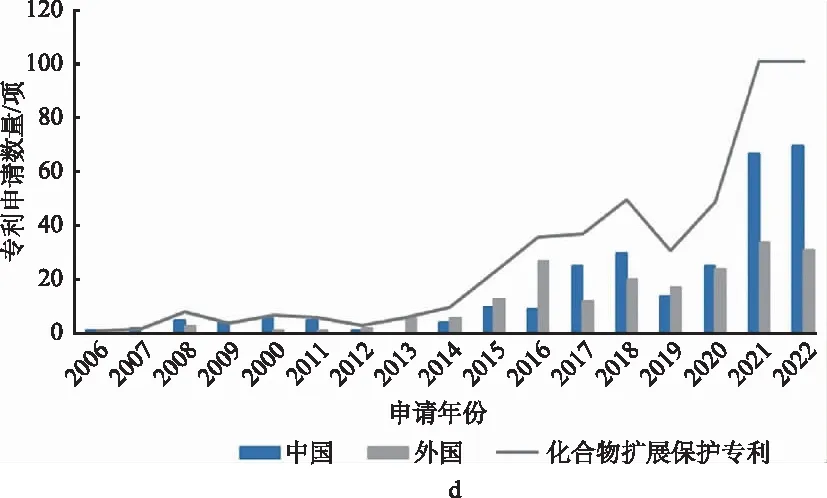
图2 药物共晶专利申请量的时间分布情况
1.2专利申请人分析 对药物共晶技术专利第一专利申请人分布进行统计,结果见图3,能发现该技术领域的第一申请人中国内外制药企业占比58.1%,大专院校占比30.5%,科研单位占比8.4%,制药企业的创新主体作用愈发显现,且可见药物共晶是理论研究与实际工业应用紧密联系的研究领域[1]。其中制药企业排名前三的是鲁南制药集团股份有限公司(38项)、吉林三善恩科技开发有限公司(15项)和广东东阳光药业有限公司(14项),大专院校中排名前三的是中国药科大学(30项)、天津理工大学(15项)和天津大学(14项),科研院所排名前三的是中国医学科学院药物研究所(21项)、中国科学院上海药物研究所(19项)和国家卫生健康委科学技术研究所(11项)。
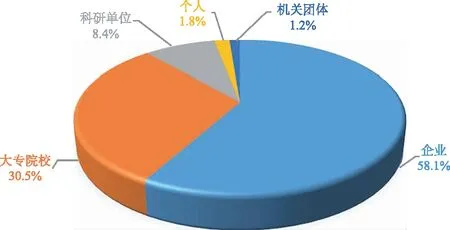
图3 药物共晶专利第一专利申请人分布
1.3专利申请的法律状态 结果见图4。在统计的629项专利申请中,已获得授权且维持有效的专利209项,占比33.2%;已公开并进入实质审查阶段的185项,占比达29.6%;失效的包括驳回、未缴年费和放弃的占比18.5%,其中驳回62项、未缴年费35项、放弃2项。保护扩大化专利已公开和实质审查329项,占比75.6%;已获得授权且维持有效的申请79项,占比18.2%;失效的包括驳回、未缴年费和放弃的占比9.0%,其中驳回11项,未缴年费22项,撤回5项,放弃1项。
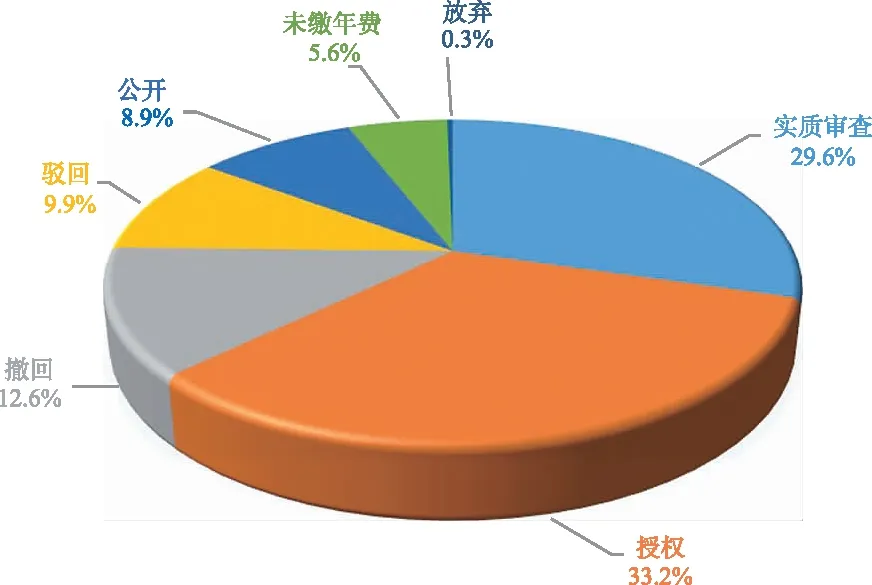
图4 药物共晶专利当前法律状态分布
我国共晶专利中授权且维持有效的专利只占四成,表明申请人在申请文本的撰写过程中,对专利三性——新颖性、创造性、实用性的认识与把握尚不够充分,专利申请质量有待提高。
1.4专利保护主题 在制药领域,药物共晶专利与药物晶型专利类似,是继化合物结构之后在物质层面的二次保护,其保护力度类似于新化学实体,属核心专利,优于制剂、制备方法、制药用途、药物组合物等其他外围专利。共晶专利保护的内容也多种多样,如新共晶固体物质、共晶物质的制备工艺技术、共晶药物制剂技术以及临床适应证等相关的用途等。
在629项药物共晶专利中,保护共晶物质及制备方法的占60.3%,保护共晶物质、制备方法及其临床适应证的占33%,保护共晶药物制剂方法的占3.8%,保护共晶制剂制备方法及用途的占3.0%,见图5。由此可见,药物共晶专利的保护中心在重要保护内容——共晶物质状态及制备方法,而在药物共晶的临床适应证方面稍有欠缺。对于共晶制剂方法和共晶制剂制备方法及用途,因其技术领域研发耗时长、研发难度大的问题,在保护对象中没有很大的占比。
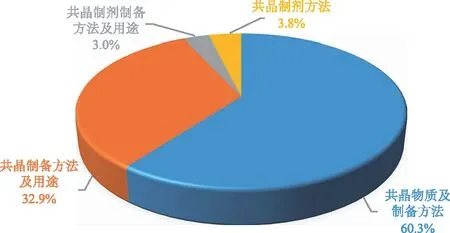
图5 药物共晶专利保护对象分布
1.5API分类 在药物共晶中,API是发挥药理作用的主要成分,CCF与API以非共价键结合后,可能改善API溶解度、引湿性、稳定性及生物利用度等物理化学及生物学性质,当两种活性成分形成药物-药物共晶时还会发挥协同作用或互补作用。通过对API进行分类统计,分析共晶中API的特点,可以为后续共晶的设计提供思路。
1.5.1化学合成药物、先导化合物或天然产物 将共晶专利中涉及的API按照其所属的研发阶段并结合化合物来源分为已上市药物、来源于合成的先导化合物、来源于天然的先导化合物(天然产物)三类,以时间为轴进行统计分析,结果见图6。由图6可知,从2007年有药物共晶专利以来,以上市药物为API一直是药物共晶专利申请中的主体部分,且随着该领域技术的发展逐年增长,这是由于上市药物多以固体制剂形式给药,且大多数上市药物属BCSⅡ和Ⅳ类,溶解性较差,具有很大的提高溶解性改善成药性需求,这为药物共晶技术的发展提供了巨大的市场。以合成来源的先导化合物和天然产物为API的共晶专利申请分别在2009年和2012年开始出现,并整体呈上升趋势。这表明在先导物开发过程中,共晶技术凭借其能够改善API成药性的优势越来越受到关注,并且在新药的专利布局中发挥着越来越重要的作用。
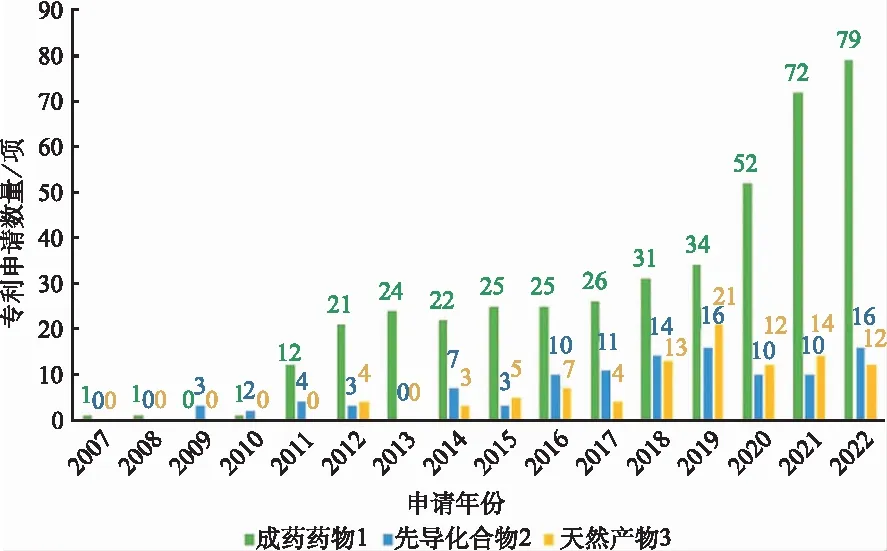
图6 药物共晶技术专利API种类时间分布
1.5.2疾病药物种类 为更深入地了解共晶专利中API的分布,笔者对共晶专利中API药物的疾病种类进行归纳统计,结果见图7。由图7可知,心脑血管药物共晶研究最多,包括地平类(尼莫地平、氨氯地平等)、沙坦类(替米沙坦、缬沙坦等)等,申请的专利量高达111项,占总申请量的19.9%;排名第二的是抗肿瘤药物共晶,包括替尼类(伊马替尼、吉非替尼等)、非尼类(瑞戈非尼、索拉非尼等)等,申请的专利103项,占总申请量的18.1%;抗炎药物共晶排名第三,共78项;排并列第四的是抗感染类药物共晶和抗糖尿病药物共晶,均有70项以上,中枢神经药物、糖尿病药物、激素类和肠胃类药物紧随其后,申请的专利量分别是49,47,22,16项;其他疾病种类专利申请量不超过15项,合计63项。随着我国老年人口增多,心脑血管类和降血糖药物市场巨大,其中降血压类、口服抗凝血类以及降血脂类药物的共晶研究都相对活跃。肿瘤作为人类高频杀手一直受到国内外医药界广泛关注,此类药物普遍存在成药性短板,如水溶性差、生物利用度低等,药物共晶技术在该领域拥有巨大发展潜力。
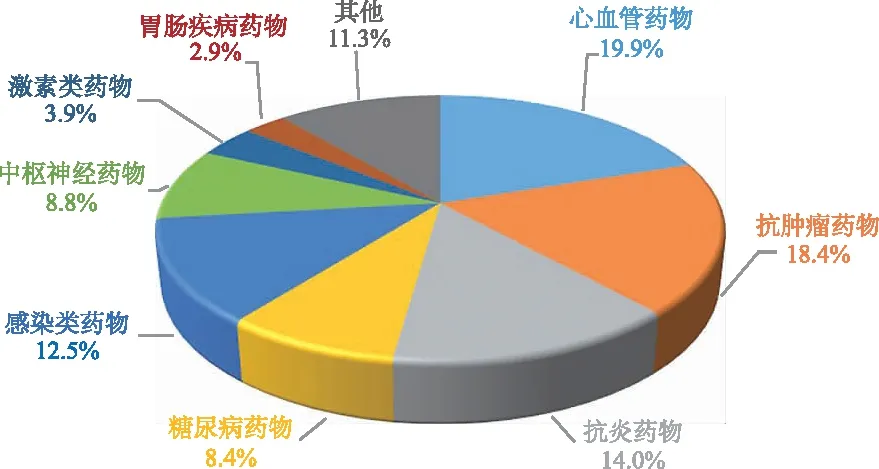
图7 药物共晶技术专利API种类分布
1.5.3CCF种类 CCF种类影响药物共晶性质,在选择合适的CCF时,不仅要考虑其与API是否能形成较强的分子间相互作用,还必须保证CCF安全无毒无副作用。通过对专利CCF统计分析可知,在629项共晶专利中,有140项为药物-药物共晶,该类专利主要目的是利用共晶技术达到药效协同和拮抗作用;居第二的CCF是药物-芳香族酸共晶,如水杨酸、苯甲酸、苯磺酸等多达129项;排名第三的是药物-脂肪族羧酸共晶,共91项专利,其中包括草酸、富马酸、马来酸等;接下来是氮杂环衍生物(吡啶、呋喃、哌嗪类)、氨基酸、药用辅料(糖精、乳糖、山梨醇等)及无机物(水占主导),分别有82,50,35和14项,其共有结构特点是含有电负性大的O、N元素,易与API生成X(O、N)-H…Y形式的分子间相互作用,且具有方向性和饱和性[22]。其他如脂肪酸、芳族化合物、人体营养物质(维生素、胆固醇等)、酰胺类衍生物及脂肪醇等均不足10项,结果见图8。由此可见,药物-药物共晶占市场主体,这因其有诸多显著的优势所致,此种新型联合用药方法不仅具有药物共晶本身的特点,还能实现降低药物剂量、毒性、耐药性以及提高治疗效果的潜在优势[23]。但CCF的设计选择不仅局限于此,还可根据API分子构象、所需要达到制备、运输和储存稳定性以及各项设计目的来选择其他惰性CCF。
1.6专利记载的技术效果分类 药物共晶可能从稳定性、溶解性、渗透性、生物利用度、熔点、机械加工性能及生物活性[24-26]等多个方面来改善API性质,这些改善常常作为体现专利技术方案具有创造性的有益技术效果而被记载在申请文件中。通过统计专利申请中公开的主要技术效果发现,有280项专利改善了API稳定性,紧跟其后的是生物利用度、溶解性、机械加工性能和熔点等方面技术效果的记载,分别有174,100,40和11项,还有少数专利记载了渗透性方面改善(图9)。专利不仅仅只针对一种技术效果进行保护,统计发现,只保护一种技术效果的专利仅55项,记载两种技术效果者574项,但总专利授权数为235项,只占专利总数的37%。
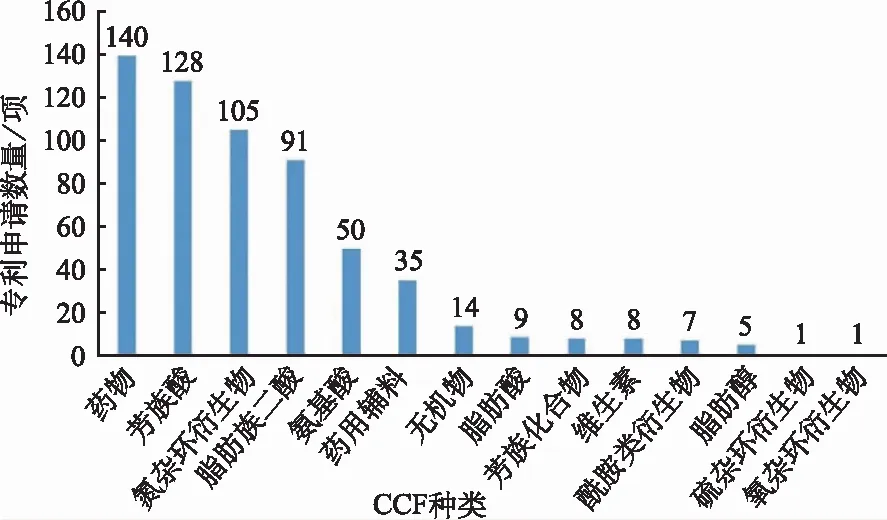
图8 药物共晶技术专利CCF种类分布
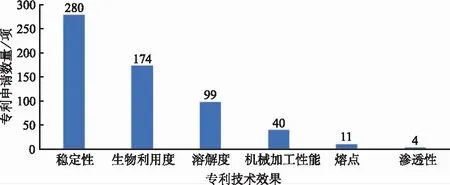
图9 药物共晶专利中达到技术效果的分类统计
2 药物共晶技术知识产权布局策略
药物共晶逐渐成为晶型领域关注的新重点[27],不仅因为其具有晶型能够改善药物稳定性、疗效及制备工艺的优点,还因其筛选得到非共价键结合的新型单体结构,实现药物联用新思路。重视药物共晶专利就能优化专利管理和占据市场优势,既降低了研发成本,又有效延长了专利保护周期[28]。因此,药物共晶专利经常在专利保护中被提起,在侵权诉讼中被利用,成为晶型领域新的发展方向。
药物共晶专利自2006年出现至今,其技术研发日趋成熟,相关专利申请量逐渐增加,权威机构的专利审查机制也在不断更新和发展。但该领域专利授权率不高,且授权后无效诉讼发生率较高,这对专利申请时的撰写质量提出了更高要求。为提高共晶专利授权率并保证授权后专利稳定性,应重点从新颖性、创造性、说明书充分公开3个方面入手。
2.1新颖性 2020年版《中华人民共和国专利法》第22条第2款规定:新颖性是指该发明或者实用新型不属于现有技术;也没有任何单位或者个人就同样的发明或者实用新型在申请日以前向国务院专利行政部门提出过申请,并记载在申请日以后公布的专利申请文件或者公告的专利文件中。
就药物共晶专利所保护的是共晶物质而言,因技术的发展很难做到发明间参数的完全对比,因此在专利撰写时必须确保已经正确、详尽地表征和记录参数并且公开地指出区别特征,尤其是共晶物质要对比参照API和CCF标注形成新的特征峰,详尽地记录发生变化的数据,并必须在提交申请材料的时候正确地并且公开的区别特征。根据欧洲专利局的实践,已知的晶型并不能通过用其新的制备方法来使其具有新颖性[29],所以对于保护方法的共晶专利而言,必须明确通过方法定义共晶的形式新颖来满足专利申请的需要。
2.2创造性 2020年版《中华人民共和国专利法》第22条第3款规定:创造性是指与现有技术相比,该发明具有突出的实质性特点和显著的进步,该实用新型具有实质性特点和进步。
药物共晶专利申请人在撰写该专利时,应该提供所要求保护的发明专利与最接近的现有共晶之间的对比数据,在这种情况下依据共晶技术领域的技术人员所提供的实验数据,详尽地描述技术效果可以改进诸如稳定性、溶解度、生物利用度等性能,因为药物的共晶在结构上与API接近的化合物,所以在评判共晶的创造性时,评审重点在于相较于现有技术是否取得了预料不到的技术效果。因此,在药物共晶专利的撰写过程中,有益技术效果的记载尤为重要[30]。
2.3公开充分性 2020年版《中华人民共和国专利法》第26条第3款规定:说明书应当对发明或者实用新型作出清楚、完整的说明,以所属技术领域的技术人员能够实现为准;必要的时候,应当有附图。摘要应当简要说明发明或者实用新型的技术要点。即通过参照说明书公开的内容,本领域的技术人员能够实现专利技术、解决实际问题及产生预期效果。
为了使专利内容得到充分的公开,同时避免专利挑战带来的隐患,需要注意以下内容:就共晶物质而言,专利撰写中必须对所述共晶表征的参数描述清楚,共晶表征的方法有很多种,如单晶X-射线衍射法(single crystal X-ray diffraction,SXRD)、红外光谱法(fourier transform infrared spectroscopy,IR)、差示扫描量热法(differential scanning calorimetry,DSC)和热重分析法(thermogravimetric analysis,TG)等。相比共晶物质的参数,共晶的制备技术和方法更复杂,撰写药物共晶专利方法时应将方法描述得足够清晰和完整,以便本领域技术人员可以通过有限的实验重复再现出来。如果申请人为避免他人很容易复制而在专利申请中提供不完整的信息,所缺少的信息是该领域普通技术无法获得的,则认为其不具有充分公开性[31-32]。
3 讨论
从上述药物专利的统计可以看出,我国药物共晶技术在发展中日趋成熟,专利申请数量也在不断增加,体现了国内制药企业、科研机构及高等院校对药物共晶研究的关注与重视。从共晶技术应用的对象分析发现,不仅包括有成药性改善需求的先导物,还包括已上市的药物,因此共晶技术不仅成为成药性改善技术的重要分支,也为已上市药物的再利用与再开发提供了技术支撑。从专利公开的技术内容看,解决API溶解性、稳定性、生物利用度问题仍然是共晶技术的主要需求,但共晶技术在改善API渗透性、机械加工性、熔点等方面的技术效果也逐渐引起药学领域的关注。最后,虽然药物共晶专利的书写有一定的规范要求,专利申请文件的撰写质量是影响共晶专利能否授权及授权后是否稳定的关键。从本文分析结果可知,药物共晶领域的专利授权率不高,本领域科技人员可以重点从新颖性、创造性、公开充分等关键角度加以重视,充分挖掘,合理布局,恰当公开,高质量申请保护。

