药物共晶及其连续热熔挤出制备技术研究进展*
李鹏丽,贾兰妮,步玉如,杨微微,张家祥
(1.青岛海洋生物医药研究院制剂研发中心,青岛 266100;2.中国海洋大学医药学院,青岛 266003)
现阶段,小分子化学药物仍是医药市场的主流产品。在小分子药物开发初期,新药分子往往被设计成复杂的结构或添加较为复杂的官能团以增强其药效、靶向性从而降低毒副作用[1]。然而复杂的结构和官能团往往导致药物分子水溶性和渗透性较差,口服生物利用度较低,从而增大药物开发难度[2-3]。因此,如何通过低成本高效药物递送技术,实现药物增溶、促渗、控释等以提高药物生物利用度,是制剂研究必须解决的难题[4-5]。热熔挤出技术(hot melt extrusion,HME)作为近年来新兴的制剂技术,创造性地将药学与工程学结合起来,不仅能实现固体分散体共晶的制备,并且能实现高效连续操作、不使用有机溶剂,或将成为理想的共晶药物制备技术[6]。笔者主要综述药物共晶在药物递送以及制药领域的应用及优势,以及HME在共晶制备层面的应用及发展现状,并分析该技术面临的挑战和机遇。
1 药物共晶
1.1药物共晶的概念 自1961年SEKIGUCHI等[7]首次报道磺胺噻唑和尿素的共晶混合物以改善药物溶解度以来,共晶体系受到学术和制药工业界的广泛关注。2018年,美国食品药品管理局(FDA)颁布的《Regulatory Classification of Pharmaceutical Cocrystals Guidance for Industry》将共晶定义为:共晶药物是指在同一晶格中,两种或以上不同分子以固定的化学计量比通过非离子键和非共价键结合形成的晶体物质。其中一种分子是活性药物成分(active pharmaceutical ingredient,API),另一种是在晶格中与API非离子键结合的配体,通常是非挥发性的,不能是溶剂或水。从共晶药物定义来看,与单一的API相比,共晶的形成也为原有活性成分提供了改善溶出、稳定性、吸湿性和体外药物组合活性的机会[8]。近年来上市或进入临床的部分共晶药物见表1。

表1 已上市或进入临床试验的部分共晶药物
1.2药物共晶在制剂领域的应用 现阶段共晶药物在制剂领域的应用主要是提高难溶性药物溶解度、增加物理稳定性等。笔者以几个案例详述共晶药物的应用及优势。
1.2.1提高溶解度 目前,接近40%的药物存在溶解性差的问题,溶解性差极大地限制了药物的临床应用。HAYASHI等[9]制备了依托度酸分别和对乙酰氨基酚、盐酸普萘洛尔的共晶,并对共晶的理化性质及体外溶出度进行了评价。依托度酸本身具有较低溶解度,且流动性、可压性差,通过湿法研磨分别形成共晶后,依托度酸溶出速率显著提高。
1.2.2增加缓控释作用 替莫唑胺是一线肿瘤化学治疗(化疗)药物,口服后消除较快,且由于其在中性环境中较稳定,在碱性环境中易水解,限制了其临床应用。王洁[10]选择具有弱酸性的黄酮类化合物如橙皮素、木犀草素、杨梅素,分别与替莫唑胺制备成为共晶体,共晶体在pH值1.2、pH值6.8的溶出介质中,降低了药物的溶出速率,避免了潜在的突释,实现了较好的缓控释效果。同时共晶中黄酮类物质的溶解度得到短暂提高,显著改善了共晶中两种物质溶解度差异问题。
1.2.3产生疗效协同或互补作用 常用于治疗肺结核的异烟肼因引发脂质过氧化而易导致肝损伤,而临床上可将抗氧化剂槲皮素与异烟肼联用以起到保肝作用,但与异烟肼合用时,槲皮素口服剂量是异烟肼的7.5倍,这大大降低了患者的依从性。LIU等[11]采用冷却结晶法制备异烟肼-槲皮素共晶体,通过体外/体内实验证实,共晶通过优势互补,可以增强槲皮素生物利用度,同时几乎消除了异烟肼肝毒性。
1.2.4掩味 在某些情况下,药物不良味道限制了制剂的开发和临床应用,目前常用的掩味方法如微囊化和包衣技术等复杂且成本昂贵,甜味剂不能完全掩盖苦味,而共晶技术不失为一种掩味方法。SOLIMAN等[12]制得摩尔比1:1的加巴喷丁与糖精共晶,通过志愿者评定苦味,结果显示共晶可显著降低加巴喷丁本身苦味,其苦味低于加巴喷丁溶液及其物理混合物。因此共晶可以在一定程度上降低人工甜味剂使用量,更有利于人体健康。
2 HME制备药物共晶
目前制备共晶的方法主要有溶液和固体合成法两大类。溶液合成法包括溶剂蒸发法、冷却结晶法、反应结晶法、混悬结晶法等。虽然现在常用的药物共晶制备方法主要是溶剂蒸发法,但这类方法需要消耗大量溶剂,且为残留溶剂杂质控制带来隐患[13-14]。固体合成法主要基于机械化学原理,利用研磨、高剪切造粒等制备共晶,常用固体合成法有干法研磨法、湿法研磨法和熔融法,这类方法需要额外输入机械能和热能。
2.1HME 见图1。HME是将药物、高分子载体、增塑剂等辅料加入分区域控温的料筒,采用机械手段,经熔融或软化充分混合均匀,通过螺杆旋转以及相互啮合研磨,使反应物在一定空间被加热、剪切、压缩,达到分子层面均匀混合的技术[15]。
共晶的形成依赖药物分子与配体之间的非共价键结合,因此当药物与配体分子间有氢键给/受体时,在熔融混合冷却后较容易形成共晶。综合近些年采用HME制备药物共晶的研究结果,典型实例见表2。
HME制备共晶的工艺参数选择十分重要,主要关键参数包括螺杆设计、挤出温度、螺杆转速以及喂料速度等。MORADIYA等[21]在制备卡马西平与反式肉桂酸共晶实验中,比较了双螺杆设计和单螺杆设计,结果发现双螺杆能够提供更多剪切力和机械能,相较于单螺杆能够得到产品质量更好的共晶产品,并且所得共晶溶出速率更快。
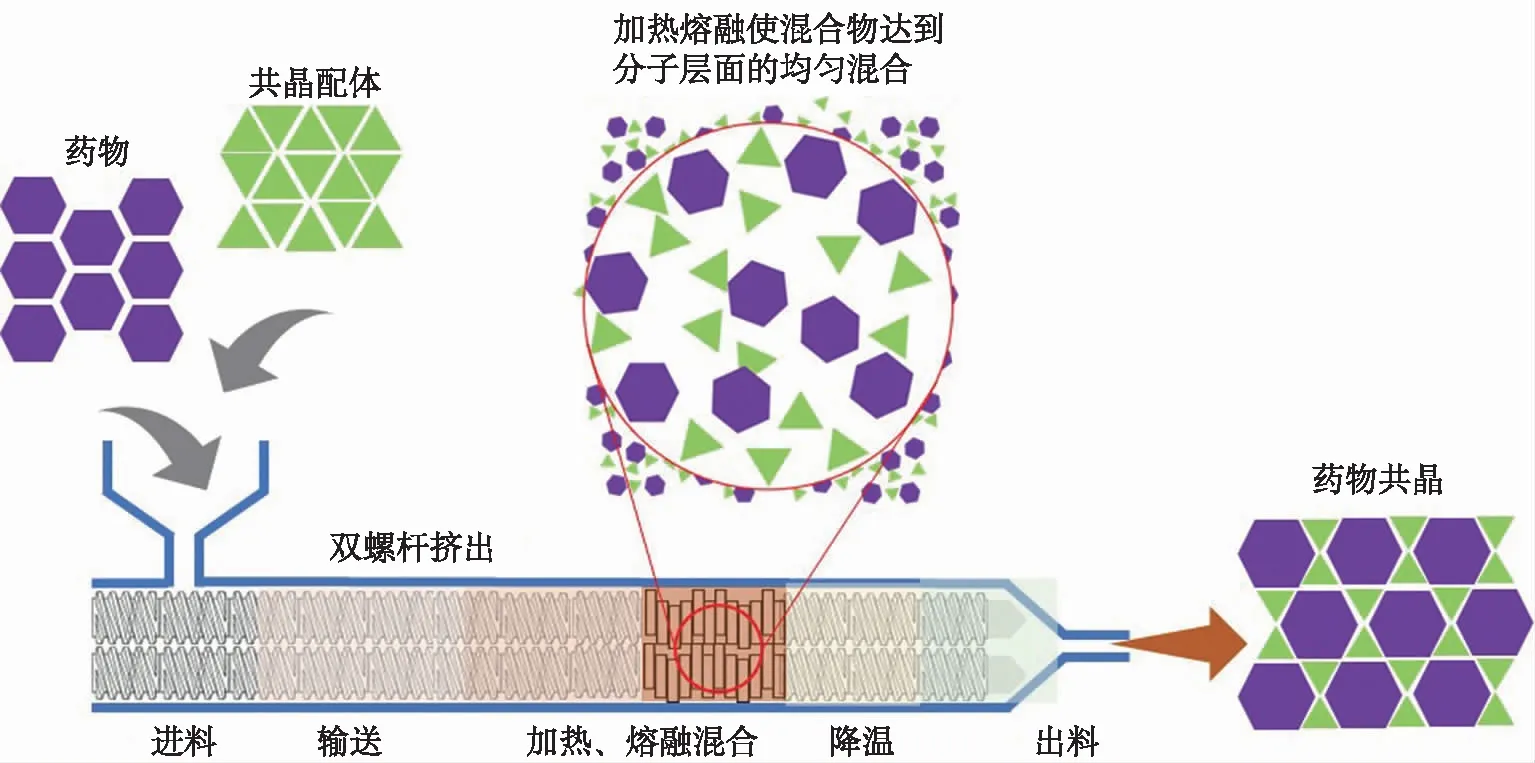
图1 热熔挤出形成药物共晶示意图
2.2HME的优势 与传统共晶制备方法如研磨法、熔融法和溶剂法等相比,HME具有制备工艺简单、自动化程度高、实验及生产设备配套成熟以及可连续化生产等优点。HME可以制备得到高质量共晶,制备过程中不使用有机溶剂,被认为是一项绿色环保技术。此外,HME工艺易于放大生产,提高设备效率,减少人为干扰,从而缩短药品上市时间。
DAURIO等[25]研究证实,HME可以连续生产4种模型的药物共晶,其中,混合和温度是影响共晶形成的关键参数。使用双螺杆挤出可以实现药物各组分之间的紧密包裹和高效混合,促进共晶形成。LIU等[22]采用HME成功制备了卡马西平-烟酰胺-聚合物共晶,实现了卡马西平20 min内从共晶聚合物中完全释放出来,证明了HME制备共晶是应用于难溶性和热敏性药物制备化学稳定的固体分散体的有效方法。MORADIYA 等[21]研究采用HME连续制备了卡马西平-反式肉桂酸共晶,发现采用双螺杆与单螺杆挤出或溶剂结晶法相比,挤出加工产生的晶体具有更快的溶解速率。共晶体在加速条件下6个月保持稳定,证明HME可以制备得到稳定性好的药物共晶。
3 HME制备共晶药物的机遇与挑战
共晶药物制备的一大挑战是工业化放大生产。传统液体共晶体的生产方案尚没有成熟的放大技术,且容易造成潜在的溶剂残留。同时传统溶剂法间歇操作的先天劣势,使最终共晶产品化学计量的可复制控制成为一大难题[17]。而作为连续操作的HME适用于放大制备共晶,有专利报道在12 m2实验室挤出条件下就可达到2.3 kg·h-1产率,并且在粒径、纯度等方面均优于传统制备技术。
目前已有多种HME制备共晶的相关创新药物经FDA批准上市。而在国内药物研发领域中,该技术还处在前期工艺摸索和优化阶段,将其应用到商业化生产仍存在大量挑战,以下对HME目前存在的难点及突破口进行阐述。
3.1过程分析技术(process analytical technology,PAT) 目前已应用的PAT技术包含紫外可见、近红外和拉曼光谱等。MORADIYA等[19,21]通过在挤出机机筒的不同区域安装在线监测的近红外(near infra-red,NIR)光纤探头,得出共晶生成方式,并获得最优卡马西平-糖精共晶产品。KELLY等[18]通过NIR光谱实时监控布洛芬-烟酰胺共晶形成,并实现了在线检测共晶纯度。因此,结合热熔挤出设备的结构特点和共晶反应条件,仔细选择过程分析模式,了解药物共晶体的相互作用并将过程优化,对获得高纯度、高质量、稳定的药物共晶十分关键。
3.2药物的热稳定性 由于热熔挤出是一个高温高剪切过程,要保证药物热稳定性,温度设置和配体选择都至关重要。首先,为使药物与载体能够共融,载体材料应具有较好的热塑性和热稳定性。在挤出时,设备的操作温度应低于药物和载体材料的降解温度,以保证其稳定性。因此载体熔化温度或玻璃转化温度与API降解温度不宜相近,两者的差距越大,越适合HME工艺[26]。
3.3药物配体与载体的选择 将药物共晶开发成上市药品仍然存在一些挑战,其一是选择合适的配体。理论上可与目标化合物形成共晶的配体数量非常多,然而目前载体的筛选依旧依赖于大量实验,时间和人力成本巨大。目前通过结合氢键倾向、剑桥结构数据库、超分子合成子方法、pKa规则和Hansen溶解度参数的筛选方法,可达到对共晶组成的预测,大大节约了研发时间和成本,逐渐被制药行业接纳并成功应用于新药研发[27-28]。
共晶制备过程中需要面对的另一个挑战是共晶与辅料的相互作用。因为共晶在制剂中存在潜在解离的可能性,比如活性成分与赋形剂、填充剂等形成分散体而非以共晶形式存在,共晶的化学计量比变化,以及在溶解过程中转化为较难溶解的母体药物等,都将导致药物的低效、无效甚至毒副作用,因此筛选适宜的载体也是HME制备共晶的关键。
4 结束语
综上所述,药物共晶是比传统成盐、溶剂化和多晶型更好的替代方法,可以改善原料药的物化性质及加工特性。尤其适用于一些含溶剂化物、晶型数量有限,且缺乏合适的电离基团的活性成分。
虽然热熔挤出共晶的工艺具有连续操作、无有机溶剂等一系列优势,但仍需面对现阶段的一些挑战。例如,在开发共晶制剂时,不但应仔细考虑共晶与其他辅料之间的相容性、药动学特征、疗效和毒性问题,还应仔细考量药物和配体是否能耐受高温、高剪切力、高压的环境以及在加热过程中潜在的降解和相互反应。同时,热熔挤出工艺在处理物理性质、熔点等相差较大的化合物组合时也面临工艺参数选择空间较窄的挑战。尽管现阶段该工艺面临多种多样的挑战,热熔挤出结合在线的过程分析工具仍是制药材料高效、高质量、低成本生产的一种新模式。
近年来连续HME也获得了制药行业的认可,并有越来越多的热熔挤出剂型产品上市销售。技术创新和全面的监管指导将推动医药共晶体在医疗应用中的转化发展。未来会有更多的基于HME的共晶药物上市并造福患者。

