原发性肺滑膜肉瘤1例并文献复习
蔡静静 张雪梅 杨光霞 田刚 葛继文 姜鲁宁
原发性肺滑膜肉瘤(primary pulmonary synovial sarcoma,PPSS)是一种侵袭性非常高且罕见的肺部肿瘤,最常见的发病部位为关节组织,肺部是PPSS极其罕见的发病部位,占恶性肺部肿瘤的0.1%~0.5%[1]。现报道1例,从临床表现、影像、病理特点、诊断及治疗方面进行文献复习,提高对本疾病的认识。
病例资料
患者,男,49岁,农民,因“咳嗽20余天”于2022年5月23日收入我院。患者20余天前受凉后出现阵发性咳嗽,以干咳为主,偶有少量白痰,咳嗽时伴胸闷、气短,无低热、盗汗,无胸痛,无咯血,于当地医院完善胸部CT平扫检查:右侧胸腔占位(图1)。既往体健,无吸烟史、偶有饮酒史。无家族性遗传病、传染病史。入院查体:神志清,精神可,胸廓无畸形,双侧呼吸动度均等,右侧语颤减弱,无胸膜摩擦音,右肋下压痛,叩诊左侧清音,右侧浊音,左肺呼吸音粗,右肺呼吸音低,未闻及干湿性啰音。入院后辅助检查回示:血尿便常规、凝血常规、癌胚抗原、神经元特异性烯醇化酶、细胞角蛋白19片段、肝肾功能、血糖血脂、心肌酶谱、电解质结果均在正常范围。血沉23.00 mm/h;乙肝五项示小三阳,乙型肝炎病毒DNA定量 2.91×102IU/mL;凝血常规:血浆纤维蛋白原 4.4g/L,D-二聚体 9.07mg/L;排除禁忌后行CT引导下肺穿刺活检,镜下见梭形细胞肿瘤,肿瘤细胞呈束状排列,可见细胞密集区及细胞稀疏区,核分裂象易见,并可见病理性核分裂象,间质胶原纤维增生,形态学及免疫组化首先考虑梭形细胞型滑膜肉瘤,待分子病理进一步证实(图2),免疫组织化学:肿瘤细胞START6、Vim、CD99、BCL-2(+++),Desmin、SMHHC、CD117、Dog-1、Mygenin、MyOD1、EMA、CD21、CD34(-),Ki-67(+,10%~15%),分子病理:SYT断裂基因检测阳性(图3),确诊为“原发性肺滑膜肉瘤”。完善PET/CT(图4)及颅脑磁共振进行临床分期,结果示:1.右侧胸腔占位,代谢增高,考虑间叶来源恶性肿瘤性病变可能性大,滑膜肉瘤?请结合病理明确;右侧胸腔积液、右侧锁骨区、纵隔(2R、3A)区增大淋巴结,代谢增高,考虑转移可能性大,余纵隔及右膈上小淋巴结,代谢不高,随诊。2.双肺散在微小实性结节,代谢不高,随诊。3.双肺散在慢性炎症,右肺部分实变、不张。4.主动脉及冠状动脉壁钙化。5.甲状腺双叶低密度结节,代谢不高,请结合超声检查。颅脑磁共振平扫+增强:1.双侧额叶皮层下缺血变性灶。2.颅脑MR增强未见明显异常。3.副鼻窦轻度炎症。患者出现右侧胸膜、右侧锁骨区及纵隔淋巴结转移,临床分期为IV期,无手术指征,完善基因监测无基因突变,建议化疗联合免疫治疗,患者拒绝,要求上级医院继续诊治。
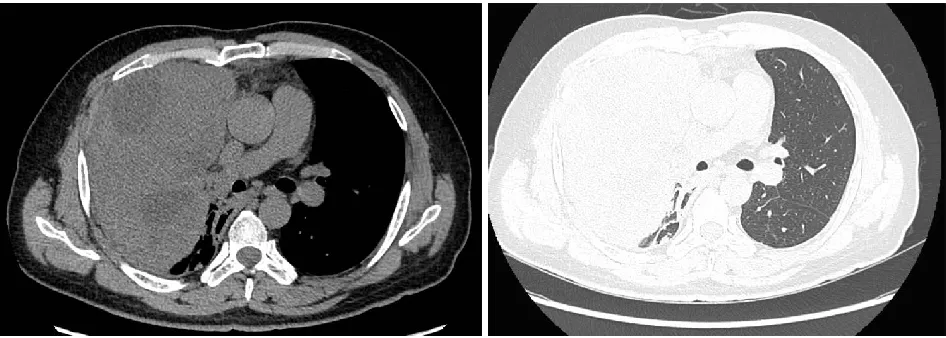
图1 胸部CT右侧胸腔内见巨大占位,其内密度不均,见多发坏死
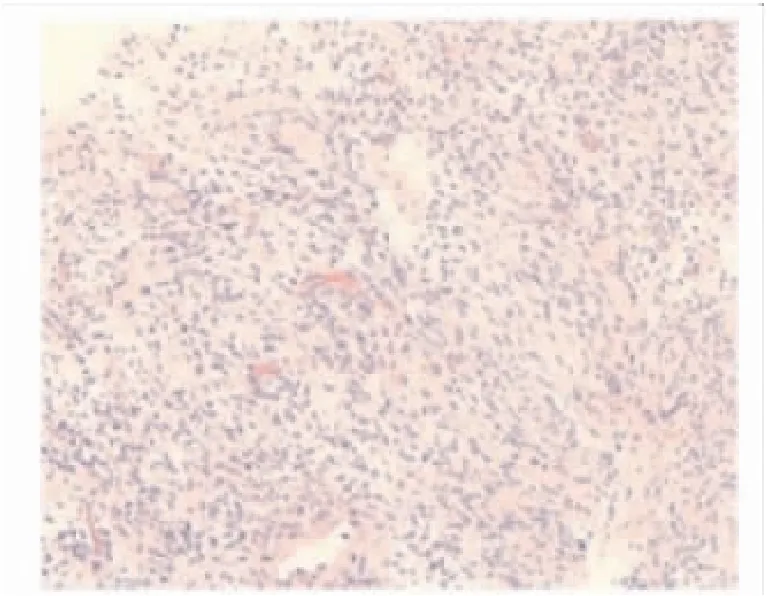
图2 CT引导下肺穿刺活检病理(HE×400)

图3 SYT断裂基因检测阳性(50%的肿瘤细胞可见SYT红绿信号分离)

图4 PET/CT右侧胸腔内见团块状软组织密度影,大小约17.5cm×10.9cm×14cm,FDG摄取不均匀增高,SUVmax 10.1
文献复习
以“primary pulmonary synovial sarcoma”为关键词在Pubmed数据库检索从 2017年1月至2022年7月相关文献,共检索到13篇,平均年龄 42.9岁,最小年龄26岁,最大年龄61岁;男 8例,女 5例;咳嗽6例,胸痛6例,憋喘6例,咯血2例,无症状2例,声音嘶哑 1例;左肺上叶 2例,右肺下叶 4例,右肺上叶 3例,左肺2例,右肺 1例,左肺下叶 1例;手术 10例,新辅助化疗 1例,术后放疗2例,化疗7例,其中术后化疗 5例,1例治疗方式不详。
以“原发性肺滑膜肉瘤”为关键词在万方、中国知网数据库检索到相关文献31篇,相关病例37例,平均年龄44岁,最小年龄19岁,最大年龄71岁;男 24例,女 13例;咳嗽 24例,胸痛 19例,胸闷 9例,咯血 11例,咳痰 14例,发热 2例,无症状 2例;右肺上叶 11例,左肺下叶 9例,左肺上叶 7例,右肺下叶5例,右肺中下叶 1例,右肺门 1例,右肺中叶 1例,左肺门 1例,左肺 1例;手术 28例,对症 2例,7例治疗方式不详。
讨 论
临床特点 PPSS是一种间叶来源的恶性肿瘤,主要发生于不吸烟的青少年和年轻人,在性别上无差别,其最常见的发病部位为关节组织[2]。肺部是PPSS极其罕见的发病部位,但原发性肺外肉瘤的继发性肺转移更为常见[3]。患者通常首先出现阻塞性肺炎的症状,即咳嗽、呼吸困难和咯血。外周肿瘤较少见,最初无症状,但可浸润邻近器官,表现为胸痛、胸膜或心包积液、血胸和复发性气胸[4]。本病例也是一名不吸烟的成年男性,主要表现为劳力性呼吸困难和胸腔积液。
影像特点 PPSS影像特征大多数为非特异度的,增加了诊断的难度。其在胸部增强CT上,通常表现为边界清楚、不均匀强化的肿块,内部伴有坏死,可引起同侧胸腔积液,很少发生淋巴结转移。PPSS在PET/CT上主要表现为肺内团块状FDG代谢增高灶。据研究报道[5],滑膜肉瘤的最大标准摄取值(maximum standardized uptake value,SUVmax)从1.2到13.0不等,中位数为4.35,约65%的原发性肺滑膜肉瘤SUVmax>4.35,其无病生存率明显下降,具有局部复发和转移的风险。PPSS与其他类型的肺部肿瘤有代谢重叠范围,致使PET/CT对诊断PPSS缺乏特异度。因此PET/CT可以用来排除胸外原发性滑膜肉瘤,进行临床分期、诊疗计划及疗效评价[6]。在我们的病例中SUVmax为10.1,并伴有胸膜、淋巴结转移。
病理特点 组织学上,这些滑膜肉瘤主要由两种形态不同类型的细胞组成,即上皮细胞或成纤维细胞样梭形细胞,并分为四种类型:双相、低分化、单相纤维型(梭形细胞)和单相上皮型。单相亚型需与纤维肉瘤、血红细胞外皮细胞瘤和平滑肌肉瘤相鉴别[7]。其中单相亚型很难与其他肉瘤进行鉴别,因此免疫组织化学检测对鉴别诊断至关重要。PPSS在免疫组化方面常为EMA、Vimentin、Cytokeratin、BCL-2呈阳性,S-100、Desmin、CD34等呈阴性。据报道,80%~90%的滑膜肉瘤具有特异度的染色体易位(X:18)(p11.2:q11.2),表现为18号染色体上的SYT基因与Xp11染色体中的SSX基因融合,其对诊断具有特异度[8]。本例患者Vimentin、CD99、BCL-2(+++),CD34表达阴性,FISH检测示SYT断裂基因阳性,结合以上指标,患者最终确诊为原发性肺滑膜肉瘤。
治疗与转归 PPSS目前尚无统一治疗方案,手术目前是主要的治疗方法,肿瘤切缘阴性是预防局部复发的关键,但是PPSS具有高度侵袭性,且肿块体积很大,外科手术很难做到根治性切除[9]。滑膜肉瘤目前认为对化疗相对敏感,单独使用阿霉素或与异环磷酰胺联合治疗仍然是此类转移性疾病的标准方案[10]。本例患者已经出现胸膜及多发的淋巴结转移,无法行手术治疗,建议化疗联合免疫治疗。
总之,原发性肺滑膜肉瘤是一种侵袭性高且罕见的恶性肿瘤,临床症状及影像学表现无明显特异度,临床确诊需要病理、免疫组化和FISH检测SYT-SSX融合基因。PET/CT对诊断PPSS缺乏特异度,但其有助于PPSS的临床分期、诊疗计划及疗效评价,治疗包括手术、化疗、放疗等。

