免疫检查点抑制剂CTLA-4在实体肿瘤治疗中的临床应用
李 涛,张 侃,杨文雨,刘 鹿,郑 轩,张 帆,胡 毅
中国人民解放军总医院第一医学中心 1肿瘤内科 全军肿瘤学重点实验室 肿瘤靶向治疗和抗体药物教育部重点实验室 5营养科,北京 100853 2中国人民解放军总医院(解放军医学院)研究生院,北京 100853 3中国人民解放军总医院第八医学中心呼吸与危重症医学部,北京 100853 4南开大学医学院,天津 300000
Hanahan等[1]于2011年首次提出肿瘤免疫逃逸这一新兴特征,并于2022年1月再次总结了肿瘤发生发展机制及治疗策略[2],其中包括免疫检查点抑制剂(immune checkpoint inhibitors,ICIs),该类药物通过激活机体自身免疫应答发挥抗肿瘤作用。近年来,针对细胞毒性 T 淋巴细胞相关蛋白4 (cytotoxic T-lymphocyte-associated protein 4,CTLA-4)、程序性死亡[蛋白]-1 (programmed cell death protein-1,PD-1)及其配体- 1(programmed death-ligand 1,PD-L1)等免疫检查点相关抑制剂在肿瘤的免疫治疗方面取得了一定进展,开启了肿瘤治疗的新时代。本文就CTLA-4单抗在晚期实体肿瘤中的临床治疗进展进行综述,以期为肿瘤的免疫治疗提供参考。
1 免疫检查点抑制剂及其作用机制
免疫检查点是维持自身免疫稳态的免疫调节因子,可调节机体免疫应答[3]。正常情况下,肿瘤细胞使部分免疫检查点失活,造成抗肿瘤免疫反应失调,从而促进肿瘤生长和增殖。而ICIs可通过抑制免疫检查点介导的免疫耐受,增强免疫细胞活性,激活机体自身的免疫应答,从而发挥抗肿瘤作用。目前,以PD-1/PD-L1为代表性的ICIs类药物广泛用于临床治疗,包括PD-1抑制剂(Pembrolizumab、Nivolumab)和PD-L1抑制剂(Atezolizumab、Durvalizumab)等。除此之外,ICIs类药物还包括CTLA-4单抗(Ipilimumab、Tremelimumab)、淋巴细胞活化基因3(lymphocyte activation gene-3,LAG-3)单抗(Relatlimab)[4]、T细胞免疫球蛋白(T cell immunog-lobulin)和免疫受体酪氨酸抑制基序(immuno-receptor tyrosine-based inhibition motif,ITIM)结构域单抗(Tiragolumab)[5]等。相较于PD-1/PD-L1抑制剂单药在肿瘤治疗领域的广泛应用,CTLA-4抑制剂在双免疫疗法中的应用丰富了肿瘤免疫治疗方式,其中以PD-1/PD-L1抑制剂联合CTLA-4抑制剂的双免疫疗法最为常见。
1.1 CTLA-4抑制剂
CTLA-4(CD152)与CD28同源,均表达于活化的CD4+和CD8+T细胞表面,CD28与其配体B7-1/2结合后产生刺激性信号,激活TCR信号通路,使CTLA-4高表达并竞争性结合B7-1/2,抑制白细胞介素(interleukin,IL)-2分泌,从而发挥负性调控作用[6-9]。此外,CTLA-4与CD80/CD86结合可抑制T细胞活化,而调节性T(regulatory T,Treg)细胞可通过CTLA-4下调CD80/CD86的表达水平,进而抑制CD28共刺激信号通路[10-11]。CTLA-4抑制剂通过上述机制发挥抗肿瘤作用[12],阻止Treg细胞下调CD80/86表达水平[13],并通过抗体依赖性细胞介导的细胞毒性作用(antibody-dependent cell-mediated cytotoxicity,ADCC)及吞噬作用(antibody-dependent cell-mediated phagocytosis,ADCP)耗竭Treg细胞,从而增加CD4+/CD8+T细胞对肿瘤组织的浸润,同时使记忆T细胞克隆性增多[14-17]。
1.2 CTLA-4联合PD-1/PD-L1抑制剂
PD-1/PD-L1或CTLA-4单抗治疗的反应率均较低,而二者联合治疗的反应率升高,联合治疗作用机制可能为:(1)增加CD4+/CD8+T细胞对肿瘤组织的浸润,从而提高CD4+/CD8+T细胞与Treg细胞的比例,发挥抗肿瘤作用;(2)同时作用增强共刺激,从而进一步促进T细胞活化,且由于CTLA-4与PD-1细胞内信号传导均与PI3K/AKT/mTOR信号通路相关,可同时阻断双免疫检查点[18-21]。
2 抗CTLA-4治疗
与PD-1/PD-L1单抗相比,CTLA-4单抗类药物虽然起步与临床应用较早,但药物种类较为单一且多联合其他ICIs使用。目前仅Ipilimumab获得美国食品药品监督管理局 (Food and Drug Administration,FDA)批准用于肿瘤的临床治疗,也是首个被证实可延长晚期黑色素瘤患者总生存期 (overall survival,OS)的药物[22]。
2.1 CTLA-4单药治疗
一项Ipilimumab联合黑色素瘤相关糖蛋白(HLA-A*0201)治疗黑色素瘤的疗效及安全性临床试验(MDX010-20)研究表明,联合治疗与Ipilimumab单药治疗的生存获益均优于对照组,可显著延长黑色素瘤患者的中位OS(median OS,mOS),Ipilimumab于2011年5月获美国FDA批准上市[22]。一项Ipilimumab与安慰剂用于黑色素瘤术后辅助治疗的Ⅲ期临床试验(CA184-029)研究表明,Ipilimumab可降低28%的黑色素瘤患者死亡风险,5年生存率为65.4%,中位随访6.9年时各项生存获益仍持续存在,且各亚组的长期获益一致,于2015年10月获美国FDA批准用于黑色素瘤术后辅助治疗[23]。
2.2 “O+Y”联合治疗
2.2.1 一线治疗
(1)黑色素瘤:一项Ⅱ期临床试验(CheckMate-069)研究表明,与Ipilimumab单药治疗相比,“O+Y”[Nivolumab(PD-1单抗)+Ipilimumab(CTLA-4单抗)]联合治疗BRAF 野生型患者客观缓解率(objective response rate,ORR)与完全缓解率均较高(61%比11%,22%比0),“O+Y”联合治疗BRAF 突变型患者中位无进展生存期(median progression free survival,mPFS)显著延长(8.5个月比2.7个月),于2015年9月获FDA批准用于治疗不可切除或转移性BRAF 野生型黑色素瘤[23]。“O+Y”联合治疗与Ipilimumab及Nivolumab单药治疗不可切除黑色素瘤患者的临床试验(CheckMate-067)表明[24],联合治疗PFS及OS均优于单药治疗组,可显著改善mOS,于2016年1月获美国FDA批准用于治疗不可切除黑色素瘤。
(2)肾细胞癌:一项随机、开放性Ⅲ期临床试验(CheckMate-214)研究表明[25],与Sunitinib 单药治疗相比,“O+Y”联合治疗使中高风险肾细胞癌患者OS由26.6个月延长至47个月,死亡风险下降34%,PFS由8.3个月延长至12个月,进展或死亡风险降低24%,于2018年4月获美国FDA批准用于治疗晚期或转移性肾细胞癌。
(3)非小细胞肺癌(non-small cell lung cancer,NSCLC):一项治疗EGFR/ALK阴性晚期NSCLC的Ⅲ期临床试验(CheckMate-227)研究结果于2021年美国临床肿瘤学会(American Society of Clinical Oncology,ASCO)年会公布,详见表1[26-27]。另有一项Ⅲ期临床试验(CheckMate-9LA)表明[28],与单纯化疗相比,“O+Y”联合治疗+2周期化疗的mOS、2年总生存率、mPFS、中位持续缓解时间 (duration of response,DOR)均较高(15.8个月比11.0个月,38% 比26%,6.7个月比5.3个月,13.0个月比5.6个月),基于上述两项研究,“O+Y”联合治疗于2021年5月获美国FDA批准用于治疗EGFR/ALK阴性晚期NSCLC。
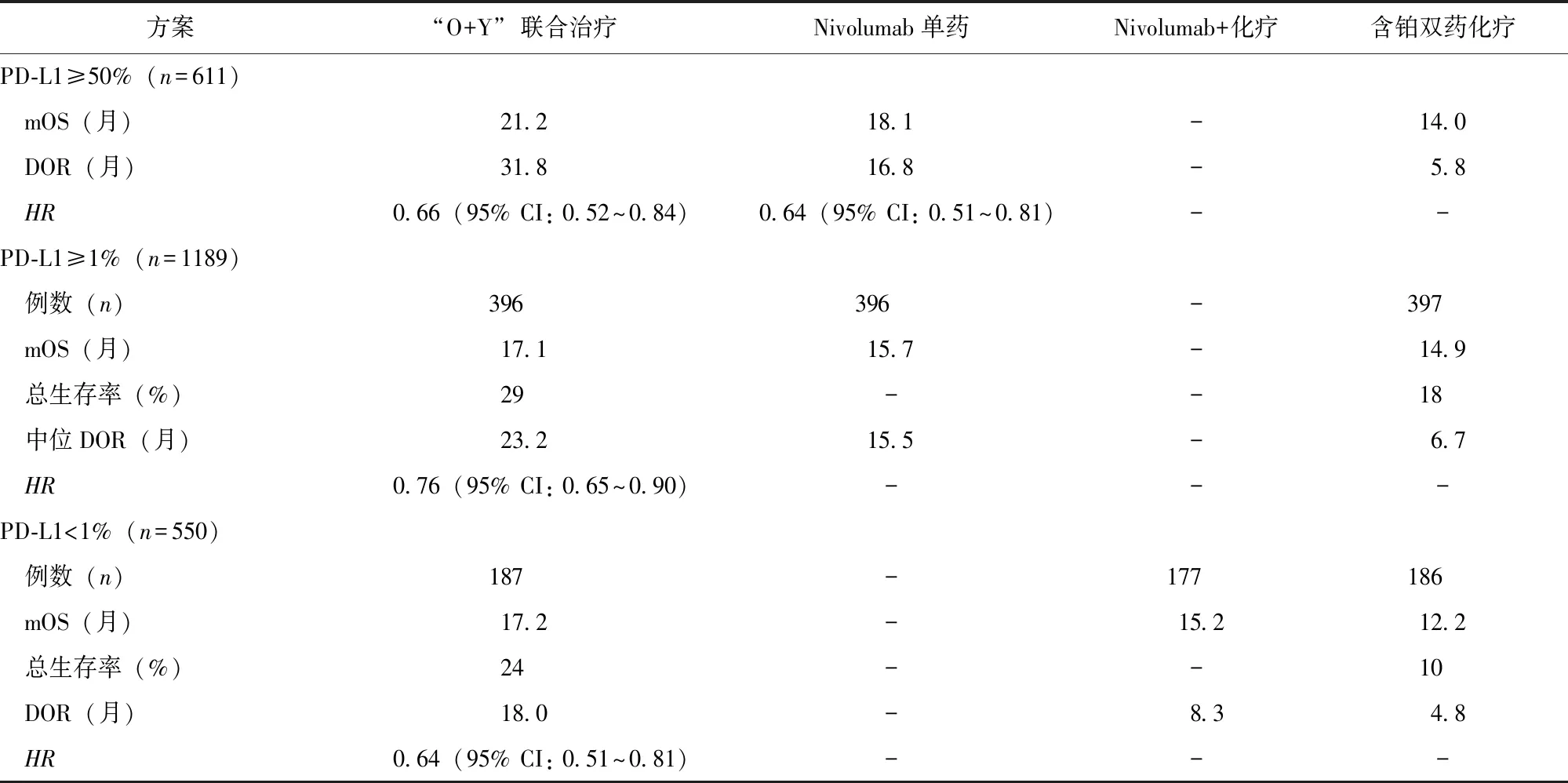
表1 CheckMate-227临床试验结果
(4)恶性胸膜间皮瘤(malignant pleural mesothelioma,MPM):一项Ⅲ期临床试验(CheckMate-743)研究表明[29],与单纯化疗相比,“O+Y”联合治疗可显著延长MPM患者的mOS(18.1个月比14.1个月),提高2年总生存率(41%比27%),有效改善MPM患者的生存获益,随访35.5个月即患者停药1年后,3年总生存率是单纯化疗的1.5倍(23.2% 比15.4%),死亡风险降低27%,为首个且唯一证明“O+Y”联合治疗可改善生存获益的临床试验,并打破了MPM 15年内缺乏新药的僵局,于2020年10月获美国FDA批准用于MPM的治疗。
(5)晚期肝细胞癌(hepatocellular carcinoma,HCC):一项治疗HCC 的Ⅲ期临床试验(HIMALAYA)结果显示[30],相较于索拉非尼(Sorafenib)单药治疗,“D+T”[Durvalizumab(PD-L1单抗)+Tremelimumab(CTLA-4单抗)]联合治疗的mOS较高(16.4个月比13.8个月,HR=0.78,95% CI:0.66~0.92,P=0.0035),mPFS分别为3.8 个月和4.1个月,ORR分别为20.1% 和5.1%,3年总生存率分别为30.7%和20.2%,于2022年10月获美国FDA批准用于HCC的一线治疗。
2.2.2 二线及后线治疗
(1)转移性结直肠癌(metastatic colorectal cancer,mCRC):一项临床试验(CheckMate-142)研究表明[31],119例曾接受氟尿嘧啶+奥沙利铂或伊立替康治疗,且为高度微卫星不稳定(microsatellite instability high,MSI-H)/错配修复缺陷(deficient mismatch repair,dMMR)转移性mCRC患者接受4周期“O+Y”联合治疗后序贯Nivolumab 3 mg/kg,每2周治疗直至病情进展或死亡。入组患者的BRAF和KRAS突变率分别为24%和37%,研究显示ORR为49%,其中完全缓解率和部分缓解率分别为4%和45%,“O+Y”联合治疗于2018年7月获美国FDA批准。
(2)HCC:一项Ⅰ/Ⅱ期、多队列研究(CheckMate-040)中队列1、2研究针对Nivolumab剂量爬坡与扩展试验[32]结果显示未接受Sorafenib治疗的一线治疗和接受过Sorafenib治疗的二线治疗ORR分别为20%~23%和16%~19%,一线初治患者mOS达28.6个月,二线经治患者mOS分别为15.6个月(扩展组)和15个月(递增组),于2017年9月获美国FDA批准用于HCC二线治疗,2019年ASCO年会公布了队列4研究对于“O+Y”联合治疗在曾接受Sorafenib治疗的HCC患者中的安全性及有效性研究结果,HCC患者ORR为31%,mDOR为17.5个月,疾病控制率为49%。基于上述研究结果,“O+Y”联合治疗于2020年3月获美国FDA批准。
(3)宫颈癌:一项Ⅱ期临床试验结果显示,我国自主研发的卡度尼利(Candonilimab)单抗[33]用于治疗既往接受含铂化疗失败的复发或转移性宫颈癌患者的ORR为33.0%,随访6个月及12个月时中位持续缓解率分别为77.6%和52.9%。mPFS为3.75个月,mOS为17.51个月,3级及以上不良事件(adverse event,AE)发生率为27.0%,该药物于2022年6月获我国国家药品监督管理局(National Medical Products Administration,NMPA)批准附条件上市。CTLA-4及“O+Y”联合治疗获美国FDA/我国NMPA批准的适应证见表2。
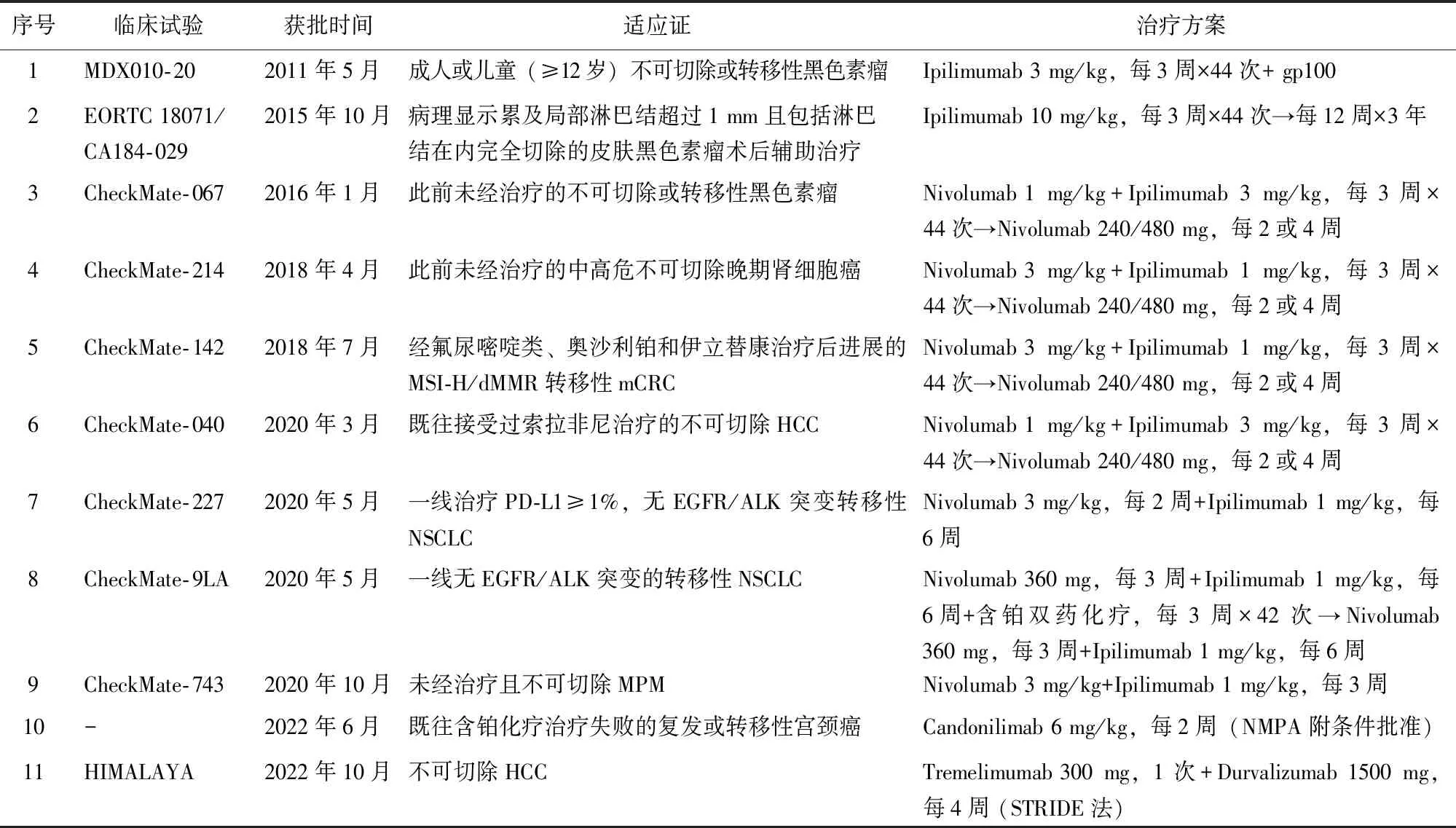
表2 CTLA-4及“O+Y”联合治疗获美国FDA/我国NMPA批准的适应证
3 抗CTLA-4治疗剂量
3.1 CTLA-4单药治疗剂量
一项临床试验(EORTC 18071)结果表明Ipilimumab单药辅助治疗术后高危黑色素瘤剂量为10 mg/kg[23],而另一项研究(E1609)显示[34],与高剂量干扰素α (79%)相比,Ipilimumab剂量分别为3 mg/kg和10 mg/kg时,3级及以上AE发生率分别为37%、58%,Ipilimumab剂量不仅与AE发生率及药物毒性呈正相关,且疗效并不优于高剂量干扰素α,但3 mg/kg的Ipilimumab治疗剂量有利于远期的生存获益。两项临床试验(CA184-156、CA184-104)研究显示,在小细胞肺癌(small cell lung cancer,SCLC)和晚期肺鳞癌患者中Ipilimumab联合治疗(10 mg/kg,每4周×4个周期治疗后予以每12周维持治疗)中半数患者未完成治疗,3级及以上AE发生率较高,OS并未改善[35-36]。
3.2 “O+Y”联合治疗剂量
目前,Ipilimumab在不同瘤种中的联合使用剂量无法统一,但多数临床试验均保持长期低剂量(1 mg/kg,每3周或每6周)疗法且联合治疗效果优于单药治疗,联合治疗患者ORR较长且缓解程度更高。联合治疗不同剂量组合方式及药物安全性,见表3,4[27-28,37-42]。

表3 CheckMate系列研究中联合治疗剂量
4 小结与展望
CTLA-4使临床医生对于免疫治疗的认识更进一步,对双免疫疗法更加期待。目前,已被美国FDA获批的CTLA-4抑制剂仅有Ipilimumab和Tremelimumab。Ipilimumab仅在黑色素瘤的特定情况下获批单药治疗,其余均为联合治疗。目前,仍存在药物种类少、适应证范围窄、缺乏最佳剂量和治疗策略等问题。截至目前,在ClinicalTrails.gov 网站登记记注册的CTLA-4临床试验共238项,其中正在开展的有119项。在中国临床试验注册中心(China Clinical Trail Registry)注册开展的CTLA-4临床试验均为联合治疗但数量不多。此外,现有的联合治疗虽然有不同组合的尝试和探索,但疗效有限。一项Ⅲ期临床试验(CheckMate 451)研究表明[43],“O+Y”联合治疗SCLC未能改善患者OS和PFS,另一项Ⅱ期STIMULI临床研究显示[44],对于“O+Y”联合治疗用于同步放化疗后局限期SCLC的维持治疗效果有限。“D+T”一线治疗Ⅳ期NSCLC相较于含铂标准化疗未能改善患者OS[45],另一项Ⅱ期MYSTIC临床研究显示Durvalumab单药或“D+T”联合治疗均未能显著提高Ⅳ期NSCLC患者OS[46]。此外,联合治疗效果并不一定优于单药治疗,一项针对PD-L1 TPS≥50%且无EGFR或ALK基因突变转移性NSCLC患者的Ⅲ期临床试验(KEYNOTE-598)显示,Pembrolizumba+Ipilimumab(“K+Y”)治疗与Pembrolizumba单药治疗相比,OS及PFS均未显著提高,且AE发生率高达76.2%,其中3级及以上AE占比35.1%[47]。未来应针对双免疫疗法在不同瘤种中合适的治疗时机、不同组合形式和应用策略进一步进行探索和研究。
此外,还需深刻意识到免疫治疗的复杂性、不确定性和风险性。应重视抗CTLA-4单药治疗及“O+Y”联合治疗的AE发生情况,早期临床试验多采用高频率、大剂量Ipilimumab单药治疗,一项采用10 mg/kg,每3周×4个周期Ipilimumab单药治疗的临床试验(CA184-104)显示,AE发生率高达53%,停药率28%,高于化疗组,且仅有46%的 Ipilimumab组患者完成治疗,其中还包括调整了化疗或Ipilimumab剂量的患者,最常见AE(发生率≥5%)为疲乏、腹泻、皮肤瘙痒、皮疹和结肠炎[35]。而“O+Y”联合治疗的AE也有不同程度的叠加,尤其是免疫相关不良反应(immune-related adverse events,irAE)(包括胃肠道、肺部及皮肤发生AE及肝毒性等)(表4),因而在CheckMate系列研究中,逐步对Ipilimumab采用低剂量、长疗程、大间隔治疗策略。CheckMate743研究显示[38],联合治疗的AE发生率由高至低依次为皮疹(25%)、疲乏(22%)、腹泻(21%)、瘙痒(16%)、甲状腺功能减退(11%)、恶心(10%),绝大多数为轻度至中度(1级或2级)。此外,并非联合治疗的毒副反应一定高于化疗、靶向治疗,如在HIMALAYA研究中[30],“D+T”组合的3级及以上AE发生率仅为25.8%,并未增加严重肝毒性和出血风险,而Sorafenib组为36.9%。以Ipilimumab为代表的CTLA-4抑制剂上市多年但未能在多种实体肿瘤有较大突破,原因可能是CTLA-4作用机制及与PD-1/PD-L1信号通路相关性尚不明确,不同IgG抗体类型、PH依赖性抗体、抗原表位差异等导致药物疗效难以达到预期目标[48-51],随着PD-1/CTLA-4联合治疗药物的出现或许能够解决上述问题。
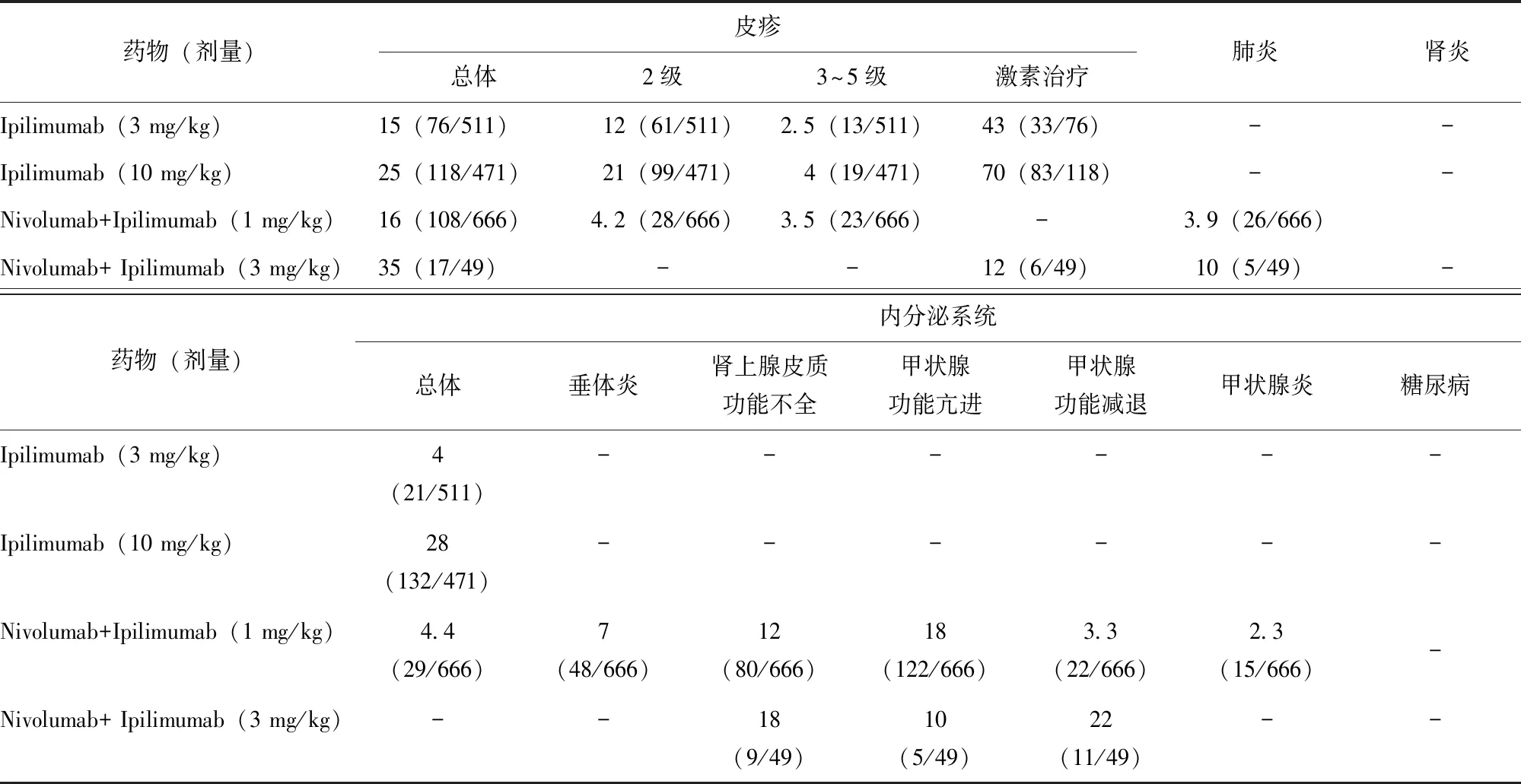
表4 CTLA-4单药或联合治疗AE发生率[%(n/N)]
综上所述,由于免疫治疗具有复杂性、不确定性及一定风险,故仍需更充分的循证医学证据,通过精确的生物标记物筛选出免疫治疗的优势人群,精准预测免疫治疗疗效和风险。对于不同瘤种、不同治疗阶段的CTLA-4抑制剂联合使用,应在循证医学、国内外相关指南的指导下审慎进行。
作者贡献:李涛、郑轩和张帆负责论文撰写;张侃、杨文雨、刘鹿负责文献查阅及资料收集;胡毅负责组织选题及论文审校。
利益冲突:所有作者均声明不存在利益冲突

