胸主动脉夹层腔内修复术后感染继发主动脉食管瘘1例
顾晓龙 官格 林霖 向定成
1 临床资料
1.1 第1次住院
患者 男,53岁。因“上腹撕裂样疼痛5 h,伴大汗、呕吐1次”于2021年2月17日就诊于中国人民解放军南部战区总医院。患者既往高血压病史1年,未服用降压药。入院急诊行胸腹CT血管造影(CT angiography,CTA)示:主动脉夹层(Debakey Ⅲ型),破口位于左锁骨下动脉(left subclavian artery,LSA)开口后2 cm,螺旋撕裂至双侧髂动脉,假腔较大,真腔受压显著(图1A)。于2月18日8:00行主动脉腔内隔绝术,术中于胸主动脉置入34 mm×34 mm×200 mm(美敦力公司)覆膜支架1枚,因假腔太大,支架远端真腔仍严重受压,为降低截瘫风险于远端接24 mm×24 mm×70 mm裸金属支架1枚(波科公司)进行限制(图1B~D)。患者术后疼痛感明显好转,但出现间断发热,体温最高38.7℃,查降钙素原3.2 ng/ml,C-反应蛋白(C-reactive protein,CRP)183 ng/L,予哌拉西林4.5 g、每隔8 h用药1次抗感染治疗,后体温波动于36.2℃~38.0℃。3月3日患者因单位工作原因签字离院。
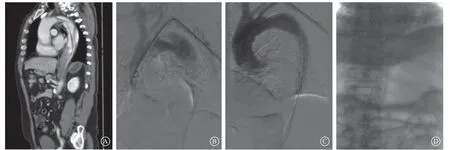
图1 第1 次住院(2021-02-17)主动脉CTA 及造影图像 A.术前主动脉CTA 示Debakey Ⅲ型主动脉夹层,破口位于LSA 开口后,呈螺旋形撕裂,假腔较大,真腔明显受压;B.第一次TEVAR 术前主动脉造影提示Ⅲ型主动脉夹层;C.第1 次TEVAR 于LSA 开口后置入34 mm×34 mm×200 mm覆膜支架;D.于覆膜支架远端接1 枚24 mm×24 mm×70 mm 裸金属支架Figure 1 Aortic CTA and angiography images at the f irst hospitalization (2021-02-17)
1.2 第2次住院
出院当日(3月3日)晚间21:00患者突发上腹痛,位于剑突下,伴呕吐,呕吐物为胃内容物,立即返回中国人民解放军南部战区总医院急诊。急查胸腹主动脉CTA示:左侧新发大量胸腔积液,结合覆膜支架远端形态考虑主动脉被支架远端扎破渗血可能,遂急诊入导管室行主动脉造影,于原覆膜支架远端裸金属支架近端接34 mm×28 mm×160 mm覆膜支架1枚(微创公司,图2A~C)。术后患者症状明显缓解,但仍有发热,体温最高39℃,予注射用亚胺培南西司他汀钠1 g、每隔8 h用药1次抗感染治疗48 h后,体温无下降趋势。3月6日加用万古霉素1 g、每隔8 h用药1次,体温逐渐下降,3月15日体温降至36.5℃~37℃。患者无不适,于3月20日出院,出院前复查降钙素原1.39 ng/ml,白细胞计数8.77×109/L,中性粒细胞百分比71.1%,血红蛋白71 g/L,CRP 106 ng/L。出院后患者感乏力,未诉发热等不适,3月下旬开始出现纳差,3月29日门诊复查主动脉CTA示(图3A):胸腔积液较前吸收,主动脉未见渗漏,嘱继续观察。
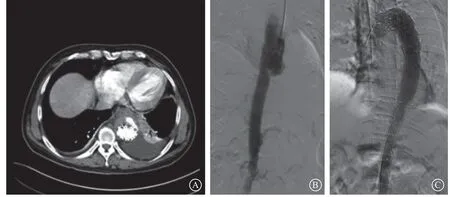
图2 第2 次住院(2021-03-03)主动脉CTA 及造影图像 A.胸部CTA 提示左侧新发大量胸腔积液;B.急诊主动脉造影提示覆膜支架远端主动脉可疑损伤渗漏;C.在原覆膜支架远端接34 mm × 28 mm × 160 mm 覆膜支架Figure 2 CTA and angiography of aorta in the second hospitalization (2021-03-03)
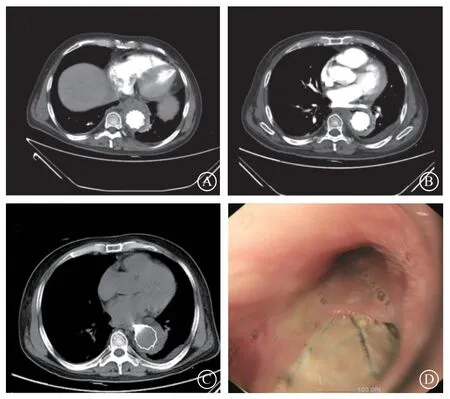
图3 主动脉CTA 联合胃镜检查图像 A.第2 次出院后10 d(2021-03-29)复查主动脉CTA 无渗漏迹象;B.第3 次入院(2021-05-05)主动脉CTA 提示食管紧贴主动脉支架且支架外侧缘可疑气泡影;C.(2021-05-06)口服对比剂后CT 平扫提示主动脉支架内侧有滞留;D.(2021-05-07)胃镜检查提示食管瘘口内可见支架,表面覆盖白色分泌物Figure 3 Images of aortic CTA combined with gastroscopy
1.3 第3次住院
4月2 8日患者因纳差、乏力加重,再次入院中国人民解放军南部战区总医院。入院后急查红细胞计数1.91×1012/L,血红蛋白50 g/L,白细胞计数10.63×109/L,中性粒细胞百分比71.2%,降钙素原0.10 ng/ml,立即输O型红细胞悬液2 U。入院后患者反复出现发热,体温波动在37.4℃~38.8℃,复查降钙素原仍正常,但CRP 112 ng/L。5月5日行主动脉CTA(图3B)示:T6~T7水平食管与主动脉紧邻无间隔,支架外侧缘可见可疑气泡影,不排除移植物感染合并主动脉食管瘘(aortoesophageal fistula,AEF)可能,考虑主动脉支架感染的可能。于5月6日上午行食管吞对比剂透视检查,但对比剂在食管通过太快,未捕捉到阳性结果,考虑到如果有对比剂渗出食管外应该会滞留,于是立即换至另外检查室行主动脉CT平扫(图3C),发现T6~T7水平食管左后侧壁对比剂与金属网格相贴及少许对比剂外渗沿降主动脉支架右旁分布,高度怀疑食管瘘。立即安排次日胃镜检查(图3D),结果提示食管距门齿32~34 cm见两处瘘口,大小0.5~2.0 cm,大瘘口内可见支架,负压吸引可见白色分泌物。患者最终移植物感染合并AEF诊断明确,跟家属谈话须行外科手术,手术复杂,经多医院、多学科会诊后家属决定转外院实施外科胸腹主动脉重建加移植物切除术。
1.4 转院手术
患者转至外院后先行抗生素充分抗感染治疗,制定方案后手术分两期完成,第1期于5月24日完成,全身麻醉下分别行升主动脉+腹主动脉、无名动脉、左颈总动脉、左锁骨下动脉转流术(图4),主动脉弓及胸主动脉远段离断术+空肠造瘘术,手术顺利;第2期手术于6月8日完成,于全身麻醉下行感染支架取出术+胸主动脉切除术+食管瘘修补术,手术顺利。术后予抗炎补液对症支持治疗,恢复良好,无发热,无不适。患者于7月26日康复出院,随访至今无不适。
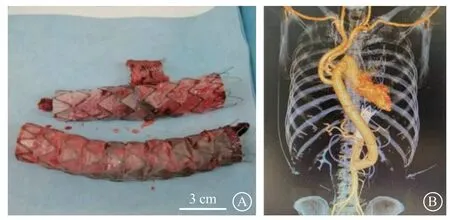
图4 外科手术后检查图像 A.外院手术取出的所有支架;B.转外院后行去分支+升主动脉-腹主动脉转流术Figure 4 Post-surgical examination images
2 讨论
对于胸降主动脉疾病的治疗,胸主动脉腔内修复术(thoracic endovascular aortic repair,TEVAR)因免于开放性外科手术和良好的中远期疗效,已成为首选治疗方法[1-2]。移植物感染和AEF是TEVAR罕见但严重的术后并发症。TEVAR术后移植物感染发生率为1.53%~4.77%[3-4]。移植物感染的主要原因包括:(1)手术路径带入细菌;(2)术中因无菌操作不严格导致细菌从器械带入体内致移植物污染;(3)主动脉夹层附壁血栓及血肿内存在其他部位移行的细菌;(4)身体其他部位的感染源通过血行或局部扩散感染移植物,如泌尿系统感染、肺部感染等;(5)患者自身存在糖尿病、自身免疫疾病等引起抵抗力低下的因素,体内定植菌群即可引起感染。AEF是TEVAR术后更为罕见的并发症,为继发性食管瘘,其发生率为1.9%[5],但死亡率达90%以上,临床表现缺乏特异性,多表现为呕血、胸背痛、吞咽困难、发热等[6-7]。随着瘘口的增大,食物渗入纵隔引起纵隔感染加重甚至出现化脓,感染一旦累及动脉将发生破裂引起大出血,因此对于AEF要早发现、早治疗,才能减少严重不良事件的发生。AEF发生的原因可能有:(1)金属支架或者增大的主动脉压迫食管的分支血管引起食管缺血性坏死;(2)食管被支架金属梁持续机械性压迫引起坏死;(3)支架感染灶蔓延至食管并直接侵蚀食管壁[8-10]。
本病例报道的患者同时出现两种并发症,诊疗过程中症状和临床指标均不典型,给诊疗带来巨大的困难和挑战。考虑先发生移植物感染,后发生AEF。虽然引起这两种并发症的可能原因很多,但就本病例而言,其原因具体分析如下。患者第1次入院顺利完成TEVAR,但术后反复出现发热、纳差、乏力,不同于常见的置入后综合征(post implantation syndrome,PIS),因为PIS多为自限性,而本病例发热迁延不愈,白细胞计数和降钙素原反复升高,经过头孢类和碳青霉烯类抗生素治疗,患者降钙素原下降,表明使用抗感染诊疗有效,但患者降钙素原和CRP反复升高,可能感染控制不彻底,未长期服用抗生素变为慢性炎症。患者发生感染的原因最大可能为患者假腔较大,同时第2次入院时合并左侧胸腔积液,这两种情况给细菌准备了较好的天然培养基,细菌来源一方面可能为肺部细菌的迁移,同时不排除介入手术路径可能通过血液携带少量细菌,其次患者术后纳差抵抗力低下也有关系。至于发生AEF的原因,考虑与食管营养血管受压、金属支架紧挨食管产生一定的压迫、感染蔓延至食管发生侵蚀均有关系。本病例报道的患者较为特殊的情况是,促使患者最终就诊的原因是重度贫血,临床表现为乏力和纳差。入院后筛查贫血原因未能发现明确原因,最终分析可能原因为较长时间发热消耗,以及纳差导致摄入不良,同时AEF的出现加重了患者的贫血,因此TEVAR术后长期慢性严重贫血需警惕移植物感染的可能。
此外,本病例报道的患者后期一直无胸背痛,AEF表现不典型,诊断难度相对较大,反复阅读并对照多次的CT片才怀疑有无AEF可能。因此移植物感染诊断需综合临床表现、影像学、实验室检查等多方面决定。虽然血培养是一个相对可靠的指标,但毕竟只有部分患者血细菌培养为阳性。提示移植物感染的证据在CT影像常表现为瘤壁增厚伴强化,瘤体周围液体集聚,可见气泡影等,但这类影像并不常见或同时出现,该患者仅在支架边缘存在一点点可疑的小气泡影。因为患者持续发热及红细胞沉降率持续升高,排除其他原因后才怀疑移植物感染,同时因食管紧贴支架怀疑AEF的可能,后续进行了针对性检查,先行食管吞对比剂检查,发现可疑外渗影,然而对比剂在食管停留时间太短,未能获得理想的结果,考虑到如果对比剂渗入食管外应该滞留,因此立即送患者入CT室平扫,在主动脉外侧可见高密度影,至此诊断才基本明确。为了明确AEF部位,次日送患者行胃镜检查明确了食管瘘的部位以及面积。
移植物感染单纯行内科保守治疗效果较差,有研究显示短期病死率超过70%,长期随访显示患者全部死于主动脉病变[11]。因此,外科切除感染组织及支架成为目前公认的主要治疗手段[12-13],但其早期手术病死率依然高达47%。对于病情轻、感染局限的患者可以先采用保守治疗,但是移植物感染可能同时存在多种致病菌混合感染,早期常难以确定致病菌,最重要的是感染灶位于动脉壁与支架之间密闭腔隙内,静脉或者口服使用抗生素很难到达病原菌部位,因此难以彻底消灭感染灶,中长期预后较差,很多病例后期仍需要外科手术干预。目前比较可行也比较常用的方法是充分抗感染的基础上进行外科手术,主要目的是促使炎症局限,为手术创造条件。而本病例诊断为移植物感染同时发现AEF,保守治疗几乎成为不可能,因此果断作出建议外科切除移植物的决定,没有尝试抗生素为主的保守治疗。因手术较为复杂最终手术分两期完成,制定正确的治疗策略患者最终才得以康复出院。
最后要强调的是,对于移植物感染最关键的是预防,具体而言手术操作环境应该严格消毒,手术人员应该严格遵守无菌操作规程,对于术前存在感染的患者应尽量在得到严控制后再行TEVAR,术后发生其他部位感染的患者,应积极使用敏感抗生素尽快控制感染。
利益冲突所有作者均声明不存在利益冲突

