重度肺动脉高压并发自发性三尖瓣腱索断裂2例并文献复习
杨静 黎婧怡 荆志成
三尖瓣腱索断裂临床上少见,常见的原因包括胸部闭合伤、感染性心内膜炎、心肌梗死、医源性损伤[1-3]。自发性三尖瓣腱索断裂罕见,其中重度肺动脉高压作为其基础病因文献中偶有报道[4]。现综合分析北京协和医院2例患者的资料并查阅相关文献,探讨其临床特点和治疗方法,加深医师对这一临床危重疾病的认识。
1 资料与方法
查阅北京协和医院收治的2 例重度肺动脉高压并发自发性三尖瓣腱索断裂患者的临床资料;同时以“Tricuspid valve chordal rupture and pulmonary hypertension or Tricuspid valve papillary muscle rupture and pulmonary hypertension”为检索词在美国生物医学文献数据库(PubMed)中检索到3例临床资料完整病例报道(除外新生儿)。对这5例患者临床资料结合相关文献进行综合分析。
2 结果
2.1 北京协和医院病例资料
病例1 女,44岁。因“水肿、气促4年,发作性意识丧失半个月”于2020年12月8日入住北京协和医院。患者于2016年出现进行性加重水肿,气促,活动耐量明显下降,步行100 m后需休息。2017年就诊外院,入院查体血压102/76 mmHg(1 mmHg=0.133 kPa)。CT肺动脉造影(CT pulmonar y angiography,CTPA)及肺血管造影未见明确狭窄、充盈缺损或闭塞性病变,诊断为特发性肺动脉高压。右心导管检查示:肺动脉压力(pulmonary artery pressure,PAP)105/53/72 mmHg,肺血管阻力(pulmonary vascular resistance,PVR)13.25 Wood Unit。超声心动图示:重度肺动脉高压(估测肺动脉收缩压115 mmHg),右心增大(右心室前后径41 mm),右心室收缩功能减低[右心室三尖瓣环收缩期位移(tricuspid annular plane systolic excursion,TAPSE)11 mm],轻度三尖瓣关闭不全。给予安立生坦5 mg、每日1次,他达拉非20 mg、每日1次(2019年自行改为西地那非50 mg、每日1次),靶向治疗及强心、利尿等对症治疗。患者症状改善,N末端B型脑钠肽前体(amino-terminal probrain natriuretic peptide,NT-proBNP)由入院3 471 pg/ml下降至2 543 pg/ml。出院后长期服药,病情稳定,轻度下肢水肿,可步行1 000 m,爬6层楼,未规律复查超声心动图。2020年11月,患者晨起进食时剧烈呕吐,随后发作意识丧失,口唇发绀,二便失禁,约1分钟后患者清醒,随后水肿、气促明显加重,无法行走,为进一步诊治收入北京协和医院。病程中无发热、胸痛。入院查体:体温36.4 ℃,血压78/47 mmHg,呼吸18次/分,血氧饱和度(oxygen saturation of blood,SpO2)83%,全身皮肤、巩膜黄染,四肢末端厥冷,心界扩大,心率89次/分,心律齐,P2亢进,胸骨左缘可闻及4级收缩期吹风样杂音,双下肢膝以下重度可凹性水肿。血气分析示:pH 7.48,二氧化碳分压(partial pressure of carbon dioxide,PCO2)22 mmHg,氧分压(arterial partial pressure of oxygen,PO2)51 mmHg,乳酸2.8 mmol/L,NTproBNP 6 423~9 690 pg/ml,心肌肌钙蛋白I(cardiac troponin I,cTnI)0.023~0.067 µg/L。化验检查示:肝肾功能不全,血尿素氮16.84 mmol/L,血肌酐122 µmol/L,总胆红素98.8 µmol/L,直接胆红素80.5 µmol/L,丙氨酸氨基转移酶正常。心电图示:窦性心律,右心室肥厚。超声检查示:双侧胸腔积液、大量腹腔积液。超声心动图示:右心明显增大,右心室基底部横径61 mm,三尖瓣前叶收缩期“连枷样”脱入右心房(图1),超大量三尖瓣反流(图2),估测肺动脉收缩压为60 mmHg,TAPSE 19 mm,少量心包积液。CTPA提示左肺动脉主干及左肺动脉多发血栓。考虑患者存在重度肺动脉高压、三尖瓣前叶腱索断裂、重度三尖瓣关闭不全、心功能不全、心原性休克、肺动脉原位血栓形成。给予储氧面罩吸氧,应用多巴胺、去甲肾上腺素、新活素等多种血管活性药物及其他对症支持治疗,加用利伐沙班15 mg、每日1次抗凝治疗,同时逐渐调整药物至安立生坦5 mg、每日1次,他达拉非30 mg、每日1次,加用曲前列尼尔静脉及皮下泵入序贯加量,皮下泵入最终剂量15 ng/(kg.min)治疗肺动脉高压。患者症状有一定程度缓解,可室内轻微活动,血压98/61 mmHg,SpO292%(储氧面罩吸氧5 L/分),复查NT-proBNP 4 379 pg/ml,cTnI 0.023 µg/L,总胆红素31.7 µmol/L,直接胆红素15.8 µmol/L,血肌酐81 µmol/L。右心导管检查示:PAP 58/36/43 mmHg,右心房压(right atrial pressure,RAP)32/8/19 mmHg,PVR 18.75 Wood Unit。转外科计划行三尖瓣手术及房间隔造口术,多科会诊认为手术风险极大,药物治疗病情稳定后转外院行肺移植手术,术后死于感染性休克。
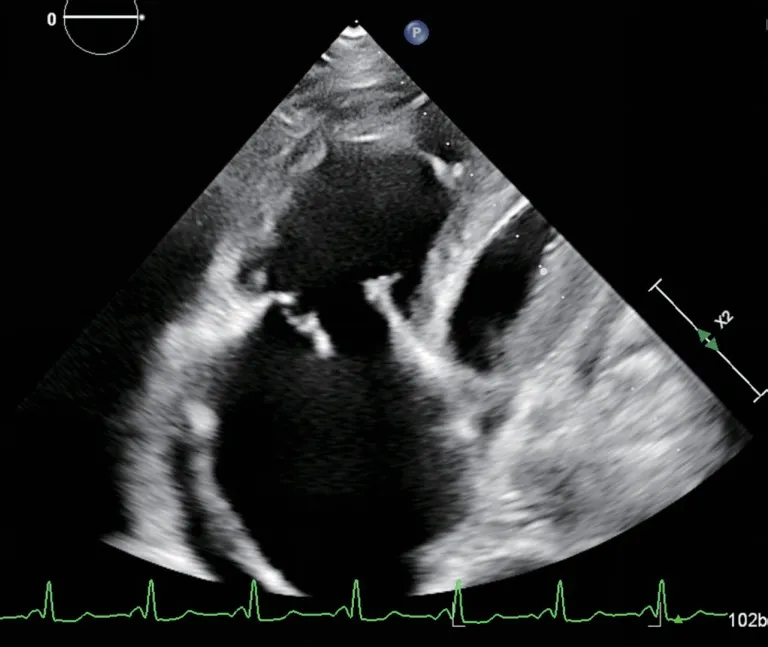
图1 病例1 胸骨旁四腔心切面显示收缩期三尖瓣前叶呈“连枷样”脱入右心房Figure 1 Case 1:Parasternal fourchamber view shows that the anterior leaf let of the tricuspid valve "f lails" into the right atrium during systole
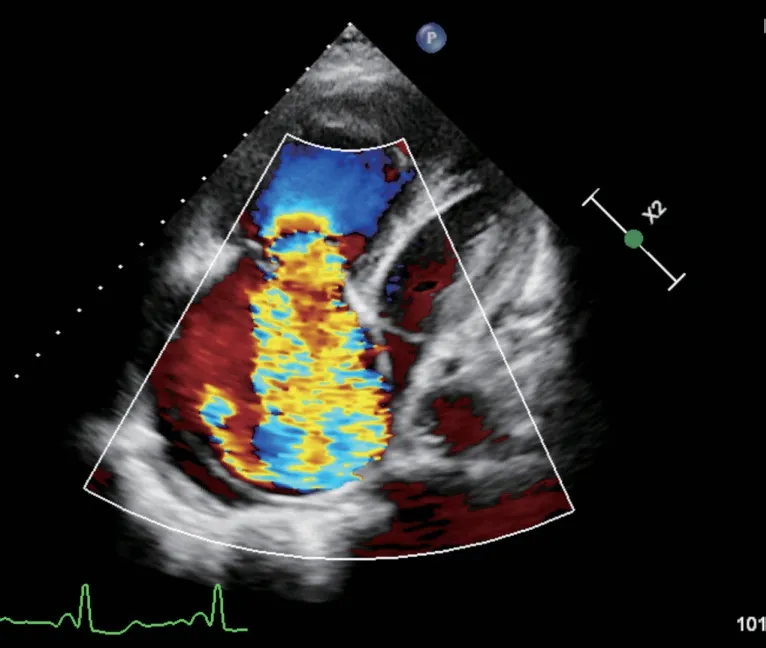
图2 病例1 胸骨旁四腔心切面显示收缩期三尖瓣超大量反流Figure 2 Case 1:Parasternal fourchamber view showing excessive systolic tricuspid regurgitation
病例2 男,51岁。因“气促、水肿9年,加重2个月”于2021年7月12日入住北京协和医院。患者于2012年出现气促、水肿,不能平卧,就诊于外院,诊断为特发性肺动脉高压。右心导管检查示:PAP 78/36/50 mmHg,PVR 7.6 Wood Unit。超声心动图示:右心房增大,重度三尖瓣关闭不全,TAPSE 19 mm。先后给予吸入用伊洛前列素溶液(万他维)、安立生坦、波生坦、利奥西呱、他达拉非、马昔腾坦口服及曲前列尼尔皮下泵入治疗肺动脉高压。患者病情仍有进展,复查超声心动图示:PAP无下降,右心室进行性增大,三尖瓣重度关闭不全,肺动脉瓣中度关闭不全,TAPSE下降至10~13 mm,少量心包积液。相关医院除外肺移植可能,期间行冠状动脉CT血管造影(CT angiography,CTA)示:冠状动脉左前降支及右冠状动脉轻度狭窄。2021年6月患者症状再次加重时就诊外院复查超声心动图见三尖瓣前叶异常条索回声(赘生物可能),超大量三尖瓣反流,中-大量心包积液,肺动脉收缩压80 mmHg,大量腹腔积液。为进一步诊治收入院,入院查体:体温36.6℃,血压89/57 mmHg,呼吸急促SpO292%(鼻导管吸氧5 L/分),口唇发绀,杵状指/趾,双肺散在哮鸣音,心界扩大,心率102次/分,心律不齐,P2亢进,胸骨左缘可闻及4级收缩期吹风样杂音,腹部膨隆,移动性浊音(+),双下肢无水肿。入院后体温正常。连续两次血培养阴性。血气分析(吸氧条件下)示:pH 7.51,PCO229 mmHg,PO257 mmHg,乳酸1.2 mmol/L,NT-proBNP 5 926 pg/ml,cTnI 0.028 µg/L,肝肾功能正常范围。心电图示:心房颤动、右心室增大、室内阻滞、肢体导联低电压。复查超声心动图示:肺动脉收缩压63 mmHg,右心明显增大,右心室基底部横径61 mm,三尖瓣前叶部分瓣叶收缩期“连枷样”脱入右心房,考虑三尖瓣前叶腱索断裂,右心室收缩功能减低(TAPSE 12 mm),大量心包积液。入院后给予吸氧,入院时靶向药物马昔滕坦10 mg、每日1次,他达拉非40 mg、每日1次,曲前列尼尔皮下泵入30 ng/(kg.min)。继续降肺动脉压及对症支持治疗。并于入院后11天行球囊房间隔造口术(balloon atrial septostomy,BAS),造口直径8 mm左右,术中右心导管检查示:PAP 64/40/50 mmHg,RAP 27 mmHg,PVR 12.27 Wood Unit。术后当日SpO2较术前下降,储氧面罩吸氧15 L/分,SpO266%~68%,给予BIPAP呼吸机支持后升至80%~90%;次日改为储氧面罩吸氧10 L/分,SpO280%~89%;第3天鼻导管吸氧5 L/分,SpO280%~84%,同时加强利尿治疗。术后2天尿量明显增多,由1 350 ml增至3 900 ml,NT-proBNP 3 858 pg/ml。术后1周复查超声心动图示:房间隔水平右向左分流,分流束6~7 mm,房间隔凸向左心房程度明显减轻(图3~5)。患者病情稳定出院,出院后间断在当地医院住院治疗,到2022年10月23日为术后15个月,密切随访中。

图3 病例2 胸骨旁四腔心切面球囊房间隔造口术前见右心房球形扩张,房间隔明显凸向左心房Figure 3 Case 2:Spherical dilation of the right atrium and prominent protrusion of the atrial septum to the left atrium were seen on the parasternal four-chamber view before the balloon atrial septostomy
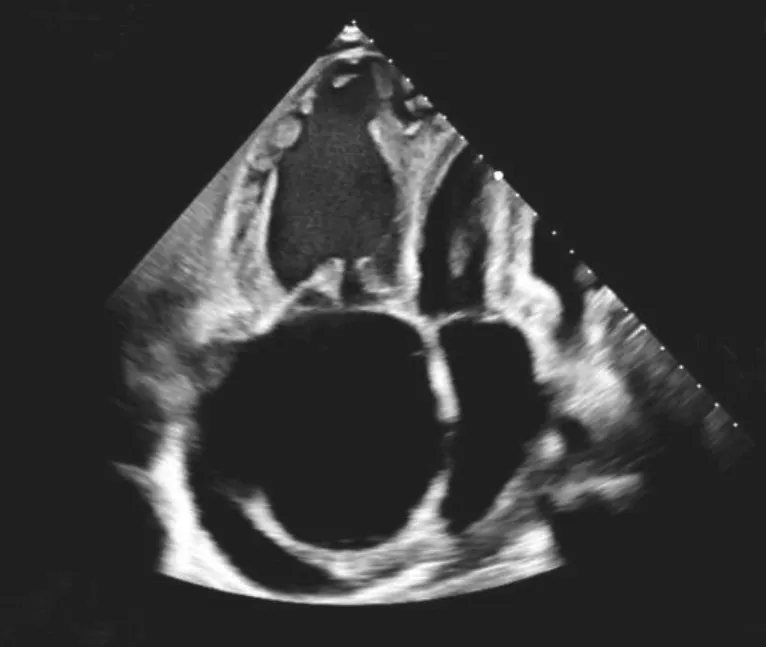
图4 病例2 四腔心切面球囊房间隔造口术后1 周,右心房球形扩张减轻,房间隔凸向左心房程度减轻Figure 4 Case 2:One week after the balloon atrial septostomy on the fourchamber view,the spherical dilation of the right atrium was reduced,and the degree of atrial septal protrusion to the left atrium was reduced
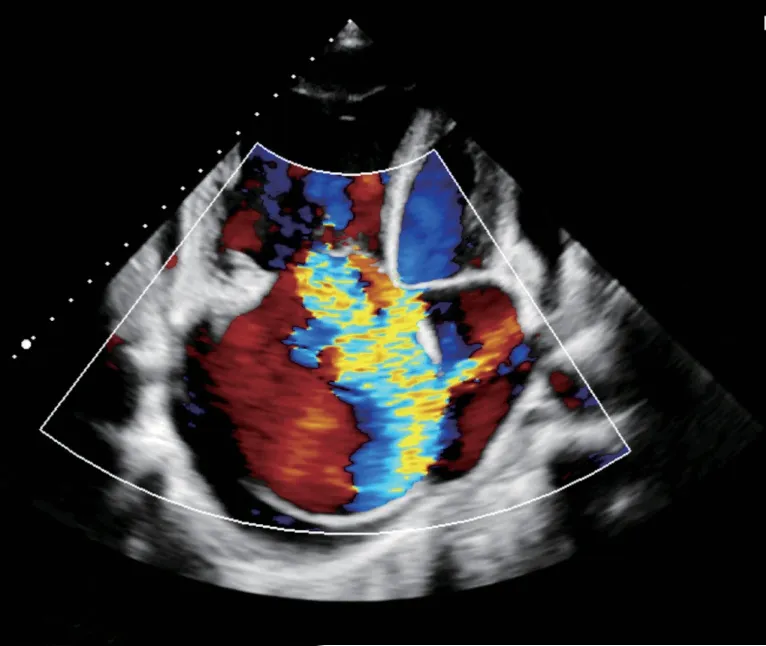
图5 病例2 四腔心切面见三尖瓣大量反流及经房间隔造口处分流至左心房的分流束Figure 5 Case 2:A large amount of tricuspid regurgitation and a shunt bundle from right atrium to the left atrium via atrial septostomy were seen on a four-chamber view
2.2 数据库中病例资料
病例3[4]女,28岁。特发性肺动脉高压,药物治疗效果不佳,计划肺移植,移植前评估超声心动图示:三尖瓣叶轻度增厚,轻度三尖瓣关闭不全,右心增大,右心室收缩功能减低,TAPSE 14 mm。2个月后病情突然恶化,心原性休克,胸骨右缘新发响亮的收缩期杂音,超声心动图示:新发三尖瓣前叶腱索断裂,三尖瓣重度关闭不全,右心室收缩功能指标TAPSE升至20 mm,考虑为右心室功能容量依赖性代偿性增强,计划病情稳定后同期行肺移植手术以及三尖瓣手术,但患者病情进展快,4周时死于心原性休克和多脏器功能衰竭。
病例4[5]男,42岁。人类免疫缺陷病毒治疗中,进行性加重呼吸困难2个月,未规律诊治。就诊时表现为 心原性休克和严重右心衰竭,超声心动图示:三尖瓣前叶脱垂,大量三尖瓣反流,肺动脉收缩压75 mmHg。多种血管活性药物及降肺动脉压靶向治疗效果不佳,急诊行三尖瓣生物瓣置换,术中见三尖瓣前叶腱索断裂,术后PAP升高,积极降肺动脉压治疗后缓解,随访病情稳定。
病例5[6]男,25岁。有劳力性气促病史3年,原因不详。就诊前8个月骑车时突发胸部不适、气短加重,活动耐量明显下降,病情进行性加重,查体心前区闻及5级收缩期杂音。病例报告于1980年,缺乏超声心动图资料。就诊后不久出现心原性休克,心导管及心室造影检查提示PAP升高,82/56/64 mmHg,右心增大,三尖瓣大量反流。2天后死于心原性休克,尸检证实患者存在慢性肺动脉高压,三尖瓣隔叶乳头肌和腱索连接处断裂,病理可见片状纤维化,而且断裂乳头肌和其他右心室心肌无论大体病理还是组织学检查均无明显差异。
3 讨论
三尖瓣腱索断裂多见于胸部闭合伤、感染性心内膜炎、心肌梗死、医源性损伤[1-3]。本研究中,各病例无外伤史,体温正常,心电图及心肌酶不符合心肌梗死的演变,发病之前无介入操作史,可排除以上原因引起的三尖瓣腱索断裂。其三尖瓣腱索断裂的原因考虑为重度肺动脉高压继发自发性腱索断裂,可能的机制有以下几点:右心室重构扩张牵拉瓣叶、腱索和乳头肌使其张力明显增加易于受损;肺动脉高压患者慢性缺氧进一步增加断裂可能性。5例患者中有4例腱索断裂发生在三尖瓣前叶,考虑与右心室向三尖瓣前叶方向扩张明显相关。
三尖瓣反流在肺动脉高压患者中常见。Chen等[7]前瞻性分析了727例1型肺动脉高压患者,其中96.5%(702例)患者有三尖瓣反流,包括中度三尖瓣反流患者279例和重度三尖瓣反流患者165例,三尖瓣反流的程度与肺动脉高压严重性和5年生存率相关。Medvedofsky等[8]的研究也证实肺动脉高压患者中三尖瓣反流程度的变化与肺动脉高压病情变化和右心重构相关。在这些病例中,三尖瓣反流多为功能性反流,与右心室重构、三尖瓣环扩张、乳头肌移位以及瓣叶牵拉相关[9]。本研究中,病例2最初几年病情进展的同时伴有三尖瓣反流增多以及右心室重构加重,与此相符。

表1 PAH 并发自发性三尖瓣腱索断裂病例资料Table 1 PAH complicated with spontaneous rupture of tricuspid valve chordae tendineae
三尖瓣腱索断裂时三尖瓣重度关闭不全,大量血液回流至右心房,超过其代偿能力时右心房压力和静脉压升高,表现为右心衰竭的症状和体征,同时右心室前向血流减少,而右心室容量负荷异常导致的右心室收缩功能障碍进一步加重了右心室前向血流减少,严重时会出现心原性休克。患者的临床表现与其基础疾病以及代偿能力有关,差异很大。重度肺动脉高压患者在长期压力负荷和不同程度容量负荷下多存在右心室重构扩张、心功能降低、三尖瓣反流、心脏代偿能力差,在此基础上出现三尖瓣腱索断裂,短时间内容量负荷显著增加和右心室前向血流减少。这种变化对于之前三尖瓣反流不严重的患者尤其明显,病情进展快,很容易出现心功能不全加重和心原性休克,如病例1和病例3。而对于之前就有中-重度三尖瓣反流的肺动脉高压患者,三尖瓣腱索断裂加快了患者病情的进展,如病例2。值得注意的是,超声检查中部分患者病情早期会出现右心室收缩功能指标容量依赖性增强,如病例1和病例3,TAPSE由降低变为正常,同时由于严重三尖瓣反流导致的前向血流减少,PAP测值较前下降,临床上在分析结果时应加以注意。总体而言,和无肺动脉高压患者相比,重度肺动脉高压患者心脏代偿能力差,出现急性三尖瓣腱索断裂后病情危重。本研究中大多数患者出现了心原性休克。
重度肺动脉高压并发自发性三尖瓣腱索断裂患者治疗困难,针对三尖瓣情况,单纯药物治疗效果不佳,手术治疗是首选治疗方案,但患者存在严重的肺动脉高压和不同程度的心功能不全,手术治疗风险大。介入治疗方面,目前的指南对于存在重度肺动脉高压及严重右心室扩张及心功能不全的患者不推荐[10],国内开展的机构不多,技术方面不成熟。本研究组认为应针对每个患者的具体情况制订治疗方案。对于三尖瓣腱索断裂前、病情稳定、三尖瓣反流不重、心功能代偿的患者,尽快手术治疗应该是首选方案,如病例4三尖瓣置换术结合围术期积极降低肺动脉压治疗取得了很好的效果。对于有肺移植适应证的患者,联合心肺移植或单纯的肺移植加上手术治疗三尖瓣病变理论上可以作为患者最后的治疗选择,但由于供体以及技术上的限制,实施起来困难。由于急性严重三尖瓣反流的存在,单纯的肺移植是否能够改善预后资料有限。
BAS是难治性肺动脉高压合并右心衰竭患者的一种姑息治疗,通过心房水平的右向左分流,降低RAP和右心室舒张末期压力,改善右心功能,缓解体循环静脉淤血,同时增加左心灌注,提高心排量。由于右向左分流会引起体循环动脉SpO2下降,而且右心房压力越高,术后发生难治性低氧血症的风险越高,一般要求拟行BAS的患者静息时SpO2>90%,右心房压力10~20 mmHg[11]。病例2在三尖瓣腱索断裂前,病情危重,三尖瓣大量反流,而且无肺移植的条件,腱索断裂进一步加重了其病情,表现为顽固的右心功能不全。患者应用多种药物治疗效果不佳,虽然其不是最佳的BAS适应证,但在充分理解其病情的基础上,入院后第11天尝试给予患者BAS治疗,手术顺利。术后第1天患者出现短时间严重低氧血症,储氧面罩吸氧15 L/分,SpO266%~68%,经呼吸机治疗后很快缓解,第3天鼻导管吸氧5 L/分,SpO280%~84%,同时其尿量明显增多,临床症状轻度缓解,超声心动图示房间隔凸向左心房程度明显减轻。到2022年10月23日为BAS术后15个月,患者病情相对稳定。
肺动脉高压患者病情复杂,病例1在本次入院CTPA提示左肺动脉主干及左肺动脉多发血栓,结合病史考虑肺动脉内原位血栓形成,这也是其病情加重的一个因素。但结合整个病程来看,三尖瓣急性腱索断裂是本次病情加重的主要原因。
综上所述,自发性三尖瓣腱索断裂是重度肺动脉高压患者的少见并发症,患者病情危重,多进展为心原性休克,预后不佳;部分患者可以通过三尖瓣手术治疗缓解病情;心肺移植或单纯的肺移植加上手术治疗三尖瓣病变可能是此类患者最终的治疗方案,对于部分没有手术条件的患者,BAS可以作为一种姑息治疗的方法。临床医师应加强对此并发症的认识,结合患者具体病情尽快制订治疗方案。
利益冲突所有作者均声明不存在利益冲突

