ICP-OES内标法及标准加入法测定食品中铝
高喜凤,韩晓晓,赵寅,张寒霜,冉佼艳,刘艳明
山东省食品药品检验研究院,国家市场监管重点实验室(肉及肉制品监管技术),山东省食品药品安全检测工程技术研究中心,山东省特殊医学用途配方食品质量控制工程技术研究中心(济南 250101)
铝元素在地壳中的含量居第3位,仅次于氧和硅,是地壳中含量最丰富的金属元素,但是铝并不是人体必需的元素,多项医学研究表明,过量摄入铝对人体健康有着很大的危害,铝具有聚积性,会在大脑、肝、脾、肾、甲状腺等组织器官蓄积,容易导致阿尔茨海默症、婴幼儿智力障碍、肾功能障碍、骨质疏松、关节疼痛等疾病,过多的铝也会危及消化系统,影响人体对磷、铁、钙等营养元素的吸收[1-5],多项调查研究数据显示,食物是人体铝来源的最主要途径,特别是含铝添加剂的食物[6],油条、粉丝、糕点、水产品等食品在各地抽检监测中经常出现铝含量超卫生标准限量的情况,主要是因为食品在加工过程中过量使用明矾、泡打粉等含铝添加剂[7-9]。GB 2760——2014《食品安全国家标准 食品添加剂使用标准》中明确规定面制品等食品中添加剂的使用范围、用量和残留量,但是仍有不法商贩为了降低成本、改善卖相,在食品中违规使用含铝食品添加剂,造成铝含量超标,严重危害,因此加强对食品中铝的监管具有非常重要的意义。
GB 5009.182——2017《食品安全国家标准 食品中铝的测定》中规定4种铝的检测方法[10]:分光光度法、电感耦合等离子体质谱法(ICP-MS)、电感耦合等离子体发射光谱法(ICP-OES)和石墨炉原子吸收光谱法。分光光度法容易受到显色时间、显色稳定、溶液酸碱度和体系内其他成分的干扰,试验操作繁琐、灵敏度低[11-13];石墨炉原子吸收光谱法测定铝存在着非光谱干扰,导致测定灵敏度降低和干扰增加[14-17];ICP-MS法具有检出限低、动态线性范围宽、干扰少、精密度高、分析速度快等明显优势[18-20],但由于仪器价格昂贵,使用成本太高,普及性不广;而ICP-OES法具有线性范围宽、试剂用量少、结果重现性好等优点,被企业和检测机构广泛应用于食品中铝的测定,但是由于ICP-OES法测定铝容易出现谱线重叠干扰或基体效应的干扰,致使测定值偏高,因此如何应用电感耦合等离子体发射光谱法准确测定食品中的铝非常重要。
ICP-OES内标法根据分析元素与内标元素在等离子体中的行为相似,可在很大程度上抵消由于分析条件波动引起的谱线强度波动等因素带来的影响,从而改善方法的精密度提高测定的准确度。标准加入法可以最大限度地消除基体干扰,当样品基体成分很高,而且变化不定或样品中含有固体物质而对吸收的影响难以保持一定时,采用标准加入法非常有效。
由于单纯采用外标法不能够很好地解决电感耦合等离子体发射光谱法存在的光谱干扰现象和基体影响,试验建立内标法和标准加入法2种方法,对ICPOES测定食品中铝进行方法优化和改进,并应用ICPMS法进行结果比对验证,为准确应用电感耦合等离子体发射光谱法测定食品中的铝提供技术保障。
1 材料与方法
1.1 材料与试剂
硝酸、盐酸、30%过氧化氢(优级纯,国药集团化学试剂有限公司);铝标准溶液、钇标准溶液(均为1 000 μg/mL,中国计量科学研究院);铟标准溶液、钪标准溶液(均为1 000 μg/mL,国家有色金属及电子材料分析测试中心);标准物质粉条(批号F0022308,北京曼哈格生物科技有限公司);硝酸(酸纯化仪纯化后使用)。
1.2 仪器与设备
Optima 8000电感耦合等离子体发射光谱仪(美国PerkinElmer公司);Mars 6微波消解仪(美国CEM公司);Advantage A10超纯水机(美国密理博公司);MS204S电子天平(瑞士梅特勒-托利多公司,精度0.1 mg);FED240电热恒温鼓风干燥箱(上海新苗医疗器械制造有限公司)。
1.3 试验方法
1.3.1 样品前处理
称取0.5 g左右经过干燥、粉碎等手段进行预处理后的样品于聚四氟乙烯消解罐中,加入8 mL硝酸和1 mL过氧化氢进行微波消解,设定微波消解程序,见表1,消解完毕冷却后取出内罐,置于赶酸电热板上,140 ℃赶酸至近干,用超纯水定容至50 mL容量瓶中。

表1 微波消解程序
1.3.2 仪器工作条件
功率1 500 W;等离子体流量10 L/min;雾化器流量0.55 L/min;辅助气流量0.2 L/min;进样延迟30 s;选取Al 396.153 nm作为分析谱线进行测试。
1.3.3 标准溶液配制
1.3.3.1 内标法标准溶液
用体积分数2%的硝酸溶液将1 000 μg/mL的铝标准溶液逐级配制成质量浓度为0,0.10,0.50,1.00,1.50,2.00,5.00,10.00和20.00 μg/mL的一系列标准溶液,并分别取0.1,0.2,0.4和0.5 mL 1 000 μg/mL的钪、铟、钇内标溶液至50 mL的铝标准系列中,配制成内标浓度分别为2,4,8和10 μg/mL的铝标准系列溶液。
测定标准曲线溶液中铝元素的信号响应值,以各标准曲线溶液中铝元素与内标元素响应信号值的比值为纵坐标,铝元素浓度为横坐标,绘制标准曲线。
1.3.3.2 标准加入法标准溶液
将微波消解前处理后的实际样品溶液均分成6份,第1份样品溶液不加入铝标准溶液,另外5份样品溶液分别加入100 μg/mL的铝标准溶液,使加标的溶液质量浓度分别为0.10,0.50,1.00,1.50和2.00 μg/mL,将未加标样品作为标准零点处理到标准溶液中,加标曲线反向延长线对应的浓度即为样品溶液中铝的浓度。
2 结果与分析
2.1 分析谱线的选择
铝的常见分析波长有396.153,308.215,394.401,237.313和309.271 nm,以2.0 μg/mL的铝标准溶液作为测试液,在仪器最佳条件下,观察各谱线的干扰和背景影响情况,选择其中峰形窄、干扰少、背景值低、信噪比高的谱线396.153 nm作为分析谱线进行测试。
2.2 内标元素及浓度的选择
ICP-OES中普遍存在基体效应,内标法和标准加入法是消除基体效应引起的非光谱干扰的主要手段[21-23],内标法是根据分析谱线相对强度进行定量分析,可使由光源波动引起的谱线强度变化得到补偿,从而消除干扰。一般的内标元素有Sc、In、Tb、Lu、Re、Rh、Bi和Y,试验选取Sc、In和Y进行内标法研究和结果比对,因为其与铝元素有相近的蒸发性质、相近的激发电位和电离电位,相近的光谱背景影响[24]。
按照1.3.1的方法配制成内标元素钪、铟、钇质量浓度分别为2,4,8和10 μg/mL的铝标准系列溶液,并制作标准溶液工作曲线。
选取购买的标准物质粉条(铝标示值169±17 mg/kg),在85 ℃电热恒温鼓风干燥箱中干燥4 h后进行称样测定,样品溶液同样与内标溶液相匹配,并对样品进行3次加标回收测定,测定结果如表2。

表2 不同内标溶液的加标回收情况(n=3)
分析数据发现,Y作为内标元素浓度为4~10 μg/mL时,加标回收率较好、检测结果与质控样中位值更接近,由于选择内标元素时,内标元素的浓度在100倍检出限时为最佳[25],试验测得仪器Y的检出限为30 μg/L,所以选择Y作为ICP-OES测定铝的内标元素,将内标Y的浓度确定为4 μg/mL。
2.3 方法学验证
2.3.1 线性方程、相关系数
应用ICP-OES对标准溶液进行测定,线性相关系数如图1~图3所示。R2大于0.999,说明无内标和选用内标Y的质量浓度在4.0 mg/L时,在0.10~20.0 μg/mL的浓度范围内、标准加入法0.10~2.0 μg/mL的质量浓度范围内均呈现良好线性关系。

图1 外标法标准溶液工作曲线
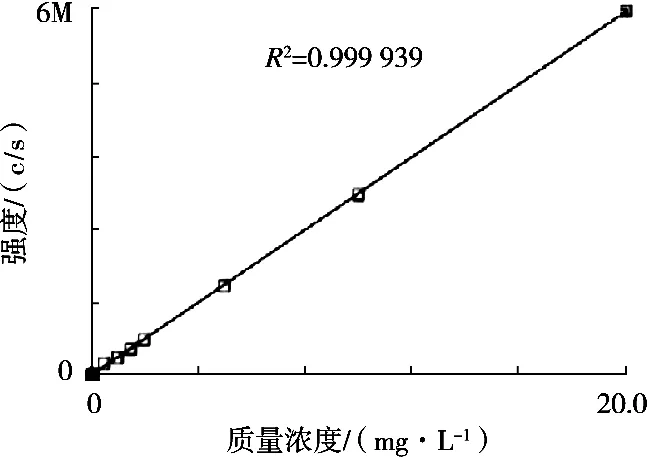
图2 内标Y为4.0 mg/L时标准溶液工作曲线

图3 标准加入法标准溶液工作曲线
2.3.2 方法一致性研究
选用小麦粉、粉条等不同基质、不同含量水平的样品进行样品的微波消解前处理,通过ICP-OES外标法、内标法和标准加入法进行检测分析,并应用ICPMS法进行方法一致性验证。
验证结果如表3所示,应用ICP-OES外标法质控样检测值不在标准要求范围内,相对误差(SRE)、加标回收率均不符合GB/T 27404——2008《实验室质量控制规范》的要求,ICP-OES标准加入法、内标法和ICP-MS法测定标准物质粉条的检测结果符合质控样的要求,加标回收率分别为94.2%~107.2%,95.7%~104.7%和96.7%~103.6%,均符合GB/T 27404——2008对于加标回收率的要求,且对每种样品进行5次平行测定,SRSD分别为4.82%,2.14%和1.54%,相对偏差小、方法精密度高,说明ICP-OES内标法、标准加入法和ICP-MS法均能准确测定食品中的铝。

表3 不同方法间结果比对
3 结论
试验通过选用不同基质的样品进行电感耦合等离子体发射光谱法测定食品中铝的方法研究,并将测定结果与电感耦合等离子体质谱法进行比对分析,对同一样品的测定,ICP-OES外标方法其测定值高于ICPMS的测定值,为此建立ICP-OES内标法和标准加入的方法测定食品中的铝,并进行质控样试验和加标回收试验,均满足实验室质量控制的要求。这2种方法精密度好、准确性高,能够有效解决ICP-OES可能存在的谱线重叠和基体效应的影响,是对电感耦合等离子体发射光谱法测定食品中铝的方法的优化和改进,从而更好地为企业和监管部门提供技术支持。

