微创Bentall手术新进展
高竣迪 谢进生
(首都医科大学附属北京安贞医院微创心脏外科中心,北京 100029)
微创心脏手术在临床上具有创伤小、切口美观,术后某些固有并发症减少且恢复快等特点。随着外科手术技术、麻醉管理水平,特别是材料科学领域的突破,心脏手术微创化已经成为未来心脏外科的主要发展方向。在主动脉根部病变复杂、主动脉瓣病变合并升主动脉扩张,尤其是主动脉瓣瓣叶质量欠佳无法保留时,通常需行主动脉根部置换术(Bentall手术),这是外科治疗此类疾病的首选术式[1-2]。近年来,在微创主动脉瓣置换术日渐成熟的基础上,越来越多的患者倾向于选择微创Bentall手术,以期追求更小的创伤和更加美观的手术切口,加快术后康复进程。
微创Bentall手术是在全胸骨正中切口基础上发展出来的一种新的术式,目前主要分为经正中部分胸骨入路和经右前外侧肋间入路两大类[3-4]。然而,与全胸骨正中切口相比,微创Bentall手术由于操作空间狭小、主动脉根部位置过深、工作距离增加,导致术野显露困难、操作难度增大、学习曲线更长,甚至可能延长手术时间、增加手术风险。目前国内外仅有少数心脏中心开展了此类手术,已有文献报道的队列样本量均较小,并且缺少远期随访结果。为更好地了解这一新技术,现从手术入路、手术技术、手术效果、手术适应证和禁忌证等方面对微创Bentall手术新进展进行综述。
1 经正中部分胸骨微创Bentall手术
1.1 手术入路
理论上讲,所有主动脉根部病变患者,均可通过全胸骨正中切口Bentall手术重建主动脉根部。近年来,随着微创主动脉瓣手术的日渐成熟,在严格把握手术适应证的前提下,可经正中部分胸骨切口行Bentall手术[5-6]。与全胸骨正中切口相比,该术式仅需行6~8 cm皮肤切口(如图1所示)、胸骨上半段或各种形状变化的部分胸骨切口,包括倒“T”形、“J”形、“L”形、“S”形部分胸骨切口,以及“Z”形、“I”形、“V”形小切口等[7-8]。由于冠状动脉开口通常位于第3肋间水平位置,因此上述切口可以充分显露主动脉根部和升主动脉,利于瓣环置线和冠状动脉再植[5]。与全胸骨正中切口相比,正中部分胸骨切口术后胸骨稳定性更高,利于减轻疼痛和改善呼吸功能[7,9],但二者在胸骨后感染发生率上并无显著差异[10]。
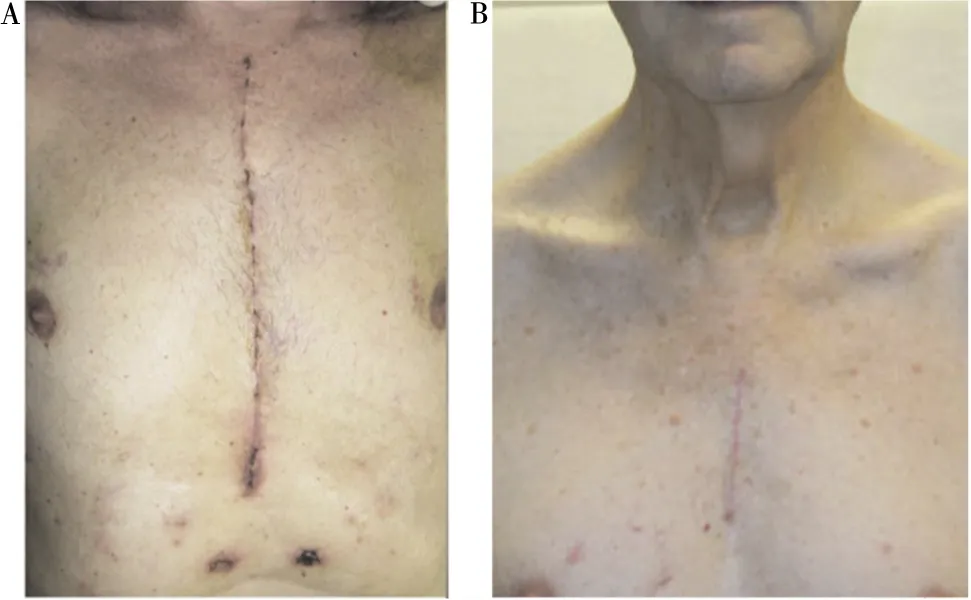
图1 全胸骨正中切口(A)与经正中部分胸骨切口(B)术后对比图[10]
1.2 手术技术
与全胸骨正中切口相似,经正中部分胸骨微创Bentall手术大多无需特殊器械,可经升主动脉和右心房直接插管建立体外循环;为保证足够手术操作空间,多通过股动脉、股静脉建立外周体外循环,此时利用负压辅助静脉引流装置可保证良好的静脉回流。手术方式同全胸骨正中切口基本相似。由于手术空间限制、操作难度增大,最初进行经正中部分胸骨微创Bentall手术多需较长的体外循环时间[(166.12±40.61)min vs (162.88±45.89)min]和主动脉阻断时间[(122.24±27.42)min vs (113.44±22.57)min],Hillebrand等[6]的研究便证实了这一结论。为了缩短体外循环时间和主动脉阻断时间,减少手术并发症,Mikus等[5]在术中使用了Cor-Knot自动打结器和康斯特(HTK)心肌停跳保护液,加快了手术进程。如果手术切口过小,难以操作常规的主动脉阻断钳,可于腋中线单独做皮肤切口,使用Chitwood主动脉阻断钳(Scanlan International,Inc,St Paul,MN USA)阻断主动脉[5],从而留出更大的操作空间。
经正中部分胸骨微创Bentall手术与全胸骨正中切口相同,一旦心脏复跳后出现不可控制的根部出血,常规缝合方法往往难以有效止血。虽然有文献报道,微创Bentall术后二次开胸止血率低于全胸骨正中切口[5-6],但仍有6.0%~12.5%的二次开胸止血可能[6,11]。针对止血困难的问题,除利用自体动脉壁联合自体心包包裹人工血管并与右心房建立分流外,还可以考虑采用Copeland等[12]提出的Bentall手术近端两层缝合方法:先将瓣膜缝合环近端与主动脉瓣瓣环间断缝合,然后再将瓣膜缝合环远端与近段残余升主动脉壁连续缝合。然而此法只适用于机械瓣带瓣管道;若使用生物瓣与人工血管组合带瓣管道,由于缝环过小,无法缝合两层。为解决这一问题,Yan等[13]提出了“French Cuff”技术:首先将人工血管近端向外翻转折叠,置入人工瓣膜后,瓣环缝线首先穿过人工瓣膜缝环,再穿过折叠的人工血管,下瓣、打结,完成近端第一层缝合;然后再将翻转折叠的人工血管游离缘与近端残余主动脉壁连续缝合。该方法既适用于机械瓣管道,也适用于生物瓣管道,同时还可用于再次主动脉根部手术和主动脉瓣瓣环严重钙化的患者,在行胸骨小切口Bentall手术时可以达到较为理想的止血效果,但上述两种方法在一定程度上可能会增加手术的复杂程度。此外,在仔细检查除外活动性出血之后,可应用“生物胶”辅助止血。
1.3 手术效果
经正中部分胸骨微创Bentall手术死亡率为0%~3%[5-7,10,14-16],切口美观,术后恢复更快、并发症较少、手术效果满意。Mikus等[5]和Abjigitova等[17]认为,与全胸骨正中切口相比,经正中部分胸骨微创Bentall手术后房颤发生率降低、机械通气时间更短。Shah等[14]的研究也指出,经正中部分胸骨微创Bentall手术后撤呼吸机更快,术后并发症发生率和死亡率更低。与Hillebrand等[6]的研究结果不同,近期Harky等[10]进行的一项meta分析结果表明:经正中部分胸骨微创Bentall手术在体外循环时间[(101.7±33.5)min vs (109.6±52.9)min,P=0.009]、术后重症监护室停留时间[(1.41±1.75)d vs (2.31±2.28)d,P=0.000 9]和住院时间[(6.81±3.76)d vs (7.66±4.41)d,P=0.03]等方面均优于全胸骨正中切口,且输血量更少[(1.92±3.17)U vs (2.75±5.64)U,P=0.01]、手术死亡率(0.41% vs 1.34%,P=0.02)更低,讨论认为这与学习曲线和经验积累、围手术期处理水平的提高相关。此外,术后随访结果证实,经正中部分胸骨微创Bentall手术和全胸骨正中切口Bentall手术的近期效果相似[5,7,11,18-20]。Elghannam等[21]进行了一项中期随访研究,全组47例患者中有36例接受正中部分胸骨微创Bentall手术,随访24个月,2例患者死亡,1例患者术后6个月发生心肌梗死,1例患者术后12个月因主动脉生物瓣膜毁损行二次手术,1例患者术后24个月因人工瓣膜感染再次手术,其余患者手术效果良好。
1.4 手术适应证和禁忌证
在熟练掌握全胸骨正中切口Bentall手术后,所有择期行Bentall手术的患者,在完善超声心动图、主动脉CT血管造影成像、冠状动脉造影等检查的基础上[22-23],均可经正中部分胸骨入路。此外,还应关注主动脉壁钙化程度及钙化斑块分布范围,以确定体外循环插管策略和主动脉阻断钳放置位置等[24];对合并巨大升主动脉瘤的患者,倒“T”形胸骨切口可以更好地显露术野[17],但在开胸时需格外小心,可以在体外循环开始后劈胸骨,避免损伤主动脉,同时还应注意保护乳内动脉和乳内静脉;Abjigitova等[17]和Svensson等[25]的研究也指出,二次开胸行主动脉根部置换时,由于仅需行上半段胸骨切口,不仅能够较好地显露术野,而且操作相对安全,不容易损伤右心室。急危重症(如急性A型主动脉夹层)、感染性心内膜炎急性期、同期需要行其他手术(如冠状动脉旁路移植术或其他瓣膜手术)、胸廓严重畸形的患者,则不适合选择部分胸骨切口[5,23]。
2 经右前外侧肋间微创Bentall手术
2.1 手术入路
经右前外侧肋间微创Bentall手术是在右前外侧肋间切口主动脉瓣置换手术基础上发展起来的、经肋间进行的微创Bentall手术。该术式通常于第2肋间、距胸骨右缘2横指处向外侧切口,皮肤切口长度5~7 cm(如图2所示),既能保持胸骨和肋软骨的完整性,又可以不损伤右乳内动脉和乳内静脉,出血少、损伤小,术后疼痛减轻、康复更快。

图2 全胸骨正中切口(黑色尖头所示)与经右前外侧肋间切口(白色尖头所示)术后对比图[26]
2.2 手术技术
2018年Johnson等[27-29]首先报道了7例右前外侧肋间微创Bentall手术,通过右前外侧第2肋间切口、离断第3根肋骨并结扎右侧乳内动脉和乳内静脉以更好显露术野,同期经股动脉和股静脉插管建立外周体外循环,利用Chitwood主动脉阻断钳阻断升主动脉后,于主动脉根部灌注HTK心肌停跳保护液进行心肌保护。当温度降至15~18 ℃时,体外循环流量降低为25~50 mL/min,开放升主动脉阻断钳,完成远端吻合,随后夹闭人工血管、恢复循环并复温,近端采用自动缝合(RAM装置和SEW-EASY装置,LSI SOLUTIONS,Victor,UY USA)和Cor-Knot自动打结装置[30]固定带瓣管道,随后进行左、右冠状动脉再植,并重建升主动脉连续性。上述7例手术均是在胸腔镜引导下进行,手术效果良好,无围手术期死亡。2021年Jawarkar等[31]报道了1例利用常规缝合方法完成的右前外侧肋间微创Bentall手术,仍通过股动、静脉建立体外循环,近端利用2-0换瓣线褥式缝法固定带瓣管道,再进行左冠状动脉再植,随后进行远端吻合,避免了深低温停循环,待吻合完成后再进行右冠状动脉再植,手术利用常规器械在胸腔镜引导下进行,在缝合完成后用神经拉钩收紧缝线,并且在开放升主动脉前仔细检查结线的松紧程度;尤其当组织脆弱、出血风险较高时,通常对冠状动脉吻合口进行两层缝合,防止发生术后出血及吻合口漏。2022年Ji等[26]报道了15例行右前外侧肋间微创Bentall手术的患者,均保留了乳内血管及肋骨的完整性,手术方式与Jawarkar等报道的总体相似,仅在进行冠状动脉再植时,为防止吻合口漏,于自体“冠状动脉纽扣”和人工血管之间衬垫了自体心包组织,同时在缝线处喷洒生物胶辅助止血。
2.3 手术效果
右前外侧肋间微创Bentall手术,术后重症监护室停留时间(1.0~3.0 d)和住院时间[(5.8±1.2)d]均较短,无住院死亡、出血和神经系统并发症。在术后早期随访过程中,所有患者均未再次进行手术干预,心功能分级得到明显改善,超声心动图检查未见明显瓣周漏及瓣膜功能障碍[26]。这表明该术式安全、近期效果尚好。但是因为这种术式发展时间尚短,暂时缺乏中、远期随访结果。
2.4 手术适应证和禁忌证
Johnson等[27]认为,与全胸骨正中切口和正中部分胸骨切口相比,经右前外侧肋间微创Bentall手术的主要缺点是需行深低温停循环,同时体外循环时间[(202.9±47.8)min]和主动脉阻断时间[(161.9±32.1)min]更长。但是与Johnson等[27]的研究结果不同,Jawarkar等[31]和Ji等[26]报道的队列中,右前外侧肋间微创Bentall手术的体外循环时间(112 min和138.5 min)和主动脉阻断时间(96 min和95 min)显著缩短,且避免了深低温停循环,这可能与术者经验和标准化手术操作步骤有关;此外,两组患者均经过了严格筛选。只有年龄<75岁,左室射血分数正常或接近正常,无严重冠心病、主动脉弓疾病(如有,则不超过半弓置换)、外周血管疾病且无需同期进行其他心脏手术的患者,才考虑行右前外侧肋间微创Bentall手术;急性主动脉夹层、主动脉壁间血肿、保留主动脉瓣的主动脉根部置换术则不适合选择该入路[26-27,31]。所有患者术前均需常规进行胸部CT检查明确解剖结构和主动脉钙化程度,左位主动脉弓、升主动脉严重钙化、瓷化主动脉、胸廓畸形、冠状动脉起源异常和肺功能较差的患者,也不适合选择肋间入路[26-28]。之前有研究[32]指出,曾经接受过心脏手术的患者,再次手术时不建议选择右前外侧入路。然而,Ji等[26]成功为一位曾经接受过胸骨正中切口二尖瓣成形术的患者实施了右前外侧肋间微创Bentall手术,他们认为,胸骨正中切口二尖瓣手术史并不是右前外侧肋间微创Bentall手术的禁忌,但合并或不合并升主动脉置换的主动脉瓣手术史则是此类手术的相对禁忌证。
与胸骨正中切口和经正中部分胸骨微创Bentall手术相比,经肋间入路的微创Bentall手术技术难度高、主动脉根部显露困难,尤其是在缺乏腔镜辅助的情况时,可能会延长手术时间,有时甚至需要离断肋骨和右乳内动脉以暴露术野;此外,术中经股动脉插管行外周体外循环有发生医源性主动脉夹层的可能,增加手术风险。因此经肋间入路的微创Bentall手术前,需要严格筛选患者,谨慎操作,在保证患者生命安全和手术效果的前提下,追求更为美观的切口和更加快速的康复。
3 问题与展望
与全胸骨正中切口不同,微创Bentall手术前需预先行双腔气管插管、安装体外除颤装置并进行切口标记,同时还应有经食管超声心动图检查监测。针对微创Bentall手术技术难度高、学习曲线长等问题,Shrestha等[23]的研究提出了由微创主动脉瓣置换到微创升主动脉置换,再到微创主动脉根部置换的“阶梯式”学习方法,因此心脏外科医生首先需要熟练掌握全胸骨正中切口Bentall手术和经肋间主动脉瓣置换术,在此基础上,根据患者症状、身体状况、个人意愿以及经济情况等综合评估,仔细筛选患者,开展微创Bentall手术。然而,目前文献所报道的微创Bentall手术,多数是在较大的心脏中心、由微创手术经验丰富的术者进行,并未考虑学习曲线对手术结局的影响,相关研究结果的差异性也较大[33-34],因此“学习曲线效应”未来还需进一步的深入研究。
与全胸骨正中切口相比,经过严格筛选且符合适应证的患者,经正中部分胸骨微创Bentall手术出血量更少、重症监护室停留时间和住院时间更短、术后并发症发生率更低,因此手术安全性高、技术可行。此外,虽然目前报道的经右前外侧肋间微创Bentall手术效果尚可,但是由于手术经验有限、技术门槛高且符合标准的患者少,仅适用于少数患者。总的来说,目前文献报道的微创Bentall手术队列,由于样本数量较小、数据异质性较大、随访时间较短,尤其是缺乏右前外侧肋间微创入路与全胸骨正中切口Bentall手术的对比研究,结果存在较大不确定性,因此仍需进行大规模前瞻性随机研究和长期临床随访。外科手术微创化是当今医学界的主要发展趋势。未来术者将在不断学习探索的基础上,充分利用先进科技,突破现有技术瓶颈,扩大微创Bentall手术的适应证,更好地服务于患者。