膝关节水平小剂量测试技术在大螺距、低千伏下肢动脉CT 成像中的应用研究
胡蓝月 周文珍 王薇 许权 尚晓彤 张娅梅 赵晓静 李同
下肢动脉硬化闭塞症(peripheral arterial occlusive disease,PAOD)是中老年人常见的动脉疾病之一,易引起患者下肢慢性缺血,出现疼痛、间歇性跛行等症状,准确评估PAOD 可及时指导临床治疗,目前CT 血管成像(computed tomography angiography,CTA)是评价PAOD 的重要方法之一,其优势在于无创、简单易实现,其局限性主要是存在X线辐射。关于低辐射剂量下肢动脉CTA 的研究报道较多,其中比较成熟的技术为降低管电压[1-3]和管电流自动控制(automatic tube current modulation,ATCM)[4]技术,较新的低辐射剂量技术主要有大螺距[5]、迭代重组(iterative reconstruction,IR)[6,7]。本研究联合使用多种降低辐射剂量的技术行下肢动脉CTA 检查,包括低千伏、ATCM、大螺距、IR,旨在降低下肢动脉CTA 的辐射剂量,采用膝关节水平小剂量对比剂测试(test bolus)技术来计算大螺距下肢动脉CTA 扫描触发时间,同时评价低辐射剂量下肢动脉CTA 图像质量及辐射剂量。
资料与方法
1.临床资料
本研究回顾性分析60 例怀疑PAOD 的患者,男47 例,女13 例,平均(67±13)岁,范围39~88岁。主要临床表现为患侧肢体皮温低、疼痛、间歇性跛行、腘动脉或足背动脉搏动减弱。分为两组,每组各30 例,A 组为2022 年1 月~2022 年10 月于我院经临床诊断怀疑PAOD 的患者,其中男24 例,平均(68±12)岁,范围39~86 岁;B 组为2021 年2月~12 月于我院就诊的30 例既往连续性患者,其中男23 例,平均(66±14)岁,范围45~88 岁。排除标准:有碘剂过敏史、肝肾功能不全、髋关节置换及体质量指数(body mass index,BMI)大于等于30 kg/m2者。
2.CT 扫描技术
所有患者均采用128 层双源CT(dual-source CT,DSCT)(Definition Flash,Siemens Medical Solutions,Forchheim)行下肢动脉CTA 扫描。下肢CTA 扫描范围自腰2 椎体水平至踝关节,仰卧位,足先进方式。所有患者下肢动脉CTA 对比剂注射方案均为采用高压注射器以3 ml/s 注入80 ml 非离子对比剂碘普罗胺(370 mg I/ml)及50 ml 生理盐水。
A 组扫描参数:大螺距(3.0),80 kVp,参考管电流210 mAs,应用ATCM(Care Dose 4D,Siemens Healthcare);层厚5 mm;准直2×64×0.6 mm。CTA扫描前先行膝关节水平Test bolus 扫描。Test bolus扫描参数为80 kVp,20 mA,延迟时间为10 s,时间间隔为2 s,对比剂总量12 ml,3 ml/s 流率,20 ml生理盐水冲洗。于双侧腘动脉可获取两条时间密度曲线,达峰时间记录为T1。对于腘动脉闭塞的患者,可于侧支循环获得时间-密度曲线。双侧峰值时间不同者,以时间长的一侧为准。下肢动脉CTA 扫描触发时间计算方法为T1+10 s。图像重组采用IR 法。
B 组扫描参数:标准螺距(1.0),120 kVp;参考管电流210 mAs,应用ATCM(Care Dose 4D,Siemens Healthcare);层厚5 mm;准直2×64×0.6 mm。CTA 扫描采用对比剂示踪法(bolus tracking),兴趣区(region of interest,ROI)位于肾下主动脉水平,CT 值达160 HU 时,延迟时间7 s 后触发扫描。重组方法为滤过反投影法(filtered back projection,FBP)。
3.图像后处理与分析
薄层图像传输至Siemens 后处理工作站,运用多平面重组(multiplanar reformation,MPR)、最大密度投影(maximum intensity projection,MIP)、曲面重组(curve planar reformation,CPR)、容积重组(volume rendering,VR)及轴位图像观察血管。由两位有经验的阅片医师独立评价图像质量。如评估结果不一致,则通过协商达成一致。
测量下肢动脉强化CT 值对图像进行定量分析,ROI 放置时尽可能包括除管壁及斑块外的所有动脉管腔。分别于以下4 个平面进行测量:主动脉分叉(aortic bifurcation,AA)、双侧股动脉(bilateral common femoral arteries,CFA)、双侧股浅动脉中段(bilateral midsuperficial femoral arteries,SFA)以及双侧小腿中部(bilateral midcalf,CA)。计算图像信噪比(signal-to-noise ratio,SNR)及对比噪声比(contrast-to-noise ratio,CNR),计算方法分别为:
(SD:standard deviation,标准差)。图像噪声为4 个测量层面皮下脂肪噪声的平均值。
定性评价CTA 图像包括3 个解剖学区域,分别为腹髂、股腘和小腿区域。采用3 级评价体系:3级为极好,动脉强化明显,边界清晰,无明显静脉污染,可完全评价血管病变;2 级为良好,动脉强化良好,边界清晰,静脉轻度污染,可以诊断;1 级为差,动脉未充分强化,静脉污染严重,无法诊断血管病变。
4.辐射剂量
记录扫描时间、扫描长度、剂量长度乘积(dose length product,DLP)和CT容积剂量指数(volume CT dose index,CTDIvol)。
5.统计分析
使用SPSS 16.0 统计学软件,统计量采用均值±标准差描述,采用非参数Mann-Whiteney 检验进行两组图像质量评级之间的比较,采用独立t检验进行组间连续性变量的比较。P<0.05 视为具有统计学意义。计算Cohen’s Kappa 值(κ)比较两位阅片医师评价图像质量的差异。
结果
1.图像分析
A 组的平均CT 值、平均SNR 及平均CNR 分别为(494.41±89.27)HU,50.12±19.21,43.37±16.83,均较B 组[分别为(320.52±73.29)HU、36.71±10.43、26.27±9.54]高,且具有显著统计学差异(P<0.001),具体结果见表1。B 组的图像噪声[(9.33±3.79)HU]较A 组[(11.24±3.79)HU]低(P<0.001)。两组间图像质量评级差异无统计学意义(表2)。A 组30 例患者均获得满足诊断图像(图1、2)。两位阅片医师图像质量评级结果一致性良好(κ=0.76)。

图1 64 岁,女,A 组。a)MIP 图示腹髂及股腘区域图像质量为3 级,左侧小腿区域图像质量为2 级,MIP 图示左侧腘动脉瘤(箭);b)膝关节水平轴位图像示左侧腘动脉瘤(箭);c)Test bolus 扫描获得的腘动脉时间-密度曲线,左(曲线1)/右(曲线2)腘动脉的达峰时间分别为38 和32 s 图2 61 岁,男,A 组。a)MIP 图示三个解剖区域图像质量均为3 级,右侧股浅动脉支架植入(箭);b)曲面重组图示支架管腔内部分再狭窄(箭);c)Test bolus 扫描获得的腘动脉时间密度曲线,右(曲线1)/左(曲线2)腘动脉的达峰时间分别为36 和34 s 图3 Test bolus 扫描获得的膝关节水平动脉峰值时间,平均值为33 s,范围20~48 s

表1 两组间血管强化CT 值、CNR 和SNR 比较
Test bolus 扫描A 组共获得60 条时间密度曲线,其中1 条来自侧支循环,膝关节水平动脉平均峰值时间为33 s,范围自20~48 s(图3)。
2.辐射剂量
A、B 两组平均DLP、CTDIvol及扫描时间 均存在统计学差异(P<0.001),两组间平均扫描长度无统计学差异(P>0.05)(表3)。
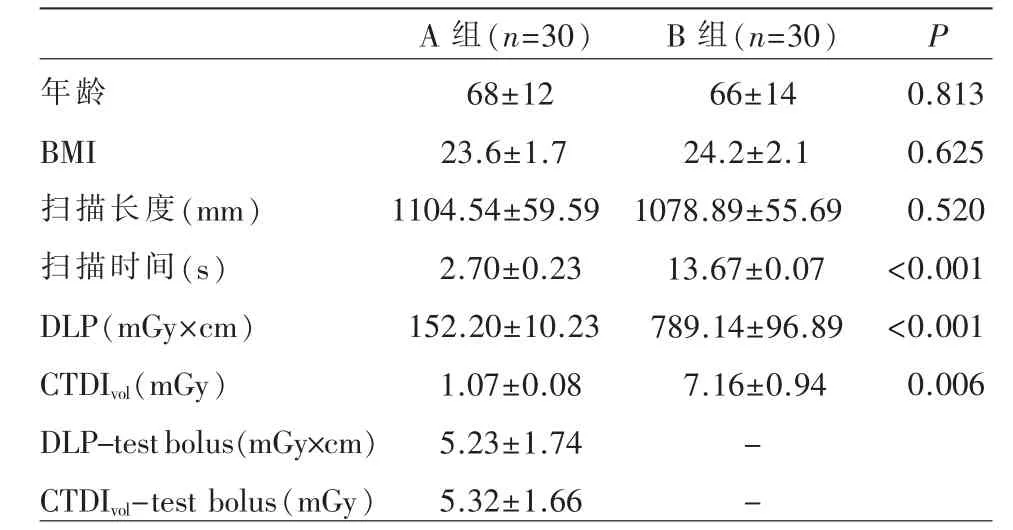
表3 两组CTA 辐射剂量比较
讨 论
本研究证实80 kVp、大螺距双源CT 下肢动脉成像可获得满足诊断用图像,且可以显著降低辐射剂量。利用小剂量测试(test bolus)技术获得膝关节水平动脉峰值时间,可以个体化计算该扫描模式的触发时间。
随着CT 设备硬件和图像后处理软件的不断发展,目前CTA 检查已成为评估动脉病变可靠手段。有研究认为,CTA 在诊断PAOD 中有较高敏感性和特异性,可以替代DSA[2,8]。CT 扫描的缺陷在于较高的辐射剂量[2,9]。Utsunomiya 等[2]报道下肢动脉CTA 成像DLP 可以高达1464.7 mGy×cm,既往低剂量研究中,采用降低千伏值的技术较多[2,10],将千伏值自120 kVp 降至80 kVp[2],辐射剂量可降低30%。近来为了最大限度降低患者辐射剂量,采用多种低辐射剂量技术联合使用成为趋势,有研究分别采用70 kVp[5]和80 kVp[11]联合大螺距行下肢动脉CTA 低辐射剂量扫描,平均DLP 分别为83.7 mGy×cm 和266.6 mGy×cm。本研究采用80 kVp、大螺距和ATCM 联合行下肢动脉CTA 检查,平均DLP 为152.20 mGy×cm,结果与既往研究类似[5,11]。本研究中低辐射剂量技术之一的大螺距模式,又称为Flash 扫描模式,增大螺距可缩短扫描时间,从而降低辐射剂量[12],在常规胸部和腹部CT 扫描发现,将螺距从1 增加至3.2 时,平均辐射剂量可分别减少了20%和45%[13]。Flash 扫描最初是用于低辐射剂量冠状动脉CTA 成像。目前为了实现低剂量CT 扫描,有研究其他部位的CT 成像也采用了该技术[5,14,15],将该技术运用下肢动脉CTA成像的既往报道较少。由于大螺距下肢动脉CTA 成像的扫描速度非常快,平均扫描时间只有2.70 s,类似于给下肢动脉进行“快照”。因此大螺距下肢动脉CTA 成像扫描触发时间的确定就成为该技术的难点。既往研究下肢动脉CTA 成像的触发技术多为腹主动脉水平的Bolus tracking[16,17]或者Test bolus[18,19]技术,然而位于腹主动脉水平监测的技术并不适用于大螺距扫描模式,大螺距扫描模式下,若于腹主动脉进行监测,则并不能准确把握整个下肢血管完全强化的时间。另有研究[5]将腘动脉近段作为检测层面,使用Bolus tracking 技术触发大螺距下肢CTA 扫描,该方式有一定的局限性,一方面腘动脉相对较细,ROI 放置相对较难;另一方面部分PAOD 患者可能存在腘动脉闭塞,此种情况下Bolus tracking 技术则无法追踪到血管的 强 化。Nakaya 等[20]报 道 了64 排 下 肢 动 脉CTA成像的研究,该研究扫描触发时间为股动脉达峰时间,平均扫描时间为10 s,该研究获得了符合诊断用的下肢动脉CTA 图像。本研究通过膝关节水平Test blous 技术可以获得膝关节水平动脉强化的峰值时间,将其作为大螺距CTA 扫描延迟时间的依据,为大螺距下肢动脉CTA 扫描成功完成提供保证。若患者腘动脉发生闭塞,Test blous 扫描后,可从侧支循环获取时间-密度曲线;对于腘动脉与侧支循环均无强化的患者,此种情况可以改用标准扫描模式完成检查。本研究结果中,所有患者均获得了时间-密度曲线,其中有1 例患者从侧支循环获取时间-密度曲线。另外本研究A 组采用了膝关节水平Test blous 技术,该扫描的平均DLP 值为5.32 mGy×cm,膝关节水平的转换因子k非常小,只有0.0004 mSv/mGy×cm,其有效辐射剂量平均为0.002 mSv,基本可忽略不计,因此采用膝关节部位Test blous 扫描并不会给患者增加较多的辐射剂量。
另外低千伏和ATCM 是常见且成熟的降低辐射剂量的技术,既往研究较多[1,2,4]。本研究采用80 kVp 和ATCM 设置,符合既往研究的结果。低千伏和大螺距会导致图像噪声增加,通过IR 可提高图像质量[6,21]。因此本研究中即使A 组的图像噪声较B 组高,但两组的图像质量评级不存在统计学差异。
本研究的局限性:第一,研究的样本量较小;第二,西门子第二代DSCT 其中一套球管的探测器扫描野只能达到33 cm,较胖患者腹部皮下部分组织可能会超出扫描野,虽然并不影响位于中心位置的血管成像,但扫描信息会有一定缺失。
综上所述,利用腘动脉达峰时间计算大螺距下肢动脉CTA 扫描延迟时间有效可行,80 kVp、大螺距、ATCM 联合IR 技术行下肢动脉CTA 检查,相较于标准扫描模式,同样可获得满足诊断用图,同时显著降低辐射剂量。