基于网络药理学分析文痴方治疗阿尔茨海默病的作用机制
孔玉凤 谭浩 肖幸


[关键词]阿尔茨海默病;文痴方;网络药理学;槲皮素
阿尔茨海默病(Alzheimer’sdisease,AD)是以认知障碍、精神及行为异常和社会功能减退为特征的疾病,是痴呆的最常见病因。根据2019年《世界阿尔茨海默病报告》,预计到2050年全球AD患者人数将增加至15200万[1]。AD主要表现为认知功能障碍,在中医上属于“痴呆”“健忘”等范畴,病位在脑,为本虚标实证,肾虚、髓海亏虚为本,痰浊瘀血闭阻脑络为标。文痴方是全国第一批名老中医药专家胡毓恒在前人的基础上总结得出的良方,由人参、肉苁蓉、淫羊藿、三七、何首乌等组成,治以补肾健脾、豁痰祛瘀,具有很好的临床疗效[2]。网络药理学是近年来研究中药治疗疾病的有效手段,通过数据库检索、数据分析等揭示药物-基因-靶点-疾病相互作用的网络关系,本文从网络药理学角度探讨文痴方治疗AD的潜在作用机制。
1 材料与方法
1.1 文癡方活性成分及对应靶点筛选
在中药系统药理学数据库与分析平台(TCMSP,https://tcmspw.com/tcmsp.php)检索文痴方中所有组成药物的化学成分,设置生物利用度(OB)≥30%、类药性(DL)≥0.18对化学成分进行筛选,获得文痴方的活性成分。将有意义的活性成分的InChlKey输入PubChem数据库进行搜索,得到标准SMILES结构文件,并将其导入SwissTargetPrediction数据库,限定物种为“Homosapiens”,获得活性成分靶点信息,选择Probability>0.5的预测靶点。将重复值删除后,最终得到活性成分的靶点。
1.2 疾病靶点获取
在TherapeuticTargetDatabase(TTD)数据库和GeneCards数据库中以“Alzheimer’sdisease”作为关键词对AD相关靶点进行检索,在GeneCards中设定RelevanceScore≥15为筛选条件,并将两个数据库检索到的疾病靶点合并,去重后获得AD的疾病相关靶点。
1.3 筛选关键靶点
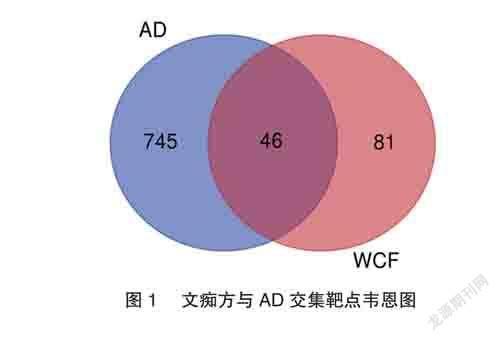
将药物活性成分作用靶点与AD疾病相关靶点进行韦恩分析,取交集,得到药物-疾病共同靶点,即为文痴方治疗AD的关键靶点。
1.4 GO富集和KEGG通路分析
将关键靶点输入DAVID数据库,进行GO功能富集分析和KEGG分析
1.5 药物-活性成分-作用靶点-通路-疾病网络构建
使用Cytoscape3.7.2软件构建药物-活性成分-作用靶点-通路-疾病网络,再利用NetworkAnalyzer功能获得的度和中介度等参数对模型进行分析。
2 结果
2.1 活性成分和作用靶点预测结果
通过TCMSP数据库的检索,并剔除重复值,共获得文痴方153个活性成分及127个作用靶点。
2.2 疾病相关靶点
在GeneCards数据库中检索出9600个疾病靶点,设定RelevanceScore≥15,可筛选出706个疾病相关靶点,在TTD数据库中检索出139个疾病相关靶点,去重后共获得791个AD相关靶点。
2.3 获得关键靶点
将药物活性靶点及疾病相关靶点进行韦恩分析,共获得46个关键靶点(图1)。
2.4 GO富集分析
运用DAVID数据库对关键靶点进行GO富集分析,富集结果设置以P值<0.05进行筛选,共富集到生物学过程208条、分子功能63条、细胞组成45条,分别筛选出前10位使用微生信网站将富集结果进行可视化分析(图2)。
发现生物过程包括:G蛋白偶联5-羟色胺受体信号通路、激酶活性的积极调节、蛋白质自磷酸化等;分子功能包括:酶结合、神经递质受体活性、G蛋白偶联乙酰胆碱受体活性等;细胞组分包括:树突、质膜、受体复合物等。
2.5 KEGG通路分析
运用DAVID数据库对关键靶点进行KEGG通路富集分析,富集结果设置以P值<0.05进行筛选,共富集到56条通路,使用微生信网站将富集结果进行可视化(图3),包括癌症信号通路、钙信号通路、AD、PI3K-Akt信号通路等。
2.6 文痴方-活性成分-作用靶点-通路-AD相互作用网络分析
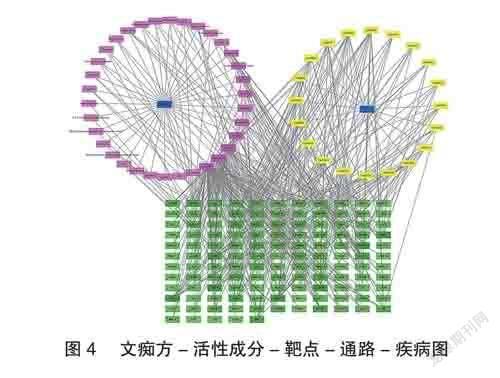
将文痴方的主要活性成分、潜在作用靶点及信号通路、疾病信息导入Cytoscape3.7.2软件,建立文痴方-活性成分-作用靶点-通路-AD相互作用网络(图4),该网络中共包含182个节点和463条边,每条边代表两者之间存在相互作用的关系,边数越多表示该节点的关键程度越高。从图中可以看出,槲皮素度值最大,其次是山柰酚、木犀草素,由此可以认为,文痴方治疗AD的主要活性成分可能是槲皮素、山柰酚和木犀草素。同时,在该网络中,AKT1、EGFR、VEGFA、SRC、MMP9、MMP2、GSK3B、KDR是排名前8的靶点基因,这些靶点可能是文痴方治疗AD的关键靶点。癌症信号通路、AD、PI3K-Akt信号通路、钙信号通路、神经退行性变的信号通路是排名前5的信号通路,提示这些通路可能是文痴方治疗AD的关键信号通路。由此可见,文痴方可能通过多成分、多靶点、多通路治疗AD。
3 讨论
《内经精义》云:“事物所以不忘,赖此记性,记在何处,则在肾经。益肾生精化为髓,而藏于脑”,提示肾虚髓海不足会引起痴呆健忘。陈士铎《石室秘录》指出“痰气最盛,呆气最深”,提示痰浊也是痴呆健忘的致病因素之一。《脾胃论》曰:“上气不足,脑为之不满……皆由脾胃先虚,而气不上行之所致也。”提示脾虚生化乏源,气不上行可以导致痴呆;同时,脾为生痰之源,脾胃虚弱运化失常致痰浊内生亦可发生痴呆。《伤寒论》有云“其人喜忘者,必有蓄血。所以然者,本有久瘀血,故令喜忘”,提示瘀血也可导致痴呆健忘。因此有人提出[3],“肾虚髓亏为本,痰瘀阻滞为标”是AD的病机特点。文痴方从其病机入手,补肾健脾、豁痰祛瘀,有中医理论的支持。
从现代医学角度,本研究借助网络药理学方法对文痴方治疗AD进行分析。以上数据表明,AKT1、EGFR、VEGFA、SRC、MMP9、MMP2、GSK3B、KDR是文痴方治疗AD的关键靶点。PI3K/Akt是一条调节细胞代谢、生存及凋亡的信号传导通路,神经系统中广泛存在,在AD发生发展过程中具有重要调控作用。研究证实[4],AD模型小鼠中,PI3K/Akt通路活性被抑制后β-淀粉样蛋白(Aβ)大量沉积可导致小鼠学习记忆能力出现障碍。郑清等[5]通过电针改善AD模型大鼠的学习记忆和认知功能障碍,并推断其机制可能与调控PI3K/AKT/mTOR信号通路、诱导自噬、促进神经原纤维缠结清除有关。(vascularendothelialgrowthfactor,VEGF)又称血管内皮生长因子,具有直接营养神经的作用,还可以促进移植和内源性神经前体细胞的增殖、存活和分化,具有潜在的促进脑修复的作用[6]。糖原合酶激酶3β(GSK3B)能够促进Aβ的沉积和以过度磷酸化Tau蛋白为核心的神经原纤维缠结的形成。一项研究通過生物计算方法整合了大量文献数据及基因表达数据,数据研究显示,VEGFA、AKT1、GSK3B与AD的发病息息相关[7]。表皮生长因子受体(epidermalgrowthfactorreceptor,EGFR)可参与调节脑发育和神经元的存活与功能调节等活动,被认为是治疗β-淀粉样蛋白诱导的记忆丧失的首选靶点[8]。研究表明,Src基因编码形成的Src蛋白激酶可能可以促进淀粉样蛋白依赖性小胶质细胞增生,从而促进炎症变化及AD的发生发展,抑制Src激酶活性可减轻AD小鼠模型中淀粉样蛋白相关的小胶质细胞增生,减轻炎症反应,减缓AD的发展[9]。MMP又称基质金属蛋白酶,可通过影响Aβ的代谢、参与Tau低聚物的形成、破坏脑部屏障功能、促进神经炎症、影响突触可塑性等改变AD的病理进程[10]。
槲皮素、山柰酚和木犀草素是文痴方治疗AD的主要活性成分,三者都属于黄酮类化合物,具有抗炎、抗氧化的作用,可通过减少Aβ的形成、抑制Tau蛋白磷酸化、减少神经细胞凋亡等途径治疗AD[11]。槲皮素具有神经保护作用[12],可改善AD的学习、记忆和认知功能[13]。据报道,槲皮素可逆转细胞外β-淀粉样变性,并减少海马和杏仁核中的tau蛋白变性、星形胶质细胞增生和小胶质细胞增生,从而保护三重转基因AD模型小鼠的AD病理表现和相关认知缺陷[14]。多项研究显示[15-18],山柰酚具有神经保护作用,可作为AD的潜在神经保护剂。一项体外实验研究显示[19],木犀草素可能通过激活PI3K/Akt通路,抑制氧化应激及Tau蛋白的磷酸化来实现神经保护作用。
综上所述,本研究基于网络药理学,初步探讨了文痴方治疗AD的潜在机制,通过槲皮素、山柰酚和木犀草素等关键成分对核心靶点AKT1、EGFR、VEGFA、SRC、MMP9、MMP2、GSK3B、KDR的调控,最终作用于PI3K-Akt信号通路、AD、癌症信号通路、钙信号通路、神经退行性变等相关通路,为文痴方治疗AD提供了理论依据。

