伊班膦酸钠注射液的过敏性、溶血性和刺激性比较试验
顾蕾蕾 何若琦 张逸民
(江苏省药物安全性评价中心,江苏 南京 211800)
双膦酸盐是一类人工合成的焦磷酸盐类药物,此类有机化合物由一个碳原子连接2个磷原子形成“P-C-P”结构,碳原子上的2个侧链取代基(R1和R2)决定其药物效应。R1常常是羟基、氯基、氢基或烷烃基等化学集团。伊班磷酸钠是第3代双膦酸盐,R2取代基中具有杂环,称为异环型含氮双膦酸盐[1]。伊班膦酸钠可以有效地抑制破骨细胞活性并诱导破骨细胞凋亡从而用于肿瘤骨转移疾病的治疗[2]。本文通过主动过敏试验,被动皮肤过敏试验,体外溶血试验和血管刺激性试验来评价伊班膦酸钠(南京恒生制药有限公司)的过敏性,溶血性和刺激性,并与参比制剂伊班膦酸钠(Roche Pharma(Schweiz)Ltd)比较。
1 材料与方法
1.1 受试物 伊班膦酸钠注射液(南京恒生制药有限公司,批号191205),伊班膦酸钠注射液(Roche Pharma(Schweiz)Ltd,批号H1101H03)
1.2 实验动物 豚鼠(Hartley,SPF级)70只,来源北京维通利华实验动物技术有限公司,(合格证号1100112011017489、1100112011017490),雌雄各半。豚鼠46只,雌雄各半,来源南京市浦口区莱芙养殖场(合格证号202003586、202003587)。新西兰兔11只,6雌5雄,南京市浦口区莱芙养殖场,(合格证号202001461)。饲养房间温湿度控制范围:温度18~26 ℃;相对湿度40%~70%。换气次数≥8次/h。工作照明>200 Lux;动物照明15~20 Lux(照明时间12 h/d,6:00开灯~18:00关灯)。本研究中涉及内容经过本研究所伦理委员会批准。
1.3 仪器 9903WOW电子计重秤(上海英展机电企业有限公司),BS124S分析天平(赛多利斯科学仪器有限公司),DNP-9052电热恒温培养箱(上海精宏试验设备有限公司),ALH-30电子秤(上海英展机电企业有限公司),DL-5低速大容量离心机(上海安亭科学仪器厂),ST4040自动染色机(Leica),RM2245半自动切片机(Leica),ASP200全自动真空脱水机(Leica),BMJ-1B生物组织包埋机(天津爱华),BX41光学显微镜(OLYMPUS)。
1.4 方法
1.4.1 全身主动过敏试验方法 实验用健康豚鼠36只(Hartley,SPF级),每组6只,雌雄各半,致敏给药3次,隔日分别腹腔注射给予受试物高剂量和低剂量、对照品高剂量和低剂量、阳性对照组(鸡蛋清白蛋白)和阴性对照组(0.9%氯化钠注射液)。在末次注射后的第14 d和21 d各激发一半动物。所有激发的动物在激发注射到注射后约3 h详细观察并记录过敏反应情况、症状的起止时间。致敏阶段高剂量组采用临床原液,剂量为1.67 mg/kg,低剂量组剂量为0.5 mg/kg,阴性对照组采用0.9%氯化钠注射液,阳性对照组采用5 mg/只鸡蛋清白蛋白,给药体积均为0.5 mL/只。激发阶段每组剂量为致敏阶段的2倍,给药体积均为1.0 mL/只[3]。过敏反应症状见表1,全身致敏性评价标准见表2。
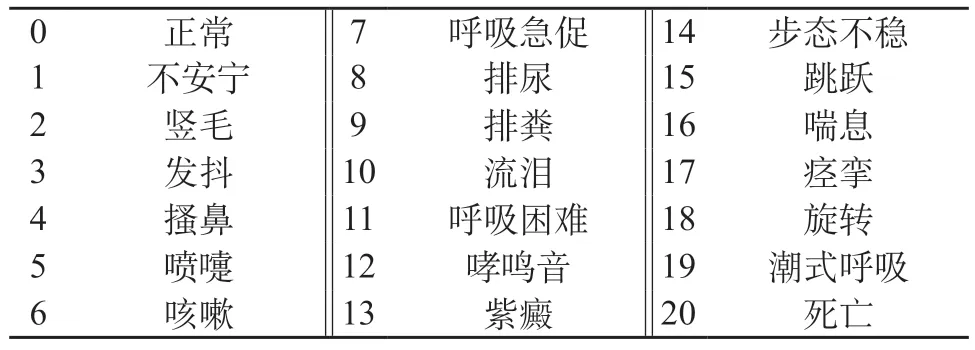
表1 过敏反应症状
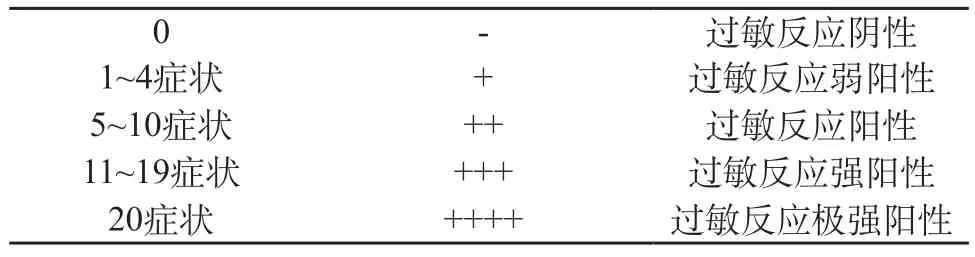
表2 全身致敏性评价标准
1.4.2 被动皮肤过敏试验方法 本实验分为抗血清制备阶段和皮内致敏激发阶段共2个阶段[3]。①阶段1:抗血清制备阶段。实验用健康豚鼠24只(Hartley,SPF级),雌雄各半,分为6组,分别为对照品高剂量组和低剂量组、受试物高剂量组和低剂量组、阳性对照组和阴性对照组,每组4只,各组分别腹腔给予受试物和对照品高剂量(剂量为1.67 mg/kg),低剂量(剂量为0.5 mg/kg),0.9%氯化钠注射液及鸡蛋清白蛋白5 mg/只,给药体积均为0.5 mL/只,隔日1次,共3次。末次致敏后14 d,心脏取血,3 000 r/min离心10 min,制备血清,每组动物血清合并,制成混合抗血清。②阶段2:皮内致敏激发阶段。实验用健康豚鼠36只,雌雄各半,分为6组,分别为对照品高剂量组和低剂量组、受试物高剂量组和低剂量组、阳性对照组和阴性对照组,每组6只。皮内致敏时在脊柱左侧选取1个点,右侧选取2个点。取各组含IgE的抗血清,用0.9%氯化钠注射液等倍稀释抗血清至3个梯度,分别为原浓度的1/2、1/4、1/8,依次在上述各点皮内注射体积为0.1 mL/点的抗血清。24 h后,各组豚鼠静脉注射与致敏相同剂量的抗原和0.5 mL的0.5%伊文思蓝混合液进行激发。给药约30 min后所有动物麻醉后处死。剪取动物背部皮肤以观察蓝斑,测量皮肤内层的蓝斑直径。蓝斑直径>5 mm为阳性,过敏反应表示成出现阳性反应的最大稀释倍数。
1.4.3 溶血试验方法 取试管14支,受试物和对照品各7支,按下表依次加入2%的红细胞混悬液和0.9%氯化钠注射液,混匀后按下表加入不同量的药液,第6、7分别为阴性、阳性对照管。在摇匀后,置37 ℃恒温箱中。开始每隔15 min观察1次,1 h后,每隔1 h观察1次,观察3 h,判断溶液是否出现溶血。最后1 h观察结束后对所有试管进行拍照,拍照后轻轻摇晃试管使之混悬,观察是否有红细胞凝聚发生[4]。
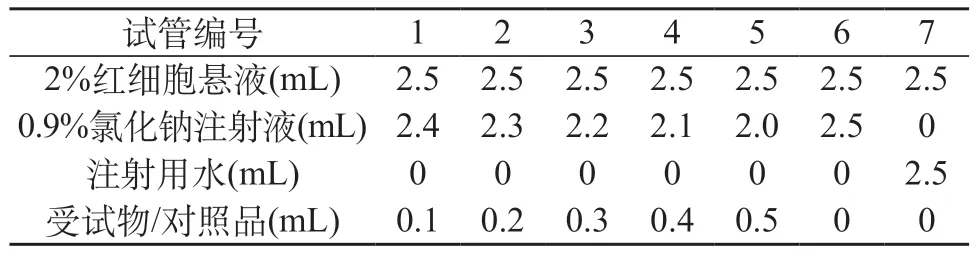
表3 溶血试验加样表
1.4.4 血管刺激性试验 取10只新西兰兔(6雌4雄),受试物组新西兰兔(3雌2雄)、对照品组新西兰兔(3雌2雄),采用自身对照。受试物组左耳给受试物,浓度为1 mg/mL,给药容积为1 mL/kg,右耳给等量的0.9%氯化钠注射液,对照品组左耳给对照品,浓度为1 mg/mL,给药体积1 mL/kg,右耳给等量的0.9%氯化钠注射液,给药1次,观察左右耳的刺激反应来考察伊班膦酸钠注射液的血管刺激情况。首次给药后及每次给药前、给药后详细观察给药部位的刺激反应,末次给药72 h后受试物组3只(2雌1雄)、对照品组3只(2雌1雄),麻醉后处死,剩余4只(2雌2雄)动物恢复期观察14 d后处死。动物处死后进行常规取材,剖取包括进针部位及耳缘静脉的整个耳组织固定于12%乙醛中,从耳尖到耳根取近、中、远三段。最后脱水、包埋、染色和光镜检查。肉眼观察血管注射部位和周围组织的刺激性反应情况,刺激性症状如下:0表示无明显刺激性、1表示红斑、2表示水肿、3表示溃疡;严重程度:+表示轻微、++表示明显、+++表示严重。根据肉眼观察结果与组织病理学检查结果综合判定动物的血管刺激性[3]。
2 结果
2.1 全身主动过敏试验 本实验阴性对照组动物在2次激发注射后均无过敏症状。阳性对照组动物在2次激发注射后均出现步态不稳、跳跃、死亡等过敏反应症状。受试物和对照品低剂量组、受试物和对照品高剂量组动物在2次激发注射后均无过敏反应症状。在本中心GLP实验室条件下,受试物伊班膦酸钠注射液(批号:191205)无过敏反应。对照品伊班膦酸钠注射液(批号:H1101H03)无过敏反应,全身主动过敏反应为阴性。结果见表4~5。
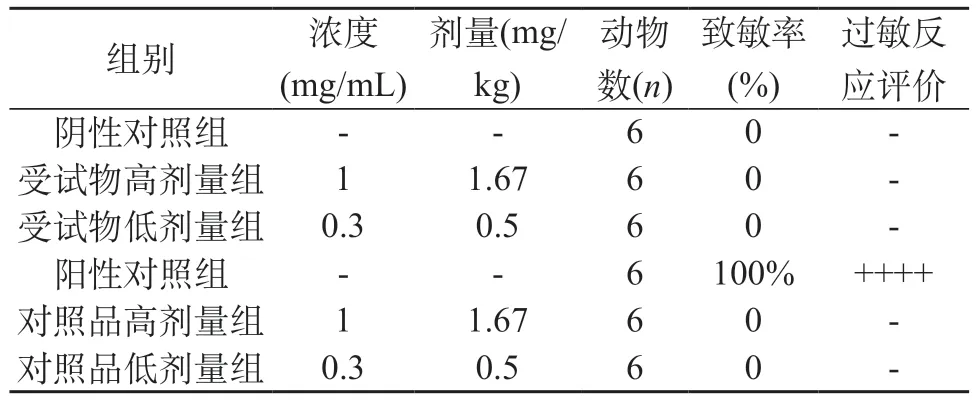
表4 过敏反应汇总表

表5 各组个体过敏反应记录表
2.2 被动皮肤过敏试验 阳性对照组豚鼠背部皮肤1﹕8稀释点蓝色反应斑的直径均值为15.7 mm,1﹕4稀释点蓝色反应斑的直径均值为16.2 mm,在1﹕2稀释点蓝色反应斑的直径均值为28.5 mm,受试物高、低剂量组和对照品高、低剂量组动物激发注射后,豚鼠背部皮肤未见蓝色反应斑点。阴性对照组动物激发注射后,豚鼠背部皮肤未见蓝色反应斑点。在本中心GLP实验室条件下,受试物伊班膦酸钠注射液(批号:191205)和对照品伊班膦酸钠注射液(批号:H1101H03)在高剂量1.67 mg/kg和低剂量0.5 mg/kg下,被动皮肤过敏反应均为阴性。结果见表6。
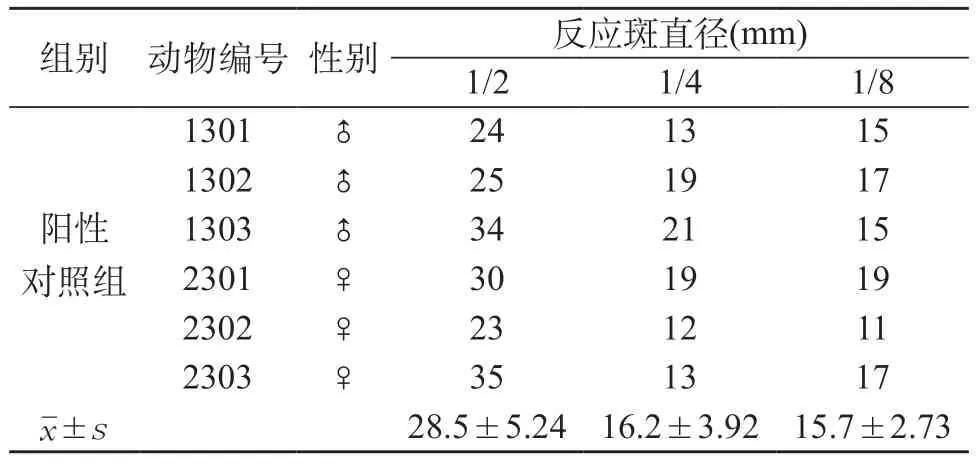
表6 蓝斑直径汇总
2.3 溶血试验 阴性对照未见溶血或红细胞凝聚,阳性对照可见溶血,表明本实验中实验系统可靠有效。受试物1~5号管(药物浓度1 mg/mL,试管中浓度依次0.02 mg/mL、0.04 mg/mL、0.06 mg/mL、0.08 mg/mL、0.1 mg/mL)在3 h观察时间内,受试物1~5号管未见有溶血现象,拍照后轻轻摇晃试管,各管管底红细胞能分散,未见红细胞凝聚现象。对照品1~5号管(药物浓度1 mg/mL,试管中浓度依次0.02 mg/mL、0.04 mg/mL、0.06 mg/mL、0.08 mg/mL、0.1 mg/mL)在3 h观察时间内,对照品1~5号管未见有溶血现象,拍照后轻轻摇晃试管,各管管底红细胞能分散,未见红细胞凝聚现象,受试物和对照品无溶血现象。具体结果见表7~8。
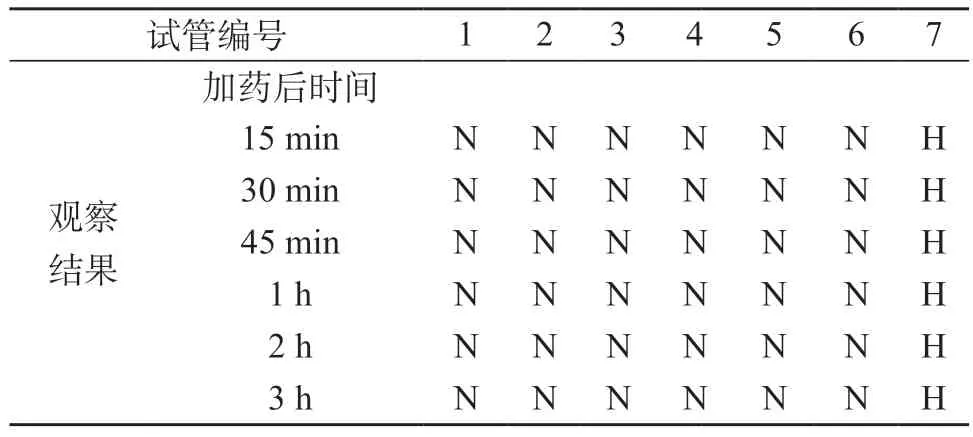
表7 伊班膦酸钠注射液溶血试验结果-受试物
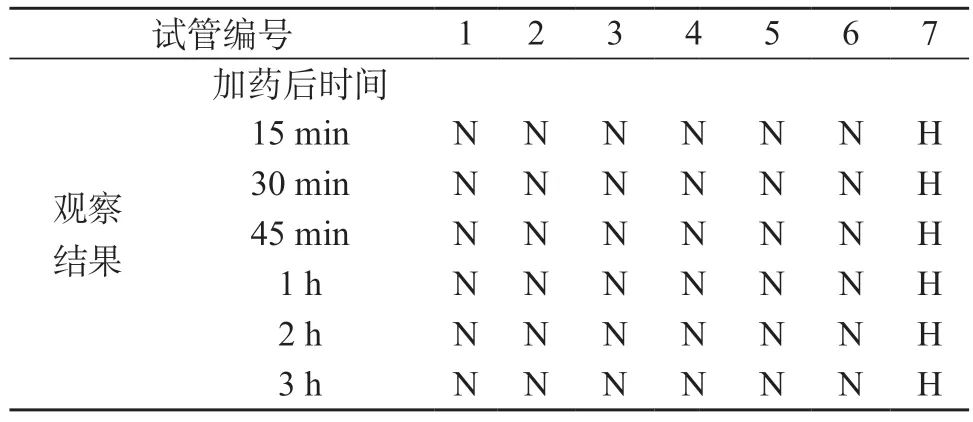
表8 伊班膦酸钠注射液溶血试验结果-对照品
2.4 血管刺激性试验 在给药期和恢复期肉眼观察血管,受试物组和对照品组各例兔耳均无明显刺激性。病理检查显示给药末期,受试物组(受试物)见1例兔耳血管近段内皮细胞轻微肿胀,少量中性粒细胞边集,其余各组各例兔耳血管均未见明显病变。恢复期,受试物组(受试物)及对照品组(溶媒对照品)各见1例兔耳血管中段内皮细胞轻微肿胀。受试物与对照品均未引起注射局部血管明显的病理改变。结果表明,受试物和对照品对兔耳血管无刺激性。图片见图1~12。
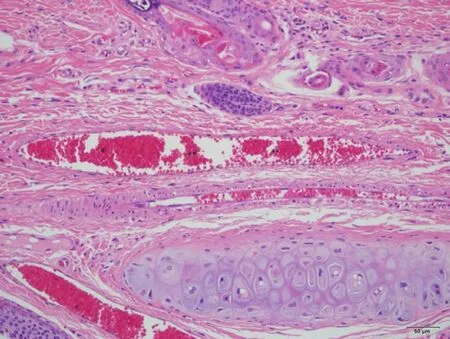
图1 受试物组左侧T3451 号近段 HE ×200未见明显病变。
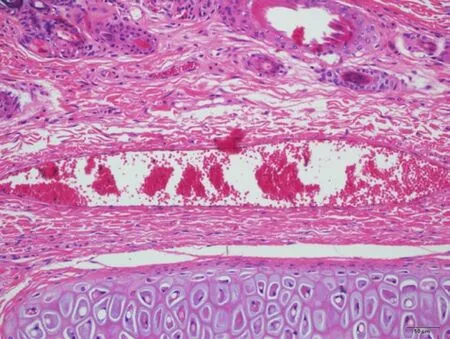
图2 受试物组右侧T3451 号近段 HE ×200未见明显病变。
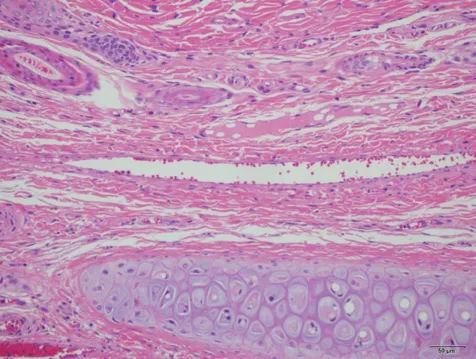
图3 受试物组左侧T3451 号中段 HE ×200 未见明显病变。
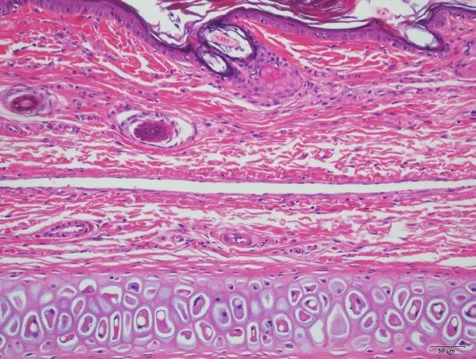
图4 受试物组右侧T3451 号中段 HE ×200未见明显病变。
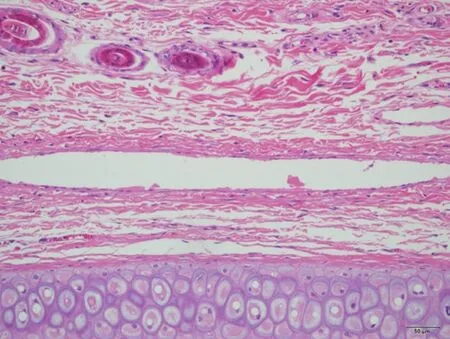
图5 受试物组左侧T3451 号远段 HE ×200未见明显病变。
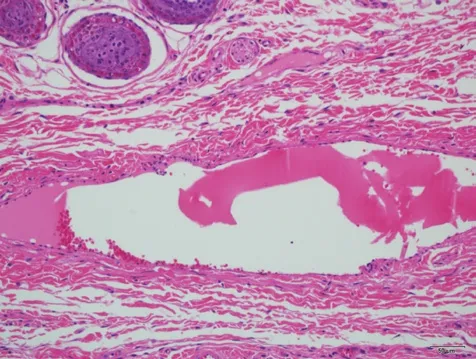
图6 受试物组右侧T3451 号远段 HE ×200未见明显病变。
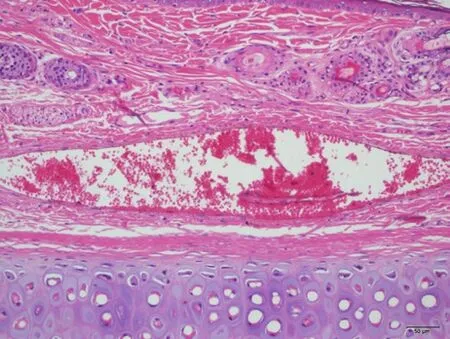
图7 对照品组左侧T3453 号近段 HE ×200未见明显病变。
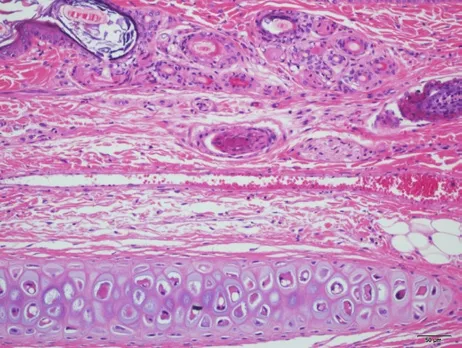
图8 对照品组右侧T3453 号近段 HE ×200未见明显病变。
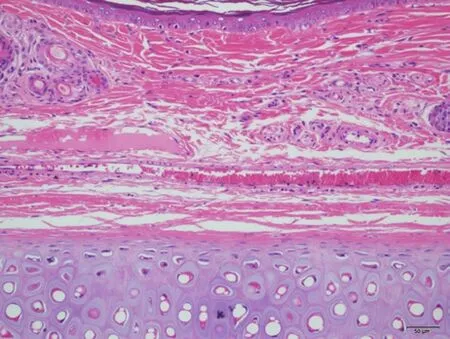
图9 对照品组左侧T3453 号中段 HE ×200未见明显病变。
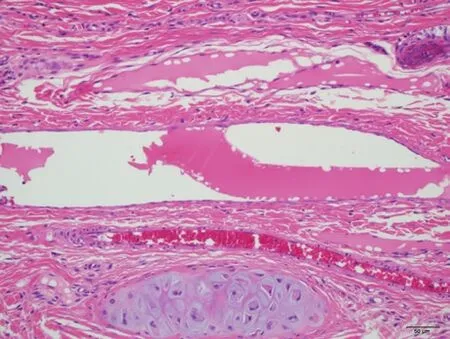
图10 对照品组右侧T3453 号中段 HE ×200未见明显病变。
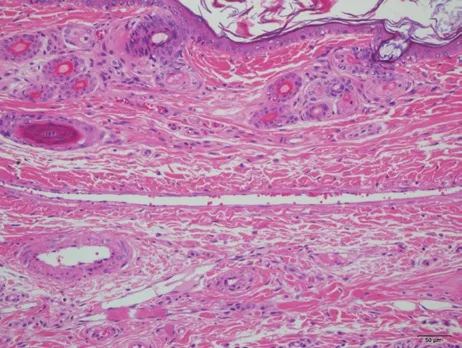
图11 对照品组左侧T3453 号远段 HE ×200未见明显病变。
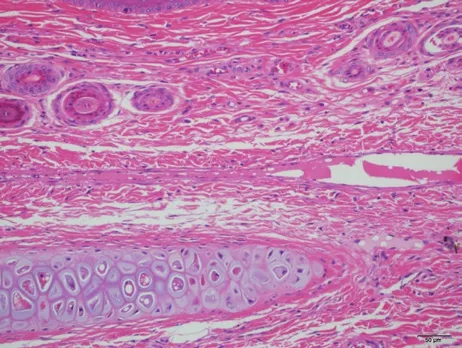
图12 对照品组右侧T3453 号远段 HE ×200未见明显病变。
3 讨论
伊班膦酸钠注射液临床用于治疗骨质疏松症,肺癌并骨转移,肝癌并骨转移,乳腺癌并骨转移等恶性肿瘤骨转移疾病,耐受性及效果良好[5-16]。也有实验表明,伊班膦酸钠可减轻牙根吸收程度,预防牙根吸收,减缓正畸牙齿移动。伊班膦酸钠抑制破骨细胞的活性从而抑制骨吸收的特性在口腔医学领域中被广泛应用[17]。本实验从过敏性、溶血性及局部刺激性方面比较了制剂(南京恒生制药有限公司)和参比制剂(Roche Pharma(Schweiz)Ltd)的毒性。结果表明两种制剂均无过敏性,溶血性和刺激性,毒性反应一致。

