轻症急性脑梗死患者继发血管周围间隙扩大的影响因素及与眼底血管病变相关性研究
庄飞,李平,何兴,师昱姗,孙丽萍
血管周围间隙扩大(enlarged perivascular space,EPVS)是脑小血管病重要影像学标志之一,可见血管周围间隙直径>0.66 mm,同时包绕在脑小血管周围。有研究显示EPVS出现与脑梗死、脑出血或认知功能障碍有关,而眼底血管病变已被证实与上述病变关系密切[1]。目前认为起源于颈内动脉的眼底血管是视网膜中央动静脉终末血管,而眼底照相检查评估眼底血管状态能够准确反映局部病变程度[2]。另有研究提示,眼底血管病变还可影响脑卒中患者微出血灶数量、腔隙性脑梗死灶数量及脑白质高信号(WMH)体积[3];但对于轻症急性脑梗死患者发生EPVS的危险因素,特别是眼底动静脉交叉征、眼底渗出等改变与EPVS的关系尚缺乏相关报道[4]。基于以上证据,本研究纳入轻症急性脑梗死患者,根据是否继发EPVS分组并分析相关临床资料,探讨轻症急性脑梗死继发EPVS的影响因素以及EPVS与眼底血管病变的相关性,旨在为EPVS早期预测及制订针对性干预方案提供更多参考。
1 资料与方法
1.1 研究对象 回顾性选取平顶山市第五人民医院和第二人民医院2015年1月至2020年12月收治的轻症急性脑梗死患者266例为研究对象,根据是否继发EPVS分为继发EPVS组(114例)和未继发EPVS组(152例)。纳入标准:(1)符合急性脑梗死诊断标准[5];(2)年龄≥18岁;(3)符合轻症急性脑梗死判定标准,即基线美国国立卫生研究院卒中量表(NIHSS)评分[6]≤3分;(4)住院期间完善颅脑影像学及眼底照相检查;(5)发病7 d内入院;(6)神经症状体征稳定。排除标准:(1)既往颅脑疾病;(2)既往颅脑手术;(3)存在磁共振成像(MRI)检查禁忌证;(4)合并其他可能影响眼底血管的疾病;(5)近6个月内接受过眼部手术;(6)重要脏器功能不全;(7)临床资料不完整。本研究已通过平顶山市第五人民医院伦理委员会审批〔科教科(研)201704号〕。
1.2 研究方法
1.2.1 观察指标 查阅医院病历系统收集记录患者一般资料、实验室检查及影像学检查资料。(1)一般资料:年龄、性别、吸烟史(平均≥10支/d,持续10年以上)、饮酒史(平均≥40 g/d,持续5年以上)、高血压史、糖尿病史、心房颤动史、冠心病史、颈内动脉狭窄史、收缩压(SBP)、舒张压(DBP);(2)实验室检查资料:总胆固醇(TC)、三酰甘油(TG)、空腹血糖(FBG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、血尿酸(SUA)、血肌酐(Scr)、同型半胱氨酸(Hcy),于患者入院第2天清晨采集空腹静脉血,采用罗氏Cobas C3000型全自动生化分析仪检测;(3)影像学检查资料:颅脑MRI检查,分别在T1加权成像(T1WI)、T2加权成像(T2WI)、液体衰减反转恢复序列(FLAIR)及扩散加权成像(DWI)序列下完成扫描。
1.2.2 NIHSS评分 NIHSS主要用于评估脑梗死患者的神经缺损程度,包括语言、运动功能、感觉功能、意识、视野、眼外肌运动、共济运动及忽视等15个项目,分值范围为0~42分[6]。将各个项目分为5个等级,0~1分为正常或趋于正常,2~4分为轻度卒中,5~14分为中度卒中,15~20分为中-重度卒中,21~42分为重度卒中,分数越高,神经缺损程度越严重。分别于入院48 h、7 d时对患者神经缺损程度进行评估,并记录NIHSS评分。
1.2.3 EPVS评估 采用视觉量化法完成EPVS评估,对称情况下选择大脑单侧且数量最多层面计数,不对称情况下选择数量较多侧;根据基底节区/半卵圆中心EPVS计数分为0~4级,无EPVS为0级,EPVS计数1~9个为1级,EPVS计数10~20个为2级,EPVS计数21~40个为3级;EPVS计数>40个为4级;中脑EPVS计数分为有(1级)或无(0级)两类[7]。其中基底节区/半卵圆中心EPVS计数为1~4级、中脑EPVS计数为1级时即可判定为继发EPVS。
1.2.4 眼底血管病变评估 依据45°眼底彩照摄影资料评估视网膜血管,测量距离视盘边缘1/2至全部视盘直径范围内视网膜动静脉直径。视网膜中央动脉直径和视网膜动静脉比值的计算依据修订Parr-Hubbard公式[7]。眼底动脉硬化程度评估参考Scheie分级[8]。眼底血管弯曲度计算方法:根据血管的实际长度除以该血管的第一个和最后一个点间欧几里得距离(即连接两个点的直线的长度)[8]。血管瘤判定标准为检眼镜下呈大小基本相同的针尖样小红点,散在分布于黄斑及其周围[8]。视网膜动静脉交叉征判定标准为检眼镜下可见眼动脉与静脉交叉处静脉隐匿,动脉两侧的静脉管径瘦削、静脉向视网膜深层移位或侧位偏斜等改变。眼底血管病变评估均由1名神经内科和1名眼科医生共同阅片后完成,两者意见不一致时交由上级医生最终判断。
1.3 统计学方法 采用SPSS 18.0统计学软件进行数据处理。正态性评估采用Kolmogorov-Smirnov检验,符合正态分布的计量资料以(±s)表示,两组间比较采用成组t检验;非正态分布的计量资料以M(P25,P75)表示,两组间比较采用Mann-Whitney U检验;计数资料以相对数表示,两组间比较采用χ2检验。采用多因素Logistic回归分析轻症急性脑梗死患者继发EPVS的独立影响因素。采用Spearman秩相关分析和多元线性回归分析EPVS严重程度和数量与眼底血管病变间的相关性。以P<0.05为差异有统计学意义。
2 结果
2.1 基线资料 266例轻症急性脑梗死患者中,男178例、女88例,平均年龄(67.8±12.9)岁;两组患者年龄、高血压史、眼底动脉硬化程度、视网膜中央动脉直径、视网膜动静脉比值、血管瘤、视网膜动静脉交叉征比较,差异有统计学意义(P<0.05);两组患者性别、吸烟史、饮酒史、糖尿病史、心房颤动史、冠心病史、颈内动脉狭窄史、SBP、DBP、TC、TG、FBG、HDL-C、LDL-C、SUA、Scr、Hcy、48 h NIHSS评分、7 d NIHSS评分、眼底血管弯曲度比较,差异无统计学意义(P>0.05),见表1。

表1 两组患者基线资料比较Table 1 Comparison of clinical data between mild acute cerebral infarction patients with and without secondary enlarged perivascular spaces
2.2 轻症急性脑梗死患者继发EPVS影响因素的多因素Logistic回归分析 以轻症急性脑梗死患者是否继发EPVS(赋值:是=1,否=0)为因变量,以2.1中差异有统计学意义的指标年龄(赋值:实测值)、高血压史(赋值:有=1,无=0)、眼底动脉硬化程度(赋值:实测值)、视网膜中央动脉直径(赋值:实测值)、视网膜动静脉比值(赋值:实测值)、血管瘤(赋值:有=1,无=0)、视网膜动静脉交叉征(赋值:有=1,无=0)为自变量进行多因素Logistic回归分析,结果显示,高血压史和眼底动脉硬化程度是轻症急性脑梗死患者继发EPVS的独立影响因素(P<0.05),见表2。
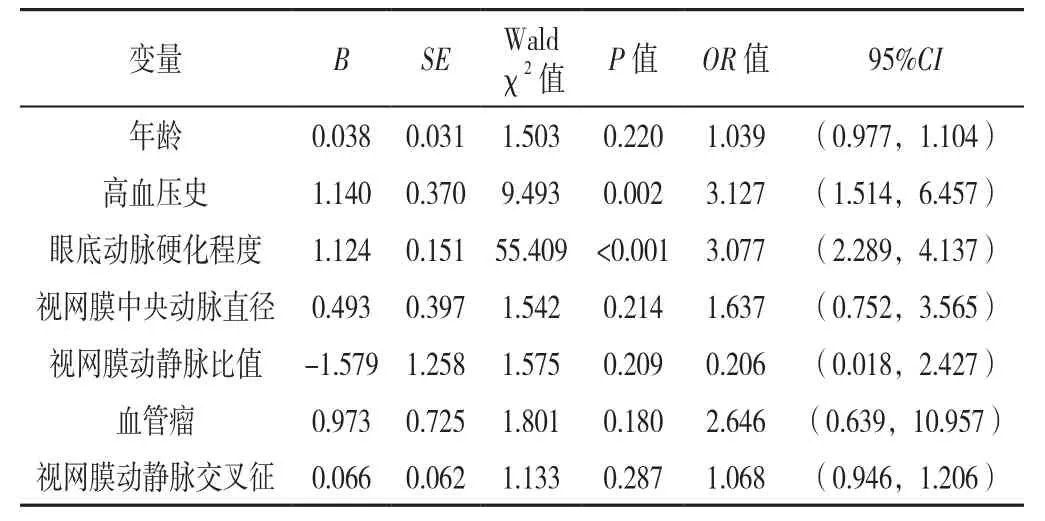
表2 轻症急性脑梗死患者继发EPVS影响因素的多因素Logistic回归分析Table 2 Multivariate Logistic regression analysis of factors associated with the severity of enlarged perivascular spaces secondary to mild acute cerebral infarction
2.3 EPVS严重程度与眼底血管病变的Spearman秩相关分析 EPVS严重程度与眼底动脉硬化程度、血管瘤、视网膜动静脉交叉征呈正相关,与视网膜中央动脉直径、视网膜动静脉比值呈负相关(P<0.05),见表3。

表3 EPVS严重程度与眼底血管病变的Spearman秩相关分析Table 3 Spearman's rank correlation analysis of the severity of enlarged perivascular spaces with fundus vascular lesions
2.4 EPVS数量与眼底血管病变的相关性分析 以EPVS数量(赋值:实测值)为因变量,以眼底动脉硬化程度(赋值:实测值)、视网膜中央动脉直径(赋值:实测值)、视网膜动静脉比值(赋值:实测值)、血管瘤(赋值:有=1,无=0)、视网膜动静脉交叉征(赋值:有=1,无=0)为自变量进行多元线性回归分析,结果显示,EPVS数量与眼底动脉硬化程度和视网膜动静脉交叉征呈正相关,与视网膜动静脉比值呈负相关(P<0.05),见表4。

表4 EPVS数量与眼底血管病变的多元线性回归分析Table 4 Multivariate linear regression analysis of the number of enlarged perivascular spaces with fundus vascular lesions
3 讨论
眼底血管是目前评估颅内血管病变及微循环的重要部位。视网膜中央动脉与脑皮质及穿髓小动脉直径相当,且均来源于颈内动脉系统;而从胚胎发育角度分析,视网膜属于间脑延伸组织,两者在血管发育模式方面接近,均不存在动静脉吻合;上述证据均支持眼底血管病变与脑小血管病间的关系[9]。另有报道认为,眼底血管病变程度能够直接影响急性脑梗死患者微出血、腔隙性脑梗死及WMH发生[10]。而EVPS作为脑小血管病变的重要影像学指标,主要为软脑膜随穿支血管进出脑实质在血管周围绕行而出现[11]。以往对于急性脑梗死患者视网膜病变与EPVS的关系研究较少,本研究纳入轻症急性脑梗死患者,探讨轻症急性脑梗死患者继发EPVS的影响因素,进一步评估EPVS与眼底血管病变间的关系。
本研究多因素Logistic回归分析结果显示,高血压史和眼底动脉硬化程度是轻症急性脑梗死患者继发EPVS的独立影响因素(P<0.05),提示轻症急性脑梗死患者如合并高血压和眼底动脉硬化则继发EPVS的风险更高,与既往研究结果一致[12-13]。以往观点认为EPVS发生与血管内皮功能障碍及血脑屏障损伤关系密切[14]。小血管性脑梗死患者在合并EPVS时常可见血脑屏障通透性改变;此外眼底血管所形成的血视网膜屏障损伤因素亦与血脑屏障一致[15-16]。此外一项眼底照相检查研究提示,视网膜微血管直径可反映EPVS严重程度[17]。但上述研究观察的均是体检健康人群,且仅评估视网膜微血管直径,所得结论存在一定局限。本研究中未证实入院时血压水平与EPVS发生的独立关系,但高血压史是轻症急性脑梗死患者继发EPVS的独立影响因素,但有研究认为基线异常的血压水平是EPVS发生的危险因素[18],形成这一现象可能与部分高血压患者降压药物的使用使得入院时血压控制在参考范围内有关。
本研究结果显示,EPVS严重程度与眼底动脉硬化程度、血管瘤、视网膜动静脉交叉征呈正相关,与视网膜中央动脉直径、视网膜动静脉比值呈负相关(P<0.05);EPVS数量与眼底动脉硬化程度和视网膜动静脉交叉征呈正相关,与视网膜动静脉比值呈负相关(P<0.05),提示视网膜中央动脉直径和视网膜动静脉比值越小则EPVS病变越严重,眼底血管病变严重患者颅内EPVS亦更为严重,特别是合并视网膜动脉变窄和视网膜动脉硬化的患者,以上研究结果均提示视网膜病变严重程度可间接反映EPVS损伤;有研究证实,急性脑梗死患者合并EPVS比例较高,同时EPVS周围常伴有小动脉壁胶原性增生、管壁增厚或管腔狭窄等表现[19]。YANG等[20]的研究认为EPVS发生与视网膜中央动脉直径改变及有无动脉硬化有关,即继发颅内EPVS者视网膜中央动脉更窄,且常存在视网膜动脉硬化,本研究结果与之相符。
综上所述,本研究证实合并高血压和眼动脉硬化的轻症急性脑梗死患者更易出现EPVS,且EPVS病变严重程度与眼底血管病变情况具有相关性,以上证据可为轻症急性脑梗死患者继发EPVS早期预测提供更多借鉴,进而指导临床医生针对高危人群制订更为积极有效的治疗方案。本研究纳入样本量较少,且属于回顾性报道,难以完全排除混杂因素的影响;同时目前对于脑小血管病发生、发展机制尚无统一观点,因部分患者同时存在微出血和WMH表现,分析时未纳入上述因素;而后续研究可采用眼底相干光层析血管成像术等更为准确的自动化检测手段取代眼底照相。
作者贡献:庄飞提出研究思路,设计研究方案,负责论文起草;李平、师昱姗负责进行试验;何兴负责数据收集、采集、清洗和统计学分析;孙丽萍负责最终版本修订,对论文负责。
本文无利益冲突。

