人免疫球蛋白冲击疗法在川崎病患儿中的治疗效果分析
侯宁宁 李 静 古开心
河南省鹤壁市人民医院儿科 458030
川崎病是一种常见于5岁以下儿童或婴幼儿的全身性血管炎综合征,临床主要表现发热、皮疹、眼球结膜充血、指端硬性水肿及颈淋巴肿大,如果不及时干预导致其发展至中后期,将会诱发冠状动脉损伤,促发后天性心脏病,严重威胁患儿生命[1]。一直以来临床多将阿司匹林作为常规治疗,通过阿司匹林的抗炎、抗血小板聚集作用以改善患者临床症状,但并未取得显著的干预效果[2]。终于在20世纪80年代,世界上出现首例应用静脉注射人免疫球蛋白治疗川崎病成功的案例,应用至今,这种治疗方案可以将川崎病患儿临床冠状动脉损害发生率下降至4%左右[3],但是如果按照常规剂量进行治疗,仍会有部分患儿出现无反应状态,故而临床考虑增加用量,人免疫球蛋白冲击疗法便是在常规人免疫球蛋白使用剂量的基础上将其增为2g/kg,为进一步探求其在川崎病患儿中的治疗效果,本文将对其展开研究分析。
1 资料与方法
1.1 一般资料 选取我科2019年6月—2021年5月治疗的119例非典型川崎病患儿进行观察。纳入标准:(1)符合川崎病诊断标准[4],发热>5d、口部、咽部黏膜充血、双侧眼结膜充血、急性手足水肿等;(2)无心血管性质疾病;(3)经患儿家属同意,且经我院医院伦理委员会批准。排除标准:(1)患有血液循环障碍性疾病;(2)患儿依从性较差;(3)对本研究治疗药物过敏患儿。采用抽签法将其分为两组,对照组59例,男39例,女20例;年龄0.5~4岁,平均年龄(3.19±0.75)岁;病程2~15d,平均病程(10.52±2.64)d。观察组60例,男38例,女22例;年龄0.7~4.2岁,平均年龄(3.24±0.79)岁;病程3~17d,平均病程(10.55±2.67)d。两组患儿一般资料比较无统计学差异(P>0.05)。
1.2 方法 两组患儿均给予常规干预以及常规抗感染、维持水电解质平衡等,同时接受阿司匹林口服治疗(拜耳医药保健有限公司,国药准字J20130078,规格100mg×30s),100mg/kg,分3次服用,待体温恢复正常3d或联用14d后,将剂量调整为3~5mg/kg,1次/d。对照组在此基础上,于病程开始第5天给予人免疫球蛋白(上海莱士血液制品股份有限公司,国药准字S10980061,规格2.5g∶50ml)静脉输注,400mg/(kg·d)连用5d;观察组给予人免疫球蛋白注射治疗2g/kg单次静脉输注,8~12h内完成输注,1次/d,两组连续用药1~2个月直至患儿血沉、冠状动脉病变恢复正常。注意事项:(1)本药品仅供静脉输注用。(2)如需要可以用5%葡萄糖溶液稀释本品,但糖尿病患儿应慎用。(3)药液呈现混浊、沉淀、异物或玻瓶有裂纹、过期失效等情况,不得使用。(4)本品开启后,应一次输注完毕。(5)有严重酸碱代谢紊乱的患儿应慎用。
1.3 观察指标 (1)症状消失时间:对比两组发热、黏膜充血、手足发硬、颈淋巴结肿大消失时间;(2)炎性指标:采集患儿治疗前后清晨空腹静脉血,采用酶联免疫吸附法检测肿瘤坏死细胞因子-α(TNF-α)、C反应蛋白(CRP)及白细胞介素-6(IL-6)水平;(3)血清基质金属蛋白酶:采集患儿治疗前后清晨空腹静脉血,离心后取血清,经酶联免疫吸附法检测基质金属蛋白酶-2(MMP-2)、基质金属蛋白酶(MMP-9)水平;(4)统计两组不良反应发生情况。

2 结果
2.1 症状消失时间 观察组发热、黏膜充血、手足发硬、颈淋巴结肿大消失时间均短于对照组(P<0.05)。见表1。

表1 两组症状消失时间比较
2.2 炎性指标 治疗后,两组TNF-α、CRP、IL-6水平较治疗前下降,且观察组各炎性指标较对照组下降明显(P<0.05)。见表2。

表2 两组炎性指标比较
2.3 血清基质金属蛋白酶 治疗后,两组MMP-2、MMP-9水平较治疗前下降,且观察组各项血清基质金属蛋白酶水平低于对照组(P<0.05)。见表3。
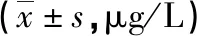
表3 两组血清基质金属蛋白酶水平比较
2.4 不良反应 治疗期间,两组均未出现明显不良反应,仅对照组出现1例腹泻、1例恶心呕吐,不良反发生率为3.39%;观察组出现1例恶心呕吐,不良反应发生率为1.67%。两组不良反应比较无统计学意义(χ2=0.359 4,P=0.548 8)。
3 讨论
目前临床尚未明确川崎病发病机制,但已通过多种实验分析得出多种发病机制,目前被广泛认可有免疫系统异常活化机制,同时还有炎性细胞因子释放,加重血管内皮损伤,诱导血管炎发生机制[5]。根据发病机制分析,治疗川崎病的重点应侧重于控制炎性反应,改善临床症状。阿司匹林作为治疗川崎病的基础药物,其可以发挥抗炎、抗血小板聚集作用,抑制患儿体内炎性反应,同时预防冠心病发生[6]。作为基础药物,阿司匹林只能在一定程度上改善患儿临床症状,故而临床考虑在阿司匹林的基础上增加用药。
经临床实验分析得出,注射人免疫球蛋白可封闭内皮细胞、血管巨噬细胞、单核细胞,进而减少血管内皮损伤,阻滞血管内皮炎性反应;同时可以中和患儿体内抗原和致病原,激活血小板生长因子及血管途径,有效缓解血管壁损伤,改善机体内细胞免疫功能,进而缓解免疫系统的异常活化。此外,其可以有效减少炎性因子分泌、释放,降低机体内免疫复合物反应,从而发挥降温作用,在川崎病治疗中作用明显[7]。但仍存在小部分患者对常规剂量注射人免疫球蛋白无明显反应,所以临床考虑在常规剂量上增加人免球蛋白用量,以提高治疗效果。人免疫球蛋白冲击疗法是在常规注射使用人免疫球蛋白基础上,将注射用量增加至2g/kg。
本文中,治疗后两组的TNF-α、CRP、IL-6、MMP-2、MMP-9水平均较治疗前下降,且观察组较对照组下降更明显,考虑可能是大剂量注射免疫球蛋白促使机体内免疫球蛋白含量迅速升高,提升整体免疫球蛋白浓度,进而影响患儿全身外周血淋巴细胞活化,减少炎性因子分泌,相比常规剂量可以快速提升人体循环中IgG浓度,直接中和病毒,封闭效应细胞受体,抑制和阻断炎性介质的形成和释放,有效阻止补体所介导的免疫损伤;同时人免疫球蛋白冲击疗法可以有效减少多次输注带来的血管损伤,进一步保护患儿冠状动脉,抑制血小板凝集,促进患儿健康成长。
本文中,观察组发热、黏膜充血、手足发硬、颈淋巴结肿大症状消失时间短于对照组,通过大剂量使用人免疫球蛋白促使其在患儿机体内大量扩散,作用于患儿不同组织器官,进而促使患儿快速产生抗病毒抗体,加快退热速度,有效控制病情持续发展为患儿带来的黏膜损伤以及手足发硬、颈淋巴结肿大;同时大剂量的一次性输注可以有效缩短多次输注的药物反应时间,进而提高机体免疫抗体水平,增加患儿机体抗感染能力和免疫调节功能[8]。两组不良反应情况比较无统计学差异,且均为药物常见不良反应,说明人免疫球蛋白冲击疗法不会增加川崎病患儿不良反应发生率,具有较高药物安全性。
综上所述,人免疫球蛋白冲击疗法可以更有效治疗川崎病患儿,可以快速抑制机体内炎性反应,缓解血管内皮损伤,促进患儿临床症状恢复,且具有一定的药物安全性。

