不同工艺制备的替米考星颗粒体外释放度研究
李 敏,程富胜,郭丽华,周凯仁,白玉彬,李 冰,魏彦明,张继瑜*
(1.甘肃农业大学动物医学院,甘肃兰州 730070;2.中国农业科学院兰州畜牧与兽药研究所,甘肃兰州 730050;3.山东德州神牛药业有限公司,山东德州 253000)
随着全球养殖业的快速发展,大规模集约化养殖模式使畜禽的疾病呈现集中暴发趋势,越来越多的抗生素、抗病毒药物、抗真菌药物和抗寄生虫药物在养殖场被广泛使用。据统计,由胸膜肺炎放线杆菌、巴氏杆菌、支原体等病原菌引起的畜禽呼吸道疾病和泌乳动物乳房炎等疾病给全球养殖业造成严重的危害和经济损失。我国每年因畜禽呼吸道疾病和泌乳动物乳房炎造成的损失高达数十亿元[1]。目前对于畜禽呼吸道疾病的防控主要是通过接种疫苗或使用恩诺沙星、阿莫西林和头孢噻呋等抗生素药物,由于病原菌的不断变异,疫苗的保护范围并不能全覆盖,加上抗生素药物的大量不规范使用,导致抗生素疗效减弱,细菌耐药性不断增强。2014年世界卫生组织(WHO)宣布细菌抗药性已经成为人类面临的十大全球公共卫生威胁之一[2]。因此,亟需继续研发更有效的新型兽药来改善和适应畜禽疾病不断变化的情况。
替米考星具有与其他大环内酯类抗生素类似的特性,是畜禽专用抗生素,对革兰氏阳性细菌、某些革兰氏阴性菌、部分支原体和螺旋体等有抑制作用[3-4]。由于其抗菌谱广、吸收迅速、半衰期长、表观分布容积大、组织穿透力强、在靶细胞中快速积累和低浓度抑制的特性,被认为是最安全的抗细菌感染的大环内酯类抗生素,在澳大利亚、意大利和美国,替米考星已经被批准用于预防和治疗牛、山羊、绵羊、猪和鸡的细菌性感染的治疗,在中国已被批准用于治疗猪和牛巴氏杆菌感染以及鸡支原体感染[5-7]。但是,替米考星在胃内易受到胃酸破坏从而导致功效降低,加之存在溶解性差、渗透性差、适口性差、肠外排运和首过效应等诸多问题,导致生物利用度低,口服疗效不佳[8]。因此,为了提高替米考星生物利用度,增加胃内稳定性,降低在胃内的损耗,研发单位在原料药的基础上,采用不同的制备技术,研制出多种替米考星新型制剂。本试验对新研制的3种替米考星不同口服颗粒制剂进行了溶出度测定,为替米考星新制剂的研发和临床应用提供理论依据。
1 材料与方法
1.1 材料
1.1.1 试验药品 替米考星标准品(含量95%,批号C17582000),德国Dr.Ehrenstorfer GmbH;替米考星颗粒1(供试样品1,含量20%,批号20201006)、替米考星颗粒2(供试样品2,含量20%,20201008)、替米考星颗粒3(供试样品3,含量20%,20201103)由山东德州神牛药业有限公司自主研发; 替米考星颗粒对照品(含量20%,批号20200310),市售替米考星肠溶颗粒。
1.1.2 主要试剂 甲醇(色谱纯),美国Fisher公司产品;乙腈(色谱纯),美国Fisher公司产品;四氢呋喃(色谱纯),二丁胺(分析纯),美国sigma公司产品;磷酸(色谱纯),科密欧,天津科密欧化学试剂有限公司产品;NaOH(分析纯),盐酸(分析纯),磷酸钠(分析纯),国药集团化学试剂有限公司产品;纯水和超纯水为试验自制。
1.1.3 主要仪器 ME403型电子天平,瑞士Mettler Toledo公司产品;KQ-600DE数控超声清洗器,昆山市超声仪器有限公司产品;UPT-Ⅱ-40L优普超纯水制造系统,上海优普实业有限公司产品;FE20实验室pH计,德国Sartorius公司产品;溶出仪,德国Phmsa公司产品;Waters2695高效液相色谱仪,Waters2489紫外检测器,美国Waters公司产品;针筒式微孔滤膜,孔径0.22 μm,天津津腾实验仪器有限公司产品;Hypersil ODS-2 C18色谱柱(4.6 mm×250 mm,5 μm),大连依利特分析仪器有限公司产品。
1.2 方法
1.2.1 色谱条件 Hypersil ODS-2 C18色谱柱(4.6 mm×250 mm,5 μm);流动相为水∶乙腈∶磷酸二丁胺缓冲液∶四氢呋喃(790∶130∶25∶55);流速为1.0 mL/min;检测波长为290nm;柱温为30℃;进样量为20 μL。
1.2.2 溶液配制
1.2.2.1 磷酸稀释液 取900 mL水,加入5.71 g磷酸,用12.5 mol/L氢氧化钠溶液调节pH至2.5±0.1,加水定容至1000 mL,摇匀即得。
1.2.2.2 对照品溶液 精确称取替米考星对照品25 mg,置于50 mL容量瓶,加10 mL乙腈超声使其溶解,用磷酸缓冲液定容至刻度线,摇匀即得。
1.2.2.3 供试品溶液 精确称取25 mg替米考星待测品25 mg,置于50 mL容量瓶,加10 mL乙腈超声使其溶解,用磷酸稀释液定容至刻度线,摇匀即得。
1.2.2.4 溶出介质 根据《中国兽药典》肠溶颗粒溶出度试验方法,分别配制pH为1.0的酸溶液和pH为6.8的磷酸盐缓冲液[9]。
1.2.3 含量测定方法学验证
1.2.3.1 专属性试验 精确量取空白溶液(流动相)、对照品溶液和供试品溶液分别经0.22 μm微孔滤器过滤,注入色谱仪,依次进行样品测定。
1.2.3.2 线性考察 精确称取50 mg替米考星标准品,置于50 mL容量瓶中,加入10 mL乙腈,超声使其溶解,加入磷酸稀释液定容至刻度线,摇匀,配制成1 mg/mL的替米考星标准品母液待用。采用梯度稀释法,取标准品母液配制成的质量浓度为10、50、100、200、400、600、800、1000 μg/mL的标准品溶液,精确量取20 μL注入色谱仪,记录峰面积,以替米考星标准品的峰面积为纵坐标Y,以替米考星标准品的质量浓度(C)为横坐标,绘制峰面积(Y)-质量浓度(C)标准曲线浓度,计算标准曲线的回归方程。
1.2.3.3 回收率试验 精确称取替米考星标准品,用10 mL乙腈溶解,用磷酸缓冲液定容至10 mL容量瓶中,配制成80 μg/mL(低)、100 μg/mL(中)、120 μg/mL(高)3个质量浓度的对照品溶液,每各浓度的溶液分别进样3次,测定每个样品的实际质量浓度,根据实际质量浓度与理论质量浓度的比值,计算回收率及相对标准偏差(RSD)。
1.2.3.4 精密度试验 精确称取替米考星标准品,用10 mL乙腈溶解,用磷酸缓冲液定容至10 mL容量瓶中,配制成80 μg/mL(低)、100 μg/mL(中)、120 μg/mL(高)3个质量浓度的对照品溶液,分别考察日内精密度和日间精密度。
1.2.3.5 重复性试验 按照1.2.2.3供试样品配制方法,配制5份供试样品溶液,分别经0.22 μm微孔滤器过滤,按照1.2.1色谱条件,精密吸取每个样品溶液20 μl进样,计算含量及其RSD值。
1.2.3.6 溶出度方法 根据溶出度与释放度测定法中肠溶颗粒体外溶出度测定方法,用两种介质对替米考星不同制剂(每种3个平行)进行体外溶出试验,选用浆法,溶出介质体积为900 mL,转速为75 r/min,温度为37℃±0.5℃,用“1.2.2”中的方法配制酸和缓冲液两种溶出介质,取样时间点为5、10、15、20、30、40、50、60、75、90、120 min,取样体积为5.0 mL(同时补液5.0 mL),经滤膜过滤后测定样品在不同溶出介质中的溶出情况,记录峰面积,绘制溶出曲线。
1.2.4 溶出度方法学验证
1.2.4.1 方法专属性试验 精确量取空白溶液、对照品溶液和供试品溶液分别经0.22 μm微孔滤器过滤,注入色谱仪,依次进行样品测定。
1.2.4.2 稳定性试验 取本品90 mg,分别以酸和缓冲液900 mL为溶出介质,在5、10、15与30 min时,分别取5 mL溶液,同时在操作容器中补充溶出介质5 mL。滤过,取滤液适量,作为供试品溶液。然后分别在0、2、4、8、12、18、24 h注入液相色谱仪,记录色谱图。计算替米考星峰面积相对标准差。
1.2.4.3 滤膜吸附性试验 取两种溶出介质中120 min时的供试样品溶液5 mL,分别经 0.22 μm、0.45 μm和0.8 μm微孔滤膜处理,取滤液20 uL注入液相色谱仪,记录色谱图,比较峰面积大小。
1.2.5 统计分析方法 用Excel 2019初步整理试验数据,用SPSS 26.0软件对数据进行单因素方差分析,并采用Duncan法多重比较,P>0.05定义为不具有显著性差异,P<0.05定义为具有显著性差异,P<0.01定义为具有极显著性差异。
2 结果
2.1 含量测定
2.1.1 专属性考察 结果见图1和图2,表明空白溶液对样品含量测定无干扰,该方法专属性强。

图1 空白溶液
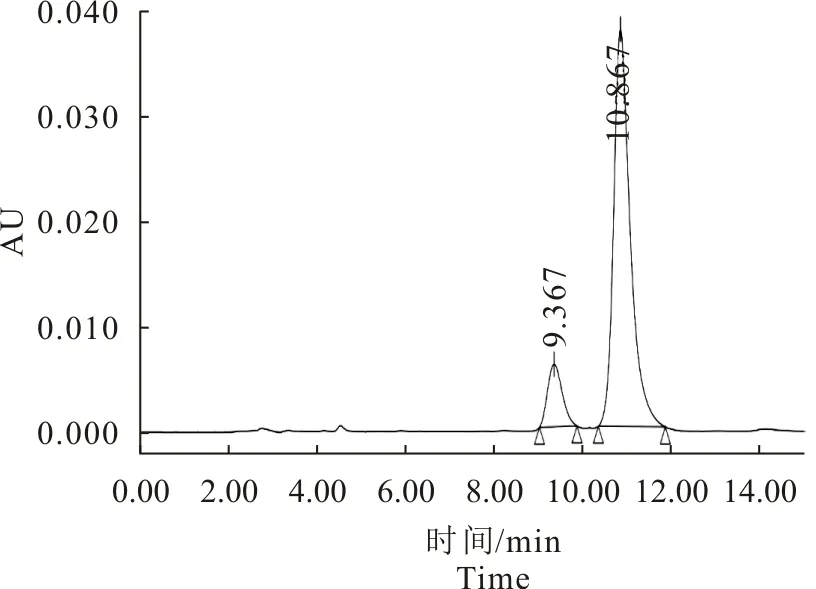
图2 替米考星标准溶液色谱图
2.1.2 线性考察 以替米考星标准品的质量浓度(C)为横坐标,绘制峰面积(Y)-质量浓度(C)标准曲线,得到的标准曲线见图3,线性回归方程为y=26 971x-196 608,R2=0.999 6,表明替米考星在浓50 μg/mL~1000 μg/mL的质量浓度范围内与对应的峰面积的线性关系良好。

图3 替米考星标准曲线图
2.1.3 回收率与精密度 替米考星的平均回收率为110.0%,RSD值均不大于2%,表明该方法的准确度较高。
2.1.4 重复性 按照1.2.2供试品的配置方法,分别配制5份供试样品,测定5份替米考星含量RSD值分别为1.25%、1.65%、1.69%、1.97%和1.06%,表明该方法重复性良好。
2.1.5 替米考星不同制剂含量测定 结果显示供试样品替米考星含量均在标示量的90%~110%,结果见表1。

表1 不同替米考星供试样品含量
2.2 溶出度
2.2.1 专属性考察 结果表明,两种溶出介质对替米考星的测定无干扰,该方法专属性强(图4~图6)。

图4 空白缓冲液色谱图

图5 空白酸色谱图

图6 替米考星供试样品色谱图
2.2.2 稳定性 在不同时间段对供试品溶液进样分析,替米考星峰面积的RSD值均小于2.0%,表明供试品溶液在24 h内稳定。
2.2.3 滤膜吸附性试验 分别对3种滤过方式的峰面积进行比较,结果发现,3种滤膜滤过后峰面积无差异。说明滤膜对替米考星无吸附作用,故选择最常用的0.22 μm PES滤膜过滤。
2.2.4 酸中溶出度 替米考星供试样品1、供试样品2、供试样品3、替米考星对照样品,在酸中的溶出度见图7。结果显示,供试样品1在酸中溶解良好,累积溶出度为100%;供试样品2在酸中的累积溶出度为5.73%,供试样品3在酸中的累积溶出度为8.29%;替米考星对照样品在酸中的累积溶出度为2.36%,因此只有供试样品2和3符合兽药典对替米考星肠溶制剂在酸中溶出度小于10%的规定。

图7 不同替米考星供试样品在酸中的溶出曲线
2.2.5 缓冲液中累积溶出度 替米考星供试样品1、供试样品2、供试样品3、对照样品在5、10、15、20、30、40、50、60、75、90、120 min时累积溶出度见图8,结果显示替米考星供试样品1、2、3以及对照样品在缓冲溶液中的累积溶出度分别为100%、97.53%、93.60%和93.15%。

图8 不同替米考星供试样品在缓冲液中的溶出曲线
3 讨论
针对不同的动物和用药途径,目前市面上有许多不同剂型的替米考星制剂,包括可溶性粉末、预混剂、注射液、肠溶颗粒、固体脂质纳米粒、固体分散体等[8,10-13]。临床上预混剂、注射剂和肠溶颗粒最为常见。研究发现,替米考星预混剂口服给药后,吸收迅速,但是吸收不完全,并且替米考星味极苦,适口性差,给药比较困难[14]。通过对替米考星的注射剂研究发现,替米考星对心脏具有很强的毒性,进入血管的替米考星可以导致动物出现心动过速和心肌收缩力下降[10]。我国《兽药典》明确指出给猪肌肉注射10 mg/kg的替米考星后,会出现呼吸急促、呕吐和惊厥等不良反应,加大剂量至20 mg/kg进行肌肉注射时,大多数猪出现死亡等现象[9]。因此,同一种药物,经过不同生产工艺和制备技术所得到的不同制剂,其药物活性成分的释放速度、吸收程度以及安全剂量范围不尽相同。
试验中3种替米考星供试样品,为不同工艺和技术生产而成的颗粒制剂。研究结果显示,在酸液中5 min替米考星供试样品1累计溶出度已达63.83%,90 min可完全溶出,说明在酸性介质中,颗粒崩解快,能快速释放出主药成分,与对照品相比极显著(P<0.01);供试样品2、3在5 min时,累积溶出度分别为2.56%和5.54%,与样品1比有显著性(P<0.05),在90 min时累积溶出度分别为5.73%、8.29%,随时间不断增加,与其初测时间点溶出度相比较无显著差异(P>0.05),但于样品1 在90 min的溶出度差异显著(P<0.05)。从累积溶出度变化趋势看,样品1主要集中在40 min前,累积溶出度达到93%以上,40 min后溶出度速率变化不大;样品2、样品3累积溶出度速率变化与对照品变化趋势基本相同,从5 min~90 min不同的测定时间点之间累积溶出度变化无显著性差异(P>0.05)。
在磷酸盐缓冲溶液中,5 min时,样品1的累积溶出度明显高于样品2、样品3和对照品,而样品2、样品3与对照品之间无明显差异。在中间点60 min时,供试样品1、2、3的累积溶出度分别为94.88%、90.23%和82.96%,对照样品在60 min时累积溶出度为79.01%,3种供试样品累积溶出度均高于对照样品,其中样品1的累积溶出度最高。120 min时试样品1中替米考星已完全释放,样品2、样品3和对照样品的累积溶出度分别为97.53%、93.60%和93.15%,供试样品之间、供试样品与对照品之间累积溶出度均无显著差异(P>0.05)。试验结果表明,在缓冲溶液中,供试样品均具有理想的溶出度。
试验结果显示,试验中所用的供试样品所采用的原辅料的不同直接影响了在酸和缓冲液中溶出度。供试样品1未经过包被工艺直接由主药替米考星与辅料加工而成的颗粒,在酸和缓冲液中均容易释放出活性成分,供试样品2和供试样品3经过包被后,在酸中,溶出度呈下降趋势,对原药的释放具有很强阻抗作用,包被所用材料和所形成的包被结构具有很强的耐酸性,与对照品的累积溶出度无显著差异(P>0.05)。在磷酸盐缓冲液中,供试样品2和供试样品3溶出度趋势有差异性(P<0.05),这主要与两者的主药成分有关,供试样品2主药为替米考星,而供试样品3为磷酸修饰过的替米考星磷酸盐,结果显示出样品2在缓冲溶液中具有良好的释放效果。综合酸和缓冲液中3种供试样品的试验结果,依据兽药典的相关规定,供试样品2、3均符合肠溶制剂在酸中溶出量小于10%,在缓冲液中供试样品均符合累积溶出度不低于70%,与对照品相比较,均可以作为替米考星肠溶颗粒新制剂进一步研发,而供试样品1不宜作为肠溶颗粒制剂研发。

