右美托咪定复合咪达唑仑对胃肠道手术患者血流动力学及肠道功能的影响
鲁金钢 陈海平 楼益飞 刘 浩 刘 湛 赵鹏程 赵延涛 王伟达
我国胃肠道肿瘤的发病率居高不下[1]。手术作为目前治疗胃肠器质性病变主要方法,被临床广泛应用。但手术操作时间长且存在多种难以避免的操作损伤,因此在保障手术质量与安全前提下,尽可能减少麻醉药物对受术者生理机能的影响,备受医者重视[2]。右美托咪定(DEX)作为一种高亲和力的α2 受体激动剂[3],镇痛、抗交感作用优于可乐定,又因其保护重要脏器及无明显呼吸抑制的特点而广泛应用于临床麻醉[4]。本研究观察DEX 复合咪达唑仑对胃肠道手术患者血流动力学及肠道功能的影响。现报道如下。
1 资料与方法
1.1 一般资料 选择2016 年1 月至2019 年1 月于浙江大学附属西溪医院麻醉手术科行胃肠道手术的患者200 例,按照随机数字表法分为对照组和观察组,每组100 例。本研究经医院伦理委员会批准(审批编号:202202230218000403228)。所有患者均签署知情同意书。
1.2 纳入及排除标准 纳入标准:(1)胃肠原发疾病行胃肠道手术治疗者;(2)年龄在18~70 岁之间;(3)无手术麻醉禁忌证者;(4)依从性好,配合治疗者。排除标准:(1)不符合纳入标准者;(2)肿瘤远处转移者;(3)伴糖尿病、凝血功能障碍等,影响刀口愈合者;(4)已接受相关治疗,可能影响指标观测者;(5)伴随可能影响指标观测的其他状况者;(6)合并严重心肝肾功能障碍或其他严重器质性疾病、发育不全者;(7)特殊人群:妊娠、哺乳期、恶性肿瘤、精神病及心理障碍患者;(8)对本研究应用药物过敏者;(9)术中出现严重不良反应者;(10)患者或者家属不配合治疗者。
1.3 研究方法 两组患者于术前行清洁灌肠,术前6 h 禁水禁食,行术区备皮。入室后开通静脉通路,给予复方氯化钠6 mL/(kg·h);持续监测无创血压、心率、心电图、血氧饱和度;监测右侧桡动脉有创血压。麻醉诱导:两组均给予0.05 mg/kg 咪达唑仑(江苏恩华制药,批号H20031071)、2 mg/kg 丙泊酚、4 μg/kg芬太尼、0.1 mg/kg 维库溴铵,静脉注射。机械通气:插管导管接麻醉机通气,调整参数:吸气浓度(FiO2)100%、潮气量(VT)8~12 mL/kg、呼吸频率(RR)12 次/min;维持血氧饱和度98%~100%,呼气末二氧化碳分压35~45 mmHg(1 mmHg=0.133 kPa)。术中4~8 mg/(kg·h)丙泊酚、0.1~0.3 μg/(kg·h)瑞芬太尼右颈内静脉持续泵注,间隔30 min 给予3 mg 顺式阿曲库铵至手术操作结束。观察组麻醉诱导前15 min 给予0.5 μg/kg DEX(扬子江药业,批号21011531)静脉泵注,气管插管后给予0.5 μg/(kg·h),DEX 持续静脉泵注至手术操作结束前30 min;对照组给予7 mL 生理盐水静脉泵注,气管插管后给予10 mL/h 生理盐水持续静脉泵注至手术操作结束前30 min。待患者清醒,监测VT>300 mL、RR<30 次/min,评估患者术后综合状况符合拔管要求予拔除气管导管插管,送入监护室。
1.4 观察指标
1.4.1 血流动力学 Drager 监测仪监测心率(HR)、收缩压(SBP)、舒张压(DBP),穿刺置管后监测平均动脉压(MAP)。分别观察并记录术前、手术开始、手术1 h、拔管10 min 时的各监测值。
1.4.2 胃肠道功能 观察并记录患者术后肠鸣音恢复时间、首次排气、排便时间。
1.4.3 肠道通透性 分别于手术前后抽取患者静脉血6 mL,离心后,取上清液,放置于-20 ℃冰箱储存备检。使用放射化学法测定D 乳酸(D-Lac)、二胺氧化酶(DAO)。
1.4.4 炎性因子 分别于手术前后抽取患者空腹静脉血3 mL,4000 r/min 离心10 min,放置于-80 ℃冰箱储存,使用酶联免疫吸附法(艾迪康生物,批号201608983)测定血清白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)的变化。
1.5 统计学方法 应用SPSS 20.0 软件分析数据,正态分布的计量资料以均数±标准差()表示,组内采用配对t 检验进行比较,组间采用两独立样本t检验进行比较,计数资料以%表示,组间采用χ2检验进行比较,等级资料采用秩和检验进行比较,以P<0.05 为差异有统计学意义。
2 结果
2.1 两组胃肠道手术患者一般资料比较 两组患者的性别、年龄、体质指数、手术时间、出血量及术后住院时间比较,差异无统计学意义(P>0.05),具有可比性,见表1。

表1 两组胃肠道手术患者一般资料比较
2.2 两组胃肠道手术患者血流动力学比较 与对照组比较,手术开始、手术1 h、拔管10 min 观察组HR更慢(P<0.05),SBP、MAP 更低(P<0.05)。见表2。
表2 两组胃肠道手术患者血流动力学结果比较()
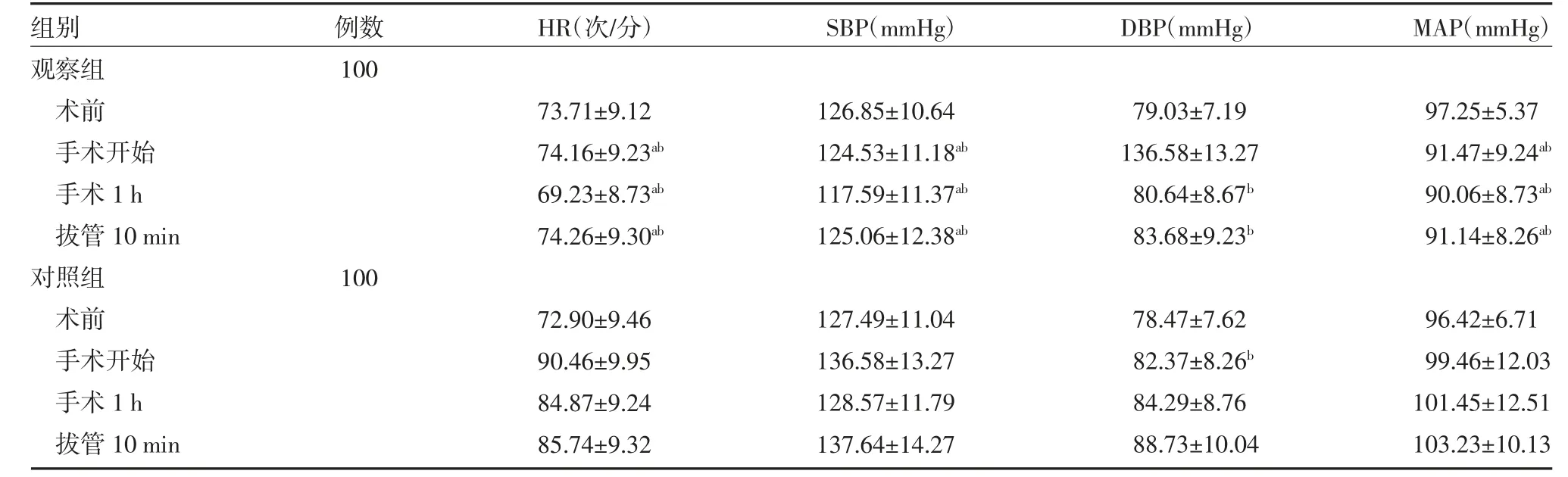
表2 两组胃肠道手术患者血流动力学结果比较()
注:观察组为右美托咪定干预,观察组为生理盐水干预;HR 为心率;SBP 为收缩压;DBP 为舒张压;MAP 为平均动脉压;与同组术前比较,aP<0.05:与对照组同期比较,bP<0.05;1 mmHg=0.133 kPa
2.3 两组胃肠道手术患者术后胃肠功能情况比较两组患者术后肠鸣音恢复时间、首次排气、排便时间观察组均短于对照组,差异有统计学意义(P<0.05)。见表3。
表3 两组胃肠道手术患者术后胃肠功能情况比较(d,)
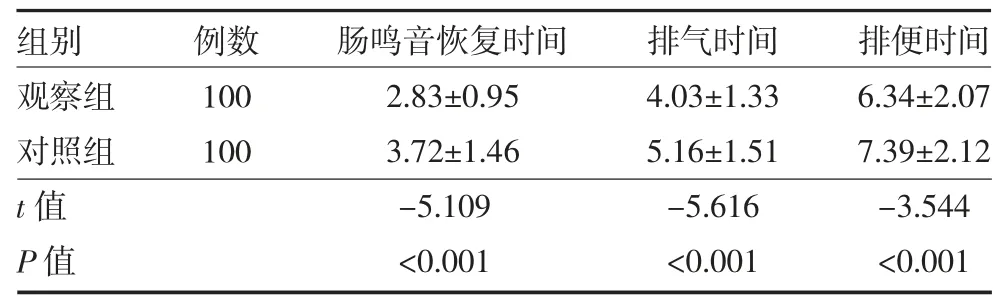
表3 两组胃肠道手术患者术后胃肠功能情况比较(d,)
注:观察组为右美托咪定干预,观察组为生理盐水干预
2.4 两组胃肠道手术患者肠道通透性比较 两组患者术前D-Lac、DAO 比较,差异无统计学意义(P>0.05)。术后与术前比较明显降低(P<0.05),观察组D-Lac、DAO 低于对照组(P<0.05)。见表4。
表4 两组胃肠道手术患者肠道通透性结果比较()
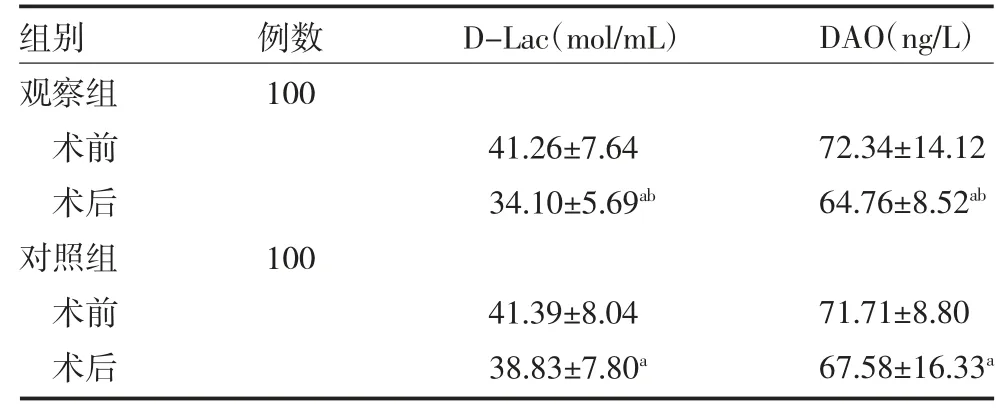
表4 两组胃肠道手术患者肠道通透性结果比较()
注:观察组为右美托咪定干预,观察组为生理盐水干预;D-Lac 为D乳酸;DAO 为二胺氧化酶;与同组术前比较,aP<0.05;与对照组同期比较,bP<0.05
2.5 两组患胃肠道手术者炎性因子变化 两组患者术前炎性因子比较,差异无统计学意义(P>0.05);术后两组血清TNF-α 明显减少(P<0.05),IL-6 均无明显变化(P>0.05)。见表5。
表5 两组胃肠道手术患者手术前后炎性因子变化比较(ng/L,)
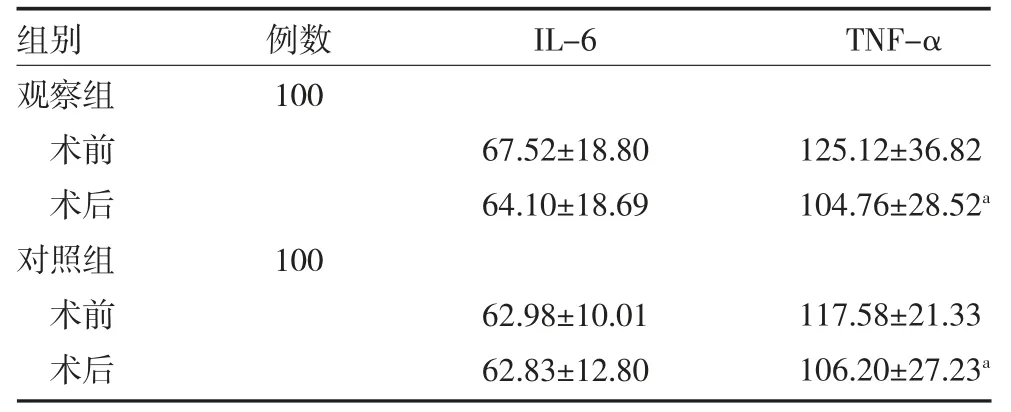
表5 两组胃肠道手术患者手术前后炎性因子变化比较(ng/L,)
注:观察组为右美托咪定干预,观察组为生理盐水干预;IL-6 为白细胞介素-6;TNF-α 为肿瘤坏死因子-α;与同组术前比较aP<0.05
3 讨论
围手术期应激反应是影响手术的关键因素,其受术中操作、麻醉以及患者自身的生理心理状况的影响,可引发消化、循环等系统的综合反应而影响预后[5]。血流动力学的波动及肠道功能作为主要的应激反应,在围手术期受到医护人员的主要关注。有研究指出,腹部手术患者在诱导麻醉前给予DEX 可降低交感-肾上腺系统的反射性兴奋,有效抑制围手术期应激反应,同时可减少麻醉药用量,降低对胃肠功能的影响,促进术后恢复[6-8]。
手术麻醉药物对循环系统有一定程度的抑制作用,加之疾病过程中患者自身生理代偿机能降低,故在诱导麻醉期间轻微的刺激即可引起心血管系统的较大波动,出现BP 增高、HR 加快[9]。麻醉诱导前DEX的使用一方面可减少气管插管时物理刺激引发的交感兴奋[10],另一方面通过结合α2 受体,抑制去甲肾上腺素引发的神经介质释放,均衡肾上腺素能与迷走张力,减少心血管系统反应[11]。本研究结果显示,手术开始、手术1 h、拔管10 min,观察组HR 明显慢于对照组,SBP、DBP、MAP 低于对照组,且与术前比较无显著变化,提示麻醉诱导前给予DEX 联合咪达唑仑较单纯咪达唑仑在围手术期更有利于维持血流动力学的稳定。DEX 抑制交感神经兴奋性,表现为血流动力学改变,主要与α2 肾上腺素能受体结合发挥镇静、催眠、镇痛、交感神经抑制、神经保护、调节儿茶酚胺释放等生理效应。
有研究指出,麻醉常用阿片类药物可引发支气管痉挛导致呛咳,出现剧烈的血流波动,甚则并发心脑血管疾病,而提前静脉注射DEX 可阻断儿茶酚胺释放引发的气管痉挛及药物性肌肉强直,维持血流稳定[12-13]。本研究结果显示,观察组肠鸣音恢复时间、首次排气、排便时间均短于对照组,提示可促进术后胃肠功能的恢复。胃肠手术中由于诸多损伤因素的存在会对患者胃肠运动产生不同程度的抑制,重者导致肠粘连、肠梗阻等并发症,因此尽早恢复胃肠功能与手术预后密切相关。在创伤、应激、缺血再灌注损伤、感染等病理状态下会出现肠道屏障功能损伤、肠道通透性增强,肠道菌群及毒素移位入血引发肠源性脓毒血症以及多器官功能障碍综合征(MODS);DEX 可通过胆碱能抗炎途径抑制炎性因子的释放,从而发挥肠道屏障功能的保护作用,促进肠道动力恢复、减轻肠道炎症反应、促进肠道微循环灌注、减轻肠道缺血再灌注损伤以及改善肠道通透性。诱导麻醉前DEX 的使用减少了麻醉期间阿片类镇痛药物的用量,从而抑制了肠道痉挛的发生,同时可减少黏膜中代谢物的产生,减少对肠道的刺激性损害,增加肠平滑肌的血液循环,促进胃肠蠕动,实现尽早排气、排便[14]。
本研究结果还显示,观察组D-Lac、DAO 低于同期对照组,观察组术后TNF-α 较对照组明显减少,两组IL-6 均没有明显变化,提示DEX 联合咪达唑仑较单纯咪达唑仑能更好地改善肠道上皮通透性,发挥抗炎作用。迷走神经在肠道构成了大量调节免疫的炎性反射弧[15],而DEX 作为α2 受体激动剂可激动迷走神经的胆碱能抗炎通路,神经胶质细胞得以活化,抑制NF-κB 信号通路系统,从而阻断链激酶对上皮蛋白的作用,调控紧密连接蛋白的表达,抑制肠道TNF-α 释放,保护因炎症因子导致的肠道损伤,两者协同,可能发挥抗炎与屏障保护作用[16-17]。
综上所述,DEX 联合咪达唑仑可有效稳定胃肠道手术患者血流动力学波动,具有抗应激、抗炎、促进术后肠道功能的恢复,保护肠道屏障,符合快速康复的理念。推荐用于创伤大、手术时间长以及经历缺血再灌注损伤的腹内手术。同时,DEX 联合咪达唑仑还可以缓解术后疼痛、减少术后阿片药物的使用量,有利于患者早期下床活动,促进术后肠道动力的恢复,具有良好的临床应用价值。

