司美格鲁肽联合二甲双胍治疗初诊2型糖尿病合并非酒精性脂肪肝的疗效分析
陈婷,邓斌,廖占林
南平市第一医院内分泌科,福建 南平 353000
糖尿病属于终身性疾病,而2型糖尿病(type 2 diabetes,T2DM)作为高发于中老年人群体中的糖尿病类型,若伴有非酒精性脂肪肝(non alcohol fatty liver disease NAFLD)病症,将加大治疗难度,故此需要优选药物,实现疾病的高效治疗。以往对于T2DM患者,常口服降糖药,保持血糖水平的平稳,而对于合并NAFLD患者,单一的降糖治疗,无法达到预期效果,长此以往将增加疾病进展风险。若能在口服降糖药的同时使用司美格鲁注射药物,可在保护心脑血管系统之上保持体质平稳,为降糖治疗起到辅助补充作用,进而提升治疗有效性,为患者提供可靠的安全保障[1-3]。本文选取2020年1月—2022年6月南平市第一医院内分泌科收治的62例初诊T2DM合并NAFLD患者,旨在分析司美格鲁肽联合二甲双胍的临床效果,现报道如下。
1 资料与方法
1.1 一般资料
选取本院收治的62例初诊T2DM合并NAFLD患者作为研究对象,以不同疗法将其划分为两组,每组31例。对照组男22例,女9例;平均年龄(45.68±3.68)岁;平均病程(1.68±0.06)个月。观察组男21例,女10例;平均年龄(44.78±3.54)岁;平均病程(1.75±0.07)个月。两组患者一般资料比较,差异无统计学意义(P>0.05)。具有可比性。本研究经过医学伦理委员会准予,科室领导给予必要性支持。
1.2 纳入与排除标准
纳入标准:①均在临床诊断(肝功检查、生化检验等)中属于确诊者,且均为成年人;②均表现出优良的依从性,遵照医嘱按时服药;③知情同意书上已有全体参与者亲笔签名;④除研究中涉及疾病外未见其他器质性病变。
排除标准:①精神疾病以及心理疾病者;②肝肾功能先天发育不全或肢体残疾、丧失自理能力者;③免疫系统异常或吞咽困难、药物过敏者;④妊娠期女性或哺乳期女性。
1.3 方法
对照组患者口服二甲双胍缓释片(国药准字H20178002;规格:0.5 g),按照整片吞服方式,选择在进餐中或餐后口服,药物剂量控制在1次/d,500 mg/d(1片)。若患者血糖指标偏高,可以考虑在医嘱下增加药量,但最大日服剂量应在2 000 mg以下,以2次/d,1 000 mg/次药量改善药效[4-6]。
观察组患者应用二甲双胍缓释片与司美格鲁肽注射液(国药准字SJ20210015;规格:3 mL,1.34 mg/mL),其中口服二甲双胍用法用量同对照组。指导患者按照每7天注射1次的药量,以注射给药方式自行注射,注射部位除了大腿及腹部外,也可以选择在上臂注射。在每一针剂药物使用期间,要求前后使用时间间隔48 h以上,不可连续给药。记录用药后患者病情好转程度[7-11]。
两组均持续治疗3个月。
1.4 观察指标
观察治疗后两组患者的不良反应发生率;观察治疗前后两组患者身体素质指标变化情况;观察治疗前后两组患者临床指标变化情况。
体质指数(body mass index,BMI)正常范围:18.5~23.9 kg/m2;空腹血 糖(fasting plasma glucose,FPG)应控制在7 mmol/L以下;餐后2 h血糖(postprandial plasma glucose,2 hPG)<9 mmol/L;三酰甘油(glycerin trilaurate,TG)与总胆固醇(total cholesterol,TC)正常值为1.7 mmol/L以下、5.18 mmol/L以下;天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)与丙氨酸氨基转移酶(alanine aminotransferase,ALT)正常值:8~40 U/L、5~40 U/L(男性),5~35 U/L(女性)。
1.5 统计方法
采用SPSS 21.0统计学软件对数据进行分析,计量资料经检验符合正态分布,采用(±s)表示,进行t检验,计数资料采用[n(%)]表示,进行χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组患者不良反应发生率比较
治疗后,观察组不良反应发生率为3.23%,与对照组的16.14%相比,差异无统计学意义(P>0.05),见表1。
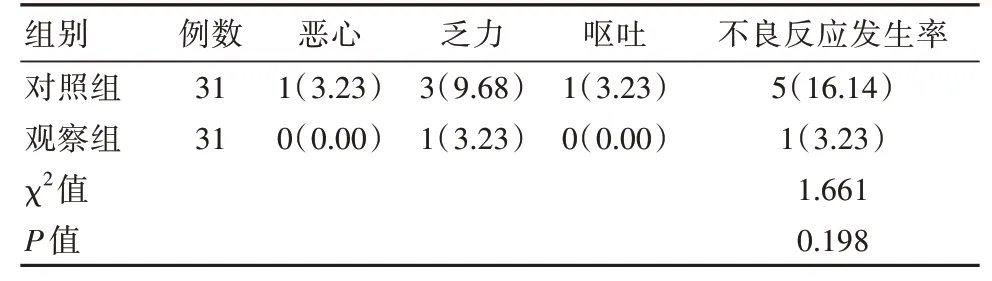
表1 两组患者不良反应发生率对比[n(%)]
2.2 两组患者治疗前后身体素质指标比较
治疗前,两组患者身体素质指标比较,差异无统计学意义(P>0.05);治疗后,两组身体素质均改善,且观察组患者指标优于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组患者治疗前后身体素质指标对比(±s)

表2 两组患者治疗前后身体素质指标对比(±s)
组别对照组(n=31)观察组(n=31)t值P值体质量(kg)治疗前79.38±6.49 79.37±6.36 0.006 0.995治疗后77.37±3.28 75.37±2.42 2.731 0.008 BMI(kg/m2)治疗前28.37±2.02 28.36±2.04 0.019 0.984治疗后28.01±1.03 27.02±0.85 4.336<0.001
2.3 两组患者治疗前后临床指标比较
治疗前,两组患者临床指标比较,差异无统计学意义(P>0.05);治疗后两组临床指标均改善,且观察组改善情况优于对照组,差异有统计学意义(P<0.05),见表3。
表3 两组患者治疗前后临床指标对比(±s)

表3 两组患者治疗前后临床指标对比(±s)
指标血糖指标(mmol/L)血脂指标(mmol/L)肝功指标(U/L)FPG 2 hPG TC TG ALT AST时间治疗前治疗后治疗前治疗后治疗前治疗后治疗前治疗后治疗前治疗后治疗前治疗后对照组(n=31)9.57±2.14 8.23±1.27 11.28±1.02 9.98±0.65 6.94±0.54 5.42±0.27 1.68±0.03 1.32±0.02 60.08±4.32 52.36±2.84 55.38±5.38 48.72±2.53观察组(n=31)9.62±2.13 7.07±0.52 11.33±1.01 9.01±0.04 6.92±0.52 4.33±0.32 1.66±0.02 0.82±0.01 60.09±4.29 22.38±2.05 55.27±5.36 30.10±2.16 t值0.688 4.706 0.582 8.293 0.589 14.495 1.238 124.199 0.599 47.657 0.588 31.164 P值0.456<0.001 0.116<0.001 0.262<0.001 0.182<0.001 0.587<0.001 0.535<0.001
3 讨论
NAFLD实则与患者的胰岛素功能障碍、肝损伤有关,初期发病时未见显著病症,多在肥胖超重人群中发作。因T2DM患者在日常治疗中,始终以血糖控制为基础,导致降糖时引起血脂指标降低,对肠道系统亦有调节作用[12]。然而,对于合并NAFLD患者,在单纯服用二甲双胍降糖药期间,虽然也能实现脂肪肝的辅助治疗,但易引起肝功能异常[13-14]。而本研究中提出联合用药计划,是将二甲双胍药物与司美格鲁肽药物进行联用,由此促进脂肪酸氧化速度的提高,减缓肝脏病变速度。依据权威性杂志理论研究结果,此种药物作为GLP-1类似物,可以优化胰高血糖素分泌水平。尤其在持续降糖中,可降低低血糖发生风险[15]。同时,此类药物作为一周仅用一次的药物,本身的安全性更强,能够合理控制患者体质量,既不会因糖尿病病症刺激出现体质量骤降情况,又能表现出优良耐受性,甚至具备显著的心血管代谢能力,在调节患者代谢水平过程中,保持降糖效果的持久性作用[16-17]。本研究结果显示,治疗后,观察组患者体质量 为(75.37±2.42)kg,BMI(27.02±0.85)kg/m2;FPG(7.07±0.52)mmol/L,2 hBG(9.01±0.04)mmol/L,TC(4.33±0.32)mmol/L,TG(0.82±0.01)mmol/L,ALT(22.38±2.05)U/L,AST(30.10±2.16)U/L,均优于对照组(P<0.05)。两组不良反应发生率比较,差异无统计学意义(P>0.05)。表明联合治疗方案的安全性较强,不易增加不良反应发生风险。在实际应用期间,针对T2DM合并NAFLD患者整体效果较好,既能有效改善身体素质,又能合理保持血糖、血脂以及肝功指标平稳。韩美芬等[18]以肥胖症为研究对象,发现在使用司美格鲁肽药物时,能够有效保护心血管,并对肝脏病变产生调节改善作用,而且可以延缓胃排空速度,对糖尿病患者的“多食”病症有针对性改善效果,联用优势明显。
综上所述,T2DM合并NAFLD在二甲双胍联合司美格鲁肽治疗下疗效突出,安全性强,可扩大应用范围,将其作为临床优选方案。

