利妥昔单抗联合糖皮质激素治疗天疱疮临床疗效和安全性评价
李晔,农祥,黄玲,王敏,俞奕彤,何黎
天疱疮是一种累及皮肤和黏膜的慢性、复发性自身免疫性大疱病,临床分型中以寻常型天疱疮(pemphigus vulgaris,PV)和落叶型天疱疮(pemphigus foliaceus,PF)较常见[1]。针对桥粒芯蛋白(Desmoglein,Dsg)1和3的自身抗体在PV/PF的发病中起主要作用,且抗体滴度与临床病情严重程度和活动度相关[2]。糖皮质激素(corticosteroids,CS)联合免疫抑制剂是治疗天疱疮的经典方案,能够降低其死亡率。但随着时代和医疗水平的进步,在降低死亡率同时,人们追求更低的不良反应和并发症,因此,靶向治疗的生物制剂越来越受关注。利妥昔单抗(rituximab,RTX)是第一代抗CD20单克隆抗体,能针对性的消耗B淋巴细胞、间接清除自身抗体。目前,英国皮肤科医生协会、欧洲皮肤病学和性病学会、法国皮肤病学会等协会指南推荐包括轻度PV、PF在内的天疱疮一线治疗中加用利妥昔单抗[3-5],我国2020年PV治疗专家建议在中重度天疱疮患者中可采用糖皮质激素联合利妥昔单抗治疗[2]。但国内关于利妥昔单抗治疗天疱疮的研究文献较少,多为个案报道,因此笔者进行本次利妥昔单抗联合糖皮质激素治疗天疱疮的前瞻性研究,评估利妥昔单抗治疗PV/PF的疗效及安全性。
1 材料和方法
1.1研究对象 2020年10月-2021年11月在昆明医科大学第一附属医院及大理大学附属医院就诊的37例天疱疮患者。纳入标准:符合PV/PF的诊断标准[2],其中酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)检测抗Dsg1抗体阳性或/和抗Dsg3抗体阳性;天疱疮疾病面积指数(pemphigus disease area index,PDAI)活动性损害评分≥9分,包括新诊断未经治疗或传统方案治疗控制不佳的患者(newly diagnosed patients, NDPs)和既往治疗后复发加重的患者(patients with previous treatment, PTPs)。排除标准:合并肝炎、结核及较严重的细菌、真菌或病毒感染;合并肿瘤;严重内脏系统损害或免疫力低下;妊娠和拟妊娠妇女;有精神疾病、不能配合治疗;不宜参加研究的其他情况。本研究经昆明医科大学第一附属医院伦理委员会批准,所有研究对象签署知情同意书。
1.2方法 37例天疱疮患者分为两组,试验组以0.4~0.8mg/(kg·d)静脉滴注甲泼尼龙(methylprednisolone,MP)联合“类风湿方案”给予利妥昔单抗共2 g(即Day0和Day14以1 g剂量静脉滴注利妥昔单抗),糖皮质激素减量:40~60 mg/d时每周减量8~10 mg,16~40 mg/d时每2周减量2~6 mg,达16 mg/d时每2周减量2~4 mg;减量至≤8 mg/d时可每3~6个月减量2 mg,减至4~6 mg/d后长期维持治疗。对照组以0.8~1.2 mg/(kg·d)单独静脉滴注糖皮质激素(以甲泼尼龙为计算)或静脉用糖皮质激素联合环孢素(cyclosporin A,CsA),糖皮质激素减量:50~70 mg/d时,每1~2周减20%;30~50 mg/d时,每1~2周减8 mg;16~30 mg/d时,每2~4周减量2~8 mg;达16 mg/d时,每月减2~4 mg,直至≤8 mg/d长期维持;环孢素以3~5 mg/(kg·d)口服,逐渐减量。基线(治疗前)、4、8、16、24周,以后每12周对患者进行随访,采用PDAI评分系统对皮肤、黏膜、头皮的活动性损害进行评分,记录用药量、不良反应发生情况,ELISA法测定抗Dsg1、Dsg3抗体值(≥20判为阳性)。
1.3疗效判定和结局指标
1.3.1疗效判定 参照《寻常型天疱疮诊断和治疗专家建议》[2];将停止治疗后完全缓解、治疗中完全缓解、停止治疗后部分缓解以及最小量(≤8 mg/d 甲泼尼龙或最低量免疫抑制剂)治疗的部分缓解均标记为完全缓解;复发:每月新发皮损超过3个,且在1周内不能自愈,或已经控制病情的患者原有皮损增多。
1.3.2主要观察指标 包括治疗24周后的完全缓解率、糖皮质激素累积剂量和不良反应的比较;次要指标为24周后抗体值的变化和比较。
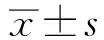
2 结果
2.1临床资料 两组患者年龄、性别、体重、临床分型、既往疾病、基线时病程、诊疗类型(初诊或复诊)、初始PDAI评分以及研究至今随访时间等基本特征差异均无统计学意义(P>0.05),组间可比性较高,见表1。其中,试验组有3例初治、经大剂量糖皮质激素(>1.2 mg/kg甲泼尼龙)联合免疫球蛋白和/或免疫抑制剂治疗后仍不能控制病情的难治性重度天疱疮患者[6]。
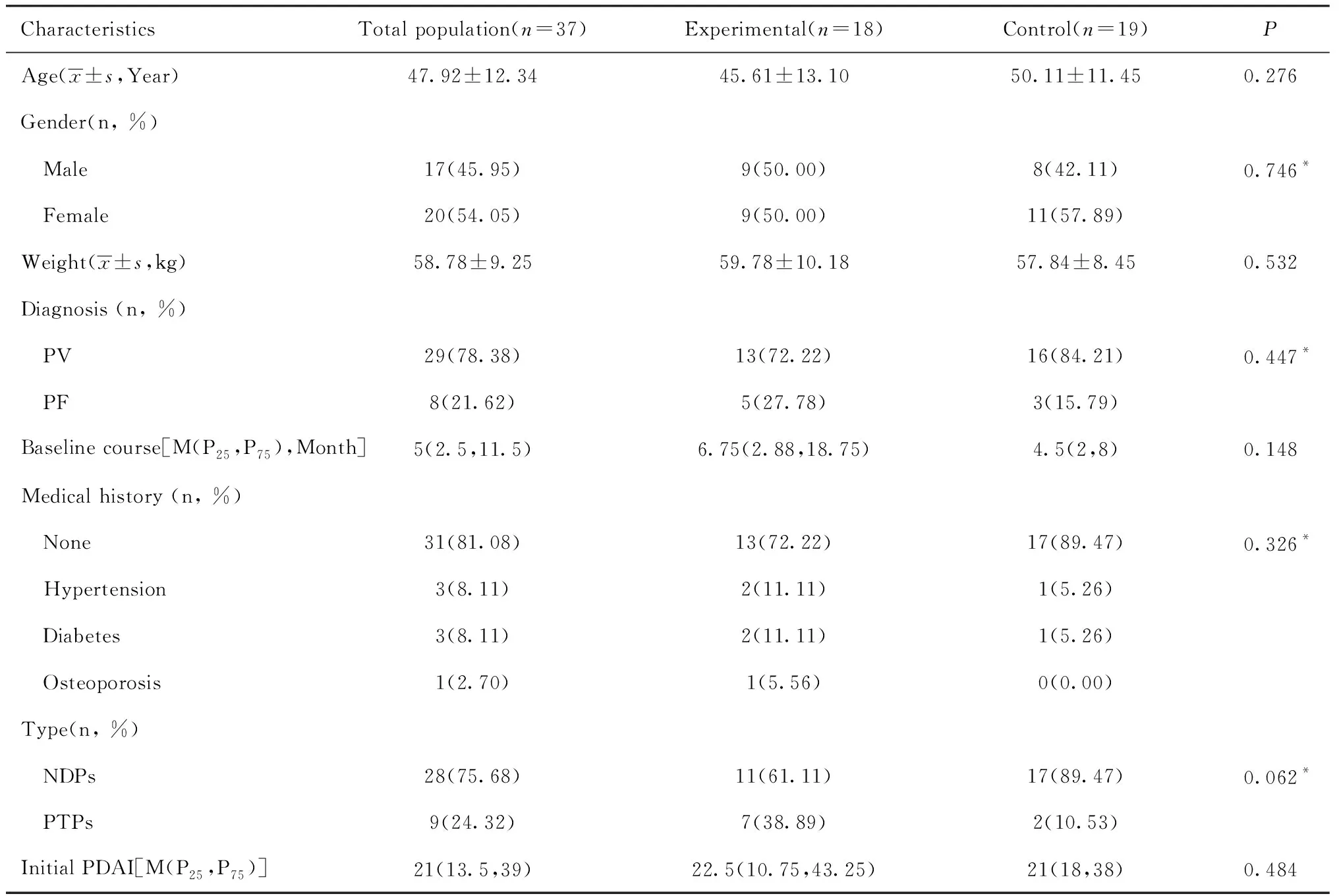
表1 研究对象的基本特征Tab.1 Basic characteristics of the research object
2.2疗效和累积糖皮质激素剂量 治疗24周后试验组9例患者达完全缓解,复发1例;对照组中2例达完全缓解,复发1例,经Fisher确切概率法检验,差异有统计学意义(P<0.05)。剔除试验组反复复发、自行调整糖皮质激素剂量的1例和对照组在16周死亡1例,24周后试验组人均累积甲泼尼龙低于对照组(t=-2.33,P<0.05),见表2。1例患者采用利妥昔单抗联合糖皮质激素治疗前和治疗24周后临床图片见图1。

表2 24周后组间疗效和累积甲泼尼龙剂量比较Tab.2 Comparison of efficacy and cumulative MP dose between groups after 24 weeks
2.3不良反应 治疗前至24周后,试验组18例患者中有12例出现不良反应,其中感染5例,发生率为27.78%,包括肺部真菌感染2例,败血症、皮肤感染和口腔黏膜真菌感染各1例,均住院治疗后好转。利妥昔单抗治疗后皮损加重2例,分别合并多形红斑和松弛性水疱、大疱、表皮松解坏死(图2),考虑并发药疹;均住院予大剂量甲泼尼龙,辅以免疫球蛋白、支持治疗等,病情控制后甲泼尼龙正逐渐减量中。血糖升高、毛囊炎及体重大幅增加(>10 kg)各1例;发热和肌痛发生在1例患者第一针利妥昔单抗输注过程中及输注后24 h内,对症治疗后缓解,再次输注利妥昔单抗时无不适。对照组19例患者共观察到42例不良反应,其中感染9例(47.37%),包括3例肺部感染,其中1例住院治疗无效死亡,2例治疗后好转;败血症和皮肤/黏膜感染各2例,肾脓肿和病毒感染各1例,住院治疗好转。其余白内障5例,骨折4例,骨质疏松3例,血压升高、血糖升高各2例,消化道出血、冠心病和心脏增大分别1例,面部激素依赖性皮炎、毛囊炎、肌无力各3例,体重大幅增加(>10 kg)和睡眠障碍各2例,月经紊乱1例,均至医院门诊或住院治疗后好转。
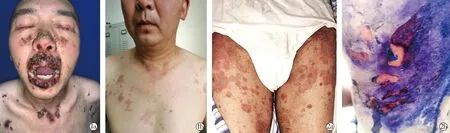
图1a 治疗前图片; 图1b 治疗24周后图片; 图2a 全身可见大小不等的红斑,大腿两侧可见靶形红斑; 图2b 全身鳞片侵蚀多,大小不一,表皮疏松脱落明显Fig.1a Clinical picture before treatment; Fig.1b 24 weeks after treatment; Fig.2a Erythema of different sizes could be seen all over the body, and target erythema could be seen on both thighs; Fig.2b There were many different sizes of flake erosion in the whole body, and the epidermis was loosened and exfoliated obviously
2.4抗体值变化 本研究中所有PV患者抗Dsg1、Dsg3抗体均阳性,PF患者仅抗Dsg1抗体阳性。采用利妥昔单抗联合糖皮质激素治疗的18例患者中,纳入规律检测抗体浓度至24周的PV患者10例,PF患者4例,因此统计抗Dsg1抗体值共14例,抗Dsg3抗体值共10例。基线时两组抗体值差异无统计学意义(P>0.05),24周后试验组抗Dsg1、Dsg3抗体值均较对照组低(P<0.05),见表3~4。试验组抗Dsg1值及抗Dsg3值在治疗后即迅速下降,16周后逐渐向阴性值转变;对照组16周前呈下降趋势,之后未再向阴性值趋近(图3)。

表3 治疗前后组间抗Dsg1抗体水平比较 [M(P25,P75),U/mL]Tab.3 Comparison of anti-Dsg1 antibody levels between groups [M(P25,P75),U/mL]
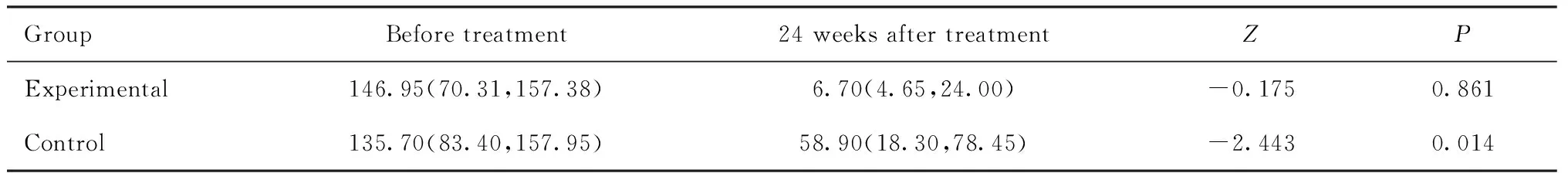
表4 治疗前后组间抗Dsg3抗体水平比较 [M(P25,P75),U/mL]Tab.4 Comparison of anti-Dsg3 antibody levels between groups [M(P25,P75),U/mL]
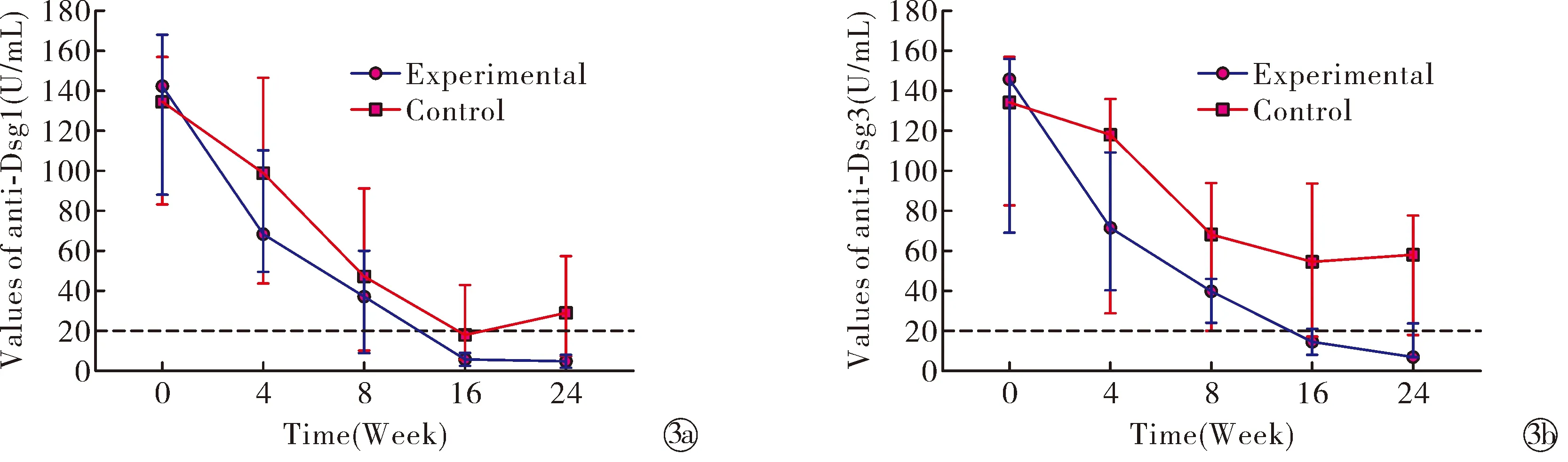
图3 治疗前后两组的抗Dsg1抗体和抗Dsg3抗体水平值Fig.3 The values of anti-Dsg1 and anti-Dsg3 in the two groups before and after treatment
3 讨论
本研究纳入37例天疱疮患者进行前瞻试验,试验组按单疗程“类风湿方案”予2次利妥昔单抗输注,糖皮质激素快速减量至最小量并长期维持治疗。与对照组相比,试验组24周后的完全缓解率更高(10.53% vs. 50.00%),人均累积糖皮质激素剂量及不良反应更少,抗体滴度在治疗后下降更快,24周后滴度更低、更稳定。可见,利妥昔单抗联合糖皮质激素治疗天疱疮具有良好疗效,能够提高患者24周完全缓解率,减少糖皮质激素用药量和大剂量糖皮质激素和免疫抑制剂相关不良反应。
国内关于利妥昔单抗治疗皮肤疱病的系统性研究报道不多,本研究采用前瞻性、对照设计,对37例患者进行治疗和随访。试验组24周后的完全缓解率为50.00%(9/18),与Toosi等[7]进行的利妥昔单抗治疗天疱疮的前瞻性研究结果相近,在他们的试验中,第3、6、9、12个月时观察到的完全缓解率分别为37.4%、61.7%、69.8%以及72.3%。国外学者Leshem[8-9]进行无对照利妥昔单抗治疗天疱疮患者临床观察,6个月时的完全缓解率为90%,高于本组数据结果,分析可能与该试验组观察例数较少(10例)以及糖皮质激素减量较快相关。
本研究初期两组PDAI评分及抗体值等均无明显差异,但与对照组相比,试验组既往治疗后复发加重的患者(PTPs)比例较高(38.89% vs.10.53%),部分新诊断的患者(NDPs)经大剂量糖皮质激素辅助免疫抑制剂或免疫球蛋白等治疗后病情仍未控制、相对顽固。治疗期间,除了2例患者罕见地出现药疹、病情加重,按“类风湿方案”两次输注利妥昔单抗联合较低剂量糖皮质激素仍能够快速控制病情,实现糖皮质激素早期快速减量,直至4~8 mg/d维持治疗,按此疗法随访>20个月的2例患者未见复发及明显不良反应,这与国外学者在12及18个月时重复利妥昔单抗输注,并3~6个月停止糖皮质激素治疗不同[10]。
抗Dsg抗体可部分反应疾病严重程度和活动情况,如随访期间出现抗体值升高,提示病情可能加重或者复发[2, 11]。研究中两组抗体值在治疗后均呈下降趋势,对照组16周后部分患者抗Dsg1或抗Dsg3抗体值出现上升,而试验组治疗后抗体更快地下降至阳性预测值以下并保持稳定。
糖皮质激素和免疫抑制剂是PV/PF治疗史上的里程碑,糖皮质激素的应用使得PV的死亡率从75%降至30%,加用免疫抑制剂后降到5%左右[12]。虽能有效降低死亡率,但长期大剂量糖皮质激素治疗易出现并发症,有研究表明,近年来大部分PV患者死于其治疗后的严重并发症,而非疾病本身[13]。本研究中,对照组19例患者共发生42例次不良反应,其中1例患者因肺部感染于16周后死亡。试验组研究期间不良反应较对照组少,与联合利妥昔单抗治疗后糖皮质激素累积剂量减少相对应。Chen等[14]对法国的随机试验数据[10]进行后期独立分析,指出接受利妥昔单抗治疗的患者糖皮质激素暴露较少,发生严重或威胁生命的糖皮质激素相关AE的可能性较小。正如报道中感染是利妥昔单抗治疗天疱疮最常见的不良反应[15],本观察中试验组共发生5例感染,包括2例皮肤感染、2例肺部真菌感染和1例败血症。但与单独糖皮质激素或糖皮质激素联合环孢素治疗相比,试验组感染发生率明显减少(27.78% vs. 47.37%)。
本研究中,单疗程“类风湿方案”输注利妥昔单抗联合后期长期小剂量糖皮质激素维持治疗天疱疮,疗效良好、安全性较高;与国外患者“3~6个月停止糖皮质激素治疗并重复利妥昔单抗输注”方案相比,患者经济负担相对较轻,但应谨防感染和药疹。利妥昔单抗相关药疹虽报道较少,但不同个体对药物反应存在差异,随着该药应用越来越广,如能寻找方法有效帮助预防相关药疹将使患者受益。

