壳聚糖改性及改性壳聚糖应用研究进展
汤 薇,董 静,赵金荣,Volodymyr BESSARABOV,蒋晓杰,杨效登
(1.齐鲁工业大学(山东省科学院) 化学与化工学院,山东 济南 250353,中国;2.火箭军士官学校,山东 潍坊 262500,中国;3.基辅国立工艺设计大学,基辅 01011,乌克兰;4.绍兴职业技术学院 建筑与设计艺术学院,浙江 绍兴 312000,中国)
壳聚糖(chitosan)又称脱乙酰甲壳素,是甲壳素在碱性条件下脱去分子中的乙酰基后的产物[1],是自然界中产量仅次于纤维素的生物多糖,也是唯一的一种碱性多糖。壳聚糖的化学名称为聚葡萄糖胺(1,4)-2-氨基-B-D-葡萄糖。固态壳聚糖是一种半结晶聚合物,表面为白色,略有珍珠光泽,是一种无定形半透明的片状固体。壳聚糖的内部呈线性双螺旋结构,6个糖残基构成一个螺旋平面,螺旋间距为0.515 mm。壳聚糖分子中的羟基、氨基和未脱去的N-乙酰氨基在分子间和分子内形成大量氢键,使壳聚糖分子形成紧密的晶体结构(即晶相区),难溶于水和碱性溶液,只能溶于盐酸、醋酸、乳酸、苯甲酸、甲酸等稀酸溶液[2]。
壳聚糖具有生物降解性、细胞亲和性和生物相容性等优良性质[3],在医药、食品、化工、化妆品、水处理、金属提取及回收生化和生物医学工程等诸多领域具有重要潜在应用。马宁等[4]发现分子质量为3 kDa的高脱乙酰度壳聚糖的吸湿性和保湿性最强,与对照组丙三醇的保湿率接近。将壳聚糖的醋酸溶液涂布于玻璃板上,可得到质地均匀的透明膜,将这些膜覆盖于果蔬食品,可以延缓它们颜色的改变,防止富含脂肪食品因氧化酸败而引起的营养质量下降。同时,壳聚糖膜可以降低果蔬呼吸强度,减少自由基对果蔬的伤害,保持果实的坚硬程度,维持果蔬较高的干物质含量[5-7];但是,壳聚糖的水难溶性限制了其在众多领域的广泛应用,因此人们尝试通过化学改性来增大其溶解度,赋予其更多功能,扩展其应用范围。本文中对壳聚糖改性和改性壳聚糖的应用进行综述和展望。
1 壳聚糖改性及改性壳聚糖的性质
壳聚糖分子有C6位伯羟基、C3位仲羟基以及C2位伯氨基等较强反应活性的官能团,可通过功能化修饰或改性方法改善其水溶性,同时赋予壳聚糖各种功能特性。常见的壳聚糖改性方法有酰基化、羧基化、醚化、烷基化、季铵化、交联、共聚改性等[8]。
1.1 酰基化改性
酰基化改性是最早的一种壳聚糖改性方法,酰基化试剂一般用酸酐、酰氯等。酰基化改性的结果是破坏大分子的结构,减小结晶度,增大溶解度。韩怀芬等[9]利用乙酸酐和邻苯二甲酸酐在壳聚糖的伯氨基上进行酰基化反应使其溶解度增大,发现以乙醇为溶剂对壳聚糖进行酰基化,有1/2的氨基被酰化。酰基化壳聚糖自身接入亲水基团,同时其晶体结构被破坏,因此能很好地溶解于水中。齐从丽等[10]利用马来酸酐对壳聚糖进行N-酰基化改性,发现改性产物的产率随N-酰化改性程度的增加而降低,但是,水溶性随着马来酰胺酸基含量的增大而改善。陈建澍等[11]用丁二酸酐在反应温度为50 ℃、反应时间为4 h的条件下酰基化壳聚糖,得到了水溶性最佳的N-琥珀酰壳聚糖,溶解度达到9.72。于沛沛等[12]利用苯甲酰氯与壳聚糖进行酯化反应,制备了具有良好水溶性的苯甲酰氯改性壳聚糖,在pH为3.5~7.5范围内,改性壳聚糖具有良好的抑菌性。该反应的最佳条件为苯甲酰氯与壳聚糖重复单元物质的量比为6∶1,反应温度为0 ℃,反应时间为3 h。Cok等[13]制备了具有pH和热双重响应性的N-异丙基壳聚糖,结果显示,异丙基的引入使壳聚糖的溶解度增大,改善了多糖骨架的柔韧性,细胞生长实验结果表明,N-异丙基壳聚糖具有良好的生物相容性。
酰基化反应也可以在羟基上进行,生成O-酰基化壳聚糖。由于羟基的反应活性弱于氨基的,因此,对壳聚糖进行O-酰化反应时需要使用苯甲醛对反应活性强的氨基进行保护,完成O-酰化反应后再脱掉保护基,否则极易同时在C2位氨基和C6位羟基上发生酰化反应。王朝等[14]先通过Eschweiler-Clarke反应再滴入乙酰氯生成具有良好水溶性的N,N,N-三甲基-O-己酰基壳聚糖。Jenkins等[15]用氯乙酸酐酰化壳聚糖,该反应在C2位氨基和C6位羟基上同时发生酰化,N-氯乙酰化率、O-氯乙酰化率分别为0.32和0.15。N-邻苯二甲酰壳聚糖衍生物比N,O-邻苯二甲酰化壳聚糖衍生物活性高,完全脱乙酰化壳聚糖与联苯二甲酸酐反应生成N-邻苯二甲酰壳聚糖在极性溶剂中溶解度较大[16]。
1.2 羧基化改性
羧甲基是亲水基团,羧甲基改性壳聚糖的水溶性明显优于壳聚糖的[17],羧甲基的取代度大于0.6时,羧甲基壳聚糖易溶于水。羧甲基的取代度越大,改性壳聚糖的溶解度越大。通常,N,O-羧甲基壳聚糖在pH<2和pH>6的水溶液中均能溶解。反应条件也影响O-羧甲基壳聚糖的溶解性。在反应温度为0~20 ℃时,由氯乙酸改性制得的羧甲基壳聚糖在所有pH范围内都具有良好的水溶性。当反应温度高于20 ℃时,制备的O-羧甲基壳聚糖在pH=7时不溶于水[18]。羧甲基改性的另一种方法是用含有醛基的羧酸与壳聚糖的伯氨基发生席夫碱反应,最后用NaBH4还原的方法得到N-羧基化壳聚糖[19]。
羧甲基化也可以在羟基上发生。王飞等[20]用壳聚糖为原料,采用两步合成法先制得N,N,N-三甲基壳聚糖,再用氯乙酸在C6位羟基羧基化,制得O-羧基-N-季铵盐壳聚糖。这种壳聚糖衍生物含有季铵根离子,因此分子内氢键被削弱,水溶性和抗菌性均显著改善。
羧甲基化反应可以同时在N、O上反应,Anitha等[21]制备了O-羧甲基壳聚糖和N,O-羧甲基壳聚糖,分别用噻吩蓝比色法和最低抑菌浓度法研究了2种羧甲基壳聚糖纳米颗粒的细胞毒性和对金黄色葡萄球菌的抗菌性。结果显示,2种壳聚糖衍生物的纳米颗粒对乳腺癌细胞几乎不呈现毒性,N,O-羧甲基壳聚糖、O-羧甲基壳聚糖和壳聚糖纳米颗粒的抗菌性依次减弱。
1.3 季铵化改性
季铵化的壳聚糖不仅溶解度增大,而且抗菌性也改善,成为改性壳聚糖比较热门的研究之一。采用环氧季铵盐改性壳聚糖除了具有壳聚糖的优点,还改善了季铵盐的正电性和杀菌抑菌性。刘新等[22]用2,3-环氧丙基三甲基氯化铵(EPTAC)接枝到壳聚糖C2位氨基,得到水溶性的壳聚糖季铵盐。季铵盐改性壳聚糖的溶解度和对金黄色葡萄球菌的抗菌性显著优于壳聚糖的。刘振儒等[23]研究了碘化N-三甲基壳聚糖季铵盐对革兰氏阳性菌和革兰氏阴性菌的抗菌性,结果表明壳聚糖季铵盐对革兰氏阳性菌的抗菌性更好。当EPTAC与壳聚糖的物质的量比为3∶1时,在反应温度为80 ℃、反应时间为3 h条件下制得的壳聚糖季铵盐取代度最大,引入的季铵盐基团破坏了壳聚糖的晶体结构,使其在pH为3.0~11.0时具有良好的水溶性,季铵盐壳聚糖膜的吸湿性、保水性和抑菌性均显著改善[24-25]。
C2位氨基和C6位羟基均具有较强的反应活性,在反应过程中是竞争关系。如果在羟基上改性,可以先通过季铵化反应将C2位氨基保护起来,再通过C6位羟基反应制得C6位羟基改性壳聚糖。车秋凌等[26]以不同分子量的壳聚糖为原料,先用甲醛和甲酸合成N,N-二甲基壳聚糖,再用碘甲烷将叔胺烷基化制得N,N,N-三甲基壳聚糖季铵盐,最后在其羟基上引入三聚氯氰,合成O-三聚氯氰-N,N,N-三甲基壳聚糖季铵盐,原理如图1所示。O-三聚氯氰-N,N,N-三甲基壳聚糖季铵盐在酸性染料中对羊毛织物的染色效果优于N,N,N-三甲基壳聚糖季铵盐的。
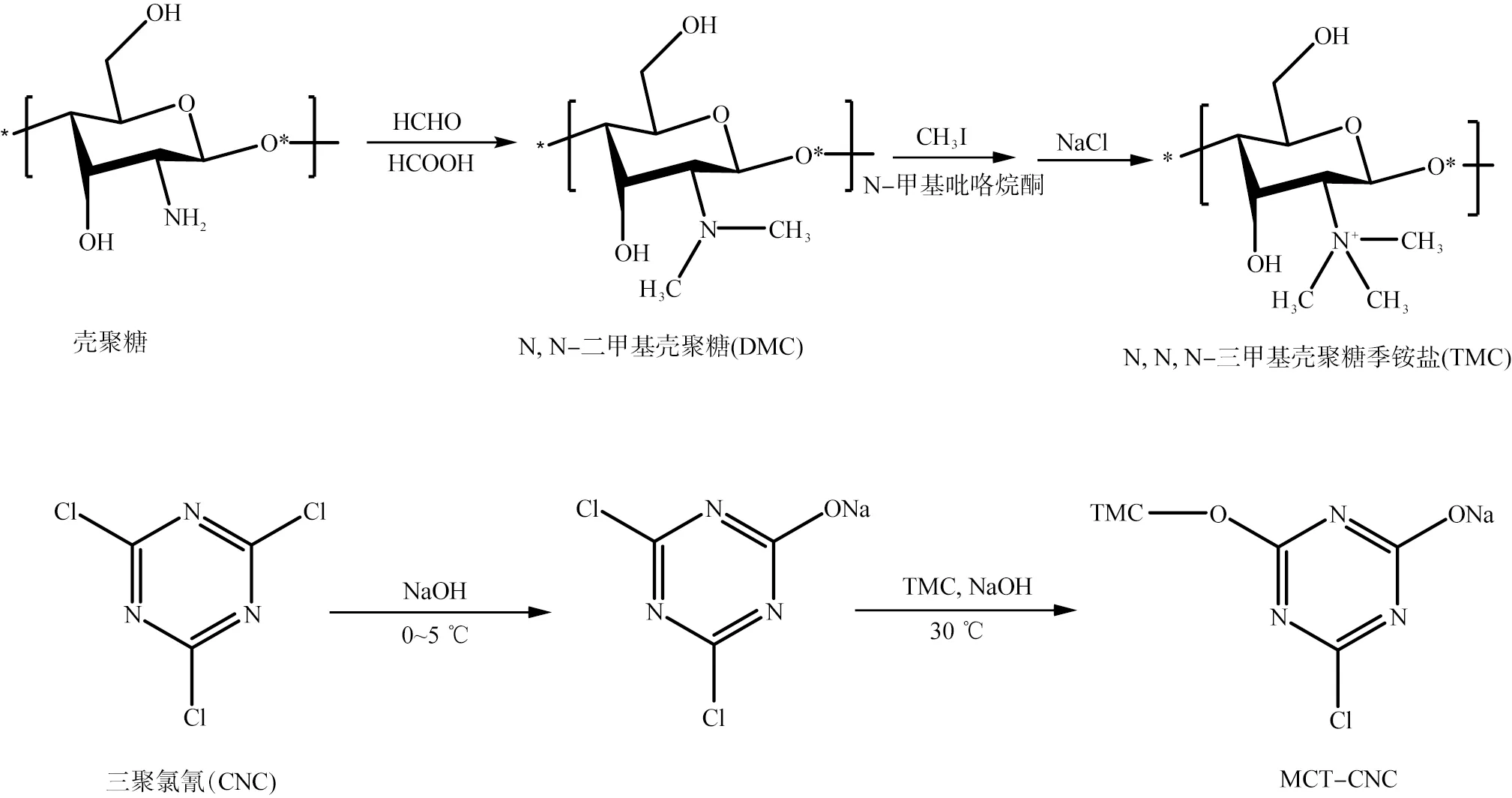
图1 O-三聚氯氰-N,N,N-三甲基壳聚糖季铵盐的合成原理[26]
张毅等[27]以甲壳素为原料,通过C6位羟基与醚化剂EPTAC反应形成醚键,再脱乙酰得到改性N-壳聚糖,制备原理如图2所示。上述2种方法都是利用官能团保护策略,在壳聚糖C6位羟基上引入基团。
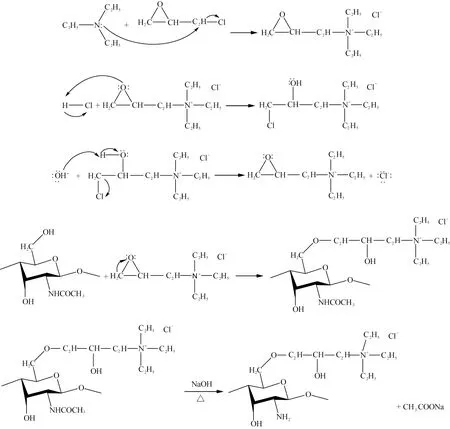
图2 O取代季铵盐壳聚糖的制备原理[27]
离子液体是壳聚糖的良溶剂,为在真溶液中通过均相反应改性壳聚糖提供了前提保障[28-29]。Yang等[30]研究表明,在1-烯丙基-3-甲基氯化咪唑离子液体(AmimCl)中,EPTAC只与C2位氨基发生反应,反应程度受反应时间和EPTAC与C2位氨基的物质的量之比影响。固定反应温度为80 ℃,EPTAC与C2位氨基的物质的量比为3∶1,反应时间由0.5 h增加到6 h,EPTAC在C2位氨基上的接枝率从11.8%快速增大到42.4%,继续延长反应时间到14 h,接枝率缓慢增大到45.5%;固定反应时间为8 h,反应温度为80 ℃,EPTAC与C2位氨基的物质的量比由1∶1增大到4∶1,EPTAC在C2位氨基上的接枝率由13.0%快速增大到45.6%,继续增加EPTAC与C2位氨基的物质的量比到6∶1,接枝率几乎保持不变。反应动力学研究结果显示,该反应为一级反应,反应动力学方程[31]为
式中:c-NH2为C2位氨基的浓度;t为时间。
AmimCl中EPTAC改性壳聚糖反应机制如图3所示[30]。在AmimCl中,EPTAC可以改性O-羧甲基壳聚糖,制备N-2-羟丙基-3-三甲基铵基-O-羧甲基壳聚糖,该壳聚糖衍生物的分子内同时具有带正电的铵基和带负电的羧甲基,属于两性壳聚糖衍生物[32]。这种两亲性壳聚糖通过分子内或分子间氢键和静电作用力形成具有一定力学性质的凝胶。在1-磺丁基-3-甲基咪唑三氟甲磺酸盐离子液体中,富马酸甲酯与壳聚糖分子中的C2位氨基反应,改性产物的水溶性和抗氧化性均明显改善[33]。
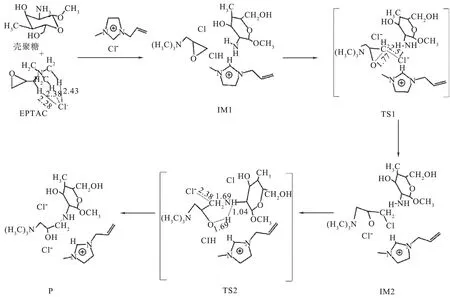
IM1—壳聚糖、AmimCl和EPTC这3种物质经过能量优化后的状态;TS1—理论计算得到的IM1的临界状态;IM2—环氧基团开环,其中的—CH2—与离子液体中的Cl-形成C—Cl键的过程(过渡态);TS2—开环后的EPTC与壳聚糖分子中的—NH2基团反应(过渡态);P—EPTC通过—NH2基团改性壳聚糖后的产物(最终产物)和溶剂AmimCl。图3 1-烯丙基-3-甲基氯化咪唑离子液体(AmimCl)中2,3-环氧丙基三甲氯化铵(EPTAC)改性壳聚糖的反应机制[30]
1.4 羟基化改性
通过醚化反应在C6位上引入羟基的方法改性壳聚糖也颇受关注。许晶等[34]通过在壳聚糖C6位反应引入了亲水基团羟乙基,制得C6位羟乙基醚取代度为65%的羟乙基壳聚糖。王旭颖等[35]以缩水甘油为醚化剂,在反应温度为60 ℃、反应时间为8 h的条件下制备了水溶性更优良的二羟丙基壳聚糖。羟基化改性是最成熟的方法之一,羟乙基改性壳聚糖衍生物已在市场上广泛存在。王莉等[36]通过1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐与N-羟基丁二酰基亚胺偶联反应和席夫碱-还原反应,并以高碘酸钠为氧化交联剂,制备了2种邻苯二酚接枝改性的壳聚糖基水凝胶组织胶黏剂。这种胶黏剂具有良好的抗菌性,成胶时间短,最大黏结强度可达40.42 kPa,高于商业化的纤维胶原蛋白的。王凤菊等[37]通过多步反应制备的8-羟基喹啉改性壳聚糖吸附剂在pH为4~7时对铀的吸附容量高达123 mg/g,在Na2CO3、NaHCO3的质量浓度分别为20、60 g/L的混合液解吸剂中铀脱附率达到90%。通过丝氨酸改性、戊二醛交联制得的丝氨酸壳聚糖树脂在室温下3 h内对铀的吸附容量为55.87 mg/g,脱附率大于90%,而且该吸附树脂具有良好的可重复使用性[38]。接枝率为16.85%的L-精氨酸改性壳聚糖对大肠杆菌和金黄色葡萄球菌的抑菌率分别为88.54%和91.38%,对测试液中质量浓度分别为25、50 g/L的Cu2+、Ni2+的去除率分别达到68.29%和75.03%[39]。
1.5 烷基化改性
壳聚糖分子中有多个羟基和氨基,具有典型的亲水性。当分子中接入烷基后,改性后的壳聚糖就变为两亲性壳聚糖。与普通壳聚糖相比,两亲性壳聚糖具有更好的抑菌性和更低的有效杀菌性浓度。烷基化改性反应可以发生在C2位氨基和C6位羟基这2个位点。
N-烷基化通常是卤代烃与壳聚糖C2位氨基反应的产物。王爱勤等[40]在异丙醇-氢氧化钠溶液中分别用乙基、正丁基、正辛基和十六烷基卤代烃改性壳聚糖,结果显示,乙基、正丁基和正辛基改性的壳聚糖具有良好的水溶性和较好的抗凝血性能,十六烷基改性壳聚糖具有良好的两亲性和抑菌性。Yodkhum等[41]采用单硬脂酸铝和脱氢热处理方法对壳聚糖进行疏水改性,在体积分数为2%的乳酸中,单硬脂酸铝解离出硬脂酸根离子,与脱氢热处理后的壳聚糖C2位氨基发生酰胺化反应,制得烷基化改性壳聚糖。
通过环氧基团的反应活性对壳聚糖进行改性也是制备烷基化壳聚糖的一种方法。Liu等[42]在AmimCl中以N,N-二甲基-N-十二烷基-N-(1,2-环氧丙基)氯化铵改性壳聚糖,制得具有两亲性的N,N-二甲基-N-十二烷基-N-(1,2-环氧丙基)改性壳聚糖,N,N-二甲基-N-十二烷基-N-(1,2-环氧丙基)的取代度高达15.4%。缩水甘油丁醚和乙基己基缩水甘油醚在AmimCl中与O-羧甲基壳聚糖反应分别制得N-2-羟丙基-3-丁基-O-羧甲基壳聚糖(HBCC)和N-2-羟丙基-3-乙基己基-O-羧甲基壳聚糖(H2ECC)[32],它们均具有良好的生物相容性、抑菌性和两亲性,临界聚集浓度受取代度和溶液pH影响,聚集体粒径为200~300 nm,可用于包载和传递油溶性药物。

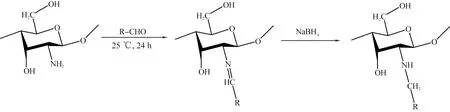
图4 N-烷基壳聚糖的合成路线[43-44]
由席夫碱法制备疏水壳聚糖的过程繁琐,使用的试剂较多,并且发生副反应,此外,醛本身有强烈的刺激性气味,在产物中难以除掉,对生物体和周围环境造成危害。长链有机酸或酸酐与壳聚糖反应也是制备两亲性壳聚糖的方法。温华强等[46]利用壳聚糖与月桂酸酐之间的反应,一步生成N-烷基取代壳聚糖,反应机制如图5所示。当反应温度为55 ℃时,月桂酸酐改性壳聚糖的取代度最大,为10.77%,壳聚糖溶液的特性黏度最低。通常,改性壳聚糖中月桂酸的取代度越大,改性壳聚糖的溶解性越差。改性壳聚糖与水之间的接触角为104.46°,远大于壳聚糖与水的(67.26°),说明月桂基烷链的接入显著增强壳聚糖的疏水性。由于月桂酸酐改性壳聚糖有显著的止血效果,因此有望开发为新型止血材料。
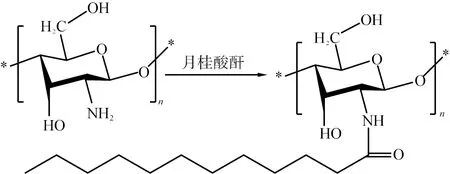
图5 有机酸或酸酐通过C2位氨基取代制备两亲性壳聚糖的反应机制[46]
Jothimani等[47]制备了N-(噻吩-2-乙酰基)壳聚糖,合成路线见图6,光谱分析结果证实了改性壳聚糖的结构,通过元素分析法求得N-取代度最大为96%。经过超细粉碎和超声波作用,N-(噻吩-2-乙酰基)壳聚糖转变为平均粒径为83.1~95.54 nm的颗粒,取代度越大,颗粒粒径越大。N-(噻吩-2-乙酰基)壳聚糖纳米颗粒的热稳定性受壳聚糖结晶度和颗粒尺寸的影响,结晶度越高或者粒径越大,纳米颗粒越稳定。
2 改性壳聚糖的应用
2.1 亲水改性壳聚糖的应用
由于亲水改性壳聚糖具有良好的水溶性,因此在食品、医药、皮革、化工工艺等领域的应用较广泛。壳聚糖及其衍生物独特的生物性能使其在食品添加剂、防腐剂、保鲜剂、保鲜膜、饮料澄清剂中得到广泛应用[48]。相对于传统的防腐剂与保鲜剂,亲水改性壳聚糖不仅用量少,保鲜效果也更加明显,且安全、无污染。范国枝等[49]在果汁中加入质量分数为2%的水溶性壳聚糖作为澄清剂,与未加澄清剂的果汁对比,果汁透光率达到85%以上,色泽也更好,并且壳聚糖无毒无害,不会影响果汁中的营养成分。壳聚糖自身具有良好的抑制细菌的效果,经过亲水改性的壳聚糖可以更好地抑制细菌微生物的入侵和生长,同时其良好的保湿性和抗氧化性还可以延长食品的保质期。利用壳聚糖良好的成膜性可制成具有抗菌性的食品包装膜,能有效阻止微生物的入侵,在食物的储藏过程中起到保鲜、降低果蔬的腐烂率的作用。
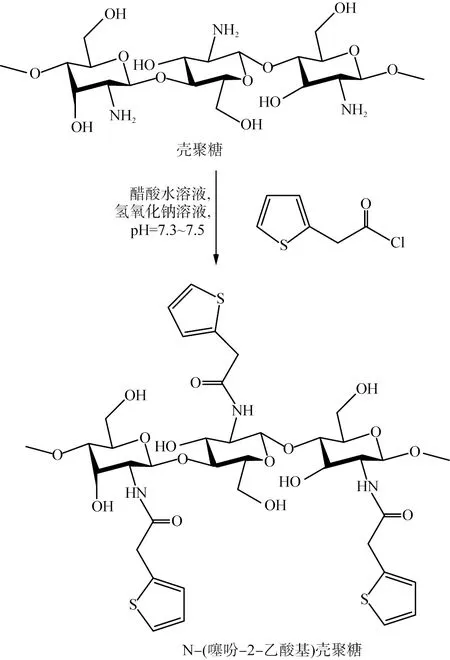
图6 N-(噻吩-2-乙酰基)壳聚糖的合成路线
另外,亲水改性后的壳聚糖具有良好的反应功能性和生理活性,优良的抗菌性、生物相容性及生物可降解性,同时能够促进软组织修复、伤口愈合,具有引导骨及软骨再生的作用[50]。N,N,N-三甲基壳聚糖季铵盐在生物医学与制药中应用也较为广泛。Boonyo等[51]研究了壳聚糖和N,N,N-三甲基壳聚糖季铵盐作为一种免疫助剂在鼻腔黏膜给药系统中诱导小鼠卵清蛋白发生免疫反应,结果表明,N,N,N-三甲基壳聚糖季铵盐在肺部输送抗体的给药系统中的应用效果很好。Fiddes 等[52]用壳聚糖季铵盐包覆制备了具有一定形貌的微通道的微凝胶胶囊,对其流体动力学问题展开了相关探究。利用2-羟丙基-3-三甲基铵基壳聚糖包覆分别带有正、负电荷的海藻酸盐凝胶形成胶囊,然后使其流过微通道小孔,观察改性壳聚糖包覆甲基氯的效果、微胶囊与通道管壁表面间的相互作用以及通过小孔的流速,结果表明,通过调控2-羟丙基-3-三甲基铵基壳聚糖所带正电荷与微通道管壁所带负电荷之间的静电作用,再通过控制流速可以得到不同直径的微胶囊,且这种微胶囊尺寸具有较好地可控性。刘庆等[53]研究发现,巯基化壳聚糖季铵盐为基因载体对脱氧核糖核酸(DNA)具有良好的包载能力,同时对还原响应性的基因具有释放能力。
涂饰在皮革纤维表面的季铵盐改性壳聚糖可有效地吸附周围带负电荷的细菌,抑制其增殖,是一种性能良好的皮革抗菌剂[54]。许晓红等[55]的研究结果显示,羧甲基壳聚糖可以作为制革过程的染色助剂,并且有助于产品颜色的加深,提高染色上染率,改善匀染性以及干湿擦性能。
亲水改性后的壳聚糖有良好的水溶性和耐热性,对重金属离子有较强的吸附能力[56],能快速吸附工业废水中的砷、铬、汞、镉、铅、铜等离子。樊丽华等[57]研究发现,羧甲基壳聚糖的羧化度为1.43、投加量为8 mg /L时对海水的絮凝效果最好,化学需氧量(COD)的去除率为55%,浊度去除率达到94%~95%。印染废水的组成复杂,颜色深,异味大,有机物浓度高,难以被生物降解,改性壳聚糖多亲水基团的结构特点使其在印染废水处理中表现出极大的优势[58]。
壳聚糖和纤维素具有相近的分子结构和优良性能,可被用作造纸添加剂和表面施胶剂等。亲水改性壳聚糖的成膜性好,可通过分子间氢键与纸张纤维紧密作用,因此可以将亲水改性壳聚糖用作纸张的增黏剂和湿部施胶助剂,提高阳离子石油树脂胶的留着率。中性施胶时,羟丙基壳聚糖中的羟基、氨基等亲水基团与碳酸钙填料相互作用,提高碳酸钙的填加量。此外,羟丙基壳聚糖与施胶剂间的强相互作用还提高了施胶剂在高剪切条件下的留着率,形成更稳定的絮聚体,有助于纸机的操作[59]。
水溶性壳聚糖还可以应用在化妆品中,如:N-羧甲基壳聚糖具有良好的保湿性,可用作过敏性护肤品的添加剂;羟丙基三甲基氯化铵壳聚糖具有良好的杀菌抑菌性和吸湿保湿性,因此可作为添加剂用于膏霜产品。
2.2 疏水改性壳聚糖的应用
疏水改性壳聚糖在医疗领域广泛应用,Logun等[60]研究发现,疏水改性壳聚糖(HMCS)是生物高聚物壳聚糖的两亲性衍生物,可在注射膨胀泡沫应用6周后成功诱导分解血栓,在病变腔中有最小的炎症和黏连状态,与未改性壳聚糖相比,HMCS具有更快的生物降解速度。黄玉芬等[61]研究发现,取代度为7%、16%、26%、40%的烷基化壳聚糖均具有较好的体外止血效果,其中取代度为16%的烷基化壳聚糖的体外止血效果最好,取代度为40%的烷基化壳聚糖体内止血效果最好。Du等[62]制备的疏水改性壳聚糖(HMCS)-氧化右旋糖酐(OD)水凝胶对铜绿假单胞菌和金黄色葡萄球菌的杀灭率分别达到96.4%和95.0%。基于静电、疏水相互作用和水凝胶的黏附性能的协同作用,HMCS(质量分数1.0%)-OD水凝胶具有较好的体内止血效果,能有效地与组织结合,有利于促进创面修复。脱氧胆酸改性壳聚糖(DCS-CS)可以自聚集成粒径为280~310 nm、表面电压为26 mV的纳米粒子,与透明质酸(HA)协同作用可实现对阿霉素的包封率达到56%。载药体系在温度为37 ℃时暴露于pH为7.4的磷酸盐缓冲溶液中,阿霉素可以保持一定的缓释性而不产生猝灭效应[63]。辛烯基琥珀酸酐酰化改性壳聚糖(OSA-CS)在水溶液中自聚集成带负电荷的聚集体,具有良好的生物相容性,对姜黄素的包载率大且有pH响应性,有利于特殊细胞对药物的提取效率,能够更好地发挥药物的抗炎、抗氧化作用[64]。以羧甲基壳聚糖为原料,通过2,3-环氧丙基正丁基和异辛基醚改性得到的两亲性壳聚糖也具有自聚集行为和pH响应性,随着溶液pH由9.18减小到1.0,聚集体的电负性由-40 mV增加到20 mV,实现对姜黄素的可控释放[32]。
由于壳聚糖具有生物相容性、抗菌性好,可降解,无毒及成膜能力优异等特性,因此是重要的新型食品包装材料。Fernández等[65]以偶氮聚合物为原料采用溶剂浇铸法制备了偶氮聚合物(PAZO)改性壳聚糖,该疏水改性壳聚糖可以形成厚度约为25 μm的薄膜,具有吸水性弱、拉伸强度高和弹性模量大的特点,在食品包装中有潜在的应用。N-2-羟丙基-3-三甲基-O-羧甲基壳聚糖与羧甲基纤维素体系的膜继承了壳聚糖和纤维素的生物相容性,膜的表面光滑平整,透光度大于90%,最大拉伸强度大于5 MPa,断裂伸长率高达120%,对大肠杆菌和金黄色葡萄球菌有明显的抑制作用,可有效延长新鲜猪肉的保鲜期[66]。
3 结论与展望
随着国家碳达峰、碳中和战略的推进,人们对可再生生物大分子的依赖性将日益增强。含量高、性质优的壳聚糖在未来经济社会的发展中将占有不可或缺的席位,特别是基于壳聚糖的高附加值、多功能或者特殊功能产品将是重点开发的对象。我国的壳聚糖及衍生物制品的研发和应用起步晚,需要设计新的分子结构,开发新的反应介质,引入新的反应物料,开辟新的反应路线,探索新的反应机制,生产新的壳聚糖基新产品并对其不断升级更新,充分展现壳聚糖的优点。开拓壳聚糖基材料在医疗器械、医药包载与靶向传递、绿色包装材料产品的应用范围,积极贯彻执行碳中和、碳达峰的发展战略将是未来壳聚糖新产品的发展方向。

