电子止吐仪联合托烷司琼和地塞米松防治恶性肿瘤患者顺铂化疗所致恶心呕吐的疗效观察
俸桃 王小兰 唐明红 罗桂梅 李万松 曾晓露 刘敏
恶性肿瘤是全球发病率最高的疾病之一,且发现时多属晚期,虽然现今靶向及免疫治疗蓬勃发展,但不可否认化疗仍然是恶性肿瘤主要的治疗手段之一[1]。针对化疗,消化道反应即恶心呕吐是常见的毒副反应,有数据表明化疗后恶心呕吐发生率高达80%~90%,尤其是以顺铂为主的化疗方案,恶心呕吐发生率高达100%[2]。若出现急性剧烈的恶心呕吐,会严重影响患者的生活质量,降低患者抗肿瘤治疗的依从性,甚至危及生命[3]。故止吐是肿瘤治疗过程中不可或缺的环节。结合美国国立综合癌症网络(NCCN)及中国临床肿瘤学会(CSCO)指南,目前常用的止吐药物有5-羟色胺-3(5-HT3)受体拮抗剂、神经激肽-1(NK-1)受体拮抗剂、糖皮质激素、非典型抗精神病药物、苯二氮类药物、吩噻嗪类药物等[4,5]。在我国,恶心呕吐的防治以5-HT3受体拮抗剂联合地塞米松作为主流方案,但30%的恶心呕吐仍未获得满意控制[6]。但若使用过多的药物联合止吐也可能会带来其他不良反应。近年来,有一项新型的电子止吐仪用于恶心呕吐的防治效果尚可,故本文选取120 例采用顺铂化疗治疗的恶性肿瘤患者作为研究对象,观察电子止吐仪联合托烷司琼、地塞米松防治其恶心呕吐的效果。
1 资料与方法
1.1 一般资料 选取2021 年5 月~2022 年4 月于本科住院的120 例恶性肿瘤患者,随机分为对照组和试验组,各60 例。对照组患者年龄30~78 岁,中位年龄62 岁;入院时体重55.50 kg。试验组患者年龄24~84 岁,中位年龄61 岁;入院时体重56.88 kg。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。见表1。
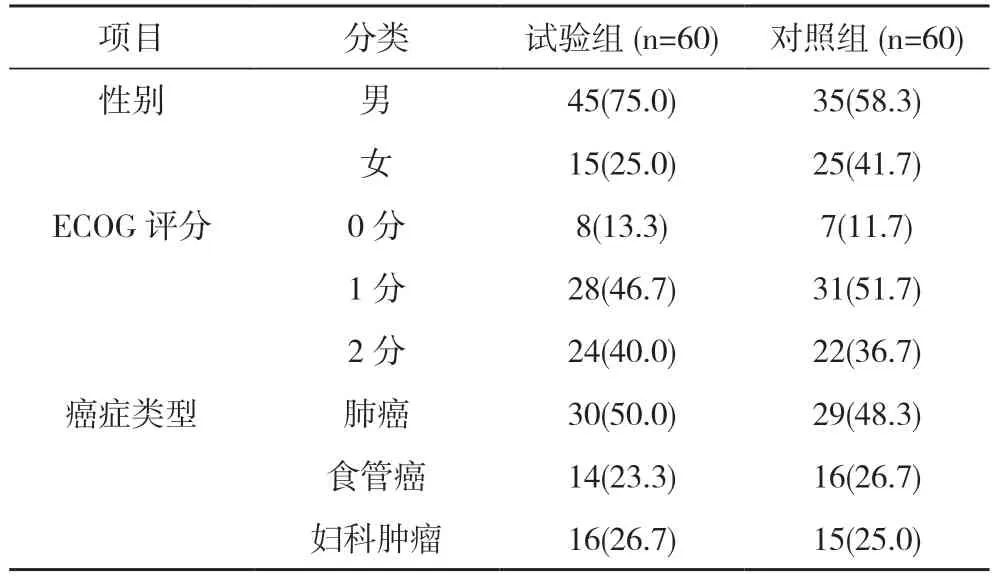
表1 两组患者一般资料比较[n(%)]
1.2 纳入及排除标准 纳入标准:①经病理学确诊为恶性肿瘤;②化疗方案为含顺铂的双药方案;③有化疗适应证,年龄≥18 岁,预计生存期>3 个月;④患者知情同意,愿意配合研究;⑤化疗前24 h 无恶心呕吐以及未使用其他止吐药物。排除标准:①佩戴心脏起搏器者或人工耳蜗等植入性或外用医疗器械者、金属接触过敏体质者、佩戴部位皮肤破损者;②使用阿片类药物,存在不完全性或完全性肠梗阻、前庭功能障碍、肿瘤脑转移、颅内高压、电解质紊乱、尿毒症、肝功能异常等导致的非化疗相关性恶心呕吐者[7]。
1.3 方法 所有患者采用顺铂化疗方案,顺铂使用第1~3 天的分量方案,另一种化疗药物为紫杉醇或培美曲塞或依托泊苷,均为3 周方案。试验组使用电子止吐仪(昆明法罗适科技有限公司)联合托烷司琼和地塞米松防治恶心呕吐,化疗开始时佩戴电子止吐仪,仪器背面的两个金属板应紧贴腕部,在桡侧腕屈肌和掌长肌之间距离远侧腕横纹大约3 cm 处的腕部正中位置(内关穴),根据个人舒适度行调节档位(共5 档),确保电池电量充足,持续佩戴3 d;化疗前30 min 静脉滴注托烷司琼(齐鲁制药有限公司,国药准字H20050535,规 格:5 mg/ 支)5 mg+生理盐水100 ml,1 次/d,第1~3 天;地塞米松磷酸钠注射液6 mg+生理盐水100 ml,1 次/d,第1~3 天。对照组使用托烷司琼及地塞米松防治恶心呕吐,化疗前30 min 静脉滴注托烷司琼5 mg+生理盐水100 ml,1 次/d,第1~3 天;地塞米松磷酸钠注射液6 mg+生理盐水100 ml,1 次/d,第1~3 天。于每晚20:00 左右询问并记录两组患者恶心呕吐及不良反应情况。
1.4 观察指标及判定标准
1.4.1 化疗第1~5 天恶心、呕吐控制情况 根据美国国家癌症研究所所制定的常用术语标准即CACTE4.0版记录及分级[8]。恶心分级标准:0 级:无恶心情况;1 级:食欲降低,不伴进食习惯改变;2 级:经口摄食减少,不伴明显的体重下降、脱水或营养不良;3 级:经口摄入能量和水分不足,或者需要管饲、全肠外营养或住院。呕吐分级标准:0 级:无呕吐情况;1 级:24 h 内发作1~2 次;2 级:24 h 内发作3~5 次;3 级:24 h 内发作≥6 次,需要管饲、全肠外营养或住院治疗;4 级:危及生命、需要紧急治疗。一次呕吐事件定义为持续时间>1 min,两次呕吐之间至少缓解5 min[9]。恶心控制RR=(0 级+1 级)/总例数×100%。呕吐控制RR=(0 级+1 级)/总例数×100%。
1.4.2 不良反应发生情况 不良反应包括头晕、头痛、便秘、疲劳等。
1.5 统计学方法 采用SPSS22.0 统计学软件进行数据统计分析。计量资料以均数±标准差 ()表示,采用t检验;计数资料以率(%)表示,采用χ2检验;等级资料采用秩合检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 两组患者化疗第1~5 天恶心控制情况比较 试验组化疗第1、2、3、4、5 天恶心控制RR 分别为85.00%、96.67%、96.67%、98.33%、98.33%,对照组分别为61.67%、83.33%、85.00%、96.67%、96.67%;试验组化疗第1、2、3 天恶心控制RR 高于对照组,差异有统计学意义(P<0.05);两组第4、5 天恶心控制RR 比较,差异无统计学意义(P>0.05)。见表2。

表2 两组患者化疗第1~5 天恶心控制情况比较(n,%)
2.2 两组患者化疗第1~5 天呕吐控制情况比较 试验组化疗第1、2、3、4、5 天呕吐控制RR 分别为98.33%、95.00%、98.33%、98.33%、98.33%,对照组分别为88.33%、83.33%、88.33%、95.00%、96.67%。试验组化疗第1、2、3 天呕吐控制RR 高于对照组,差异有统计学意义(P<0.05);两组第4、5 天呕吐控制RR 比较,差异无统计学意义(P>0.05)。见表3。
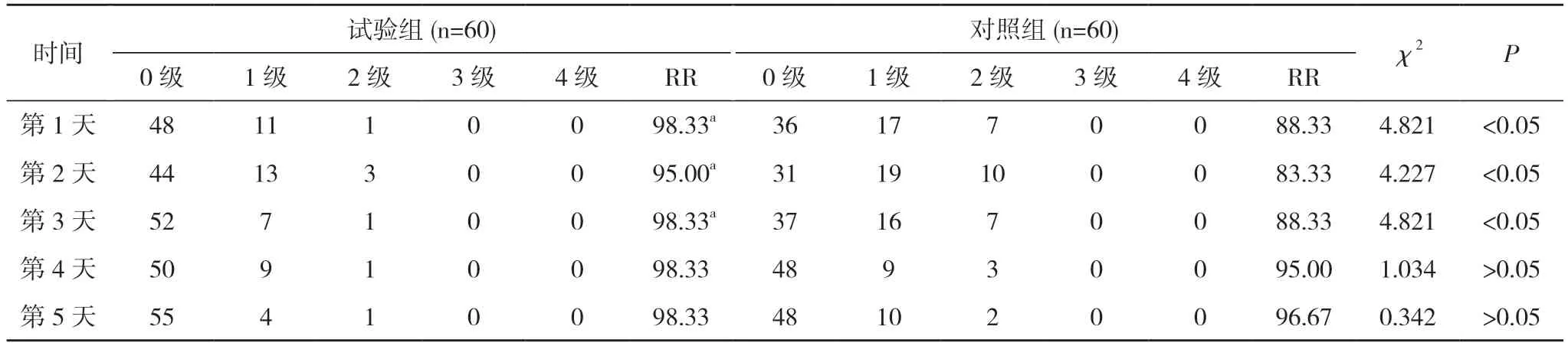
表3 两组患者化疗第1~5 天呕吐控制情况比较(n,%)
2.3 两组患者不良反应发生情况比较 两组不良反应发生率比较,差异无统计学意义(P>0.05)。见表4。

表4 两组患者不良反应发生情况比较(n,%)
3 讨论
恶性肿瘤患者由于化疗导致的恶心呕吐根据其发生时间和治疗效果可以分为急性、延迟性、预期性、暴发性和难治性。其中急性恶心呕吐是指给予化疗药物24 h 内发生的恶心呕吐,通常在治疗后5~6 h 达到高峰。延迟性恶心呕吐指在给予化疗药物24 h 后出现的恶心呕吐,其中40%~50%发生于化疗后24~48 h,有时可持续5~7 d[10]。化疗引起恶心呕吐的发生机制主要有两条途径:①化疗药物刺激胃和近段小肠黏膜、肠嗜铬细胞释放神经递质,神经递质刺激肠壁上的迷走神经和内脏神经传入纤维将信号传入到脑干直接刺激呕吐中枢;②化疗药物及其代谢产物直接刺激化学感受器触发区,然后通过神经递质受体传递至呕吐中枢引发呕吐。与化疗所致恶心呕吐关系最密切的神经递质为5-羟色胺(5-HT)、P 物质和大麻素,其他还包括多巴胺、乙酰胆碱和组胺等。5-HT 是在急性恶心呕吐中发挥重要作用的递质,在迷走神经传入纤维、化学感受器触发区(chemoreceptor trigger zone,CTZ)及孤束核中均有多种5-HT 受体。而延迟性恶心呕吐则与P 物质联系紧密[11,12]。托烷司琼是一种外周神经原及中枢神经系统5-HT3受体的高效、高选择性竞争拮抗剂[13],而5-HT 受体拮抗剂联合地塞米松是预防多日化疗所致恶心呕吐的标准治疗[6],但止吐效果有限。传统医学认为,内关穴位于前臂掌侧,腕横纹上2 寸,掌长肌肌腱与桡侧腕屈肌肌腱之间,内关穴最早见于《灵枢·经脉》篇: “手心主之别,名曰内关,去腕2 寸出于两筋之间”内,指内面;关,指关口。内关属手厥阴心包经,可主治胃痛及恶心呕吐等[14,15]。低频脉冲电子止吐仪是一种新型体外经皮神经电刺激性治疗仪,其能够周期性发出低频双向脉冲波,通过对手腕部的正中神经刺激上传到呕吐中枢,达到调节神经性呕吐的信号和往返于胃部迷走神经信号,减轻呕吐恶心及厌食症状[16,17]。同时,刺激内关穴能使上、中、下三焦气体通畅,胃气下降,达到治疗恶心呕吐的效果[18]。国内江冠铭等[19]及王小红等[20]的研究也表明电子止吐仪联合止吐药物能有效地控制恶心呕吐的发生率,且不增加不良反应。
本次研究结果显示,试验组化疗第1、2、3 天恶心及呕吐控制RR 高于对照组,差异有统计学意义(P<0.05);两组化疗第4、5 天恶心及呕吐控制RR 比较,差异无统计学意义(P>0.05)。由此说明电子止吐仪联合托烷司琼和地塞米松对于顺铂化疗所致的急性恶心呕吐有明显控制效果,对于迟发性恶心呕吐也有一定的控制效果。研究结果还显示,两组不良反应发生率比较,差异无统计学意义(P>0.05)。由此表明电子止吐仪使用较为安全,未增加不良反应。
综上所述,电子止吐仪联合托烷司琼、地塞米松防治顺铂化疗所致恶心呕吐的效果优于托烷司琼联合地塞米松,且不良反应耐受,值得临床推荐。但因未能开展较大样本的随机双盲试验,故在今后的临床工作中还需进一步研究。

