氯吡格雷精准用药对缺血性脑卒中脑动脉重建术后疗效的影响
农媛 杨智文 杨吉 秦柱贵 黄日玲
CYP2C19 基因多态性是影响氯吡格雷疗效的重要因素,尤其是CYP2C19*2 和CYP2C19*3 功能缺失型(loss of function,LoF)等位基因,其可造成氯吡格雷抵抗、血小板抑制率不足、抗栓治疗失败、血栓事件再发风险高[1,2]。而中国近60%的人群携带CYP2C19 LoF 基因[3],因此,有必要对拟用氯吡格雷治疗的患者进行CYP2C19 基因多态性检测,以优化患者的抗血小板治疗。目前心血管疾病领域的多个研究显示,基于CYP2C19 基因检测结果指导的个体化抗血小板治疗,有助于减少急性冠状动脉综合征患者冠状动脉支架置入术后主要血管不良事件的发生,同时不会增加中、重度出血风险[4-6]。但对于缺血性脑卒中(ischemic stroke,IS)脑动脉重建术后患者,氯吡格雷精准用药治疗是否有相似的效果,尚缺乏相关研究支持。本文通过比较氯吡格雷精准用药与常规用药治疗对缺血性脑卒中脑动脉重建术后患者的疗效及安全性,以期为临床提供相关数据支撑。现报告如下。
1 资料与方法
1.1 一般资料 回顾性分析2020 年1 月~2022 年1 月贵港市人民医院收治的255 例行脑动脉重建术的缺血性脑卒中患者的临床资料,研究期间失访12 例,最终纳入243 例。将患者根据是否进行CYP2C19 基因多态性检测指导氯吡格雷抗血小板治疗分为研究组(87 例,精准用药)和对照组(156 例,常规用药)。采用倾向性评分匹配(propensity score matching,PSM)方法控制两组的混杂因素,通过PSM 成功匹配77 对,研究组和对照组各77 例。见图1。纳入标准:①年龄18~80 岁;②确诊为缺血性脑卒中,且经脑血管造影检查证实存在与患者症状相关的大血管(颈内动脉、大脑中动脉、椎动脉及基底动脉)狭窄>70%;③术前美国国立卫生研究院脑卒中量表(National Institutes of Health Stroke Scale,NIHSS)评分<25 分;④患者及家属知情同意行狭窄动脉支架置入术。排除标准:①溶栓患者;②合并恶性肿瘤疾病患者;③合并必须行抗凝治疗的疾病如深静脉血栓、肺栓塞的患者;④严重心、肺、肝、肾功能不全的患者;⑤合并出血性疾病或出血倾向的患者;⑥既往有过脑卒中病史且改良Rankin 量表(modified Rankin scale,mRS)≥2 分患者;⑦孕期或哺乳期妇女。本研究通过贵港市人民医院医学伦理委员会批准(批件号:GYLLPJ-20211111-32)。

图1 研究对象纳入及排除流程
1.2 方法
1.2.1 CYP2C19 基因检测 研究组患者于术前使用真空采血管采集静脉血2 ml 行CYP2C19 基因型检测,样本处理与检测严格按照测序反应通用试剂盒(北京为朔医学数据科技有限公司)说明书进行,采用原位杂交法,使用Fascan 48E 多通道荧光定量分析仪(西安天隆科技有限公司)进行CYP2C19 位点*17、*2 及*3 的检测。根据检测结果分为正常代谢型(野生型纯合子CYP2C19*1/*1),中间代谢型(CYP2C19*1/*2、CYP2C19*1/*3、CYP2C19*2/*17),慢代谢型(CYP2C19*2/*2,CYP2C19*3/*3 和CYP2C19*2/*3) 和快代谢型(CYP2C19 *17/*17 和CYP2C19*1/*17)[7]。
1.2.2 治疗方法 研究组中间代谢型患者术后给予氯吡格雷150 mg/次、q.d.+阿司匹林100 mg/次、q.d.治疗;慢代谢型患者术后给予替格瑞洛90 mg/次、b.i.d.+阿司匹林100 mg/次、q.d.治疗;快代谢型患者术后给予氯吡格雷25 mg/次、q.d.+阿司匹林100 mg/次、q.d.治疗;正常代谢型患者及对照组患者则按指南给予氯吡格雷75 mg/次、q.d.+阿司匹林100 mg/次、q.d.治疗。所有患者按以上方案用药3 个月,3 个月后均改为阿司匹林100 mg/次、q.d.长期口服。同时根据患者病情,个体化给予脱水剂、降糖药、降压药及抗生素治疗等。
术后随访6 个月,随访频率为1 次/个月,采用门诊+电话随访模式,了解随访期间患者有无缺血性脑卒中复发、出血事件、全因死亡及mRS 评分。
1.3 观察指标及判定标准 分析研究组PSM 后CYP2C19 基因型分布;比较两组PSM 前后的临床资料,两组PSM 后的疗效及安全性。①收集两组患者的临床资料,包括年龄、性别、民族、既往病史、个人史、基线NIHSS 评分、病灶部位(前循环或后循环)、是否取栓、体质量指数(body mass index,BMI)、入院低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)水平、有无发热等。②疗效评价指标为缺血性脑卒中复发情况、术后随访6 个月时的预后结局。以6 个月时mRS 评分≤2 分为预后结局良好,mRS 评分≥3 分为预后结局不良[8]。③安全性评价指标为随访期间的全因死亡及与抗血小板治疗相关的出血事件发生情况。
1.4 统计学方法 采用SPSS26.0 统计学软件对研究数据进行统计分析。运用倾向性评分匹配PSM 最邻近法对两组间资料进行1∶1 匹配,卡钳值设定为0.2[9]。PSM 前后,符合正态分布的计量资料以均数±标准差()表示,采用两独立样本t检验;非正态分布的计量资料采用中位数和四分位数间距[M(P25,P75)]表示,组间比较采用Mann-WhitneyU检验;计数资料以率(%)表示,采用χ2检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 研究组PSM 后CYP2C19 基因型分布 PSM 后,研究组中CYP2C19 正常代谢型和中间代谢型占比一致,均为42.9%(33/77),慢代谢型占比为14.3%(11/77),快代谢型占比为0。CYP2C19*2 和CYP2C19*3 携带率为57.1%(44/77),CYP2C19*17 携带率为1.3%(1/77)。见图2。
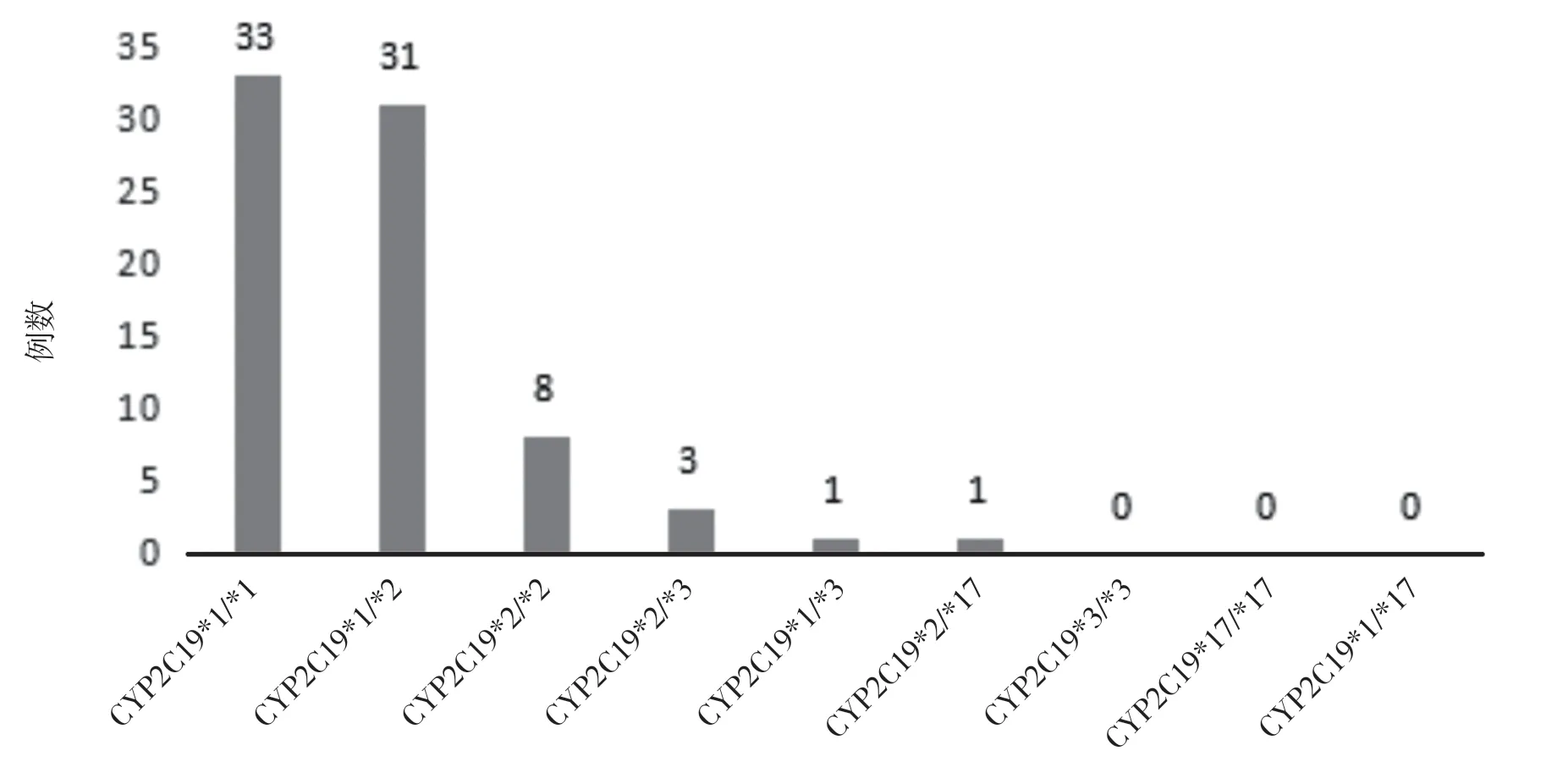
图2 研究组CYP2C19 基因型分布
2.2 两组PSM 前后一般临床资料比较 PSM 前,研究组女性占比为18.4%,高于对照组的9.6%,差异具有统计学意义(P<0.05);两组年龄、民族、糖尿病史、高血压病史、脑卒中病史、吸烟史、饮酒史、基线NIHSS 评分、责任血管、取栓情况、入院LDL-C、BMI、发热情况比较差异无统计学意义(P>0.05)。见表1。PSM 后,两组年龄、性别、民族、糖尿病史、高血压病史、脑卒中病史、吸烟史、饮酒史、基线NIHSS 评分、责任血管、取栓情况、入院LDL-C、BMI、发热情况比较差异均无统计学意义(P>0.05)。见表2。

表1 两组PSM 前一般临床资料比较[n(%),M(P25,P75)]
表2 两组PSM 后一般临床资料比较[n(%),M(P25,P75),]

表2 两组PSM 后一般临床资料比较[n(%),M(P25,P75),]
注:两组比较,P>0.05
2.3 两组PSM 后疗效及安全性比较 术后随访6 个月,研究组患者复发率为3.9%,低于对照组的15.6%,差异具有统计学意义(P<0.05);研究组患者预后结局良好率、出血事件发生率、全因死亡率均略低于对照组,但差异无统计学意义(P>0.05)。见表3。

表3 两组PSM 后疗效及安全性比较[n(%)]
3 讨论
氯吡格雷是行血管内治疗的缺血性脑卒中患者术后常用的双联抗血小板药之一,但在临床实践中,采用标准剂量氯吡格雷治疗的患者抗栓效果差异较大,相当一部分患者可出现氯吡格雷低反应或无反应,这种现象被称为氯吡格雷抵抗,其抑制血小板聚集作用下降,血栓形成风险增加;而少数患者则表现为氯吡格雷超反应,抑制血小板聚集作用增强,出血风险增加[10,11]。研究显示[12],亚洲人群出现氯吡格雷抵抗率最高,约为70%,主要影响因素为CYP2C19 基因多态性[13,14]。CYP2C19 为氯吡格雷在体内代谢转化为具有活性产物的重要的肝酶,其活性状态影响氯吡格雷活性产物的高低,而CYP2C19 基因有多个等位基因,不同等位基因编码的CYP2C19 活性各异。其中,CYP2C19*2 和CYP2C19*3 为LoF 等位基因,其可导致CYP2C19 酶活性下降,致氯吡格雷在体内的活性代谢产物减少,抗栓治疗效果差,血栓形成风险增加。荟萃分析显示,在服用氯吡格雷的患者中,携带1~2 个CYP2C19 LoF 等位基因的患者发生不良临床事件的危险性可能会增加55%~76%[15];CYP2C19*17 是功能增强等位基因,其可导致CYP2C19 酶活性增强,氯吡格雷活性代谢产物增加,抑制血小板聚集作用增强,出血风险增加[16,17]。
在我国,近60%的人群为CYP2C19*2 和(或)*3携带者,1%~3%为CYP2C19*17 基因携带者[3,18,19]。2010 年3 月美国FDA 修改的氯吡格雷说明书中黑框警示:CYP2C19 基因型检测结果应作为医生调整治疗策略的参考,对于CYP2C19 慢代谢型患者,建议考虑调整治疗方案或治疗策略[7]。而《症状性颅内动脉粥样硬化性狭窄血管内治疗中国专家共识2018》推荐对于行血管内治疗的缺血性脑卒中患者术后应用阿司匹林联合氯吡格雷抗血小板治疗至少90 d,但在应用氯吡格雷抗血小板治疗时需关注药物抵抗性,可参考相关基因检测的结果调整抗血小板药物治疗方案[20]。但具体的药物调整方案尚存争议,尤其是针对中间代谢型患者。有研究认为,对于中间代谢型患者,CYP2C19酶缺陷可以通过氯吡格雷剂量递增部分克服,并能产生足够的抗血小板作用,使风险正常化,而不会增加成本和出血风险[21]。但Wu 等[22]研究显示,携带1 个CYP2C19 LoF 基因的中重度脑血管狭窄的缺血性脑卒中患者,在服用阿司匹林基础上联合大剂量氯吡格雷(150 mg/d)较常规剂量氯吡格雷虽然3 个月内发生的血管事件更少,但两者间的差异却不显著。荟萃分析显示[23],替格瑞洛与大剂量氯吡格雷(150 mg/d)相比,能显著减少CYP2C19 中间代谢型和慢代谢型行冠状动脉介入术(percutaneous coronary interventions,PCI)后患者的主要不良心脑血管事件,虽不增加主要出血风险,但却增加了呼吸困难发生率。
本研究以行脑动脉重建术的缺血性脑卒中患者为研究对象,分析CYP2C19 基因指导的氯吡格雷个体化抗血小板治疗的疗效及安全性,其中对基因检测结果显示为中间代谢型患者采用双倍常规剂量氯吡格雷治疗,而慢代谢型患者采用替格瑞洛替代治疗。结果显示,本研究中,CYP2C19*2 和CYP2C19*3 携带率为57.1%(44/77),CYP2C19*17 携带率为1.3%(1/77),与其他研究相似[3],提示氯吡格雷抵抗在临床中普遍存在。术后随访6 个月,研究组患者复发率为3.9%,低于对照组的15.6%,差异具有统计学意义(P<0.05);研究组患者出血事件发生率、全因死亡率均略低于对照组,但差异无统计学意义(P>0.05)。提示:①依据基因型指导的抗血小板治疗,可有效识别患者对氯吡格雷的代谢能力,优化抗栓治疗方案,减少缺血事件发生,同时不增加出血及死亡风险,是安全有效的;②对于中间代谢型患者,采用增加氯吡格雷剂量治疗方案,而慢代谢型患者采用替格瑞洛替代治疗是可行的。同时,本研究结果还显示,研究组患者预后结局良好率略低于对照组,但差异无统计学意义(P>0.05)。原因可能为:①研究组患者的基线NIHSS 评分略高于对照组,神经功能缺损相对较重,故而有可能影响功能预后;②研究组取栓患者占比略高于对照组,而这有可能增加围手术期并发症的风险,影响患者术后功能的恢复;③本研究中的缺血性脑卒中复发多为非致残性卒中复发,故对预后结局影响不明显。本研究虽为回顾性研究,但通过PSM 有效降低了两组的混杂偏倚,并达到模拟随机对照研究的效果,增加了结果的可信度[24],但同时本研究样本量偏小,且为单中心研究,故结论推广需进一步多中心大样本研究数据的支持。
综上所述,通过进行CYP2C19 基因多态性检测指导氯吡格雷精准用药,虽对缺血性脑卒中患者脑动脉重建术后短期预后结局无显著影响,但可有效降低患者术后缺血性脑卒中复发风险,且不增加出血及死亡风险。故对拟行脑动脉支架置入术的缺血性脑卒中患者推荐术前行CYP2C19 基因检测,以识别患者的氯吡格雷代谢能力,并根据检测结果选择合适的抗血小板治疗方案,使得抗栓治疗效果最大化,风险最小化,使患者真正获益。

