甘蔗叶乙酸乙酯部位化学成分研究
谢安然, 韦 玮, 郝二伟, 谢金玲, 邓家刚, 侯小涛*
(1. 广西中医药大学 广西中药药效研究重点实验室, 南宁 530200; 2. 广西农作物废弃物功能成分研究协同创新中心, 南宁 530200; 3. 广西中医药大学 药学院, 南宁 530200 )
甘蔗(Saccharumofficinarum)为禾本科黍亚科草本植物,主产于热带和亚热带地区,全世界有一百多个国家出产甘蔗,其中产量最高的是巴西、印度和中国。在我国,甘蔗主要分布于江西、湖南、福建、广东、广西、四川和云南等地,是糖类加工产业的主要经济作物。同时,甘蔗产业是广西主要农业支柱产业,甘蔗种植面积连续多年稳居全国第一,蔗糖总产量占全国总产量在60%以上。甘蔗叶为甘蔗的叶,是甘蔗收获和加工过程中的主要废弃物和副产物,一般处理方法为就地焚烧或直接丢弃在田埂和河道中,造成了严重的资源浪费和环境污染。随着甘蔗种植规模的不断扩大,如何对甘蔗叶进行有效的资源回收再利用是近年来亟须解决的问题。
在新型建筑材料与建筑方案的研究下,建筑工程技术越来越要求精细化,对建筑材料以及建筑结构的要求越来越高。建筑工程技术的精细化,除了可以使建筑更加安全,还对建筑工程技术的发展奠定了基础。
甘蔗叶在广西民间及瑶族地区具有悠久的药用历史,在瑶医药记载中,甘蔗叶主要用于治疗盗汗、消渴症以及汗证。但是,甘蔗叶现多用于饲料加工或粉碎还田,药用价值有待进一步开发。近年来的研究发现,甘蔗叶中主要含有有糖、多糖、苷类、黄酮类和酚类等成分(Jian et al., 2014;何耀涛等,2016;潘王芸等,2019;张金玲等,2019)。药理活性研究表明,甘蔗叶具有抑菌、降血糖、抗炎等作用(侯小涛等,2011;Borsen et al., 2011;江恒,2012;侯小涛等,2013;韦玮等,2018)。
为了深入研究甘蔗叶的化学成分,本研究运用传统分离技术对甘蔗叶化学成分进行分离,并采用现代谱学方法及比对文献数据进行结构鉴定,从甘蔗叶70%乙醇提取物的乙酸乙酯萃取部位分离得到20个化合物(图1),包括酚酸、黄酮、倍半萜、生物碱类化合物。其中,化合物1-4、6、9-11、13-16、18和20均为首次从甘蔗叶中分离鉴定得到。
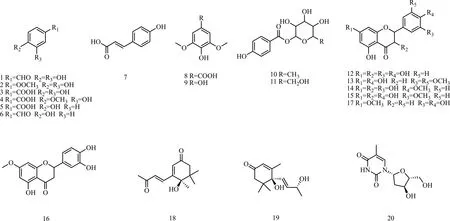
图 1 化合物1-20的结构Fig. 1 Chemical structures of compounds 1-20
1 仪器与材料
1.1 药材
甘蔗叶于2019年12月采自广西南宁市武鸣甘蔗种植区。经广西中医药大学韦松基教授鉴定为禾本科植物甘蔗(Saccharumofficinarum)的叶。标本(20191225-1)存放于广西中医药大学广西中药药效重点实验室。
1.2 仪器和试剂
1252型半制备高效液相色谱仪(Pre-HPLC,美国Waters公司);Q-Tof MicroTM型质谱仪(美国Waters 公司);Inova-600 型超导核磁共振波谱仪(美国Varian 公司);2695型高效液相色谱仪(美国Waters公司);SB25-12D超声波清洗机(宁波新芝生物科技股份有限公司);UPK-I-10T优普系列超纯水器(四川优普超纯科技有限公司);SHZ-III型循环水真空泵(上海亚荣生化仪器厂);柱层析硅胶(100~200目、200~300目,青岛海洋化工厂);柱色谱用硅胶(200~300 目)及薄层色谱用GF254硅胶预制板(青岛海洋化工厂);Sephadex LH-20葡聚糖凝胶(瑞典 Amer-sham Pharmacia公司);00G-4252-P0-AX制备色谱柱(250 mm×21.2 mm,5 μm,美国Phenomenex公司);Xseiect HSS T3分析型色谱柱[4.6 mm×250 mm,5 μm,沃特世科技(上海)有限公司];分析纯溶剂(成都市科龙化工试剂厂);色谱级溶剂(德国Merck公司);质谱级溶剂(美国 Thermo 公司)。
1.3 提取和分离
干燥甘蔗叶药材(10 kg)粗粉,先用10倍量的70%乙醇回流提取3次,合并提取液,减压浓缩得浸膏(1 135 g),蒸馏水充分分散;再依次用3倍体积的石油醚、乙酸乙酯、正丁醇进行萃取。减压回收溶剂,分别得到石油醚部位浸膏、乙酸乙酯部位浸膏、正丁醇部位浸膏和水层部位浸膏。
将乙酸乙酯部位浸膏(125.8 g)过硅胶柱色谱分离,以石油醚-乙酸乙酯(50∶1~0∶1)和乙酸乙酯-甲醇(50∶1~0∶1)梯度洗脱,得到7个流分(Fr. 1~Fr. 7)。其中,Fr. 2经硅胶柱色谱,以石油醚-乙酸乙酯(20∶1~0∶1)梯度洗脱,得到5个亚组分(Fr. 2-1~Fr. 2-5)。Fr. 2-2 经Sephadex LH-20 柱色谱分离,用氯仿-甲醇(1∶1)反复洗脱,得到化合物1(4.1 mg)、2(6.1 mg)、4(11.6 mg)、9(15.0 mg);Fr. 2-4 经 pre-HPLC以20%甲醇分离纯化,得到化合物18(9.2 mg);Fr. 2-5 经pre-HPLC 以30%甲醇分离纯化,得到化合物5(6.0 mg)、7(11.0 mg);Fr. 2-6 经 pre-HPLC 以10%甲醇分离纯化,得到化合物12(2.2 mg)、13(5.3 mg)、14(4.3 mg);Fr. 2-9 经 Sephadex LH-20 柱色谱(二氯甲烷-甲醇,1∶1)反复纯化得到化合物16(4.3 mg)。Fr. 3 经 Sephadex LH-20 柱色谱分离,用氯仿-甲醇(1∶1)反复洗脱,得到12个亚组分(Fr. 3-1~Fr. 3-12)。其中,Fr. 3-11经pre-HPLC 以35%乙腈分离纯化,得到化合物15(3.0 mg)。Fr.4经中压色谱分离凝胶(middle chromatography isolated gel,MCI)柱色谱以甲醇-水(50∶1~0∶1)梯度洗脱,得到5 个亚组分(Fr. 4-1~Fr. 4-5)。其中,Fr. 4-1经 pre-HPLC 以20%甲醇分离纯化,制备得到化合物3(4.8 mg)、8(6.7 mg);Fr. 4-2 经 pre-HPLC 以10%甲醇分离纯化,得到化合物19(3.7 mg)、20(7.4 mg);Fr. 4-5 经 Sephadex LH-20 柱色谱用氯仿-甲醇(1∶1)反复洗脱,得到化合物17(5.0 mg)。Fr. 6经硅胶柱色谱以石油醚-乙酸乙酯(50∶1~0∶ 1)梯度洗脱,得到10个不同极性的亚组分(Fr. 6 -1~Fr. 6-10)。其中,Fr. 6-2 经Sephadex LH-20 柱色谱用氯仿-甲醇(1∶1)反复洗脱,得到化合物6(5.1 mg);Fr. 6-5经 pre-HPLC 以80%甲醇分离纯化,得到化合物10(13.6 mg)、11(8.1 mg)。
(1)智慧城市感知质量、智慧城市发展水平与智慧城市建设满意度呈现正相关(H1,H2)得到验证,且在0.05水平下是显著的。这表明智慧城市感知质量与智慧城市发展水平的提高会较大程度地提高居民的生活服务水平,对市民对智慧城市建设的满意度有较大影响。
另一些有大理想的人则攻破一堵一堵的墙闯了进来,走到这个院落中心,在不知不觉中就变为这里的一分子,然后用那双毁墙的手,拾起满地散落的砖头,把墙重新垒起来,而且砌得又厚又高。
2 结构鉴定
化合物1黄色针状结晶(甲醇)。HR-ESI-MSm/z: 137.024 4 [M-H]-。1H-NMR (600 MHz, DMSO-d6)δ: 9.68(1H, s, H-7), 7.26(1H, dd,J=8.1, 1.8 Hz, H-6), 7.22(1H, d,J=1.8 Hz, H-2), 6.89(1H, d,J=8.1 Hz, H-5);13C-NMR (150 MHz, DMSO-d6) δ: 191.0(C-7), 152.6(C-4), 146.0(C-3), 128.6(C-1), 124.6(C-6), 115.5(C-5), 114.2(C-2)。以上数据与文献(王文祥等,2013)报道一致,故鉴定化合物1为原儿茶醛(3,4-dihydroxybenzaldehyde)。
化合物2黄色粉末(甲醇)。1H-NMR (600 MHz, DMSO-d6) δ: 7.43(2H, s, H-2, 6), 6.83(1H, d,J=8.4 Hz, H-5), 3.73(3H, s, 7-OCH3);13C-NMR (150 MHz, DMSO-d6) δ: 167.5(C-7), 151.0(C-4), 147.2(C-3), 125.9(C-1), 123.4(C-6), 115.0(C-5), 112.7(C-2), 55.5(OCH3)。以上数据与文献(赵明等,2020)报道一致,故鉴定化合物2为3, 4-二羟基-苯甲酸甲酯(methyl 3, 4-dihydroxybenzoate)。
(1)低成本。问卷数据显示47.13%的人觉得网约车在价格方面更加实惠。因为打车软件通过利用闲置的出租车或者私家车为广大市民的出行提供了便利,以共享经济的方式用较低的成本,为广大市民提供打车服务。
化合物14黄针晶体(丙酮)。1H-NMR (600 MHz, CD3OD) δ: 7.76(1H, d,J=8.5 Hz, H-6′), 7.74(1H, d,J=2.0 Hz, H-2′), 7.06(1H, d,J=8.5 Hz, H-5′), 6.40(1H, d,J=2.0 Hz, H-8), 6.19(1H, d,J=2.0 Hz, H-6), 3.93(3H, s, 4′-OCH3);13C-NMR (150 MHz, CD3OD) δ: 177.5(C-4), 165.7(C-7), 162.6 (C-5), 158.3(C-9), 150.7(C-4′), 147.4(C-3′), 137.7(C-3), 121.5(C-1′), 115.7(C-5′, 6′), 112.2(C-2′), 104.6(C-10), 99.3(C-6), 94.4(C-8), 56.4(C-OCH3)。以上数据与文献(邓安珺等,2008)报道一致,故鉴定化合物14为异柽柳素(tamarixetin)。
化合物13黄针晶体(丙酮)。HR-ESI-MSm/z: 329.064 7 [M-H]-。1H-NMR (600 MHz, DMSO-d6) δ: 7.32 (2H, s, H-2′, 6′), 6.97(1H, s, H-3), 6.54(1H, s, H-8), 6.19(1H, s, H-6), 3.88(6H, s, 3′, 5′-OCH3);13C-NMR (150 MHz, DMSO-d6) δ: 181.8(C-4), 164.6(C-7), 163.6(C-2), 161.4(C-9), 157.4(C-5), 148.2(C-3′, 5′), 139.9(C-4′), 120.4(C-1′), 104.4(C-2′, 6′), 103.4(C-3), 99.0(C-6), 94.3(C-8), 56.4(3′, 5′-OCH3)。以上数据与文献(邹忠杰和龚梦鹃,2010)报道一致,故鉴定化合物13为小麦黄素(tricin)。
化合物4白色粉末(甲醇)。HR-ESI-MSm/z:167.034 5 [M-H]-。1H-NMR (600 MHz, DMSO-d6) δ: 7.40(1H, dd,J=8.4, 2.0 Hz, H-6), 7.35(1H, s, H-2), 6.97(1H, d,J=8.4 Hz, H-5), 3.81(3H, s, 4-OCH3);13C-NMR (150 MHz, DMSO-d6) δ: 167.5(7-COOH), 151.4(C-4), 146.8(C-3), 129.7(C-6), 121.5(C-1), 116.1(C-2), 111.3(C-5), 55.6(4-OCH3)。以上数据与文献(邹欢等,2017)报道一致,故鉴定化合物4为3-羟基-4-甲氧基苯甲酸(3-hydroxy-4-methoxybenzoic acid)。
化合物12黄色粉末(甲醇)。1H-NMR (600 MHz, CD3OD)δ: 7.86(1H, d,J=2.1 Hz, H-2′), 7.52(1H, dd,J=8.0, 2.0 Hz, H-6′), 6.89 (1H, d,J=8.0 Hz, H-5′), 6.49 (1H, d,J=2.0 Hz, H-8), 6.20 (1H, d,J=2.0 Hz, H-6);13C-NMR (150 MHz, CD3OD) δ: 176.8(C-4), 165.8(C-7), 160.8(C-5), 157.8(C-9), 147.2(C-2), 146.4(C-4′), 145.7(C-3′), 136.8(C-3), 122.6(C-1′), 121.3(C-6′), 115.7(C-2′), 117.2(C-5′)。以上数据与文献(满兴战等,2019)报道一致,故鉴定化合物12为槲皮素(quercetin)。
化合物6白色粉末(甲醇)。HR-ESI-MSm/z: 121.029 5 [M-H]-。1H-NMR (600 MHz, CD3OD) δ: 9.76(1H, s, CHO), 7.77(2H, d,J=8.4 Hz, H-2, 6), 6.91(2H, d,J=8.4 Hz, H-3, 5);13C-NMR (150 MHz, CD3OD) δ: 192.8(CHO), 165.2(C-4), 133.4(C-2, 6), 130.3(C-1), 116.9(C-3, 5)。以上数据与文献(龚韦凡等,2017)报道一致,故鉴定化合物6为对羟基苯甲醛(p-hydroxybenzyl aldehyde)。
化合物10白色粉末(甲醇)。HR-ESI-MSm/z: 283.081 4 [M-H]-。1H-NMR (600 MHz, DMSO-d6) δ: 7.89(2H, d,J=8.8 Hz, H-2, 6), 7.11(2H, d,J=8.8 Hz, H-3, 5), 5.48(1H, d,J=1.8 Hz, H-1′), 3.84 (1H, m, H-2′), 3.64 (1H, dd,J=9.3, 3.2 Hz, H-3′), 3.39 (1H, m, H-5′), 3.29 (1H, t,J=9.3 Hz, H-4′), 1.09 (3H, d,J=6.2 Hz, H-6′),;13C-NMR (150 MHz, DMSO-d6) δ: 167.0(C-7), 159.6(C-1), 131.3(C-3, 5), 124.2(C-4), 116.0(C-2, 6), 98.2(C-1′), 71.7(C-2′), 70.4(C-4′), 70.1(C-3′), 69.8(C-5′), 17.9(C-6′)。以上数据与文献(李艳茸等,2014)报道一致,故鉴定化合物10为1-hydroxy-benzoyl-4-O-α-L-rhamnopyranoside。
化合物8白色针状晶体(甲醇)。1H-NMR (600 MHz, DMSO-d6), δ: 9.19(1H, s, OH) 7.19(2H, s, H-2、6), 3.79(6H, s, OCH3×2);13C-NMR (150 MHz, DMSO-d6) δ: 167.5(-COOH), 147.4(C-4), 140.01(C-3, C-5), 120.8(C-1), 106.8(C-2, C-6), 56.0(2-OCH3, 6-OCH3)。以上数据与文献(陈丽等,2020)报道一致,故鉴定化合物8为丁香酸(syringic acid)。
化合物9白色粉末(甲醇)。1H-NMR (600 MHz, DMSO-d6)δ: 7.20(2H, s, H-2, 6), 3.8(6H, s, OCH3);13C-NMR (150 MHz, DMSO-d6) δ: 167.4(C-1), 147.4(C-3, 5), 140.1(C-4), 106.8(C-2, 6), 56.0(OCH3)。以上数据与文献(韦玮等,2018)报道一致,故鉴定化合物9为3, 5-二甲氧基对苯二酚(3,5-dihydroxy-hydroquinone)。
施用腐熟的农家肥作底肥为主,不施碳铵、磷铵等刺激性强的化肥,避免伤害泥鳅,每亩施有机肥约500kg,水稻专用复合肥30~40kg,水稻移植后7~10天,每亩追尿素8~10kg,在孕穗期酌情施肥,肥料不撒在沟内。病虫防治要选用高效低毒、低残留对口农药,如氯虫苯甲酰胺、苯甲·丙环唑、烯啶·吡蚜酮等,喷药时保持深水。禁用毒杀酚、五氯酚钠、呋喃丹、敌百虫、菊酯类及生石灰、茶籽饼等。
化合物7无色针状晶体(甲醇)。HR-ESI-MSm/z: 137.024 4 [M-H]-。1H-NMR (600 MHz, CD3OD), δ: 7.59(1H, d,J=15.9 Hz, H-7), 7.43(2H, d,J=8.4 Hz, H-2, 6), 6.79(2H, d,J=8.3 Hz, H-3, 5), 6.27(1H, d,J=15.9 Hz, H-8);13C-NMR (150 MHz, CD3OD), δ: 171.0(C-9), 161.2(C-4), 146.6(C-7), 131.2(C-2, 6), 127.2(C-1), 116.8(C-3, 5), 115.6(C-8)。以上数据与文献(肖春荣,2019)报道一致,故鉴定化合物7为对羟基肉桂酸(p-hydroxy-cinnamic acid)。
各农村水电站企事业单位按照绿色小水电发展有关要求,首先是编制绿色小水电站创建方案并组织实施,再创建任务完成且自查结果符合《绿色小水电评价标准》的基础上,填写《绿色小水电站申报表》,然后向所在地县级以上水行政主管部门逐级申报。
化合物11无色针状晶体(甲醇)。HR-ESI-MSm/z: 299.076 7 [M-H]-.1H-NMR (600 MHz, DMSO-d6) δ: 7.88(2H, d,J=8.8 Hz, H-2, 6), 7.09(2H, d,J=8.8 Hz, H-3, 5), 4.98(1H, d,J=7.4 Hz, H-1′);13C-NMR (150 MHz, DMSO-d6) δ: 60.6(C-6′), 69.6(C-4′), 73.2(C-2′), 76.5(C-5′), 77.1(C-3′), 99.8(C-1′), 115.8(C-3,5), 124.2(C-1), 131.2(C-2,6), 160.8(C-4), 167.0(C-7)。以上数据与文献(杨晨悦和王晓玲,2018)报道一致,故鉴定化合物11为对羟基苯甲酸-β-D-吡喃葡萄糖酯苷(p-hydroxy-benzoyl-β-D-glucopyranoside)。
近年来,在我国高等医学事业的迅猛发展的背景下,医学院校实验室的软、硬件建设也得到了长足的发展。因此,实验室资源共享要求的提高、实验室仪器设备规模的扩大、参与实验室活动人员数量的增多等软、硬件完善与实验室管理体系落后之间的矛盾也就显得日益突出。
化合物5无色针状晶体(甲醇)。HR-ESI-MSm/z: 137.024 2 [M-H]-。1H-NMR (600 MHz, CD3OD) δ: 7.88(2H, d,J=8.8 Hz, H-2, 6), 6.81(2H, d,J=8.8 Hz, H-3, 5);13C-NMR (150 MHz, CD3OD) δ: 170.2(COOH), 160.7(C-4), 133.0(C-2, 6), 122.9(C-1), 116.0(C-3, 5)。以上数据与文献(向丽敏等,2020)报道一致,故鉴定化合物5为对羟基苯甲酸(p-hydroxy-benzoic acid)。
化合物3白色粉末(甲醇)。1H-NMR (600 MHz, DMSO-d6) δ: 7.31(1H, d,J=2.0 Hz, H-2), 7.26(1H, dd,J=8.2, 2.0 Hz, H-6), 6.76(1H, d,J=8.2 Hz, H-5);13C-NMR (150 MHz, DMSO-d6) δ: 115.2(C-6), 116.6(C-5), 121.9(C-1), 144.9(C-3), 150.0(C-4), 167.5(COOH)。以上数据与文献(夏明文等,2010)报道一致,故鉴定化合物3为3, 4-二羟基苯甲酸(3,4-dihydroxybenzoic acid)。
3)根据《徐氏宗谱》的推断:孺一房在永乐年间从总房分出,急迫地需要建功夸耀,替本房争取体面,孺一公的儿子徐积善捐谷助赈,终于受到朝廷的圣旨表彰,得到荣誉的孺一房没有理由不即刻建造牌坊树立本族威望,甚至会加倍付钱赶工,不会等到150年后徐积善本人已逝世多年,再立牌坊;
化合物15黄色粉末(甲醇)。HR-ESI-MSm/z: 315.049 3 [M-H]-。1H-NMR (600 MHz, DMSO-d6) δ: 7.66(1H, d,J=2.2 Hz, H-2′), 7.64(dd,J=8.7, 2.2 Hz, H-6′), 7.07(1H, d,J=8.6 Hz, H-5′), 6.41 (1H, d,J=2.0 Hz, H-8), 6.18(1H, d,J=2.0 Hz, H-6), 3.83(3H, s, 3′-OCH3);13C-NMR (150 MHz, DMSO-d6) δ: 55.6(3′-OCH3), 93.4(C-8), 98.2(C-6), 103.0(C-10), 111.8(C-2′), 114.6(C-5′), 119.7(C-1′), 123.4(C-6′), 136.2(C-3), 146.2(C-2), 146.3(C-3′), 149.3 (C-4′), 156.2(C-9), 160.7(C-5), 164.0(C-7), 175.9(C-4)。以上数据与文献(周北斗等,2018)报道一致,故鉴定化合物15为异鼠李素(isorhamnetin)。
化合物16白色粉末(甲醇)。HR-ESI-MSm/z: 301.069 7 [M-H]-。1H-NMR (600 MHz, DMSO-d6) δ: 6.74 - 6.87(3H, m, H-2′,5′,6′), 6.74(d,J=2.1 Hz, 2H), 6.07(2H, m, H-6, 8), 5.41(1H, dd,J=12.6, 3.0 Hz, H-2), 3.78(3H, s, 7-OCH3), 3.23(2H, m, H-3);13C-NMR (150 MHz, DMSO-d6) δ: 197.0 (C-4), 167.4(C-7), 163.2(C-5), 162.8(C-9), 145.8 (C-4′), 145.2(C-3′), 129.3(C-1′), 118.0 (C-6′), 115.3(C-5′), 114.4(C-2′), 102.6(C-10), 94.6(C-6), 93.8(C-8), 78.7(C-2), 55.9(7-OCH3), 42.1(C-3)。以上数据与文献(赵东保等,2005)报道一致,故鉴定化合物16为5, 3′, 4′-三羟基-7-甲氧基二氢黄酮(5,3′,4′-trihydroxy-7-methoxy-flavanone)。
化合物17黄色粉末(甲醇)。HR-ESI-MSm/z: 299.054 0 [M-H]-。1H-NMR (600 MHz, DMSO-d6) δ: 7.46(1H, d,J=2.0 Hz, H-2′), 7.44(1H, dd,J=8.0, 2.0 Hz, H-6′), 6.88(1H, d,J=8.3 Hz, H-5′), 6.72(2H, s, H-3, 8), 6.37(1H, d,J=2.0 Hz, H-6), 3.87(3H, s, 7′-OCH3);13C-NMR (150 MHz, DMSO-d6) δ: 181.8(C-4), 165.1(C-2), 164.3(C-7), 161.2(C-5), 157.2(C-9), 150.3(C-4′), 145.9(C-3′), 121.1(C-1′), 119.2(C-6′), 116.0(C-5′), 113.4(C-2′), 104.7(C-10), 102.9(C-3), 98.0(C-6), 92.6(C-8), 56.1(7′-OCH3)。以上数据与文献(张幸国和田景奎,2006)报道一致,故鉴定化合物17为7-O-甲基圣草酚(7-O-Methyleroidictyol)。
化合物18浅棕色油性物质(甲醇)。HR-ESI-MSm/z: 223.132 5 [M-H]-。1H-NMR (600 MHz, DMSO-d6) δ: 6.97(1H, d,J=15.8 Hz, H-1′), 6.27(1H, d,J=15.8 Hz, H-2′), 5.86(1H, s, H-2), 2.63(1H, d,J=17.0 Hz, H-6), 2.26(3H, s, H-4′), 2.16(1H, d,J=17.0 Hz, H-6), 1.80(3H, d,J=1.4 Hz, H-7), 0.96(3H, d,J=25.1 Hz, H-8), 0.92(3H, s, H-9);13C-NMR(150 MHz, DMSO-d6) δ: 198.2(C-3′), 197.0(C-1), 161.7(C-3), 147.2(C-1′), 130.5(C-2′), 126.6(C-2), 78.1(C-4), 41.2(C-5)。27.2(C-4′), 24.2(C-9), 49.3(C-6), 23.2(C-8), 18.6(C-7)。以上数据与文献(Yi et al.,2012)报道一致,故鉴定化合物18为[(E)-4-(1S,3R,4R)-1-hydroxy-4,5,5-trimethyl-7-oxabicyclo [4.1.0]heptan-1-yl]but-1-en-3-o-ne。
化合物19无色油性物质(甲醇)。HR-ESI-MSm/z: 269.118 2 [M+HCOO]-。1H-NMR (600 MHz, DMSO-d6) δ: 5.77(1H, s, H-4), 5.67(1H, m, H-7), 5.65(1H, m, H-8), 4.98(1H, m, H-9), 2.35(1H, d,J=16.7 Hz, H-2α), 2.07~2.01(1H, m, H-2β), 1.79(3H, d,J=1.4 Hz, H-13), 1.10(3H, d,J=6.4 Hz, H-10), 0.92(3H, s, H-12), 0.90(3H, s, H-11);13C-NMR (150 MHz, DMSO-d6) δ: 19.0(C-13), 23.1(C-11), 24.0(C-12), 24.1(C-10), 41.0(C-1), 49.4(C-2), 66.1(C-9), 125.5(C-4), 127.9(C-8), 135.9(C-7), 197.4(C-3)。以上数据与文献(曾金祥等,2017)报道一致,故鉴定化合物19为blumenol A 。
化合物20无色油性物质(甲醇)。1H-NMR (600 MHz, CD3OD) δ: 7.81(1H, s, H-6), 6.27(1H, t,J=6.8 Hz, H-1′), 4.39(1H, m, H-4′), 3.89(1H, m, H-3′), 3.79(1H, m, H-5α), 3.72(1H, m, H-5β), 2.26~2.15(2H, m, H-2′), 1.87(3H, s, CH3);13C-NMR (150 MHz, CD3OD) δ: 12.4(CH3), 41.2(C-2′), 62.8(C-5′), 72.2(C-3′), 86.2(C-2′), 88.8(C-1′), 111.5(C-5), 138.2(C-6), 152.4(C-2), 166.4(C-4)。以上数据与文献(杨顺丽等,2003)报道一致,故鉴定化合物20为胸腺嘧啶脱氧核苷(thymidine)。
3 讨论
本研究从甘蔗叶中共分离得到20个化合物,包括11个酚酸类化合物、6个黄酮类化合物、2个倍半萜化合物和1个生物碱类化合物。化合物1-4、6、9-11、13-16、18和20均为首次从甘蔗叶中分离得到。
前期研究显示,甘蔗叶具有抗炎作用(侯小涛等,2013)。其中,化合物1原儿茶醛具有抑制炎症作用(Zhou et al., 2005);化合物6对羟基苯甲醛可促进神经的修复,其作用机制与促进内皮细胞释放神经营养因子VEGF-A和BDNF有关(杨媛等,2019);化合物12槲皮素具有抗炎作用,能够抑制NF-κB的活化,继而抑制细胞因子和其他促炎因子的释放(Guazelli et al., 2018);化合物15异鼠李素具有抗炎等作用(Lee & Kim,2018),可通过减轻氧化应激,缓解对游离脂肪酸对L-02细胞诱导的脂质沉积。核因子NF-E2相关因子2通路在此过程中发挥了重要作用(周健等,2021)。甘蔗叶提取物具有体外抗肿瘤作用,乙酸乙酯提取物是其中最主要的活性部位(邓家刚等,2010)。倍半萜类化合物具有抗肿瘤活性(付佳等,2019)。本研究分离到的成分中亦包含倍半萜类成分,但它们是否为甘蔗叶的抗肿瘤活性成分,尚需后续进一步研究加以验证。本文对甘蔗叶乙酸乙酯部位的化学成分进行了研究,本研究结果丰富了甘蔗叶化学成分的结构类型,为今后甘蔗叶资源回收再利用及药用价值的开发提供了科学依据。

