固相法的制备参数对磷酸铁锂正极材料性能的影响
李立平,肖炜彬,李煜乾,黄铿齐,黄司平,谭 泽
(广东光华科技股份有限公司,广东 汕头 515000)
磷酸铁锂(LiFePO4)具有较高的比容量、较佳的放电平台和良好的热稳定性,在动力电池、储能、通信基站等领域的应用广泛[1-2]。LiFePO4为橄榄石型结构,由LiO6八面体、FeO6八面体和PO4四面体基元构成[3],晶体结构如图1所示。其中,强的P−O共价键保证了整个结构具有较高的热力学稳定性,而FeO6八面体无法形成连续的网络结构,限制了Li+的自由脱嵌,导致LiFePO4的电子导电率和Li+扩散系数仅为 10-9~10-10s・cm-1和 10-16cm2・s-1。LiFePO4材料的电化学性能差,能量密度也不高[4-6],随着对商业化LiFePO4电池性能的要求越来越高,提升材料的电化学性能已然成为一大研究热点。对LiFePO4微观结构加以改善并调控制备工艺参数,是提高LiFePO4材料性能的常用手段。

图1 LiFePO4的晶体结构示意图
LiFePO4的制备方法主要有固相法和液相法[7-9]。相比液相法,固相法具有产品纯度较高、粒度较低、形貌均一等优点,适合大规模商业化生产。固相法制备LiFePO4/C正极材料的过程,涉及包覆碳含量、元素配比、煅烧温度、前驱体等参数调控,这些制备参数最终会影响材料的电化学性能。其中,包覆碳含量和元素配比这2个工艺参数会直接影响材料的纯度和电子导电率;煅烧温度和前驱体则会影响材料的粒径和结晶性,影响Li+的扩散速率。本文简要介绍了固相法的4个关键制备参数对LiFePO4/C正极材料电化学性能的抑制或促进作用,以确定最佳的制备工艺参数,提高材料的稳定性和优异性,为规模化生产提供理论指导和技术支持。
1 固相法的4个制备参数
1.1 碳源用量
碳热还原制备LiFePO4/C材料的过程,通常会引入有机碳源如碳凝胶、蔗糖和葡萄糖等[10-13],在材料表面形成包覆碳,以提高导电性。焙烧过程中分解生成的热解炭,既作为还原剂还原FePO4,涉及的反应如式(1)所示,也作为成核剂,抑制LiFePO4晶粒的长大与团聚,从而提高电子在颗粒间的转移与传递效率,进而提高材料的导电性[14-17]。LiFePO4/C材料的包覆碳含量与碳源用量呈正相关,因此,碳源用量影响制备材料的品质与性能。碳源用量过少时,材料表面的包覆不均匀,难以完全还原Fe3+,生成的部分杂质会抑制Li+的扩散;碳源用量过多,则会导致包覆碳层过厚,并生成Fe2P等杂相,降低材料的活性物质比例、振实密度和和体积能量密度,阻碍Li+的扩散,并容易出现极化现象[18]。由于合成方法和所使用碳源的差异性,现有的研究报道对最佳的碳含量尚无定论,但根据现有的文献报道,较为适宜的碳源用量为3.0%~10%[19-22]。
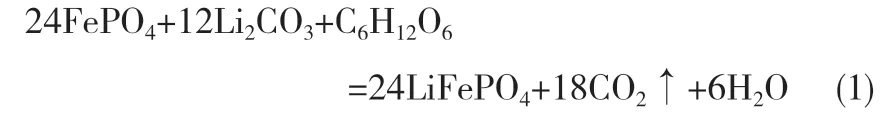
Dominko等人发现,碳层的厚度与碳源用量呈正相关,并且LiFePO4/C材料的放电比容量,随碳层厚度的增加呈降低趋势。作者认为,碳层厚度增加会抑制Li+的脱嵌效率,使得材料的充放电比容量有所下降。谭卓[23]以柠檬酸为碳源,采用喷雾干燥法制备了球形 LiFePO4/C正极材料,1C倍率下,材料的放电比容量随包碳量的增加先提高后降低。包碳量分别为1%、3%和5%时,材料的放电比容量分别 为 137.5 mA・h・g-1、148.8 mA・h・g-1和 145.3 mA・h・g-1。这是因为适宜的碳包覆量能减缓材料的极化现象,过量则会降低材料的振实密度,导致能量密度降低。曹赫[25]用葡萄糖制备了不同碳源用量的LiFePO4/C正极材料,结果显示,葡萄糖添加量为6%时材料的包覆不完整,包覆层随碳源用量的提高而不断增加;在不同的倍率下,4种材料的放电比容量均呈现先增大后减少的趋势。这是因为,厚度适中的包覆层有利于材料表面的电荷转移,但较厚的碳层则会阻碍Li+在电解液与材料内部的传输,降低材料的可逆比容量。
1.2 元素配比
采用固相法合成LiFePO4/C材料时,不同的锂铁比(Li/Fe)或磷铁比(Fe/P),同样会使材料的粒度及表面形貌发生改变。非化学计量的元素配比引起的元素过量,可能会产生杂质Fe2P、Li3PO4等。当磷铁比一定时,根据Fe-P-Li-O相图[27-29],Li元素过量时,即 Li/Fe> 1,易有 Li3PO4、Fe2O3等生成,反应如式(2)所示。其中,惰性物质Li3PO4在细化LiFePO4晶粒、减轻烧结融合程度、提高Li+扩散速率的同时,也会阻碍电子的传输。当少量缺Li时,即 Li/Fe< 1,则常有 Fe2P2O7、FeP4和 Fe2P等产生,反应如式(3)和式(4)所示。杂质的生成均会造成活性材料LiFePO4的量减少,降低正极材料的放电比容量。较佳的Li/Fe元素配比宜控制在1.00~1.05[30-36]。当锂铁比一定时,少量缺Fe,即Fe/P<1,会产生Fe空位,这能够降低Li+的扩散能垒,增加Li+在一维通道的传输速率,提高材料的倍率性能。较佳的Fe元素一般应控制在0.94~0.98[37-38]。
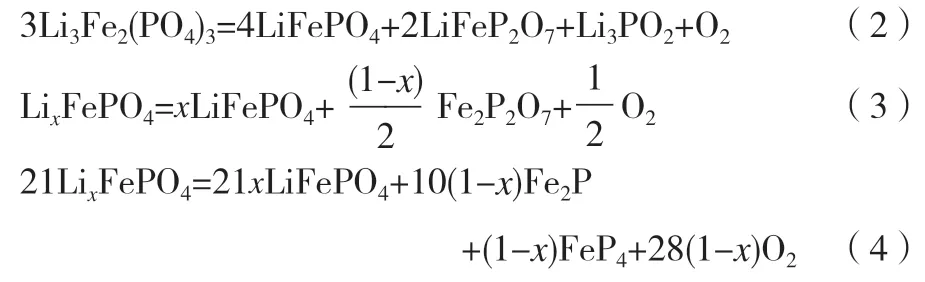
包晗以LiH2PO4和Fe(NO3)3・9H2O为原料,采用碳热还原法制备了LiFePO4/C正极材料,结果表明,材料的放电比容量随着Li用量的增多呈先增大后减小的趋势。在0.1C倍率下,Li/Fe的摩尔比分别为0.98、1.00和1.05时,放电比容量分别为92 mA・h・g-1、118 mA・h・g-1和 100 mA・h・g-1。同时,在0.1C倍率下循环20次后,容量保持率分别为93.5%、100%和95.8%。吴燕杰制备了Li过量的LixFePO4(x=1.00~1.05)材料,性能测试结果表明,0.1C倍率下,LixFePO4的放电比容量随着Li含量的增大而逐渐减小,放电比容量分别为144.8 mA・h・g-1、132.1 mA・h・g-1、126.0 mA・h・g-1和120.7 mA・h・g-1;在2C倍率下,LixFePO4的放电容量保持率分别为0.62%、54.12%、53.65%和49.63%。作者认为,过量的Li不会占据Fe位形成Li-Fe反位缺陷,生成的第二相惰性导体Li3PO4会阻碍电子传输,造成放电比容量下降;但Li3PO4固有的离子导电特性,也会提高Li+的扩散速率和材料的大倍率性能。王帆系统研究了锂铁配比对LixFePO4(x=1.00~1.04)材料形貌的影响。结果发现,Li元素过量程度的增大有助于细化晶粒,提高LixFePO4材料的倍率放电性能。1.0C和5.0C倍率下,LixFePO4的放电比容量均随着Li的不断过量呈现先增大后减小的趋势。x为1.03时,材料表现出最佳的倍率特性;x提高至1.04,开始有非活性的Li3PO4杂相生成,放电比容量有所降低,但仍高于LiFePO4。
Hu 等人制备了系列 LiFe1-xPO4(x=0、0.03、0.06和0.09)材料。结果表明,不同的倍率下,LiFe1-xPO4材料的放电比容量随着缺Fe量的增加呈先增加后减少的趋势,LiFe0.94PO4表现出最佳的倍率性能和循环性能。王帆研究了Fe/P配比对LiFexPO4(x为0.957和0.985)材料的形貌和性能的影响,LiFe0.957PO4的一次粒径显著大于LiFe0.985PO4,说明相对于Fe的过量,P有助于一次颗粒的长大。但在不同的倍率下,LiFe0.957PO4的放电比容量均显著低于LiFe0.985PO4。作者认为,在锂铁比一定的条件下,不同倍率下的放电比容量与一次颗粒的粒度呈正相关性,材料的一次颗粒越小,Li+的传输距离缩短,放电比容量越高。李鹏飞制备了系列少量缺Fe的LiFexPO4/C正极材料(x=0.94,0.96,0.98 和 1.00)。研究结果表明,0.1C倍率下,LiFexPO4/C材料的放电比容量分别为155 mA・h・g-1、152 mA・h・g-1、150 mA・h・g-1、142 mA・h・g-1,在3C 倍率下的放电比容量,则分别为107 mA・h・g-1、120 mA・h・g-1、100 mA・h・g-1、92 mA・h・g-1。XRD的精修结果表明,Li-O键的键长顺序为LiFe0.96PO4>LiFe0.94PO4>LiFe0.98PO4>LiFePO4,Li+的扩散速率和倍率性能,随着Li−O键长的增大而提高。
1.3 合成温度
合成温度同样是固相法制备LiFePO4正极材料时的重要影响因素,一般控制在500~800℃之间[39]。过低的烧结温度会造成固相反应不完全,产物中含有杂质Fe3+且结晶化程度不高,不利于Li+在一维通道的快速脱嵌,导致材料的放电比容量偏低,循环性能较差;温度过高则会使生成的无定形碳包覆层受到不同程度的破坏,同时晶粒出现团聚和长大,增长了Li+的传输路径。此外,合成温度过高容易产生 Fe2P、Li4P2O7等杂质[40-42],反应式如(5)和式(6)所示。生成的Fe2P 层可能会阻塞Li+的一维扩散通道,降低扩散系数,抑制材料的性能[43-46]。
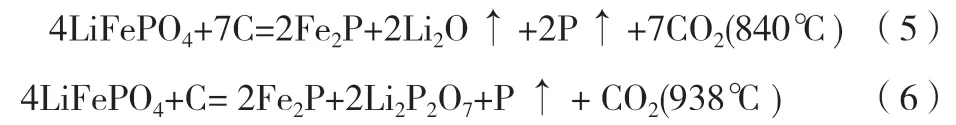
何玉林等人研究了合成温度对LiFePO4/C正极材料性能的影响。结果表明,合成温度为500~650℃时,随着温度的提升材料的颗粒有小幅增大,但总体形貌区别不大;温度超过700℃后,颗粒随温度的升高而明显增大;超过800℃后有Fe2P 杂相产生。电化学测试结果表明,0.1C倍率下,550、600、650、700、750 和 800℃下制备的材料,其放电比容量分别为142.5 mA・h・g-1、149.2 mA・h・g-1、153.7 mA・h・g-1、134.4 mA・h・g-1、123.4 mA・h・g-1和 113.0 mA・h・g-1。 李 志 文采用喷雾热解法制备了LiFePO4/C球形材料,对比了 500、600、640、700、800℃合成温度下的产物,发现材料的放电比容量分别为72.7 mA・h・g-1、90.6 mA・h・g-1、160 mA・h・g-1、130.2 mA・h・g-1和106.3 mA・h・g-1,放电比容量随着温度的升高呈先增大后降低的趋势。这是因为在较低温度下烧结得到的材料,结晶性较差,充放电电压平台的稳定性差,LiFePO4与FePO4之间的相转变过程不明显,偏离充放电电压平台后,仍对应较大比例的比容量,表现出一定的赝电容特性。超过700℃,产生的杂质导致了不可逆相变过程的发生,充放电过程的比容量损失大。李雷等人研究了合成温度(650、675、700、725、750℃)对 LiFePO4材料电化学性能的影响。结果表明,675℃下焙烧得到的材料表现出最佳的材料性能;650℃下制备的材料,颗粒晶型发育不完整,极化严重;温度超过700℃,晶粒会发生二次结晶,团聚现象明显,甚至产生了新的杂质,破坏晶体结构,抑制了Li+的扩散。
1.4 前驱体
采用碳热还原法合成LiFePO4时,通常会使用无水FePO4或含结晶水的FePO4(FePO4・xH2O)作为前驱体,这会对最终合成的LiFePO4形貌有显著的影响,使得合成材料的电化学性能存在差异。相比无水FePO4,FePO4・xH2O在高温下的脱水过程使得LiFe-PO4表面的碳含量和碳层分布不均匀,造成LiFePO4/C材料的性能恶化。根据现有文献的报道,结晶水的存在不利于材料电化学性能的提高[47-51]。
王玲利等人分别使用FePO4・xH2O和无水FePO4前驱体制备了LiFePO4/C正极材料,两者的振实密度分别为0.82 g・mL-1和1.20 g・mL-1。电化学性能测试结果表明,0.2C倍率下,两者的放电比容量接近,分别为147.4 mA・h・g-1和146.2 mA・h・g-1,但后者具有较高的充电速率和导电性能。Zhou等人分别以无水FePO4和FePO4・2H2O为前驱体,采用碳热还原法合成了LiFePO4/C材料。结果表明,与FePO4・2H2O相比,采用无水FePO4制备的正极材料具有良好的结晶度,颗粒尺寸较小且分布均匀,具有较佳的电化学性能。在0.2C、0.5C和1C倍率下,用无水FePO4制备的正极材料,放电比容量分别为160.2 mA・h・g-1、154.6 mA・h・g-1和146.7 mA・h・g-1,用FePO4・2H2O制备的正极材料放电比容量,分别为117.0 mA・h・g-1、101.0 mA・h・g-1和 88.0 mA・h・g-1。
2 展望
本文总结了固相法合成工艺对LiFePO4正极材料电化学性能的影响,阐明了碳源用量、元素配比、合成温度和前驱体等工艺参数均会显著影响LiFe-PO4的材料性能。调整固相法的制备工艺,可达到改性LiFePO4正极材料的目的,使得材料具有较佳的倍率性能和循环性能。结合基础理论研究,探索电化学性能外在表现的本质原因,仍是LiFePO4正极材料可控改性的研究方向。

