三种非洲猪瘟病毒荧光PCR 检测试剂盒和两种核酸提取方法的比对
曹东阳,朱奕霏,马晓媛,白翠,杨金鑫,胡泽宇,吴丹
(吉林省动物疫病预防控制中心,吉林长春 130211)
非洲猪瘟(African swine fever,ASF)是由非洲猪瘟病毒(African swine fever virus,ASFV)引起的猪的一种急性、热性、高度接触性传染病[1],以高热、网状内皮系统出血以及高死亡率为特征。2018 年ASF 首次在我国暴发,给我国养猪业带来了严重经济损失。世界动物卫生组织(WOAH)将其列为法定报告动物疫病,我国将其列为一类动物疫病[2]。ASFV 能够通过节肢动物传播,软蜱是其重要的传播宿主。为科学防控ASF,有效应对该病引发的疫情,我国畜牧兽医部门已建立了常态化监测方案,并更新了多版防控指南。
目前尚缺乏有效防治ASF 的疫苗或药物,因此精准发现并剔除群体中的患病动物尤为关键。常用的ASFV 检测技术主要包括普通PCR、荧光PCR、高敏荧光免疫分析法、夹心ELISA 抗原检测、间接/阻断ELISA 抗体检测、间接免疫荧光法等。其中,荧光PCR 技术因具备灵敏度高、检测便捷、污染小等特点成为ASFV 病原学主流检测方法。随着ASFV 变异株的出现以及荧光PCR 检测技术的普及,市面上的核酸提取和荧光PCR 诊断试剂不断更新、完善,但由于变异毒株排毒量较低,一些提取效率低,扩增敏感性和灵敏度差的试剂盒无法满足实际检测需求。如何选用合适的试剂产品开展防疫工作,是猪场和兽医实验室检测面临的一项重要工作。
本试验分别选取3 个厂家的ASFV 荧光PCR检测试剂盒和2 个厂家的核酸提取试剂盒,参照WOAH《陆生动物诊断试验和疫苗手册》(2018年版)1.1.6 章[3]和GB/T 18648—2020 中ASFV 荧光PCR 部分推荐的程序要求,分别对提取和扩增试剂盒的性能进行比较分析,以期为各兽医实验室ASFV 检测试剂选择提供参考。
1 材料与方法
1.1 试剂
3 个厂家的商品化ASFV 实时荧光定量PCR检测试剂盒(A、B、C),均为国产;2 个厂家的核酸提取试剂盒(D、E),均为国产;B646L基因标准物质,由哈尔滨兽医研究所馈赠,病毒载量为105copies/µL;猪瘟病毒(CSFV)、猪圆环病毒2 型(PCV2)、猪繁殖与呼吸综合征病毒(PRRSV)阳性标准品各1 份,均购自哈尔滨世纪元亨有限公司。
1.2 仪器设备
实时荧光定量PCR 仪CFX96(Bio-Rad,美国)、台式冷冻离心机(Thermo fisher,美国)、PANA9600S 全自动核酸工作站(西安天隆科技有限公司)、自动化移液处理工作站(Hamilton,瑞士)。
1.3 方法
ASFV 荧光定量PCR 扩增试剂评价分别从标准曲线、决定系数(R2)、最低检出限(LOD)、特异性、反应时间等方面进行综合评定;应用ASFV 荧光PCR 检测试剂盒,对2 个厂家的核酸提取试剂进行测试,通过比较Ct 值评价核酸提取效果。
1.3.1 荧光定量PCR 试剂盒性能比较试验 对ASFVB646L基因标准物质进行10 倍梯度稀释,得到105~102copies/µL 标准样品,使用荧光PCR绝对定量方法构建标准曲线,查看CFX ManagerTMSoftware 软件自动输出的标准曲线斜率和R2,同时对每个试剂盒的反应体系、反应条件以及反应时间进行比较。
1.3.2 荧光定量PCR 试剂盒最低检出限(LOD)检测 对ASFVB646L基因标准物质进行10 倍倍比稀释得到103~10-3copies/µL 标准样品,使用3 种荧光定量PCR 试剂盒进行检测,每个样品设置3 个重复,统计不同厂家试剂盒对标准样品的LOD,评价试剂盒的敏感性。
1.3.3 荧光定量PCR 试剂盒特异性试验 使用3种ASFV 荧光定量PCR 试剂盒分别对DEPC 水以及CSFV、PCV2、PRRSV 阳性标准品进行检测。其中,每种试剂盒配置46 份DEPC 水,CSFV、PCV2、PRRSV 阳性标准品各3 个重复孔,统计不同试剂盒特异性检测结果。
1.3.4 病毒核酸提取试剂盒评价试验 应用D、E 2个厂家的核酸提取试剂分别对105和104copies/µL 的ASFV 标准物质进行核酸提取,选用B 厂家ASFV荧光定量PCR 核酸检测试剂盒对提取的核酸进行扩增,每个样品做3 个重复,通过Ct 值比较不同试剂盒的核酸提取差异,并计算差异性和变异系数(CV)。
2 结果
2.1 荧光定量PCR 试剂盒测评
2.1.1 性能比较 3 个厂家的ASFV 荧光PCR扩增试剂盒反应体系、条件、时间以及结果判定等见表1。结果显示,A 试剂盒反应循环数为45,B、C 试剂盒为40;3 个厂家试剂检测时间依次为C <B <A,其中A 试剂盒检测时间最长(105 min),B、C 试剂盒检测时间分别为58和56 min;3 个厂家试剂所需模板含量依次为B <C <A,其中B 试剂盒所需模板量最少(0.5 µL),A、C 试剂盒所需模板量分别为2.0 和1.0 µL;A 试剂盒结果判定中样品Ct ≤38 为阳性,而B、C 试剂盒样品Ct ≤35 为阳性。对3 个试剂盒比较发现,A试剂盒循环数最多,反应时间最长,其较B、C 两款试剂盒应用更为广泛。

表1 3 个厂家ASFV 实时荧光PCR 检测试剂盒测评结果
2.1.2 标准曲线 对4 个稀释梯度(105~102copies/µL)的ASFV 核酸标准物质分别选用3 个厂家的ASFV 荧光PCR 试剂盒进行检测,最终得到标准曲线,每个梯度样品设置3 个重复。结果(图1)显示,受测试剂盒A、B、C 的标准曲线斜率分别为-2.691、-2.721、-2.675,R2分别为0.985、0.996、0.985,结果均较为理想。
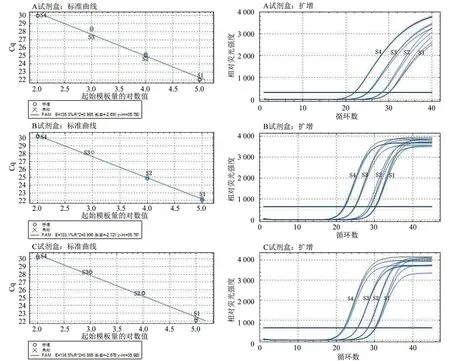
图1 A、B、C 厂家荧光PCR 试剂盒标准曲线和扩增曲线
2.1.3 最低检出限(LOD)对ASFV 标准物质进行7 个梯度的倍比稀释(103~10-3copies/µL),使用3 个厂家的ASFV 荧光定量PCR 试剂盒进行测试,每个样品设置3 个重复。结果(表2)显示,B、C 试剂盒LOD 为10-1copies/µL;A 试剂盒LOD 为10-2copies/µL,且样品重复性较好。
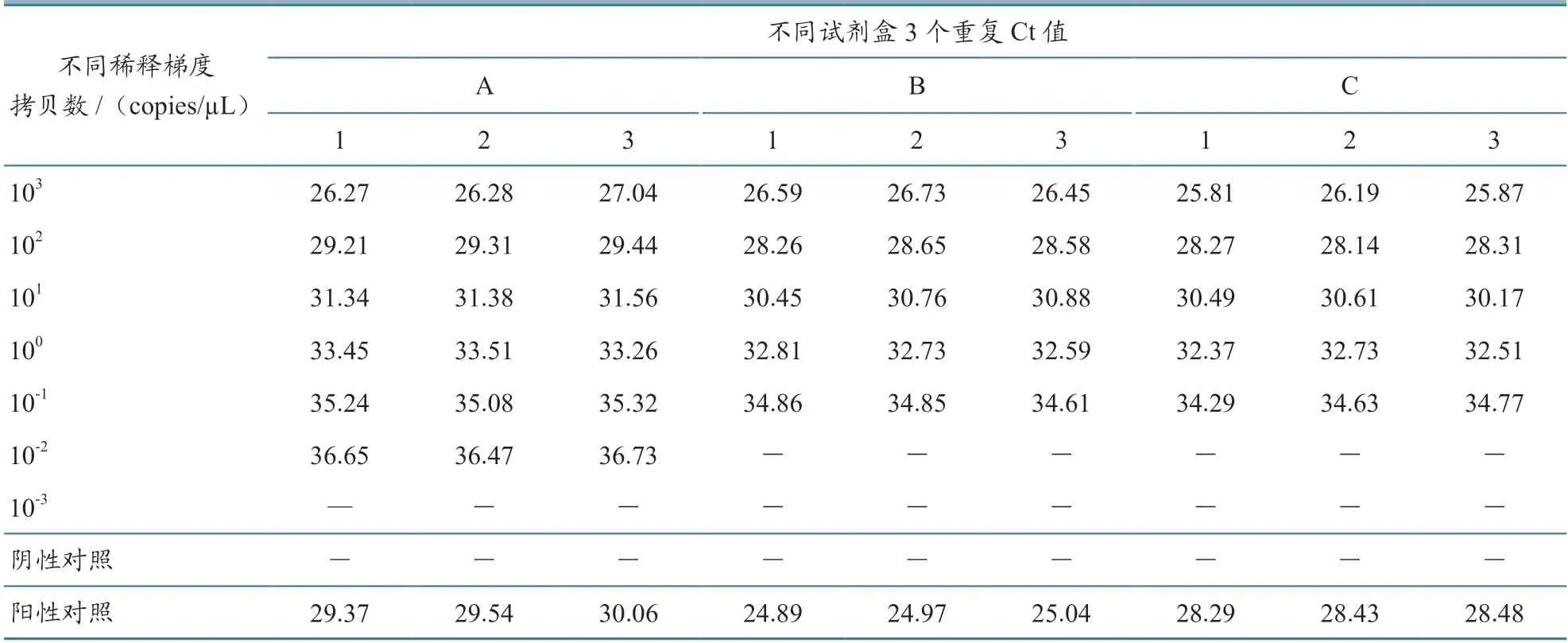
表2 3 个厂家ASFV 荧光PCR 试剂盒LOD 测评结果
2.1.4 特异性试验 结果(图2)显示,除阳性对照外,A、B、C 3 种ASFV 荧光PCR 试剂盒对DEPC 水以及CSFV、PCV2、PRRSV 阳性标准品检测均未得到Ct 值和“S”型扩增曲线,表明这3种ASFV 荧光PCR 试剂盒的特异性均较好。
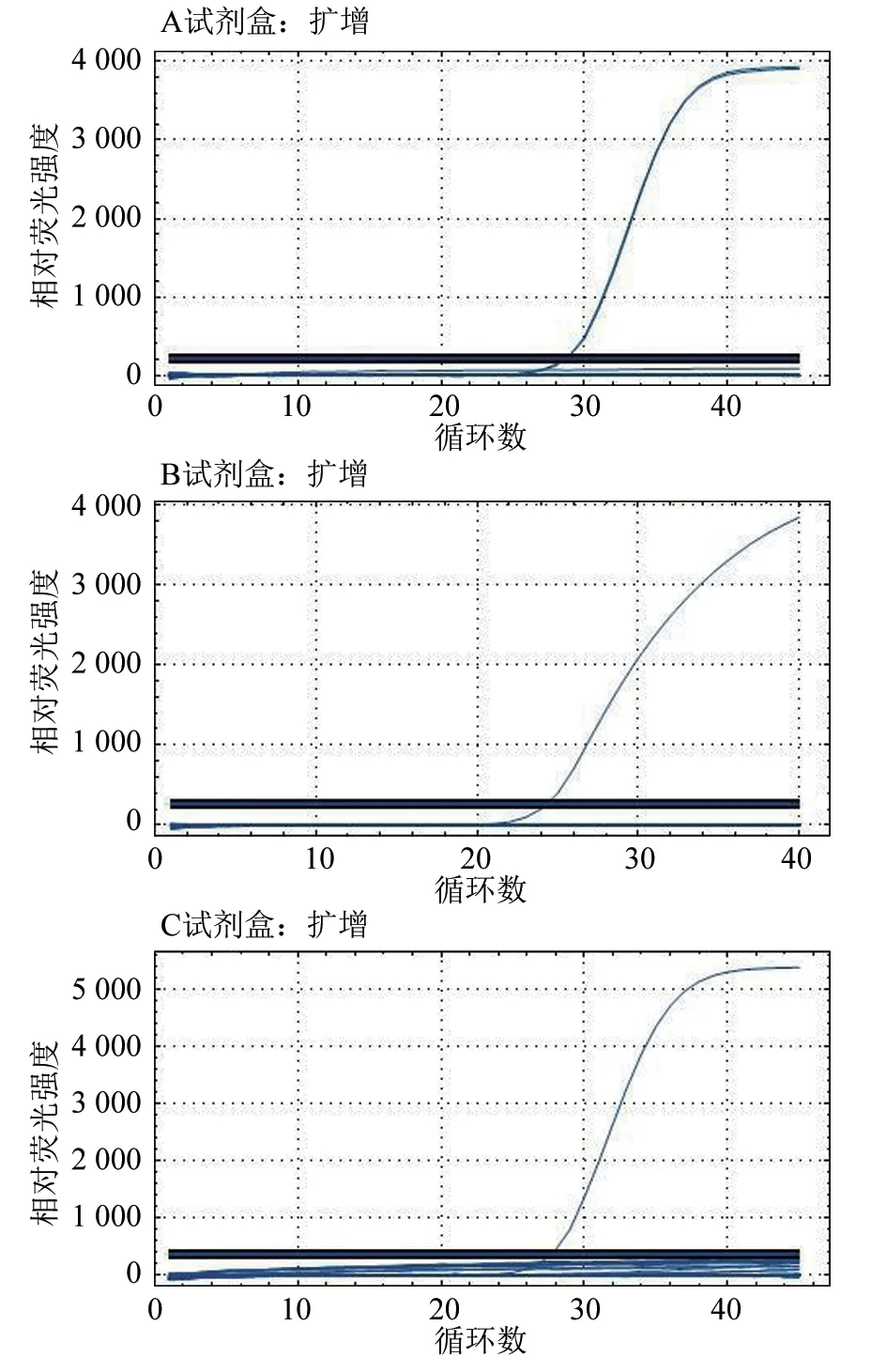
图2 3 个厂家ASFV 荧光PCR 试剂盒特异性检测结果
2.2 核酸提取试剂盒测评
选用B 厂家试剂对两个稀释梯度(105和104copies/µL)的标准物质进行核酸提取试剂测评。结果(表3)显示:手工柱式核酸提取和核酸提取工作站磁珠提取法检测的Ct 值相近,105copies/µL标准物质的Ct 值均在21.00 以上,104copies/µL 的Ct 值均在24.00 以上,两种提取方法在ASFV 扩增结果中Ct 值无统计学差异(P>0.1),试剂盒重复性较好,批内变异系数可控制在1.5%以内。

表3 不同核酸提取方法提取效率比较结果
3 讨论
自1921 年ASFV 在肯尼亚被首次报道以来,其影响范围遍布非洲、西欧、拉丁美洲等地区以及西班牙、意大利等国家,并逐步从欧洲扩散蔓延至亚洲。据报道[4],2022 年泰国、韩国、德国以及印度均有ASF 阳性病例。2018 年以后,我国一直将ASFV 检测作为猪场管理和常态化监测的重要项目。
荧光PCR 技术作为尽早发现和确诊ASF 的重要技术手段,在当前疫病防控中发挥着重要作用。随着检测技术发展,ASFV 荧光PCR 检测试剂盒和核酸提取试剂也出现了换代更新,且不同厂家的检测/提取试剂也各有优缺点。因此对荧光PCR试剂盒和核酸提取试剂盒的性能评价就显得尤为重要。标准物质/标准样品,是一种能够作为参照对象的特定、均匀、稳定且浓度/病毒含量已知的质量控制品,在仪器设备的校准、能力验证以及期间核查等项目中广泛应用。许秀琼等[5]将ASFV 核酸标准物质对不同厂家的ASFV 荧光PCR 检测试剂盒进行了比对分析;马龙等[6]也使用ASFV 病毒标准物质,评价了市面上5 种主流品牌的ASFV荧光定量PCR 试剂盒的检测性能;黄维等[7]通过ASFV 荧光PCR 试剂盒对常用的核酸提取方式进行了比较。上述均证明了标准物质在试剂盒比对中的可靠性,因此本试验应用ASFV 标准物质对3 个厂家的ASFV 荧光PCR 试剂盒和两种不同核酸提取试剂进行比较评估。ASFV 荧光PCR 试剂盒综合性能评定中,B 试剂盒R2为0.996,表现最佳,A、C 试剂盒均为0.985。试剂评定中R2大于0.985 即为优秀,证明3 个厂家试剂盒的R2均较为理想。
研究[8]显示,荧光PCR 检测方法检出下限为6 个质粒拷贝或0.1~1.0 TCID50/mL,是实现病毒精准剔除的最佳方法。并且,诊断试剂的敏感性越高,检测患病动物的阳性结果概率越高,而假阴性结果随之越少[9]。3 个厂家ASFV 荧光PCR 试剂盒的LOD 介于10-1~10-2copies/µL,且均出现Ct 值和扩增曲线,说明3 种试剂盒检测灵敏度均可满足日常监测需求。其中,A 试剂盒反应循环数在3 个厂家中最多且反应时间最长,LOD 为10-2copies/µL,灵敏度最高,推断A 试剂更适用于临床含毒量低的样品检测。特异性检测中,3 个厂家试剂盒均未出现非特异性扩增曲线和Ct 值,证明3 种试剂盒均具备良好的ASFV 检测特异性。核酸提取试剂盒测试结果显示,工作站磁珠法和手提柱式核酸提取法均可满足提取病毒核酸的需求,两核酸提取试剂盒的Ct 值重复性较好,批内变异系数可控制在1.5%以内。手提试剂盒价格较低,但随着样品数量增多提取时间延长,加溶液过程中易出现样品间的交叉污染;全自动核酸提取工作站提取试剂为预分装、提取时间固定、操作简便,但价格较手工提取试剂略显昂贵。
本试验利用ASFV 标准物质评价了3 种ASFV荧光PCR 检测试剂盒和两种核酸提取方法,各检测实验室在实际工作中也应在保证试剂盒重复性的前提下,根据试剂盒的检测时长、模板需求、检测敏感性、提取方式以及经济效益等因素灵活选择适配试剂。因局限于样品的单一性,本试验未选用临床不同感染阶段的动物或不同感染部位的样品用于测试,在今后的研究中也将聚焦于多种临床样品的收集和测试,并扩大试剂盒的选用范围,进一步完善检测试剂的比对方法并积累相关数据。

