主动脉夹层合并低氧血症危险因素的Meta分析
罗天会,向玉萍,赵 琴,曾 玲,曹 舸
1四川大学华西医院重症医学科胸心血管ICU/华西护理学院,四川 成都 610041
2四川大学华西医院心脏大血管外科,四川 成都 610041
主动脉夹层(aortic dissection,AD)是一种严重危及患者生命的心血管疾病,中国的患病率为(5~10)/10万[1]。AD起病急、进展快、病死率高,常导致患者严重的全身病理生理改变,其中低氧血症较为常见。研究显示,AD患者术前低氧血症发生率为20.50%~60.97%[2-3],由于肺泡上皮和毛细血管内皮细胞受损,低氧血症患者氧合指数≤300 mmHg(1 mmHg=0.133 kPa)[4]。研究表明,术前氧合指数≤300 mmHg是术后发生低氧血症的独立危险因素[5-7],同时,术前严重的低氧血症可能会导致术后出现严重的肺损伤,并延长术后机械通气时间,增加患者死亡风险[8],因此,积极防治AD低氧血症的具有重要意义。近年来,众多学者围绕AD合并低氧血症的危险因素进行了研究,但各研究纳入因素不一致,部分结果之间存在差异。本研究旨在全面检索AD合并低氧血症危险因素的相关文献进行Meta分析,探讨其独立危险因素,早期识别低氧血症,从而采取预防措施,改善患者预后。
1 资料与方法
1.1 文献检索
采用主题词与自由词相结合的检索策略,并追溯已纳入文献的参考文献。检索数据库包括PubMed、Embase、CENTRAL、Web of Science、中国知网、万方数据库、维普中文科技期刊数据库、中国生物医学文献数据库,检索时间为建库至2021年12月。中文检索词为“主动脉夹层”“低氧血症”“缺氧”“急性肺损伤”“急性呼吸窘迫综合征”“危险因素”“预测因子”“影响因素”“相关因素”“预测因素”“相关性”。英文检索词为“aortic dissection”“hypoxemia”“anoxia”“anoxemia”“hy poxia”“oxygen deficienc*”“acute lung injury”“acute respiratory distress syndrome”“risk factors”“risk factor”“risk*”“predictor”“predictive factor”“influence factor”“correlat*”。
1.2 纳入与排除标准
纳入标准:(1)研究类型为队列研究及病例对照研究;(2)研究对象为AD合并低氧血症,年龄≥18岁;(3)结局指标:AD合并低氧血症,低氧血症诊断标准为氧合指数≤300 mmHg[9];(4)3项及以上研究报道的暴露因素,各暴露因素定义基本相同。排除标准:(1)重复发表文献;(2)无AD合并低氧血症的独立危险因素;(3)非中、英文文献。
1.3 资料提取及质量评价
检索文献导入Endnote X7,由两名研究者严格按照纳入与排除标准独立筛选文献、提取资料并进行质量评价,如遇分歧,由两名研究者协商或由第三名研究者判断。提取资料包括题目、第一作者、发表年份,患者年龄、性别、总病例数、低氧血症组病例数、非低氧血症组病例数、AD诊断标准、低氧血症诊断标准、文献质量评价的关键要素、AD合并低氧血症危险因素中多因素分析的比值比(odds ratio,OR)及其95%CI。文献质量评价由两名研究者采用纽卡斯尔-渥太华量表(Newcastle-Ottawascale,NOS)进行评分,总分为9分,其中5~9分为高质量研究。
1.4 统计学方法
应用RevMan 5.3软件进行Meta分析,提取AD合并低氧血症独立危险因素的OR及其95%CI,采用倒方差法对OR进行合并。纳入文献异质性检验采用Q检验与I2检验,若I2≤50%,P>0.1,纳入研究无明显异质性,采用固定效应模型进行Meta分析;若I2>50%,P≤0.1,纳入研究存在异质性,采用随机效应模型进行Meta分析。
2 结果
2.1 文献检索及筛选结果
根据检索策略共检索出AD术前低氧血症危险因素相关文献509篇,根据纳入与排除标准最终纳入17篇文献[2-3,10-24]。文献筛选流程见图1。
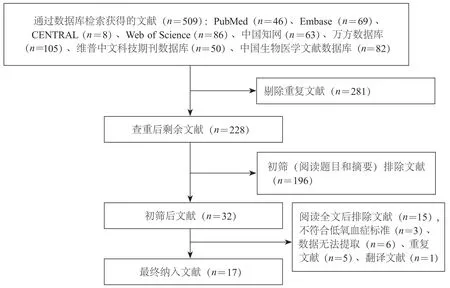
图1 文献筛选流程
2.2 文献基本信息及质量评价
17篇文献中,共纳入3452例AD患者,其中低氧血症患者1439例,AD术前低氧血症发生率为20.50%~60.97%,共纳入23个独立危险因素(表1)。17篇均为高质量研究,其中4篇文献质量评估均为满分9分(表2)。
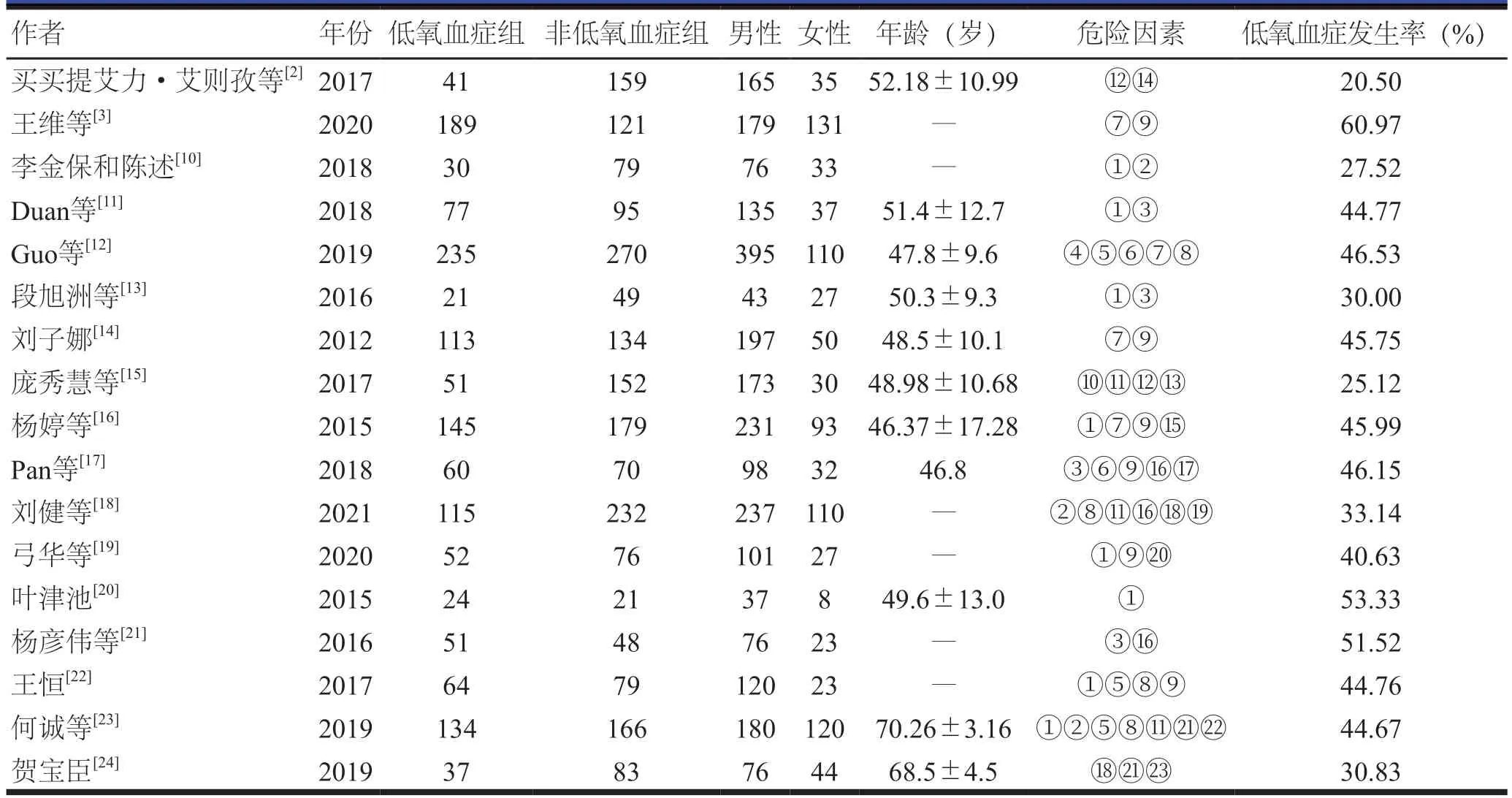
表1 纳入文献的基本信息
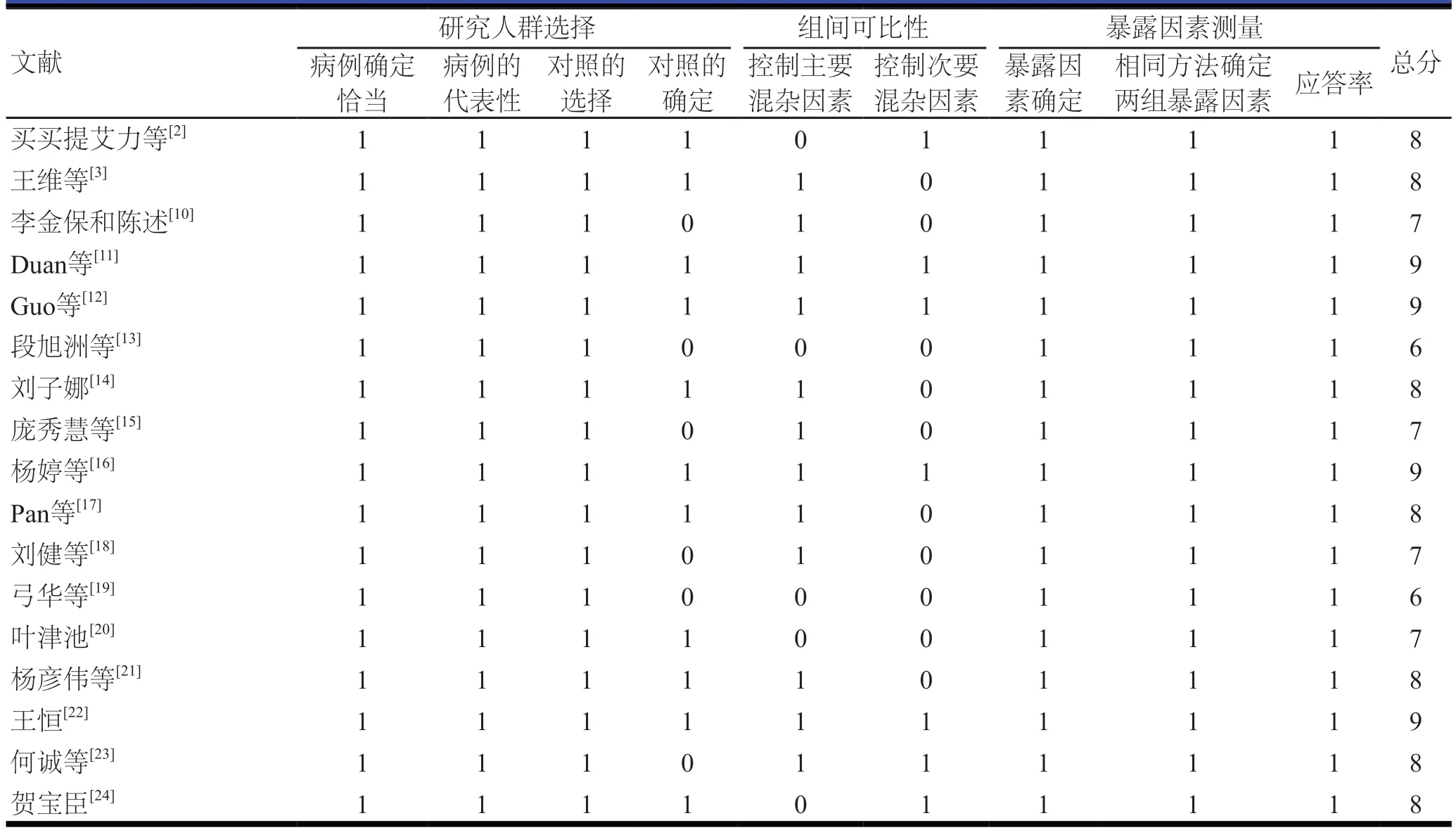
表2 纳入文献的NOS评分
2.3 Meta分析结果
2.3.1 年龄与体重指数
3篇文献[17-18,21]研究了年龄,6篇文献[3,14,16-17,19,22]研究了体重指数,经异质性检验,纳入文献存在异质性(I2=62%,P=0.01;I2=89%,P<0.01),故采用随机效应模型进行Meta分析。Meta分析结果显示,年龄(OR=1.13,95%CI:1.03~1.24,P=0.01)、体重指数(OR=1.49,95%CI:1.23~1.81),P<0.01)均是AD术前发生低氧血症的独立危险因素。(图2、图3)

图2 年龄与AD合并低氧血症发生风险的森林图
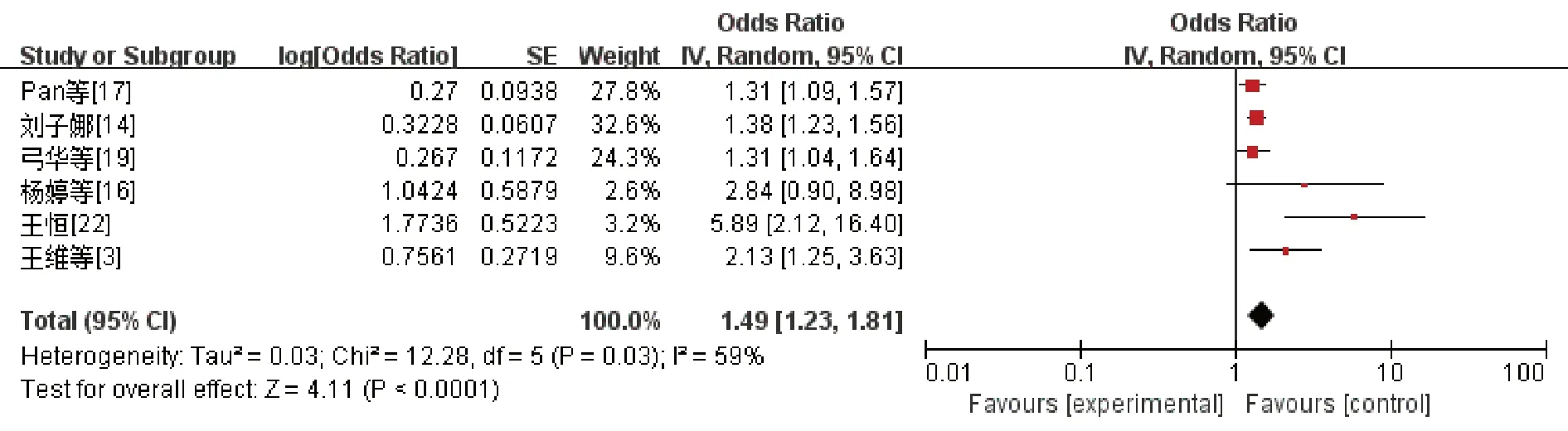
图3 体重指数与AD合并低氧血症发生风险的森林图
2.3.2 术前实验室指标
术前实验室指标中,3篇文献[12,22-23]研究了白细胞计数、8篇文献[10-11,13,16,19-20,22-23]研究了C-反应蛋白、4篇文献[11,13,17,21]研究了白细胞介素-6、3篇文献[10,18,23]研究了D-二聚体。经异质性检验,白细胞介素-6的文献无明显异质性(I2=0%,P=0.70),故采用固定效应模型进行Meta分析;白细胞计数(I2=94%,P<0.01)、C-反应蛋白(I2=82%,P=0.001)、D-二聚体(I2=71%,P=0.003)的文献均存在异质性,故采用随机效应模型进行Meta分析。Meta分析结果显示,白细胞介素-6(OR=1.03,95%CI:1.02~1.04,P<0.01)、D-二 聚 体(OR=2.69,95%CI:1.41~5.15,P=0.003)、C-反应蛋白(OR=1.18,95%CI:1.07~1.30,P=0.001)均是AD合并低氧血症的独立危险因素,白细胞计数(OR=3.98,95%CI:0.82~19.29,P=0.09)与AD术前低氧血症无关。(图4~图7)

图4 白细胞介素-6与AD合并低氧血症发生风险的森林图

图7 白细胞计数与AD合并低氧血症发生风险的森林图
2.3.3 术前合并症

图5 D-二聚体与AD合并低氧血症发生风险的森林图
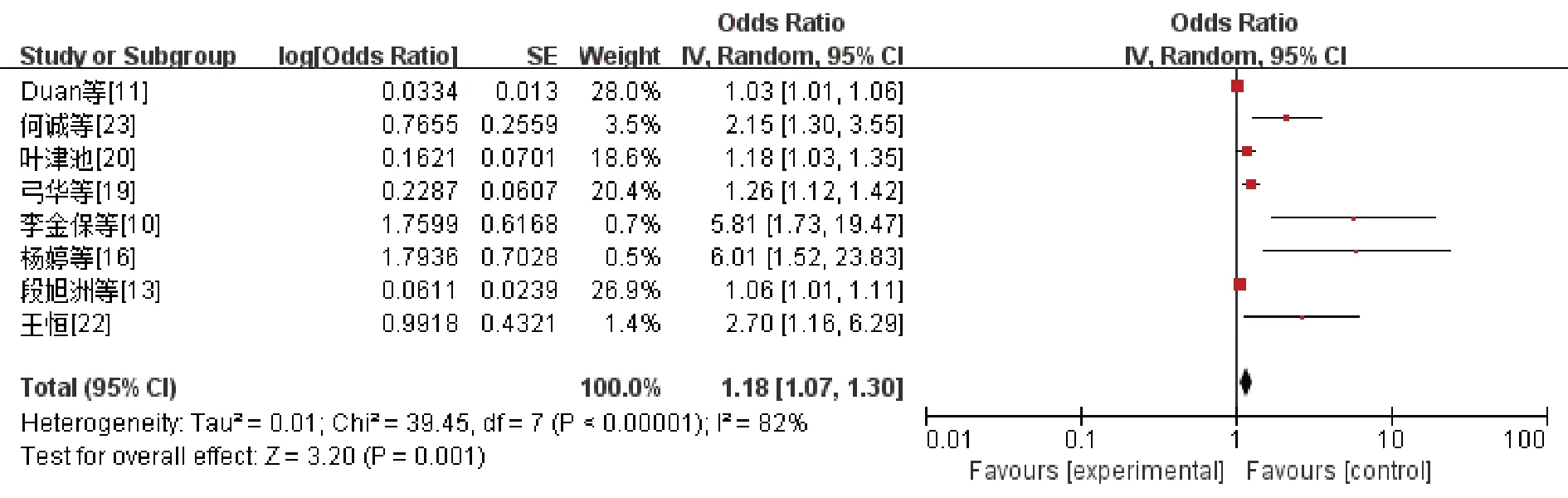
图6 C-反应蛋白与AD合并低氧血症发生风险的森林图
术前合并症中,4篇文献[3,12,14,16]研究了吸烟史、3篇文献[15,18,23]研究了夹层累及范围、4篇文献[12,18,22-23]研究了胸腔积液,经异质性检验,吸烟史(I2=40%,P=0.17)、胸腔积液(I2=0%,P=0.56)的文献间无明显异质性,故采用固定效应模型进行Meta分析;夹层累及范围(I2=82%,P=0.001)的文献间存在异质性,故采用随机效应模型进行Meta分析。Meta分析结果显示,吸烟史(OR=2.13,95%CI:1.61~2.82,P<0.01)、合并胸腔积液(OR=2.59,95%CI:1.98~3.39,P<0.01)、术前夹层累及范围(OR=2.92,95%CI:1.22~6.96,P=0.02)均是AD术前低氧血症的独立危险因素。(图8~图10)
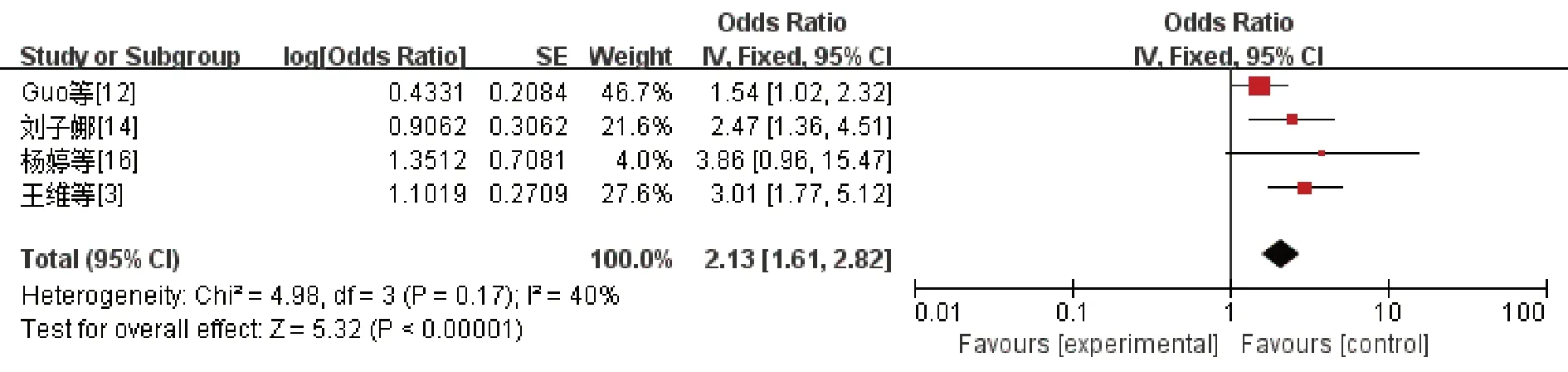
图8 吸烟史与AD合并低氧血症发生风险的森林图
2.3.4 发表偏倚分析
纳入的17篇文献中,5篇及以上文献报道的影响因素为体重指数、C-反应蛋白,对其绘制漏斗图分析有无发表偏倚。漏斗图分析结果显示,两侧均呈散在不对称点,存在发表偏倚,可能与纳入文献多为中文文献有关。(图11、图12)
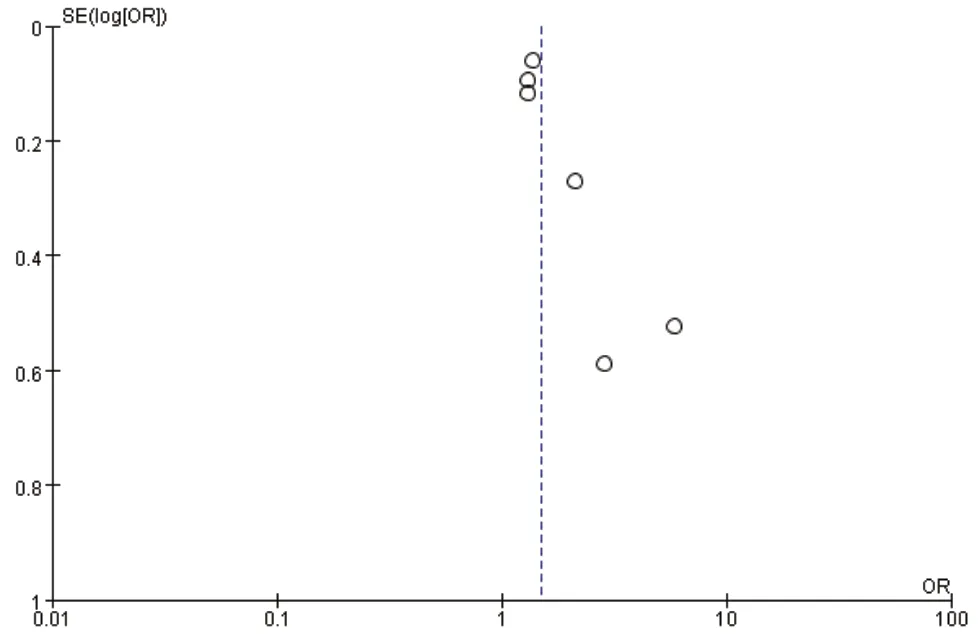
图11 体重指数的发表偏倚检验漏斗图
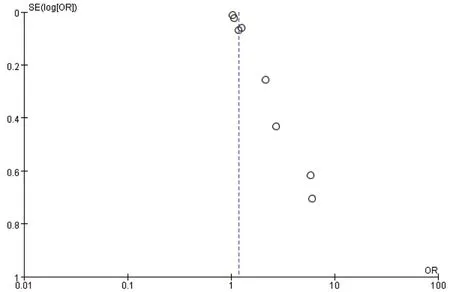
图12 C-反应蛋白的发表偏倚检验漏斗图
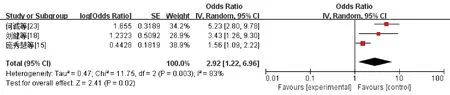
图9 夹层累及范围与AD合并低氧血症发生风险的森林图
3 讨论
本研究共纳入17篇文献,纳入研究均明确诊断AD或低氧血症。AD合并低氧血症危险因素涉及患者年龄、体重指数等一般资料,合并症及实验室检查的炎症指标,文献均考虑了主要因素,说明研究结果具有一定的可靠性。17篇文献中,共纳入3452例AD患者,其中低氧血症患者1439例,Meta分析结果显示,体重指数、年龄、C-反应蛋白、白细胞介素-6、吸烟史、夹层累及肠系膜上动脉、合并胸腔积液均是AD合并低氧血症的独立危险因素。
随着年龄增加,AD合并低氧血症患者的呼吸功能逐渐下降,更易并发低氧血症。体重指数对AD合并低氧血症的影响可能与肥胖患者的肺力学可发生改变及炎症因子过度产生有关[25]。吸烟患者更易发生慢性阻塞性肺疾病、哮喘、小气道功能异常,增加呼吸道感染、肺结核、间质性肺病的发病风险等[26],从而增加低氧血症发生风险。实验室指标中,术前高水平C-反应蛋白、白细胞介素-6均是机体炎症反应的指标,AD患者可能发生中膜撕裂和假腔形成,使血液聚集导致机体炎症系统激活[27]。纤维蛋白溶解系统激活形成的微栓子阻塞肺毛细血管,影响肺通气,因此,D-二聚体升高导致进一步的急性肺损伤[28]。AD患者肠系膜上动脉受累时,肠壁缺血水肿,诱发大量炎症因子释放入血,增加急性肺损伤的发生率;术前胸腔积液会导致患者肺扩张受限,导致肺顺应性下降,肺部因素导致肺毛细血管内皮水肿、异常通气-灌注比、肺内分流和肺气体交换减少,从而加重低氧血症的发生。
本研究的局限性:(1)大部分纳入文献为A型AD,仅小部分文献为B型AD,受纳入研究样本量限制,未进行亚组分析;(2)本研究总纳入患者病例数有限,且均为单中心研究,今后可开展大样本、多中心研究;(3)纳入文献中各个暴露因素差异较大,且结果之间差异较大,导致部分合并结果异质性较大。鉴于研究存在的局限性,本研究结果尚需进一步验证。今后可进一步纳入尽可能相关的主要、次要因素,开展前瞻性、大样本、多中心研究。
综上所述,体重指数、年龄、C-反应蛋白、白细胞介素-6、术前吸烟史、术前夹层累及肠系膜上动脉、合并胸腔积液均是AD合并低氧血症的独立危险因素,可用于高危患者的识别,为临床治疗提供指导。

