胶体金免疫层析法检测带鱼中氯霉素残留的前处理方法研究
◎ 李 倩,陈 煜,阎安婷
(山西省检验检测中心药品检验技术研究所,山西 太原 030001)
带鱼,自古以来就是我国重要的海洋作物之一,在《本草从新》《中华本草》等著作中均有记载。带鱼蛋白含量高,味道鲜美,具有补中益气、温胃养肝、补气血的作用[1]。
氯霉素为广谱抗生素,价格低,疗效显著,多用于动物的抗菌治疗预防。氯霉素理化性质稳定,不容易分解,会在人体中蓄积,从而引发血液系统疾病及抗药性。我国已明确规定禁止氯霉素在食品动物中使用[2]。氯霉素残留现有检测方法有高效液相色谱法、气相色谱法、酶联免疫法等[3-4],但这些方法前处理复杂,需要大型检测设备。胶体金免疫层析法操作简便快速,又具有很好的特异性,无需昂贵的检测仪器[5-7]。本实验通过优化前处理方法,建立以胶体金免疫层析技术为基础的带鱼中氯霉素残留快速检测方法,该方法的建立为其他动物药物残留的快速检测提供有利的技术支持,对于今后开展基层食品药品检验检测工作也具有非常重要的意义。
1 材料与方法
1.1 材料与设备
带鱼购自太原美特好超市;固相萃取小柱(Cleanert Silica,200 mg/6 mL,LOT:0170198);氯 霉 素 快速检测卡(苏州快捷康生物技术有限公司,批号:kjk20171125c)。氯霉素,购于Dr. Ehrenstorfer,CAS登录号为56-75-7;乙酸乙酯、水、正己烷、丙酮、乙腈、磷酸二氢钠(NaH2PO4·2H2O)、磷酸氢二钠(Na2HPO4·12H2O)及氯化钠均为分析纯。
Eppendorf移液器、中佳HC-3018高速离心机、IKA V2S025涡旋混合器及梅特勒-托利多ML204T电子天平。
1.2 方法
1.2.1 对照品溶液的制备
称取氯霉素用乙腈稀释至刻度,摇匀,制成浓度为0.01 μg·mL-1的氯霉素标准工作液。临用新配。
1.2.2 前处理方法研究
取粉碎均匀的带鱼样品6 g于50 mL具塞离心管中,分别采用以下4种方法进行样品前处理。
方法一:加入8 mL乙酸乙酯,涡旋提取5 min,以8 000 r·min-1离心5 min,转移全部乙酸乙酯层 40 ℃氮气吹干,置于15 mL具塞离心管中,精密加入600 µL复溶液,涡旋混合1 min,作为待测液。
方法二:依次加入4 mL水和8 mL乙酸乙酯,提取同方法一。精密加入600 µL复溶液和600 µL正己烷,涡旋混合1 min,取下层溶液作为待测液。
方法三:依次加入15 mL乙腈匀浆提取,加入 10 mL乙腈饱和的正己烷去脂,离心分层,取乙腈层用氮气吹干,加入5 mL丙酮-正己烷(1∶9)溶解残渣待净化。过LC-Si硅胶小柱,用5 mL丙酮-正己烷(6∶4)洗脱,收集洗脱液用氮气吹干,复溶为待测液。
方法四:依次加入4 mL水和8 mL乙酸乙酯,涡旋提取5 min,以4 000 r·min-1离心5 min。转移乙酸乙酯层于50 mL具塞离心管中,加入正己烷25 mL,氯化钠1 g涡旋混匀,4 000 r·min-1离心1 min,上清液待净化。净化同方法三,复溶为待测液。
1.2.3 复溶液的确定
通过查阅资料并结合试剂盒复溶液的pH值范围选择最常用的4种磷酸盐缓冲液。
称取0.12 g磷酸二氢钠置于100 mL容量瓶中,用水溶解并稀释至刻度,制成溶液A;称取7.16 g磷酸氢二钠置于100 mL容量瓶中,用水溶解并稀释至刻度,制成溶液B。①取溶液A 3.3 mL、溶液B 6.7 mL、 氯化钠0.85 g,用水溶解并稀释至100 mL,得磷酸盐缓冲液1(pH 7.1)。②取溶液A 2.8 mL、溶液 B 7.2 mL、氯化钠0.85 g,用水溶解并稀释至100 mL,得磷酸盐缓冲液2(pH 7.2)。③取溶液A 2.3 mL、溶液B 7.7 mL、氯化钠0.85 g,用水溶解并稀释至100 mL,得磷酸盐缓冲液3(pH 7.3)。④取溶液A 1.9 mL、溶液B 8.1 mL、氯化钠0.85 g,用水溶解并稀释至100 mL,得磷酸盐缓冲液4(pH 7.4)。
1.2.4 测定步骤
吸取150 µL样品待测液滴加到检测卡上的加样孔中,室温温育5 min,通过比较控制线、检测线的颜色深浅对结果进行判定。
1.2.5 测定条件研究
本方法的结果测定以竞争性免疫层析为基础,具有特异、灵敏、快速以及操作简便等优点,但其对反应条件及环境往往具有严格的要求,本方法除了对反应体系进行优化,还对测定时间和温育温度进行研究。测定时间分别考察了复溶后0 min、5 min、10 min、20 min、30 min和60 min测定效果,温育温度对比了18 ℃、25 ℃、30 ℃、35 ℃和40 ℃下的反应效果。
1.2.6 交叉反应
分别取甲砜霉素、氟甲砜霉素,制成水平为 10 ng·mL-1的标准溶液,按照本方法进行实验,考察试剂盒与上述化合物的交叉反应。
1.2.7 与参比方法一致性分析
称取空白样品带鱼为基质,分别添加3个浓度水平0 μg·kg-1、0.1 μg·kg-1、0.2 μg·kg-1的盲样各40份,其中20份按自拟方法的前处理和分析步骤进行测定,另外20份参考《动物源性食品中氯霉素类药物残留量测定》(GB/T 22338—2008)测定,对比两种方法测定结果的一致性。
2 结果与分析
2.1 前处理方法及复溶液确定
2.1.1 对前处理方法进行考察
对比4种前处理方法发现,方法一样品加乙酸乙酯后,样品凝结成块,提取过程中不能均匀分散,提取不完全,待测溶液浑浊不清,无法点样;方法二加入水后样品结块问题解决,但加入的正己烷量太少,无法完全去脂,待测溶液依旧浑浊不清;方法三虽然待测溶液可以达到满意的结果,也消除了脂肪对检测结果的干扰,但乙腈氮吹耗时过长,无法满足快检要求,需进一步优化,缩短检测时间;方法四试验样品中添加25 mL正己烷后,待测溶液清晰,点样结果满意,同时乙酸乙酯氮吹时间缩短,单样时间控制在 60 min之内。因此,采取方法四为本试验最终方法。
2.1.2 对复溶液进行考察
如图1所示,磷酸盐缓冲液2(pH 7.2)厂家试剂盒能达到较好的点板效果。
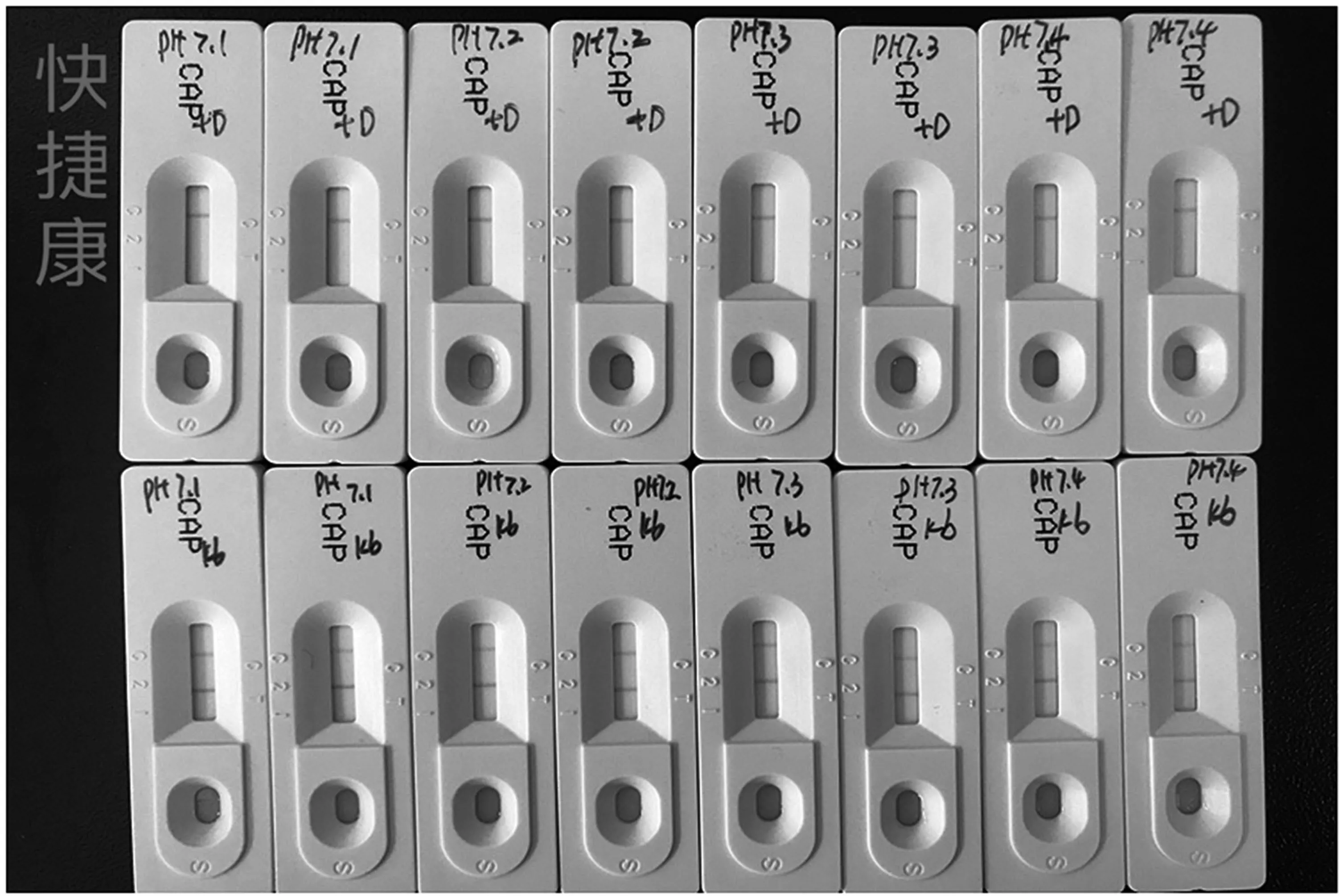
图1 测试结果图
2.2 测定条件研究结果
结果表明,在1.2.5各不同时间段下,待测液点板后T线颜色没有明显差异,时间的延长对本实验的测定结果没有影响,但是为了避免不确定因素对实验的影响,建议复溶后立即测定。在1.2.5各温度下,待测液点板后无明显差异,温度对本试验的测定结果几乎没有影响,但是为了避免极端监测环境对于检测相关各个环节的影响,建议日常检验中在室内或相对温和的检验环境中进行,故本方法中孵育温度建议为室温。
2.3 交叉反应结果
交叉反应显示,甲砜霉素、氟甲砜霉素与试剂盒点板后结果均显示阴性,表明均无交叉反应。
2.4 与国标方法对比结果
表1、表2的检测结果表明,胶体金方法中0 μg·kg-1均未检出为阴性,0.1 μg·kg-1、0.2 μg·kg-1均可以检出为阳性。液相色谱-质谱法中0 μg·kg-1检出浓度为 0 μg·kg-1视为阴性,0.1 μg·kg-1、0.2 μg·kg-1均可以检出符合回收率要求(80%~110%)的浓度视为阳性,因此胶体金试剂盒方法的结果均与参比方法一致,符合方法一致性要求。

表1 胶体金免疫层析法检测结果表
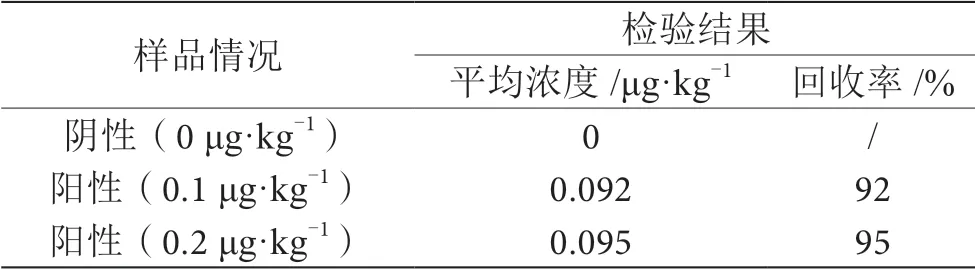
表2 液相色谱-质谱法检测结果表
3 结论
通过优化前处理方法、确定复溶液等操作建立的胶体金免疫层析技术相比于传统气相色谱、液相色谱、酶联免疫方法,具有操作简单快速、特异性强、耗时短、无需大型仪器成本低的特点,非常适合作为初筛手段用于基层现场检测。

