锂硫电池隔膜在不同抑制“穿梭效应”策略中的研究进展
马 康,高志浩,骆 林,宋 鑫,戴作强,何 田,张健敏
(1青岛大学材料科学与工程学院;2青岛大学机电工程学院;3青岛大学动力集成及储能系统工程技术中心,山东 青岛 266071)
日益严重的全球能源危机推动了先进储能技术的发展,虽然目前在储能系统领域主要应用的是锂离子电池,但是随着其实际能量密度逐渐接近理论可达到的极限值,已经难以满足消费者对电池提出的高能量、高功率的性能要求,所以目前迫切需要开发出一种能够取代锂离子电池的大容量电池[1-3]。锂硫(Li-S)电池因其较高的理论比容量(1675 mAh/g)和质量能量密度(2600 Wh/kg)、原料成本低廉、无环境污染而且易于回收再利用等众多优势而受到广泛关注,被认为是一种极具发展前景的储能电池[4-5]。
然而,在Li-S电池商业化发展的道路上遇到了一些必须解决的技术难题,比如穿梭效应、单质硫及放电产物的绝缘性、锂化时硫的体积变化等,而其中最为严重的当属溶解的多硫化物导致的“穿梭效应”。穿梭效应指的是可溶性的长链多硫化物扩散到负极,在负极附近被还原为不溶的Li2S2/Li2S和短链多硫化物,短链多硫化物在浓度差的作用下迁移回正极继续失电子氧化为长链多硫化物的循环过程,这是造成Li-S 电池容量衰减的主要原因[6]。一块完整的Li-S电池通常由正极、负极、隔膜和电解液四部分组成,隔膜处在电池的正负极之间,是多硫化物和锂离子迁移过程中的必经之路,但是传统的聚烯烃类隔膜由于其较大的孔径(50~600 nm),不能起到对多硫化物的物理阻挡作用,此外由于聚烯烃隔膜表面没有捕捉多硫化物的功能基团,无法实现对多硫化物的化学吸附,导致Li-S电池的放电比容量和库仑效率衰减过快,其高容量的优越性无法得到实现。所以有研究者通过对传统的聚烯烃类隔膜进行功能化设计和改性,如优化孔隙结构使隔膜更好地发挥其物理屏障作用、引入静电排斥作用来增强锂离子的传输、掺杂过渡金属元素提高对多硫化物的化学吸附能力以及活性物质的氧化还原速率均可改善Li-S电池的整体性能,从而推动其商业化进程[7-9]。
本工作的主要思路是根据功能性涂层是否通过化学键来固定多硫化物,将抑制多硫化物的策略分为物理限制和化学限制两种,如图1所示。物理限制一方面是根据静电排斥原理,将多硫化物留在阴极附近;另一方面由于Li+与Sx2-具有不同的孔径尺寸,通过在隔膜上引入具有尺寸筛分功能或阻挡作用的修饰材料有效抑制多硫化物的穿梭。化学限制则是利用电子转移、交换与隔膜修饰层表面的原子(或分子)形成化学键,实现对多硫化物的化学吸附,达到抑制多硫化物穿梭的效果。
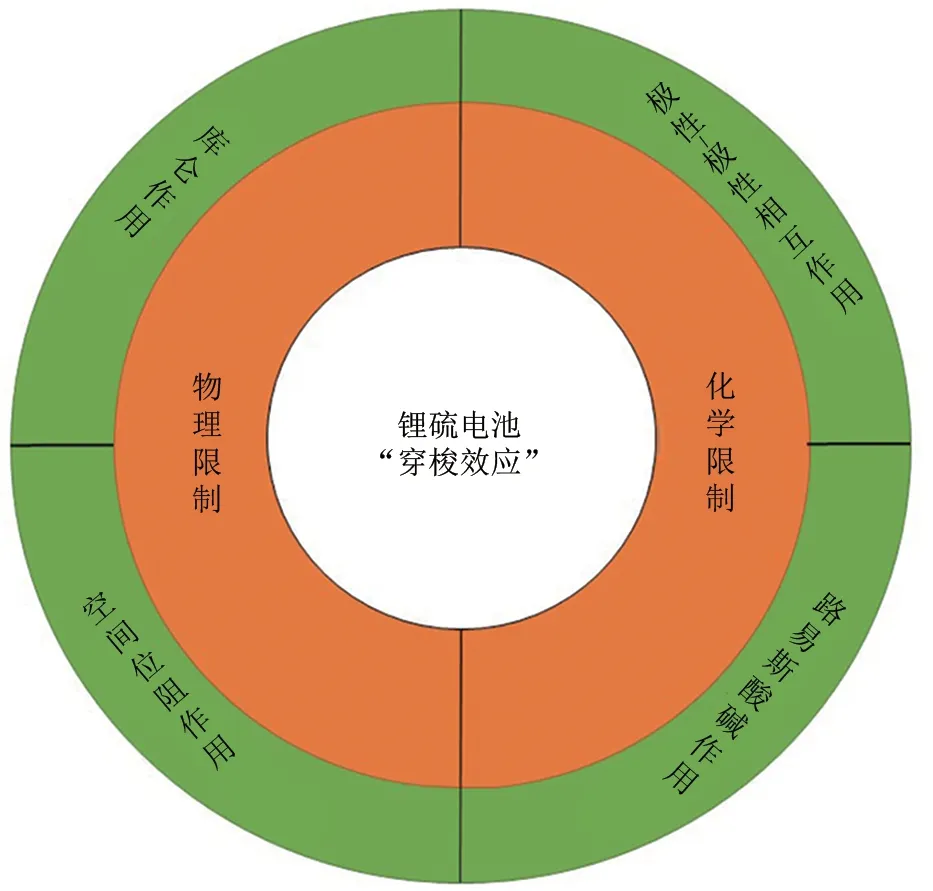
图1 抑制多硫化物扩散的方法Fig.1 Methods of limiting the diffusion of polysulfides
1 聚丙烯基改性隔膜
1.1 物理限制
1.1.1 库仑作用
鉴于多硫化物的带电特性,在靠近正极侧隔膜表面引入带负电基团的功能材料以构建选择透过性膜。通过库仑作用排斥多硫化物阴离子的同时促进Li+的传输,达到抑制多硫化物穿梭的效果。
Nafion 膜是一种具有离子特性的聚合物,由于其内部含有丰富的亲水性磺酸基团,所以可以作为Li-S 电池隔膜的修饰层[10]。Huang 等[11]将Nafion 溶液涂覆在聚丙烯膜上,通过静电排斥作用将多硫化物留在正极附近。具有Nafion 功能隔膜的Li-S 电池,在1 C 的放电倍率下,500 个周期内表现出超低的平均容量衰减率(0.08%),低于聚丙烯膜(PP)的一半。由于Nafion本身的导电性较差,可能会降低电池的初始放电容量,所以Hao等[12]在隔膜正极侧涂覆Nafion和Super P的混合溶液,其中Nafion中的磺酸基团利用静电排斥作用以阻止多硫化物,而Super P具有物理吸附性和导电性,同时充当上层辅助集流体重新激活捕获的多硫化物。将改性隔膜组装成Li-S 电池,在0.5 C 下电池的初始放电比容量从552 mAh/g 提升至1087 mAh/g。Zhuang等[13]用异丙醇和去离子水按6∶4的体积比制备稀释剂稀释氧化石墨烯(GO)和Nafion,通过真空抽滤的方法将GO、Nafion 沉积在PP 膜上,形成由Nafion、GO、PP 组成的三元层状隔膜,如图2 所示,超薄的GO层堵塞了PP基质的大孔,并且离子选择性Nafion 涂层进一步抑制了多硫化物的穿梭。具有三元层状隔膜的Li-S 电池在0.5 C 的放电倍率下,首圈的放电容量达到1057 mAh/g,循环200圈后,每周期的容量衰减率从0.34%降至0.18%。

图2 PP/GO/Nafion三元隔膜示意图[13]Fig.2 Schematic of a ternary PP/GO/Nafion separator[13]
Shi 等[14]制备了一种多壁碳纳米管/磺化聚苯胺(MWCNTs/SPANΙ)改性隔膜,在高载硫量(5 mg/cm2)的基础上,带有PP 隔膜的电池初始放电容量为1047 mAh/g 循环100 次后其容量仅为536 mAh/g,而具有MWCNTs/SPANΙ 改性隔膜的Li-S 电池初始放电容量高达1126 mAh/g,经过100 次循环后,仍能保持在913 mAh/g。这主要是因为磺化后的聚苯胺对Li+具有高度的渗透选择性,此外MWCNTs延长了多硫化物的扩散路径并为电子提供传输通道,所以使得Li-S电池的电化学性能得到大幅度提升。Zhou 等[15]将回收的硬纸板用作制备Li-S 电池隔膜涂层(CFs),利用CFs 表面丰富的羧基和苯酚基团,排斥多硫化物(图3)并重新分配Li+,在阻碍多硫化物穿梭的同时抑制锂枝晶的生长,使其同时应对了Li-S电池的两个主要挑战,推动了Li-S电池的商业化发展进程。Lei 等[16]通过共价键将木质素磺酸盐(SL)与还原氧化石墨烯(rGO)结合,制备了具有丰富负电荷的rGO@SL 复合材料,合成过程如图4所示,最后通过真空抽滤的方法将rGO@SL沉积在PP 表面。该隔膜在不影响锂离子传输的前提下,通过木质素磺酸盐侧链上的磺酸基团有效地抑制了多硫化物的扩散。经过rGO@SL 涂覆的隔膜组装的Li-S电池在2 C高倍率下,电池的初始放电容量高达707 mAh/g,在1000 次循环中电池的循环性能非常稳定,每次循环的平均衰减率仅为0.026%。He 等[17]在疏水界面的启发下,提出了一种新颖的“疏-多硫”界面,如图4 所示,具有二维性质的VOPO4通过形成V—S 键固定多硫化物,由于多硫化物的固有电负性,由VOPO4片层锚定的多硫化物演变成由库仑排斥衍生的多硫化物疏表面。将该隔膜组装成电池,在3 C 的高放电倍率下,循环2000 次之后,电池仍能提供578 mAh/g的放电容量,实现了0.012%的超低容量衰减率。
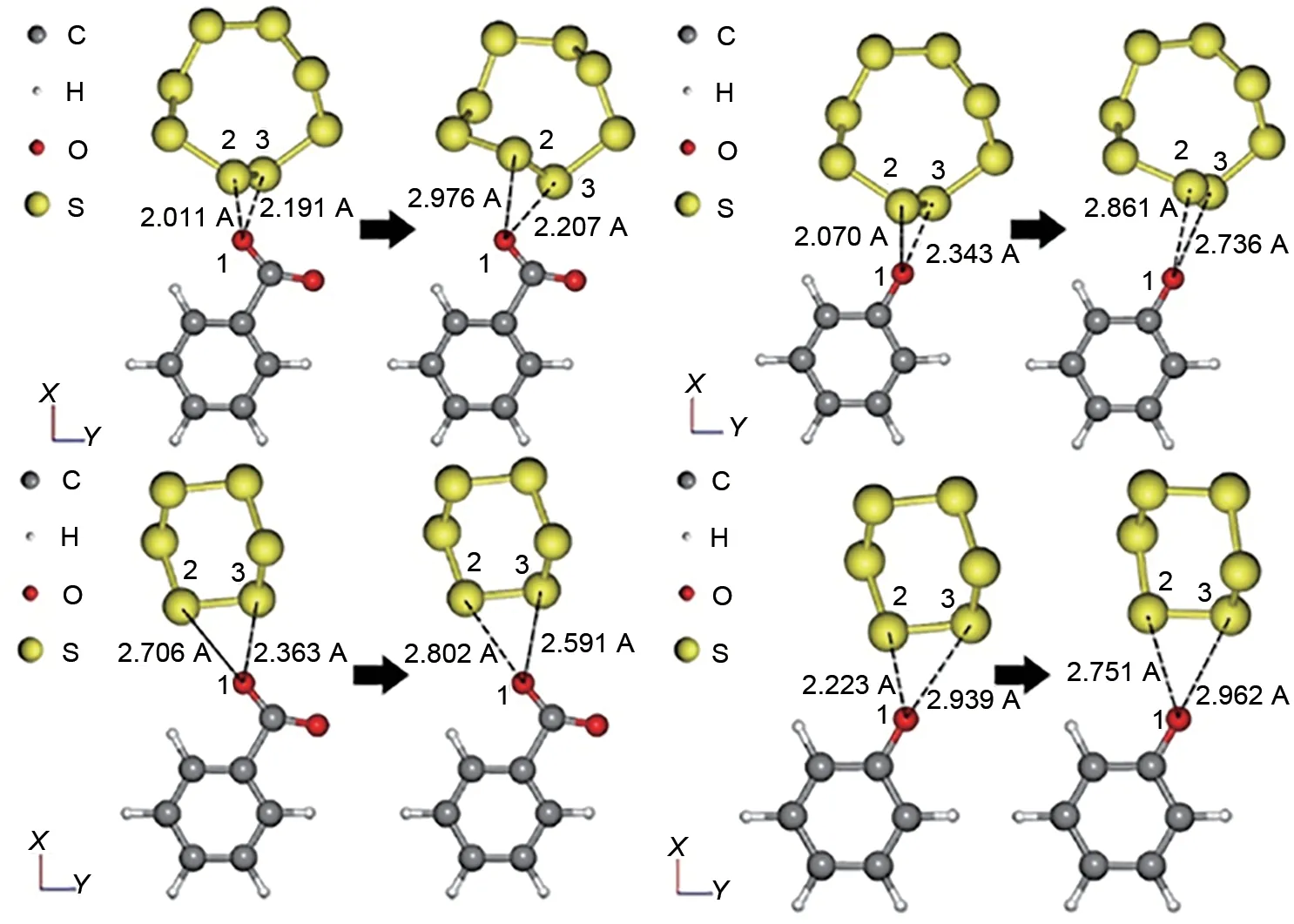
图3 DFT模拟羧基与苯酚基对S82-和S62-的相互作用[15]Fig.3 DFT simulates the interaction between carboxyl and phenol groups on S82-and S62-[15]
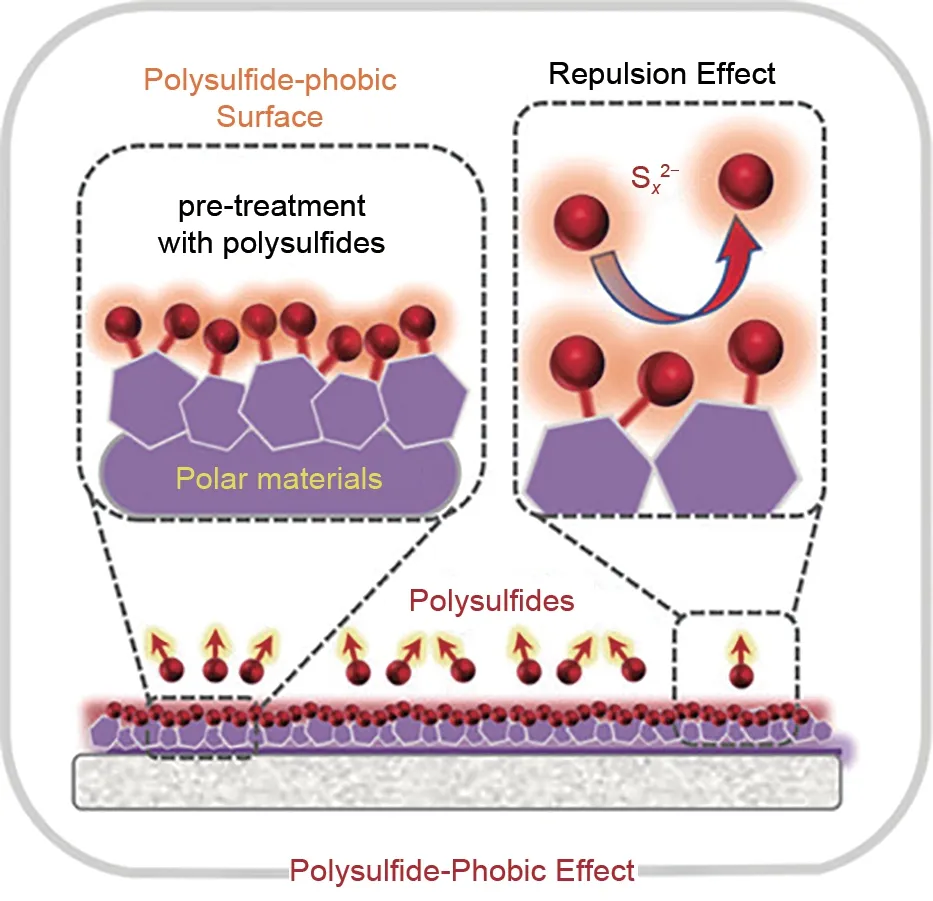
图4 将多硫化物锚定在极性材料上构建疏-多硫表面的示意图[16-17]Fig.4 Schematic illustrations of constructing a polysulfide-phobic surface by anchoring the polysulfides on the polar materials[16-17]
1.1.2 空间位阻作用
Li 等[18]通过模拟计算分析得出,多硫化物的尺寸大约为1.2~1.7 nm,如果隔膜的孔径小于多硫化物的尺寸,就能实现离子的选择性传输。但是传统的聚烯烃隔膜孔径较大(50~600 nm)很难抑制多硫化物的穿梭,所以在隔膜表面引入具有尺寸筛分或阻挡功能的修饰材料,通过物理限域作用抑制多硫化物的穿梭。零维[19]、一维[20-22]、二维[23]碳材料已经广泛地应用在Li-S电池隔膜修饰材料方面,例如,Balach等[19]应用介孔碳修饰隔膜,由于介孔碳材料具有理想的孔径(2~50 nm)、较高的比表面积和孔体积,所以对多硫化物扩散具有物理阻挡作用。相比于零维材料,一维和二维材料堆积形成的互联微米级孔道表现出更优异的物理阻挡作用。
一维碳纳米管(CNTs),由于具有高长径比的特性,不仅可以提供用于锚定多硫化物的高比表面积,还能提供连续的长程导电网络。Chung等[20]通过真空抽滤的方法将多壁碳纳米管(MWCNTs)沉积在PP隔膜表面,MWCNTs涂层作为上层集流体提高了电子的传输速度和高活性材料的利用率,其次长程有序的多孔导电网络拦截迁移的多硫化物,从而有效抑制多硫化物的扩散。Chung等[21]利用静电纺丝技术将聚丙烯腈(PAN)制成纳米纤维,碳化之后形成多孔的活性碳纳米纤维(ACNF),利用不同浓度的KOH调节纳米孔的大小和比表面积,最后通过真空抽滤均匀地将ACNF沉积在聚丙烯膜上,形成具有大量微孔结构的碳纳米纤维膜,其中质量分数为20%KOH活化的碳纳米纤维(ACNF-20)具有最高的微孔率。在使用这一隔膜后,Li-S电池在0.5 C的放电倍率下,电池的初始放电容量高达1270 mAh/g,200 次循环之后仍保留819 mAh/g 的高放电比容量,每周期的平均容量衰减率仅为0.13%。
石墨烯(Graphene)是一种二维蜂窝状碳材料,其优异的导电性(106S/cm)、极高的机械强度、超高的比表面积使之成为阻碍多硫化物穿梭的理想修饰材料[24]。Peng 等[23]通过化学气相沉积法在MgO模板上生长石墨烯层,然后去除模板得到介孔蜂窝状石墨烯框架(CGF),并利用真空抽滤法将CGF沉积在PP膜上,简称Janus隔膜,与普通PP隔膜相比Janus膜表面形成了横向尺寸为几微米的六边形CGF薄片,完全掩盖了PP表面的多孔结构,而且CGF具有100 S/cm的高导电性,3.1 cm3/g的大介孔体积,对重新激活捕捉的多硫化物以及提高硫的利用率具有积极作用。
一维材料与二维材料通过材料本身堆积形成的微米级孔道阻碍多硫化物的穿梭,所以材料的堆积方式直接影响其阻碍多硫化物的能力,例如:材料堆积形成的微米孔道可能在隔膜表面出现不连续的情况。因此需要开发一种具有连续网状结构的分子筛膜。
Bai 等[25]报道了一种具有离子筛作用的MOF/GO复合隔膜,其中Cu3(BTC)2型MOF材料孔径约为0.9 nm,小于多硫化物阴离子的直径,从而有效地抑制多硫化物的传输扩散。将具有离子筛特性的隔膜组装成电池后,Li-S 电池在1500 圈循环内的平均容量衰减率仅为0.019%,说明具有离子筛分功能的隔膜对抑制多硫化物的穿梭具有积极的作用。虽然具有微孔结构的材料有效地阻碍了多硫化物的穿梭,但是对锂离子的传输也会产生不利的影响,因此开发一种既能抑制多硫化物穿梭又能不影响锂离子传输的高孔隙率隔膜显得格外关键。
将利用物理限制策略的聚丙烯基改性隔膜电化学性能参数列于表1。

表1 物理限制聚丙烯基改性隔膜电化学性能Table 1 Electrochemical properties of polypropylene based modified separator with physical limitation
1.2 化学限制
虽然可溶性的多硫化物可以通过范德华力被吸附在碳材料表面,但多硫化物的穿梭仅在一定程度上被抑制。换句话说,相对较弱的物理相互作用无法从根本上消除多硫化物的扩散。化学限制是指修饰材料通过电子转移、交换或化学键作用固定多硫化锂,相比范德华力强很多,因此化学限制比物理限制表现出更强的吸附能力。根据多硫化锂与功能涂层的相互作用,进一步将化学限制分为两类:极性-极性相互作用和路易斯酸碱相互作用。
1.2.1 极性-极性相互作用
中间多硫化物本质上是极性的,非极性碳材料吸附多硫化物归因于范德华力,但其结合能非常小(0.1~0.7 ev)[26-28]。通过杂原子掺杂或引入极性物质对多孔碳材料进行修饰可以增强极性多硫化物与非极性碳骨架之间的弱相互作用,产生更多的活性位点从而达到抑制多硫化物的目的[29]。例如:在碳材料上掺杂N元素,形成石墨氮、吡咯氮、吡啶氮三种特殊结构。其中吡啶氮吸附多硫化物的能力最强,主要是由于吡啶氮上N的孤对电子不参与共轭,容易与多硫化物中的锂形成配位键,达到抑制多硫化物穿梭的作用,而与其他非金属元素(P、S、B)的共掺杂可进一步加强与多硫化物的结合能[30-31]。因此,探索碳涂层的极性表面,实现与多硫化物的强化学吸附是Li-S电池的关键步骤。
相比单原子掺杂,双掺杂策略可以为多硫化物提供更强大的锚定位点。Zeng 等[29]提出了利用葡萄糖、尿素和NH4H2PO4丰富的N、P 元素,经过1000 ℃碳化之后形成蜂巢状N、P 双掺杂碳,如图5所示,采用HNPC涂层隔膜的Li-S电池在0.2 C的放电倍率下显示出1387 mAh/g 的高初始放电比容量,循环200 次后电池容量保持在930 mAh/g,每次循环的平均容量衰减率仅为0.067%,而单原子N 掺杂(HNC)循环200 次后电池的放电比容量保持在817 mAh/g。具有HNPC涂层隔膜的Li-S电池表现出优异的循环稳定性归因于N 和P 双掺杂在隔膜表面形成强的N—Li 和P—S 键,能够在不牺牲锂离子扩散的情况下,实现对多硫化物的有效吸附。Li 等[32]利用富含N 官能团的小球藻作为生物质碳材料的前驱体,碳化后得到同时具有微孔和介孔复合结构的N、O共掺杂小球藻基生物质碳(CBBC)。采用改性隔膜组装的电池在0.5 C的放电倍率下,首次放电容量提高至1540 mAh/g,循环600 次后放电容量仍保持在656 mAh/g,每周期的平均容量衰减率仅为0.067%,验证了N、O 原子掺杂对多硫化物具有很强的化学吸附作用。

图5 在0.2 C下使用不同隔膜的Li-S电池的循环性能[29]Fig.5 Cycle performance of Li-S cells using different separators at 0.2 C[29]
单纯的N、O 等元素掺杂只能对多硫化物起到化学吸附作用,而过渡金属元素掺杂可以提高反应的动力学性能。例如,Liu 等[33]使用低成本和容易获得的葡萄糖和三聚氰胺作为原料,碳化之后形成氮掺杂分级多孔碳(N-HPC),按照类似的方法将四水合乙酸钴加入到N-HPC 中,合成具有碳纳米管(CNT)和分级多孔碳片(HPC)组成的氮钴掺杂碳结 构(CoN-CNT/HPC)。具 有CoN-CNT/HPC 涂 层的隔膜组装成电池在2 C 的高放电倍率下循环500 次,每循环的平均容量衰减率仅为0.04%。这种优异的性能除了CoN-CNT/HPC涂层的物理限制和化学吸附作用以外,恒电位成核实验的测试(图6)表明CoN-CNT/HPC 涂层可以促进Li2S 的快速沉积,提高反应动力学性能的同时进一步抑制了多硫化物的穿梭。

图6 Li2S6电解质中N-HPC和CoN-CNT/HPC对称电池的电化学测试:恒电位成核测试[33]Fig.6 Electrochemical testing of N-HPC and CoN-CNT/HPC symmetrical cells in Li2S6 electrolyte:Potentiostatic nucleation testing[33]
综上,常见的杂原子掺杂有硼(B)、氮(N)、氧(O)、磷(P)和硫(S)等。Hou等[34]利用密度泛函理论将不同杂原子掺杂的碳材料对多硫化物的吸附能力进行了理论计算,进一步验证了N、O掺杂后的碳材料对多硫化物的吸附能力最强(图7)。尽管通过杂原子的掺杂可以改善碳材料与多硫化物之间的非极性表面,提高对多硫化物的吸附能力,但是受制于杂原子在碳材料表面的含量,所以杂原子掺杂碳材料涂层对Li-S电池长期的循环稳定性仍不理想。

图7 不同电负性杂原子掺杂的碳材料与锂的结合能和杂原子电负性的关系图[34]Fig.7 Relationship between binding energy of heteroatom doped carbon materials with different electronegativity and Li and heteroatom electronegativity[34]
1.2.2 路易斯酸碱相互作用
根据路易斯酸碱理论的定义,路易斯碱是具有填充轨道的物质,包含不参与键合的电子对,而路易斯酸具有接受电子的空轨道,酸碱之间形成配位键。Li2Sx中Li+具有路易斯酸性质,而多硫化物阴离子(,4≤x≤8)具有路易斯碱的性质,金属氧化物、金属硫化物等金属化合物中的金属离子可以通过路易斯酸碱相互作用从Sx2-中获得额外的电子,达到化学吸附多硫化物的作用。但是并不是所有的过渡金属元素都能与多硫化物阴离子形成金属-硫键,Han等[35]发现原子序数较低的过渡金属具有较少的填充反键态和有效的d-p 轨道杂化。为了验证低原子序数的过渡金属元素更容易与多硫化物阴离子结合形成金属-硫键,进行了晶体轨道哈密顿布局(COHP)分析。如图8 所示,表明低原子序数的单原子金属催化剂(SACs)如Ti、V,金属-硫键较强,导致S—S键减弱,显示出有效的金属-硫键结合与多硫化锂中弱化的S—S 键之间的相关性。然而,具有最低价电子数的SACs Sc,由于其大原子半径和长Sc—S 键,所以Sc—S 键强度相对较弱。综上,SACs Ti与多硫化物阴离子具有优异的结合能力,以及能使长链的多硫化物更容易解离并转化为短链多硫化物,最终达到抑制多硫化物穿梭的目的。

图8 COHP分析过渡金属-硫和硫-硫键的强度[35]Fig.8 COHP analysis of transition metal-sulfur and sulfur-sulfur bond strengths[35]
金属氧化物由于其强大的极性表面和丰富的亲水氧基团,对极性多硫化物具有很高的化学亲和力。Zhang等[36]制备了多孔通道发达的氧化铝涂层隔膜,其弯曲的孔道结构可用于捕捉和沉积多硫化物。但由于Al2O3导电性较差,所以Chen等[37]将Al2O3涂层表面涂了一层碳纳米管(CNTs),CNTs的高导电性可以分别促进硫及其相应放电产物的反应动力学,用CNT/Al2O3涂层修饰的隔膜组装成的电池在0.2 C 电流倍率下,100 次循环后放电容量为760.4 mAh/g,而使用普通PP 隔膜的Li-S 电池100次循环后放电容量低至311 mAh/g,CNT/Al2O3隔膜表现出更优异的循环性能。
采用Al2O3、SiO2等陶瓷颗粒的涂层局限于对多硫化物的物理限制,并没有直接作用于调节Li+的传输。上述吸附作用在吸附过程中吸附位点可能会被消耗,锂离子的传输通道可能会被修饰层捕获的多硫化物堆积而发生堵塞,导致电池性能下降。为了进一步了解中间多硫化物的缓慢转化机理,加速多硫化物的转化是缓解多硫化物穿梭的关键途径。因此有研究提出了化学吸附和电催化协同作用来抑制多硫化物的穿梭[38]。Wang 等[39]根据酸性KMnO4的强氧化性能,将PP隔膜放在酸性KMnO4溶液中50 ℃恒温浸泡1 h,直接在隔膜的一侧构建超薄自组装MnO2涂层(SMO)。通过XPS谱图分析(图9),S 2p 谱中有6 个拟合峰,分别对应硫、聚硫酸盐、硫酸盐三种物质,Mn 2p3/2在641.0 eV处的峰值对应Mn3+,表明MnO2颗粒与多硫化物发生催化作用,导致化学价态发生改变。将SMO 隔膜组装成电池进行电化学测试,在0.5 C 的放电倍率下150 次充放电循环后,仍能保持603 mAh/g的放电容量,而普通的PP隔膜循环之后放电容量仅为408 mAh/g,随后将循环次数增加至500 次,具有SMO 隔膜的Li-S电池放电容量依旧保持在494 mAh/g,每周期的平均容量衰减仅为0.058%。

图9 SMO隔膜吸附试验后的XPS光谱图[39]Fig.9 XPS spectrum after SMO diaphragm adsorption test[39]
然而,值得注意的是由于金属氧化物本身导电性不好。大多数金属氧化物总是与导电基底材料结合以提高导电性,保证电子快速传输到隔膜修饰层,加速Li-S 电池中多硫化物的转化。对此,Liu 等[40]在隔膜上设计了多功能Nb2O5-CNT催化界面,以有效抑制多硫化物穿梭。具有Nb2O5-CNT催化界面的锂硫电池在0.2 C下首次放电容量高达1286 mAh/g,循环100次后仍能保持992 mAh/g的放电容量。优异的电化学性能主要归因于碳纳米管导电表面的超薄Nb2O5纳米粒子对多硫化物的强化学吸附能力,以及作为电催化剂加速对捕获多硫化物的转化能力。如图10所示,Nb2O5-CNT/PP隔膜的氧化还原峰发生了有利的位移,氧化还原峰间隙变窄。这些结果进一步表明,由于Nb2O5-CN表面的催化作用,使得多硫化物转化的氧化还原反应动力学增强。
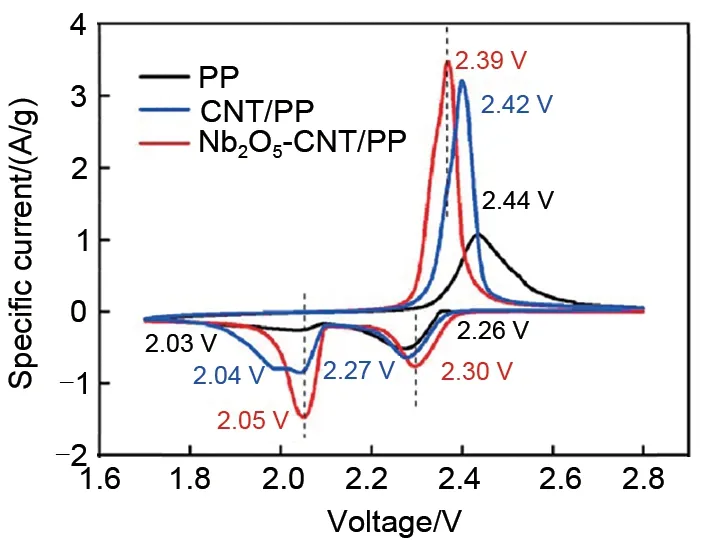
图10 采用PP、CNT/PP和Nb2O5-CNT/PP隔膜的Li-S电池电化学性能[40]Fig.10 The electrochemical performances of Li-S cells with PP,CNT/PP and Nb2O5-CNT/PP separators[40]
金属硫化物具有很强的亲硫性和相对较低的锂化电位,这使其对Li-S电池中的氧化还原反应具有良好的电催化作用,可以作为吸附多硫化物的骨架,此外金属硫化物相比金属氧化物具有更高的导电性。Tan 等[41]设计一种用于抑制穿梭效应和改善Li-S 电池电化学性能的rGO@MoS2涂层,其中rGO用作多硫化物物理屏障和电子导电网络,MoS2起到对多硫化物的化学吸附作用(图11),并充当锂导体。装有rGO@MoS2涂层隔膜组装成的电池在0.2 C 下循环200 次放电容量保持在671 mAh/g,容量保持率为70%,然而具有普通PP 隔膜的电池循环后容量为399 mAh/g,容量保持率为52%,验证了rGO@MoS2涂层可以提高电池的电化学稳定性。研究者们提出了二维结构的MoS2具有金属性和半导体性[42]。Jeong 等[43]发现电化学剥离方法不仅在横向尺寸和层数方面有效地剥离高质量的MoS2,而且能够提供1T 金属相MoS2,在捕捉多硫化物的同时促进电子转移,提高硫的利用率。将1T MoS2-CNT隔膜组装成电池在1 C高电流密度下,500 次循环之后显示出约670 mAh/g 的放电容量,而具有CNT涂层的电池在同样电流密度下在400圈之后放电容量仅为200 mAh/g。Wu 等[44]提出了一种由二维纳米材料逐层自组装制作功能涂层,由带正电的MoS2-聚二烯丙基二甲基氯化铵(PDDA)复合物与带负电的聚丙烯酸(PAA)交替沉积,形成双面的“纳米砖墙”结构,创造一条曲折的迂回路径,极大地阻碍了多硫化物穿梭。同时,MoS2纳米片和PAA以化学方式吸附多硫化物。具有超轻(M-P/P)10涂层的Li-S电池,在1 C电流密度下,循环2000次后,每循环的平均容量衰减率降至0.029%。

图11 Li2S6溶液被MoS2吸附前后的紫外吸收光谱和照片[41]Fig.11 UVabsorptionspectrum andphotograph(inset)of Li2S6 solution before and after being adsorbed by MoS2[41]
Yang 等[45]通过将分散的硫化锌纳米球包裹在石墨烯状超薄褶皱碳膜上(ZnS@WCF)制备一种新型的功能涂层。根据XPS 结果表明,ZnS 通过SZn和Li-S结合对多硫化锂表现出强烈的化学作用。此外ZnS@WCF 在Li2S 成核试验中表现出最高的成核能力(图12),证明ZnS@WCF 降低了多硫化物转化的能量势垒。得益于卓越的催化能力,基于ZnS@WCF隔膜的Li-S电池在1 C的放电倍率下循环600次后,仍能保持685 mAh/g的高放电比容量。最近,研究人员为了进一步抑制多硫化物的扩散,探索出了具有异质结构的Li-S 电池功能性隔膜。Yao等[46]通过结合SnS的强吸附性和高导电性以及ZnS的良好催化能力,在由聚多巴胺衍生的N掺杂碳壳表面获得了具有均匀立方形貌的ZnS-SnS@NC异质结构,该异质结构带来了更多的电化学活性位点,并且多孔碳结构作为离子筛,从而促进锂的均匀沉积。该隔膜所组装的电池在4 C高放电倍率下初始放电容量提高至845 mAh/g,循环2000 次后依然能够保持较高的可逆容量632 mAh/g,容量衰减率仅为0.013%,表现出良好的循环和倍率性能。

图12 ZnS、WCF、ZnS@WCF对称电池的电化学测试:Li2S 成核试验[45]Fig.12 ZnS、WCF、ZnS@WCF symmetric cell electrochemical test administered:Li2S into a nuclear test[45]
与杂原子掺杂碳材料涂层相比,过渡金属化合物涂层可以在捕获多硫化物的情况下,降低多硫化物转化能量势垒,为捕获多硫化物提供更多的吸附位点,进一步提高了Li-S电池的循环稳定性。然而导电性极差的过渡金属化合物(如过渡金属氧化物)不能保证电子传输到隔膜的修饰层,造成捕获的多硫化物堆积堵塞锂离子的传输通道,因此过渡金属化合物与导电碳材料复合。但由于导电碳材料具有多孔结构和高比表面积等特点,在其复合过程中不仅会增加隔膜厚度而且会大幅度增加对电解质的消耗,导致Li-S电池整体的能量密度下降。因此,需要开发一种导电性好、轻质、吸附性强的功能隔膜,在抑制多硫化物穿梭的同时提高Li-S电池的能量密度。
将利用化学限制策略的聚丙烯基改性隔膜电化学性能列于表2。

表2 化学限制聚丙烯基改性隔膜电化学性能Table 2 Electrochemical properties of chemically restricted polypropylene based modified separator
2 纤维素基改性隔膜
相比传统的聚烯烃隔膜,纤维素隔膜由于具有优异的浸润性和低成本等优势而备受关注[49],特别是纤维素隔膜表面丰富的羟基使纤维素成为一种极性很强的聚合物,为化学修饰功能性隔膜提供了新的基体材料[50]。
Yu等[51]利用具有纤维素基多孔的凝胶面膜作为隔膜,经过简单的处理,不仅能有效限制多硫化物的穿梭,还能保持锂离子在负极与电解液表面均匀沉积,抑制锂枝晶的生长。Li等[52]利用生物纤维素(BC)丰富的伯羟基经过TEMPO氧化成为羧酸酯基团,进而形成显电负性的界面(图13)来阻止多硫化物的穿梭。将PP隔膜和氧化后的BC隔膜(o-BC)分别组装成Li-S 电池,在高载硫量(4 mg/cm2)下,具有PP 隔膜的电池循环至100 次放电比容量就已经衰减至600 mAh/g,而具有改性隔膜的电池循环300 次后放电比容量高达735 mAh/g,对应每个循环的平均容量衰减率仅为0.07%,明显优于商用的PP隔膜。MXene相一般是通过选择性刻蚀MAX相获得层状过渡金属碳化物或氮化物,具有优异的导电性和丰富的官能团。Wu 等[53]提出了一种基于多孔细菌纤维素(PBC)的Ti3C2Tx-SnS2-PBC 隔膜。一方面PBC具有高耐温性和抗穿刺性,提高了Li-S电池的安全性能;另一方面Ti3C2Tx-SnS2涂层可以通过路易斯酸碱作用捕获多硫化物,并通过催化活性位点促进氧化还原动力学。将Ti3C2Tx-SnS2-PBC隔膜组装成电池在0.2 C 放电倍率下初始容量高达1390.9 mAh/g,循环500次后仍能保持862.1 mAh/g的放电容量,而PP 膜组装成的电池循环500 次后放电比容量仅为247.9 mAh/g,电池的容量保持率比PP隔膜高71.2%。

图13 p-BC和o-BC样品的Zeta电位[52]Fig.13 Zeta potential of the p-BC and o-BC samples[52]
Wu 等[54]开发了一种具有“漏斗效应”的先进Li-S电池隔膜,在醋酸纤维素静电纺丝隔膜(CA)上原位聚合一层具有微孔结构的环糊精(β-CD)膜,并在膜的另一侧沉积一层碳作为上集流器。具有微孔结构的复合隔膜为抑制多硫化物穿梭提供了最佳的孔径(0.6~0.78 nm),并且微孔膜表面丰富的含氧极性基团可以化学吸附多硫化物,形成阻碍多硫化物的第二道屏障。将β-CD/CA/C、PP 隔膜组装成电池,在0.2 C 放电倍率下,具有PP 隔膜的Li-S电池在600 次循环后放电比容量仅为280 mAh/g,而具有β-CD/CA/C 隔膜的Li-S 电池初始放电容量为1378 mAh/g,经过1000次循环之后放电比容量高达863 mAh/g,是PP 隔膜500 次循环之后放电比容量的3倍以上。最主要的是,环糊精特有的截锥结构造成膜两侧产生不同的流体压力,导致在充电测试中(图14),具有β-CD 膜的电池充电速率比普通PP 隔膜的电池高65.3%。该隔膜的“漏斗效应”为Li-S电池快速充电提供了一种新型高效的解决方案。Li等[55]发现纤维素纳米纤维中的异丙醇含量可以微调膜的孔隙结构,所以将纤维素纳米纤维(CNF)悬浮液与异丙醇水溶液混合搅拌,通过控制其中异丙醇与水的体积比调节CNF隔膜的孔结构,以实现最佳的电化学性能。将CNF 膜组装成电池之后,在0.2 C 放电倍率下,100 次循环后放电比容量为589 mAh/g,相比具有PP 隔膜的Li-S 电池(100 次循环之后放电比容量为459 mAh/g)有很大改善。如图15所示,通过DFT计算得出CNF隔膜中的含氧官能团也能对多硫化物具有一定的吸附能力,所以CNF 隔膜良好的电化学性能不仅取决于CNF膜具有的微孔结构,还与含氧极性官能团吸附多硫化物有关。
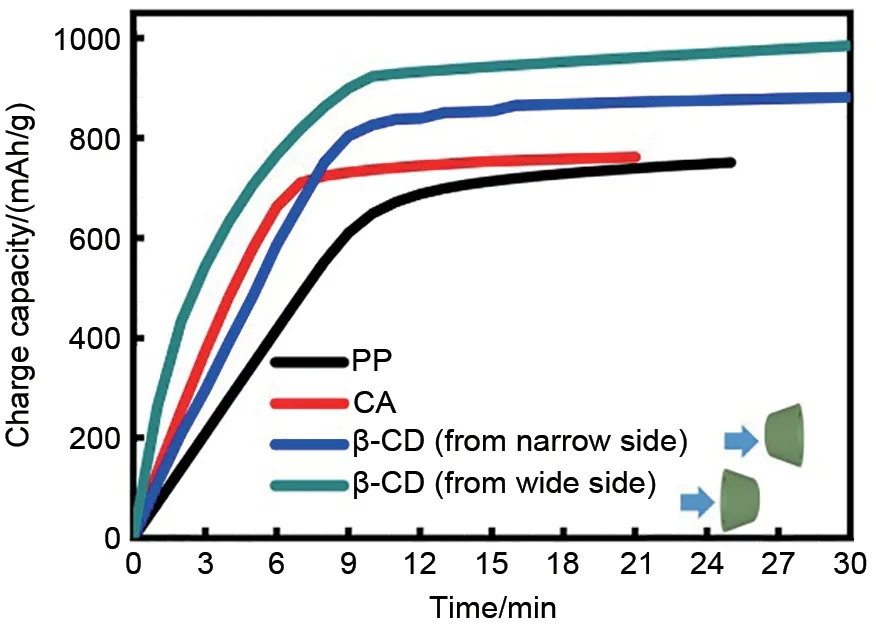
图14 快速充电性能图[54]Fig.14 Fast-charging performance diagram[54]

图15 DFT模拟Li2S6和CNF的相互作用[55]Fig.15 DFT interaction simulation Li2S6 and CNF[55]
3 结 论
本工作主要介绍了以聚烯烃隔膜和新型纤维素隔膜作为改性基体材料,不同抑制多硫化物穿梭的方法对Li-S电池充放电比容量、库仑效率、循环寿命的影响。基于传统的聚烯烃隔膜改性的功能性隔膜在不同的抑制策略下使Li-S电池表现出优异的电化学性能,为以后构建同时具有静电排斥、空间位阻、路易斯酸碱等作用的功能性隔膜奠定了基础。此外新型的纤维素隔膜表面丰富的羟基基团,可以通过化学方式修饰隔膜如酯化、氧化、醚化、接枝等,为隔膜的修饰开辟了一条新的途径。
虽然功能性隔膜研究取得了一定的成就,但是目前仍面临以下技术难题。第一,传统的聚烯烃隔膜活性位点较少,隔膜修饰只能通过物理涂覆实现,但额外的涂层不可避免地增加了隔膜的厚度,所以需要开发一种能够通过化学反应修饰传统聚烯烃隔膜的方法,来提高Li-S 电池的能量密度。第二,虽然纤维素隔膜具有丰富的活性位点,可以通过化学反应修饰隔膜,但是其受制备工艺的影响,造成纤维与纤维之间的孔隙过大,无法实现对多硫化物和锂离子的有效筛分,所以通过化学改性优化纤维素隔膜孔隙结构是现在的主要研究方向。此外纤维素膜较差的力学性能,无法避免负极锂枝晶刺穿隔膜导致电池短路所带来的安全问题,所以需要利用纤维素表面多活性位点的特性将无机材料接枝在隔膜表面,提高纤维素隔膜的机械强度和对多硫化物的化学吸附性。第三,过渡金属元素对多硫化物的催化机理和影响因素还不明确,而这是能否准确控制Li-S 电池隔膜化学改性效果的关键所在。第四,由于金属氧化物等常见极性材料导电性差,吸附的多硫化物很难有效地再利用,尤其在长循环过程中吸附的多硫化物附着在隔膜表面,无法被重新激活,导致硫的利用率降低,因此,急需开发同时具有高导电性和强多硫化物吸收性的先进隔膜涂层材料。对于以上问题的进一步探索将是推动Li-S电池商业发展的重要前提。

