以制革废弃物制备的复合氨基酸材料及其清洁脱灰
王浩,雷超,曾运航*,石碧,
(1.四川大学制革清洁技术国家工程实验室,四川成都610065;2.四川大学皮革化学与工程教育部重点实验室,四川 成都610065)
前言
脱灰是制革准备工段中衔接浸灰和软化过程的一个重要工序,具有降低浸灰裸皮pH、脱除皮内灰碱、消除裸皮膨胀状态、为后工序创造适宜条件等作用。铵盐(硫酸铵和氯化铵)因具有pH缓冲性好、渗透快、价格低等显著优势,是应用最广泛的脱灰剂[1]。然而,铵盐脱灰一方面会使脱灰过程产生有刺激性气味、危害人体健康的氨气,另一方面会造成制革废水的氨氮(NH3-N)浓度过高[2]。排放高浓度的NH3-N废水将引起水体富营养化[3],国家标准GB 30486-2013《制革及毛皮加工工业水污染物排放标准》规定现有和新建制革企业NH3-N的直接排放浓度限值分别为25 mg/L和15 mg/L。传统脱灰工序使用的大量铵盐是制革NH3-N污染物的主要来源[2],用少/无氨脱灰剂替代铵盐是从源头削减NH3-N污染的重要途径。经过多年研究,现已开发了多种无氨脱灰剂,如二氧化碳[4]、镁盐[5]、有机酸和酯类[6-7]、硼酸[8-9]等,但它们或pH缓冲性差、渗透慢,或成本较高,或具有毒性。因此,仍需继续开发脱灰效果好、价格低廉、环境友好的无氨脱灰剂。
氨基酸是既有酸性基团-COOH,又有碱性基团-NH2的两性化合物。当溶液的pH高于氨基酸的等电点(pI)时,氨基酸中的-NH3+给出质子,带净的负电荷;反之当溶液的pH低于氨基酸的pI时,氨基酸中的-COO-结合质子,带净的正电荷[10]。组成蛋白质的二十余种基本氨基酸中,仅有精氨酸(pI,10.76)和赖氨酸(pI,9.74)的pI高于9[11]。这说明多数基本氨基酸能在脱灰浴液中释放质子,中和浴液和裸皮中的碱,且具有一定的缓冲能力。另外,氨基酸可与氢氧化钙反应生成溶解度较大的钙盐[12],利于除去浸灰裸皮中结合的钙。氨基酸中的氮在水中也不以NH3-N形式存在,即不会产生NH3-N污染。因此从理论上讲,大多数基本氨基酸都具备作为清洁脱灰剂的潜力。其中,甘氨酸已被证明是一种性能优良的脱灰剂[13],但是甘氨酸多用于医药食品行业、价格较高[14],这限制了其在皮革脱灰领域的商业应用。
制革过程产生的废弃牛毛、生皮边角料等废弃物含有大量的蛋白质,可用于低成本制备复合氨基酸。酸水解蛋白质具有水解效率高、成本低的优点,是目前生产复合氨基酸的常用方法[15]。因此,本文用废弃牛毛和生皮边角料作为原料,通过硫酸水解法制备了以复合氨基酸为主要成分的脱灰剂,希望通过资源化利用制革废弃物获得价廉、高效、清洁的脱灰剂。考察了水解温度、硫酸浓度、水解时间和固液比等水解条件对废弃牛毛和生皮边角料水解产物中氨基酸产率的影响,并采用优化的水解条件制备了牛毛深度水解物(BHDH)和牛皮深度水解物(CDH);接着使用BHDH和CDH进行牛皮脱灰实验,考察了其pH缓冲性能、在裸皮内的渗透速度和脱钙能力等脱灰性能,以及对脱灰废液NH3-N、总氮(TN)和有机碳(TOC)浓度的影响。
1 实验部分
1.1 主要材料和试剂
废弃牛毛(以下简写为牛毛),经保毛脱毛法处理牛皮所得,进行酸水解实验前需水洗、晾干。浸灰牛皮(厚度2.2 mm),由盐湿牛皮经常规浸水、去肉、浸灰(硫化钠用量3%,石灰用量7.5%)和片皮等操作制备。生皮边角料(以下简写为牛皮),用二层浸灰牛皮经脱灰(温度32℃,水100%,甲酸3%,时间4 h)、水洗、剪切、干燥等处理制备。浓硫酸、氢氧化钠、硫酸铵,分析纯,成都金山化学试剂有限公司。用于脱灰剂、裸皮和废液分析检测的试剂均为分析纯,皮革化工材料均为工业级。氨氮测定预制试剂盒(高量程,0.4~50.0 mg/L),福州福光水务科技有限公司。
1.2 主要仪器
GSD型热泵循环不锈钢控温试验转鼓(Φ400 mm×200 mm),无锡市新达轻工机械有限公司;PHS-3C型精密酸度计,上海大普仪器有限公司;UV-1800PC型紫外可见光分光光度计,上海美普达公司;DR6000型水质分析仪,美国哈希公司;KSL-120X-M型箱式电阻炉,合肥科晶材料技术有限公司;K1306型全自动凯氏定氮仪,上海晟声自动化分析仪器有限公司;L-8900型全自动氨基酸分析仪,日本日立公司;LGJ-T40标准型冷冻干燥机,北京四环起航科技有限公司;M205C型体视显微镜,德国徕卡公司;Optima 2100DV型电感耦合等离子原子发射光谱仪(ICP-AES),美国珀金埃尔默有限公司;Liqui TOC型TOC/TNb分析仪,德国Elementar公司;Gemini SEM 300型场发射扫描电子显微镜,德国蔡司公司;AI7000-S型拉力试验机,中国高铁检测仪器有限公司;GT-303型皮革柔软度测试仪,中国高铁检测仪器有限公司;GX-5071-A型皮革崩裂试验机,东莞高鑫检测设备有限公司。
1.3 复合氨基酸脱灰剂的制备
1.3.1 水解条件的优化
用硫酸水解牛毛和牛皮制备复合氨基酸。我们前期的正交试验结果(略)表明,各水解条件对牛毛和牛皮氨基酸产率的影响顺序为:水解温度>硫酸浓度>水解时间>固液比。故本节在此基础上通过单因素试验依次考察了水解温度、硫酸浓度、水解时间和固液比等对牛毛和牛皮水解产物中游离氨基酸和NH3-N产率的影响。
(1)水解温度的影响
将牛毛或牛皮与7 mol/L硫酸溶液按照固液比1∶4混合,分别于80、90、100、110和120℃加热水解2 h,然后取样测定水解产物中的游离氨基酸和NH3-N产率。
(2)H2SO4浓度的影响
将牛毛 或牛皮与 不同浓度(3、4、5、6和7 mol/L)的硫酸溶液按照固液比1∶4混合,于110℃水解反应2 h,然后取样检测。
(3)水解时间的影响
将牛毛或牛皮与5 mol/L硫酸溶液按照固液比1∶4混合,于110℃分别加热水解2、3、4、5和6 h,然后取样检测。
(4)固液比的影响
将牛毛或牛皮与5 mol/L硫酸溶液按照不同的固液比(1∶2、1∶3、1∶4、1∶5和1∶6)混合,于110℃加热水解一定时间(牛毛加热5 h,牛皮加热4 h),然后取样检测。
1.3.2 水解产物中游离氨基酸和NH3-N产率的测定
采用茚三酮显色法测定所取样品中的游离氨基酸浓度[16],用水质分析仪和氨氮测定预制试剂盒测定NH3-N浓度,并根据式(1)和(2)计算水解产物中的游离氨基酸产率和NH3-N产率。
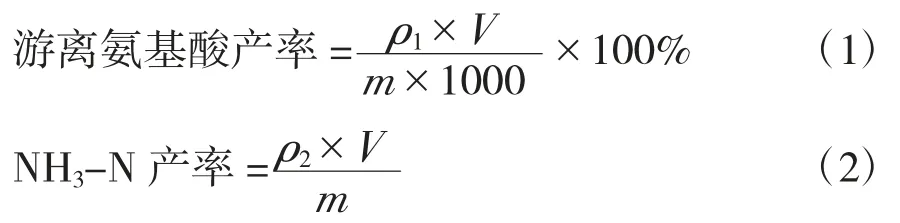
式中ρ1——水解液中游离氨基酸的质量浓度,单位mg/L;
ρ2——水解液中NH3-N的质量浓度,单位mg/L;
V——水解液的体积,单位L;
m——牛毛或牛皮的质量,单位g。
1.3.3 BHDH和CDH的制备
将牛毛或牛皮与5 mol/L硫酸溶液按照固液比1∶4混合后,于110℃水解一定时间(牛毛5 h;牛皮4 h)。然后,用10 mol/L氢氧化钠溶液中和水解液的pH至5.0~5.5,冷却后过滤去除未水解的残渣和结晶盐。最后,用冷冻干燥机将滤液冻干,得到BHDH和CDH。
1.3.4 BHDH和CDH的组分分析
采用直接干燥法测定BHDH和CDH的水分含量[17];用索氏抽提法测定脂肪含量[18];用全自动凯氏定氮仪测定粗蛋白含量,折算系数为6.25;将BHDH和CDH置于电炉中,在550℃灼烧4 h测定总灰分[19];用全自动氨基酸分析仪测定BHDH和CDH的游离氨基酸组成;用水质分析仪测定BHDH和CDH溶液的NH3-N浓度,然后计算其NH3-N含量。
1.4 BHDH和CDH的脱灰性能评价
取一张浸灰牛皮分为三组,每组均包括颈部、背部、臀部和腹部牛皮各一块。三组浸灰牛皮分别用硫酸铵、BHDH和CDH进行脱灰实验,脱灰温度32℃,水用量为100%,转动90 min。硫酸铵用量为3%,BHDH和CDH的用量为2%、3%、4%和5%(以水洗后的浸灰裸皮质量为基准)。
在脱灰10、20、30、40、60和90 min时测定脱灰浴液的pH,并用酚酞指示剂检查裸皮切口,以判断裸皮是否脱透,同时用体视显微镜拍摄裸皮切口的显微照片。脱灰结束后,根据文献所述方法测定脱灰裸皮的钙含量,并根据公式(3)计算脱灰裸皮的脱钙率[9]。

脱灰90 min后,取脱灰废液并用100目滤布过滤,然后用水质分析仪测定其NH3-N浓度,用TOC/TN分析仪测定其TOC和TN浓度。
此外,将脱灰裸皮进行软化、浸酸、铬鞣、复鞣、染色和加脂等工序的处理,制成坯革。按照标准方法取样测定加脂坯革的柔软度、抗张强度、撕裂强度和崩破强度等物理性能[20-24],并用SEM观察坯革的粒面和断面形貌。
2 结果与讨论
2.1 牛毛和牛皮水解条件的优化结果
本文的主要目的是用制革废弃物制备复合氨基酸类脱灰剂,但因为蛋白质在水解过程中会产生少量的NH3-N(脱灰工序不希望引入的污染物),所以本节以牛毛和牛皮水解产物中游离氨基酸和NH3-N的产率作为评价指标,对水解条件进行了优化。由图1(a)可知,当水解温度从80℃升至110℃时,牛毛和牛皮水解产物中的氨基酸产率分别从20.2%增至50.4%,以及从27.4%增至74.0%;水解温度继续从110℃升至120℃时,氨基酸产率的增幅较小。此外,水解产物的NH3-N产率随着水解温度的升高而逐渐增加。产生上述现象的原因应该是高温加快了肽键的水解,提高了氨基酸产率,但同时加强了硫酸对氨基酸产物的破坏,导致NH3-N产率升高。由图1(b)可知,当硫酸浓度从3 mol/L增至5 mol/L时,水解产物的氨基酸产率增加较明显,而继续增大硫酸浓度,氨基酸产率仅小幅上升;另一方面,当硫酸浓度从3 mol/L升至7 mol/L时,NH3-N产率一直增长。由图1(c)可知,牛毛和牛皮分别在水解5 h和4 h后,氨基酸产率基本不再升高;牛毛水解物中的NH3-N随水解时间的延长而逐渐增多,但牛皮水解物中NH3-N随时间的变化并不明显。由图1(d)可知,固液比为1∶4时的氨基酸产率明显高于固液比为1∶2和1∶3时的氨基酸产率,这可能是由于固液比达到1∶4后,牛毛和牛皮能更充分地接触硫酸溶液,加快蛋白质的水解。
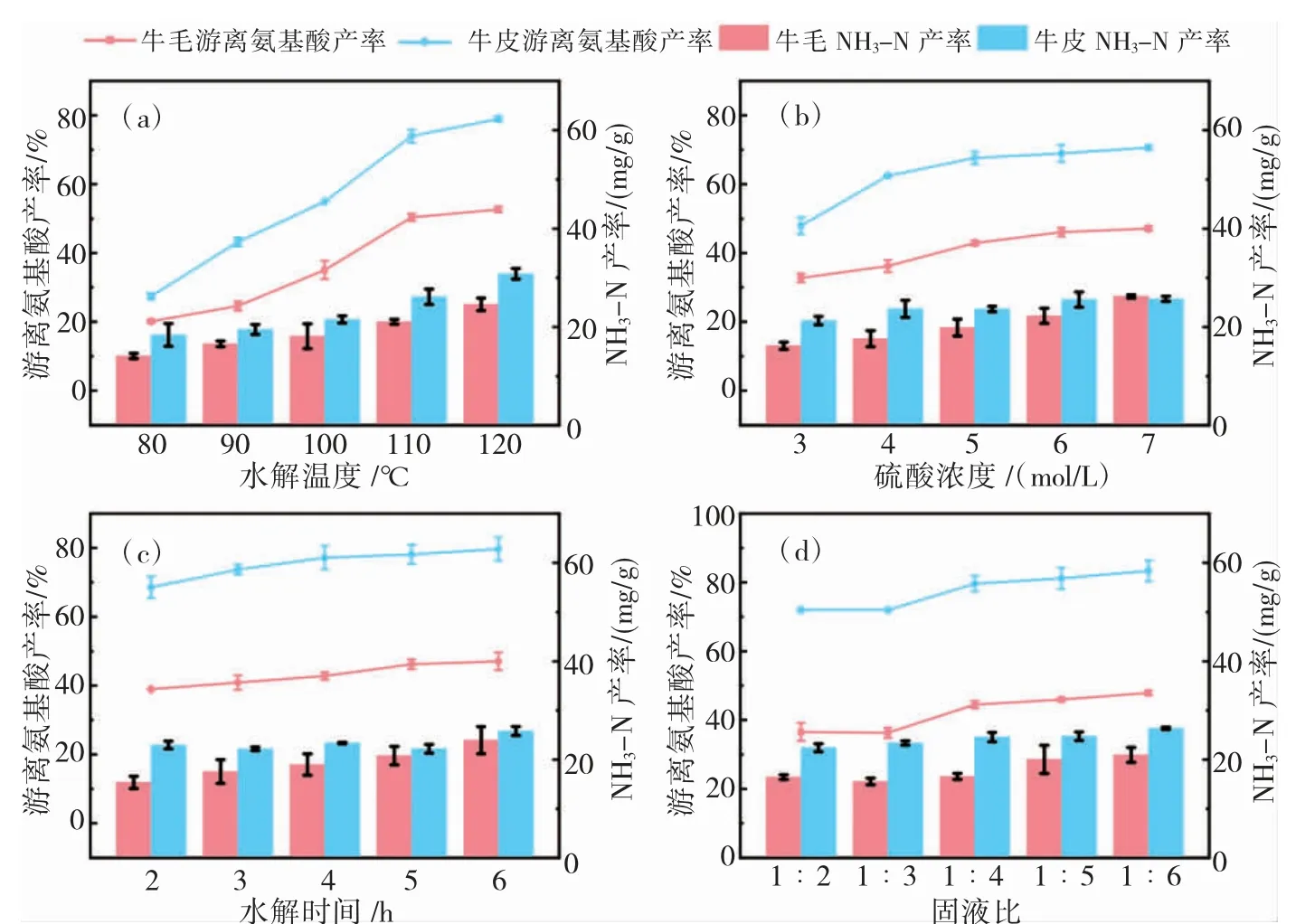
图1 水解温度(a)、硫酸浓度(b)、水解时间(c)和固液比(d)对牛毛和牛皮水解产物中游离氨基酸和NH3-N产率的影响Fig.1 Effects of hydrolyzing temperature(a),sulfuric acid concentration(b),hydrolyzing time(c)and solid-liquid ratio(d)on the yields of free amino acids and NH3-N in the hydrolysis products of bovine hair and cattle hide
综合考虑水解产物的氨基酸产率、NH3-N产生量、材料成本等因素,本文选择的最佳水解条件为:水解温度110℃,H2SO4浓度5 mol/L,水解时间5 h(牛毛)和4 h(牛皮),固液比1∶4。在最佳水解条件下,牛毛水解产物的游离氨基酸产率为44.5%,NH3-N产率为16.6 mg/g;牛皮水解产物的游离氨基酸产率为79.6%,NH3-N产率为24.6 mg/g。牛皮水解产物的氨基酸产率明显高于牛毛水解产物,这是因为牛皮的蛋白质组分主要是胶原,而牛毛的主要蛋白质组分是角蛋白,两者中胶原更易被酸水解。
2.2 BHDH和CDH的组分分析
采用上述最佳水解条件制备了牛毛的深度水解产物BHDH和牛皮的深度水解产物CDH。从表1中的数据可以看出,BHDH和CDH的水分含量均低于4%;总灰分含量约40%~47%,这是因为用氢氧化钠溶液中和牛毛及牛皮的酸水解液时产生了大量的硫酸钠;蛋白质含量约为50%,游离氨基酸含量约40%;NH3-N含量为10~12 mg/g(BHDH的NH3-N含量为10.32 mg/g,CDH的NH3-N含量为12.04 mg/g),远低于硫酸铵的NH3-N含量(254 mg/g)。图2是BHDH和CDH中各种氨基酸占总游离氨基酸的质量百分比。可以看出,BHDH含有17种氨基酸,CDH含有16种氨基酸(比BHDH少一种半胱氨酸)。在酸水解过程中,色氨酸被完全破坏,天冬酰胺和谷氨酰胺会脱酰胺基,丝氨酸和苏氨酸也被部分破坏[25]。
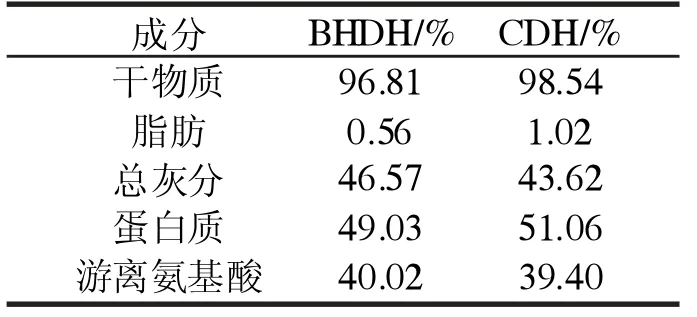
表1 BHDH和CDH的组分Tab.1 Components of BHDH and CDH
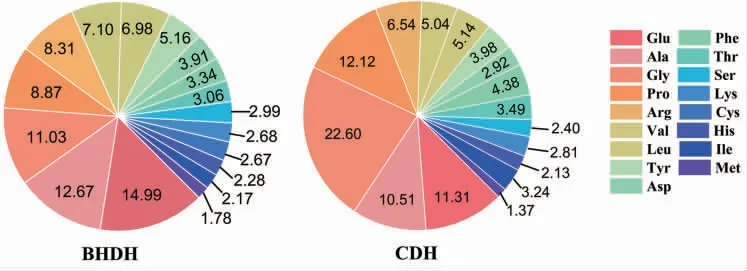
图2 BHDH和CDH中氨基酸的质量百分比Fig.2 Mass percentages of amino acids in BHDH and CDH
2.3 BHDH和CDH的pH缓冲性能
脱灰工序的主要目的之一是将浸灰裸皮的pH从12~13降至9左右,因此脱灰剂一般是酸性物质。特别地,为了避免脱灰裸皮酸肿和保证脱灰剂快速渗透裸皮,在脱灰过程中应防止浴液pH骤降,这就需要脱灰剂最好能与浸灰裸皮中的灰碱形成pH 8~9的缓冲体系[26]。图3(a)和3(b)分别是用2%~5%的BHDH和CDH脱灰时浴液pH随时间的变化曲线。用2%的BHDH和CDH脱灰10 min时,浴液的pH分别为8.62和8.70,接近3%硫酸铵脱灰10 min时浴液的pH(8.87);继续增加BHDH和CDH的用量至5%,脱灰10 min时浴液的pH有所降低,但仍然高于8。另外,在BHDH和CDH脱灰的整个过程中,浴液的pH基本稳定在8~9的范围内。这些现象说明BHDH和CDH具有非常适合脱灰的pH缓冲性能,因为它们的氨基酸、小肽等组分既有碱性的氨基,又有酸性的羧基。
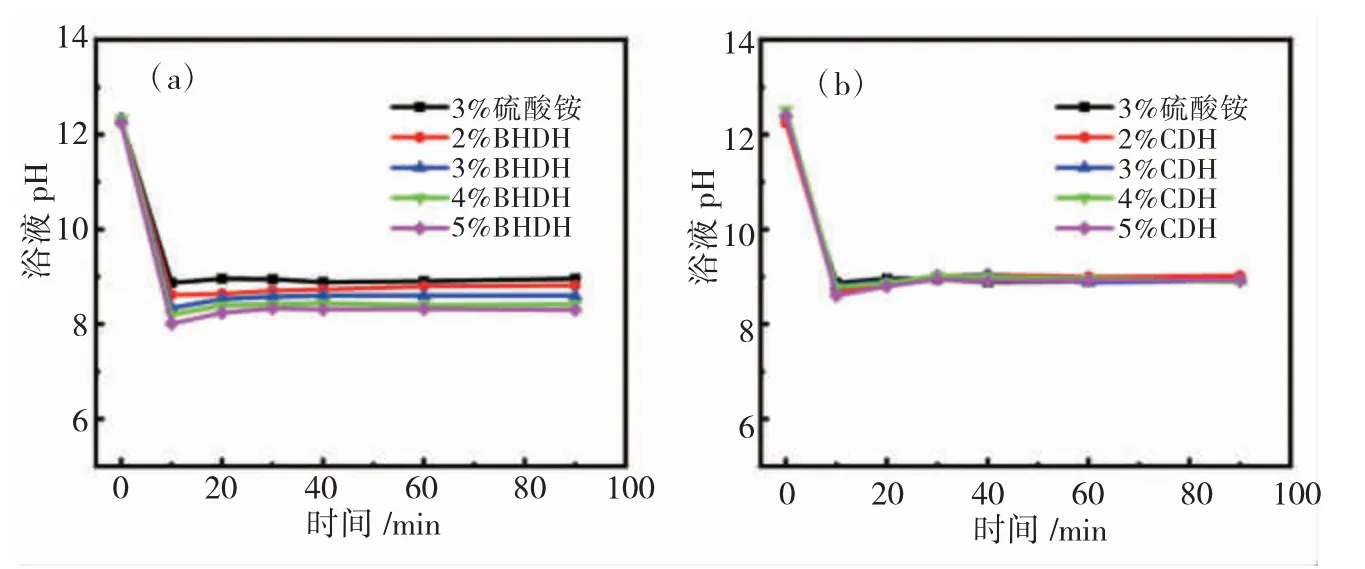
图3 BHDH(a)和CDH(b)的用量对脱灰过程中浴液pH的影响Fig.3 Effects of the dosages of BHDH(a)and CDH(b)on the float pH during the deliming process
2.4 BHDH和CDH在裸皮内的渗透速度
良好的脱灰剂应能迅速渗透裸皮,使裸皮快速消肿而变得柔软,以缩短脱灰时间和减少裸皮的机械损伤[1]。本节用硫酸铵、BHDH和CDH(用量均为3%)对浸灰牛皮的不同部位进行脱灰,结果如表2和图4所示。硫酸铵能在30 min内完全渗透裸皮颈部,在10 min内渗透其它部位;BHDH和CDH需要40~50 min才能完全渗透裸皮颈部,在20 min内能脱透裸皮的背部和腹部。与其它有机酸类脱灰剂相比,BHDH和CDH在裸皮内的渗透速率更快,更接近铵盐的脱灰效果[6]。这是因为BHDH和CDH脱灰浴液的pH(图3)始终高于浸灰裸皮的pI(6左右[13]),使得裸皮表面带负电荷,不易吸引同样带负电荷的氨基酸阴离子,这有利于BHDH和CDH向裸皮内层渗透[13]。

图4 滴加酚酞后浸灰裸皮和脱灰裸皮(脱灰20 min)纵剖面的体视显微镜照片Fig.4 Stereomicroscope images of vertical sections of the limed hide and the hides delimed for 20 min after checking with phenolphthalein

表2 BHDH和CDH在裸皮不同部位的渗透时间Tab.2 PenetrationtimesofBHDHandCDHindifferentpartsofhide
2.5 BHDH和CDH对裸皮的脱钙效果
裸皮的脱钙程度会影响后续软化工序蛋白酶的软化效果、蓝湿革及染色加脂坯革表面颜色的均匀性等[9]。本节测定了BHDH和CDH脱灰后裸皮的脱钙率,结果如图5所示。除了2% BHDH和CDH脱灰裸皮的脱钙率略低于硫酸铵脱灰裸皮外,3%~5%BHDH和CDH脱灰裸皮的脱钙率均高于硫酸铵脱灰裸皮,说明BHDH和CDH能够有效脱除浸灰裸皮内的灰碱。这是因为BHDH和CDH中的氨基酸组分能与石灰反应生成溶解度较大的钙盐[12]。
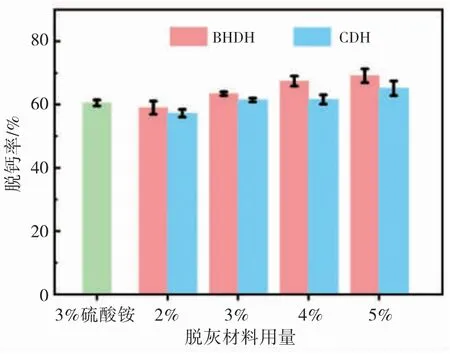
图5 脱灰裸皮的脱钙率Fig.5 Removal extents of calcium from the delimed hides
2.6 BHDH和CDH脱灰对坯革性能的影响
本节通过比较硫酸铵、BHDH和CDH(用量均为3%)脱灰裸皮制成的坯革的形貌和物理性能,评价了BHDH和CDH脱灰对坯革性能的影响。由图6中的SEM照片可以看出,三种坯革均具有清晰的粒面和相似的胶原纤维网络。此外,这三种坯革的抗张强度、撕裂强度、崩破强度和柔软度等物理性能接近(表3),说明BHDH和CDH脱灰可以保证皮革的品质。

表3 坯革的物理性能Tab.3 Physical properties of the crust leathers

图6 坯革粒面和纵剖面的SEM照片Fig.6 SEM images of grain surfaces and cross-sections of the crust leathers
2.7 BHDH和CDH脱灰对废液指标的影响
为了评估BHDH和CDH脱灰对环境的影响,本节测定了硫酸铵、BHDH和CDH(用量均为3%)脱灰废水的NH3-N、TN和TOC浓度,结果如表4所示。BHDH和CDH中仅含有少量蛋白质深度水解时产生的NH3-N,因此脱灰废水的NH3-N浓度比硫酸铵脱灰废水下降了94%以上。硫酸铵脱灰废水的TN质量浓度高达4244 mg/L,TN主要来源于铵盐的使用和皮蛋白质的分解产物;BHDH和CDH脱灰废水的TN质量浓度低于1500 mg/L,TN主要来自脱灰剂本身所含的有机氮和少量NH3-N,以及皮蛋白质的分解产物。另外,虽然BHDH和CDH作为含碳有机物,造成脱灰废水的TOC浓度约为硫酸铵脱灰废水的3倍,但这反而可以作为碳源,改善传统制革综合废水过低的C/N比,提高制革综合废水的生物处理效果。

表4 脱灰废水的NH3-N、TN和TOC质量浓度Tab.4 NH3-N,TN,and TOC concentrations of deliming effluent
3 结论
用硫酸水解制革废弃牛毛和生皮边角料适用于制备高效价廉的氨基酸类清洁脱灰剂。该类脱灰剂能与浸灰裸皮内的灰碱作用形成pH 8~9的缓冲体系,较快地脱透裸皮,且脱钙效果略优于硫酸铵。此外,该类材料能从源头大幅削减铵盐脱灰废液的NH3-N和TN浓度。虽然它们会向脱灰废水中引入TOC,但有助于提高制革综合废水的C/N比,将有利于综合废水的生物处理。

