白蛋白结合型紫杉醇联合卡铂治疗晚期非小细胞肺癌的临床效果观察
肖家骠(泰和县人民医院肿瘤血液科,江西 泰和 343700)
非小细胞肺癌是我国现阶段一种常见的恶性肿瘤,具有较高的发病率,是肺癌中最常见的疾病之一[1]。但非小细胞肺癌患者早期缺少典型性临床症状,因此在早期阶段诊断较为困难,患者一般是在体检或疾病发展至晚期阶段,临床症状较为显著时才确诊,但该阶段患者死亡率较高,预后较差[2]。化疗是晚期非小细胞肺癌的重要治疗方式,紫杉醇类是目前临床常用的化疗药物[3]。传统溶剂型紫杉醇具有高度疏水性,需以聚氧乙烯蓖麻油为溶剂,因此具有较高毒性,对治疗的安全会造成较大的影响[4]。白蛋白结合型紫杉醇以人血白蛋白为载体,具有较低毒性,能有效避免传统溶剂型紫杉醇的缺点[5]。本研究选取2018年10月至2021年3月我院收治的68例晚期非小细胞肺癌患者,分析白蛋白结合型紫杉醇联合卡铂治疗的价值。报道如下。
1 资料与方法
1.1 一般资料选取2018年10月至2021年3月我院收治的晚期非小细胞肺癌患者68例,按随机数字表法分为观察组和对照组各34例。观察组中男20例、女14例;年龄45~78(56.12±1.14)岁;鳞癌18例、腺癌16例。对 照组 中 男22例、女12例;年 龄44~79(56.38±1.25)岁;鳞癌19例、腺癌15例。两组一般资料比较,无显著差异(P>0.05),具有可比性。患者及家属对研究内容知情,且同意参与本次研究。本研究经我院医学伦理委员会审核批准。[Y(2020)18号]1.2方法对照组给予紫杉醇(北京世桥生物制药有限公司,批准文号H20059582)175mg/m2,静脉滴注,d1。患者若首次使用紫杉醇,应在使用前对患者进行静脉试敏,给予地塞米松(广东华南药业集团有限公司,批准文号H44024469)联合抗组胺药进行预处理,观察患者变化。并给予患者卡铂(云南植物药业有限公司,批准文号H10950273),依据AUC=6静脉滴注,d1。观察组给予白蛋白结合型紫杉醇(浙江海正药业股份有限公司,批准文号H20213539)130 mg/m2,静脉滴注,d1、d8;给卡铂,依据AUC=6静脉滴注,d1。两组均治疗3周。
1.3 临床观察指标(1)观察两组治疗有效率及1年生存率部分缓解:病灶消失体积在50%以上;时间保持在4周以上;稳定:病灶消失体积25%~49%,时间维持不足4周;进展:未达上述标准。治疗有效率为部分缓解所占比例。(2)观察两组CEA、CA125、CA199等肿瘤标记物水平。(3)不良反应发生率。记录两组出现恶心呕吐、腹泻、皮疹、肺炎及白细胞减少的例数。(4)免疫指标。记录两组治疗前、治疗1个月后免疫指标水平。
1.4 统计学处理数据采用SPSS 21.0统计学软件进行处理,计量资料采用(±s)表示,行t检验;计数资料采用[n(%)]表示,行χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组有效率及1年生存率比较观察组有效率及1年生存率均高于对照组(P<0.05)。见表1。

表1 两组治疗有效率及1年生存率比较[n(%)]
2.2 两组肿瘤标记物水平比较治疗前,两组CEA、CA125、CA199水平无显著差异(P>0.05);治疗后,观察组CEA、CA125、CA199水平较对照组低(P<0.05)。见表2。
表2 两组肿瘤标记物水平比较(±s)
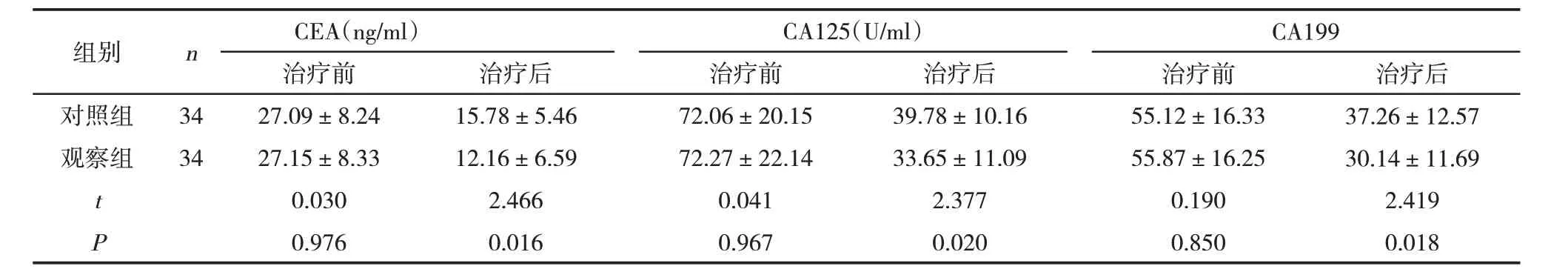
表2 两组肿瘤标记物水平比较(±s)
组别对照组观察组n 34 34 t P CEA(ng/ml)治疗前27.09±8.24 27.15±8.33 0.030 0.976治疗后15.78±5.46 12.16±6.59 2.466 0.016 CA125(U/ml)治疗前72.06±20.15 72.27±22.14 0.041 0.967治疗后39.78±10.16 33.65±11.09 2.377 0.020 CA199治疗前55.12±16.33 55.87±16.25 0.190 0.850治疗后37.26±12.57 30.14±11.69 2.419 0.018
2.3 两组不良反应发生率比较观察组不良反应发生率略低于对照组,但无统计学意义(P>0.05)。见表3。

表3 两组不良反应发生率比较[n(%)]
2.4 两组免疫指标水平比较治疗前,两组免疫指标水平无显著差异(P>0.05);治疗后,观察组优于对照组(P<0.05)。见表4。
表4 两组免疫指标水平比较(±s)

表4 两组免疫指标水平比较(±s)
组别观察组对照组t P n 34 34 CD3+治疗前53.18±6.59 53.07±6.39 0.070 0.945治疗后63.41±6.22 54.86±5.42 6.043<0.01 t/p t=6.583,P<0.01 t=1.246,P=0.217 CD4+治疗前31.40±3.20 31.28±3.14 0.156 0.876治疗后38.33±4.14 33.28±2.07 6.362<0.01 t/p 7.723/0.01 3.10/0.01组别观察组对照组t P n 34 34 CD8+治疗前29.15±3.27 29.36±3.19 0.268 0.790治疗后25.08±4.27 28.01±4.35 2.803 0.007 t/p t=4.413,P<0.01 t=1.459,P=0.149 CD4+/CD8+治疗前0.94±0.21 0.91±0.17 0.647 0.520治疗后1.65±0.33 1.11±0.25 7.606<0.01 t/p 0.584,/0.01 3.857/0.01
3 讨论
随着我国人民对健康的重视度不断提升,加之医学技术的发展,临床治疗早期非小细胞肺癌的措施不断完善,尽可能保留肺组织,保障患者的生命安全[6-7]。实施传统开胸肺叶切除术,虽能使患者的病情得到改善,延长生命,但具有较大创伤,术后疼痛感强,且多并发症,因此对患者的生活造成严重影响,甚至部分无法忍受疼痛或体质较差的患者无法实施该方式治疗[8-9]。
临床在治疗晚期非小细胞肺癌时,化疗属于常见措施,但效果不理想,晚期非小细胞肺癌患者在治疗后,仅可存活5~6个月[10]。患者在患病后会抑制免疫功能,若患者本身免疫较差,便会产生免疫漂移:患者免疫力下降,抗肿瘤免疫遭到扰乱。机体免疫防御主要依赖T细胞亚群,且内免疫也是辅助和抑制相互组成的[11]。在查阅当前的研究文献资料可知,晚期非小细胞肺癌患者大多数T细胞亚群都会出现异常,如比例失调等情况,且患者癌症程度会影响CD4+与CD8+比值,因此若患者该比值显著降低,则其可能处于晚期,患者细胞免疫无法正常运行,产生肿瘤转移问题。在采取紫杉醇联合卡铂治疗后,能进行CK细胞培养,提高对肿瘤细胞的杀伤力,并产生炎性细胞,对肿瘤细胞进行间接性杀伤,且可以对T细胞增殖进行刺激,提高抗肿瘤效果。
紫杉醇作为一种半合成的紫杉醇类细胞毒性药物,其对微管具有较强的稳定作用,可以对有丝分裂期进行作用,从而对肿瘤细胞的分裂进行抑制。紫杉醇对于癌细胞的杀伤作用主要取决于药物浓度,在进行治疗时,药物浓度较高,因此杀死癌细胞的作用较强,且其属于非水溶性的高分子化合物,所以并不容易被血管吸收,在患者体内滞留时间较长。另外,紫杉醇较难在水中融化,所以需要将其放置在乙醇或聚氧乙基蓖麻油混合溶媒之中,而聚氧乙基蓖麻油在进入人体后会出现组胺,患者从而可能会出现一定的过敏性反应。因此在利用紫杉醇对患者进行治疗之前,为保障患者的安全性,降低其出现过敏的概率,需利用地塞米松等对患者实施预处理。
白蛋白结合型紫杉醇利用人血清白蛋白作为载体,利用高压均质技术,将紫杉醇与人血清白蛋白相结合,成为紫杉醇结合白蛋白纳米颗粒。因此在将白蛋白结合型紫杉醇注入患者血液后,会快速分散为体积较小的白蛋白紫杉醇结合物,能活化血管内皮细胞上的白蛋白受体,利用胞吞转运作用,运送到肿瘤细胞间质处。因此采取白蛋白结合型紫杉醇可以有效将药物浓度集中在肿瘤组织处,更好地增加疗效,减少对正常组织的损伤。而白蛋白结合性紫杉醇正好将紫杉醇在治疗中的不足进行有效改善,临床效果较佳的同时,毒性更低。白蛋白结合性紫杉醇是将人血白蛋白作为药物载体,是一种结合型紫杉醇颗粒,其能对细胞膜上的小窝蛋白进行激活,并利用机体内的血管内皮细胞,将紫杉醇逐步向患者肿瘤组织中进行转移。除此之外,通过使用白蛋白结合型紫杉醇还能使患者体内的细胞杀伤效应及抗体依赖的细胞杀伤效应进行激发,从而间接发挥出抗肿瘤的实际作用。因此使用白蛋白结合型紫杉醇可以有效地对细胞增殖、浸润及转移进行阻断,抑制血管的形成。将癌细胞的血供进行限制,将血管的通透性进行增加,从而使化疗药物的运输性有所加快,使患者肿瘤内皮细胞的凋零能有所加快。
由此可见,白蛋白结合型紫杉醇与卡铂治疗晚期非小细胞肺癌,效果较为理想,可以降低患者的疼痛感,对患者的生活质量进行改善,值得推广。

