未足月胎膜早破不同处理方法对产妇及新生儿预后的影响观察
徐曼
山东省郓城县人民医院,山东 菏泽 274700
0 引言
未足月胎膜早破(preterm premature rupture of membranes,PPROM)是指孕周少于37周的胎膜破裂。PPROM是一种对母亲和婴儿危害极大的妊娠并发症,发生率为5%~9%,而且40%的早产儿由PPROM引起的[1]。一旦发生胎膜早破,将直接引发羊水减少、宫内感染和早产现象,使围产期婴儿死亡率显著增加。此外,60%的患者将在7天内开始分娩[2]。所以,及时诊断胎膜早破患者,选择合适的治疗方法和治疗措施是非常重要的。临床妇科学认定产妇孕周超过34周时,产妇体内胎儿肺功能已发育完善,因此,早产婴儿围产期病死率低[3]。基于此,孕周大于34周,且发生胎膜早破,医师可予以妊娠终止,以此降低母婴风险。但如果产妇胎膜早破时孕周小于34周,则需要先进行促胎儿肺成熟治疗,才能终止妊娠,现阶段临床关于以上两种理念,仍存在争议[4]。胎膜早破在目前临床上属于较为常见的产科合并症,这种疾病的临床发病率整体来说较高,此时胎膜屏障已经失效,发生胎膜早破,会增加产妇生后羊膜感染、新生儿感染风险,带来不良妊娠结局,因此,临床应根据产妇实际症状、胎儿发育情况,予妊娠终止处理,破膜后积极采取有效感染预防措施,这样才能保障患者的康复。基于此,本文深入研究对于未足月胎膜早破者实施不同处理方法对产妇及以新生儿预后的影响,具体表述如下。
1 资料与方法
1.1 一般资料
抽取2017年5月-2020年5月本院收治的130例未足月胎膜早破患者为研究对象,将孕31~33周、33~35周、小于孕36周的未足月胎膜早破患者按照不同处理方式分为终止组与保胎组,每组65例患者,终止组患者年龄21~36岁,平均(29.8±5.6)岁,入院时的体质量50~72kg;保胎组患者年龄22~37岁,平均(28.7±6.5)岁,入院时的体质量55~74kg。胎膜早破的具体临床诊断方法如下:产妇阴道分泌物较多,用pH试纸检验后,试纸变色,行阴道涂片检查,镜下可见羊齿植物叶片状结晶,行腹部超声检测,提示产妇羊水量下降。
本研究流程和内容交由院内经伦理机构审核,委员会批准后,产妇和家属共同签署知情同意书,组间研究对象资料对比无差异(P>0.05),有可比性。
1.2 方法
所有入选产妇在入院后,应立即接受相关对症治疗,并嘱其绝对卧床休息,每日定期清洁生殖器官,予消毒清洗处理。使用腹部B超检查产妇及胎儿情况,预测胎儿体重。孕34周以内的患者使用宫缩抑制剂和糖皮质激素展开治疗,若有感染或者无感染但是破膜时间超过6h的患者,应该使用抗生素预防和控制感染。如果孕周超过34周,不常规使用抑制剂和糖皮质激素,抗生素的使用方式与34周以下的待产孕妇相同。在此期间,动态化观察产妇生命体征羊水流出量、气味、性质和状态,检测血常规指标,监测胎儿基础生命体征。动态化地掌握母婴情况,预防和控制宫内感染的发生。医务人员严密监测产妇的生命体征,并详细记载,尤其是胎膜早破的产妇,有可能会出现宫腔感染,医务人员需要密切监护患者的生命体征变化状况,如果发现患者的体征突然增加至37.5℃以上,则需要立即告知医师,基于患者对应的抗感染治疗。在开展日常治疗时,医务人员还需要告知患者保持会阴部位清洁的重要性,定期应用0.5%的碘伏对患者的外阴进行擦洗消毒,尽可能减少对患者阴道以及肛门的检查,避免出现阴道或者肛门感染的情况。而在进行胎膜早破生理治疗时,由于产妇的状态较差,部分产妇可能存在其他的并发症,故而需要做好产妇的具体状况分析,合理将个性化治疗与精细化治疗进行配合,才能够保障产妇的康复质量。在对患者进行治疗时,医务人员应当指导产妇保持良好的休养,医务人员需定期协助患者翻身,指导患者在床上进行小辅助的肢体运动,告知患者在咳嗽时应当避免过于用力。由于产妇长时间卧床可能会出现肠道蠕动,所以医务人员需指导产妇多进食清淡且易消化的食品,避免出现便秘,并告知产妇在排便时不要过于用力,避免宫腔压力增加。
1.3 评定标准
产褥感染标准:在生产24h后,10d内每间隔4h以上出现两次体温高于38℃,血白细胞计数大于20×109/L,使用抗生素药物效果明显,或产妇生后切口愈合不良,予术区分泌物培养,细菌培养结果为阳性。羊膜炎诊断标准:唯一确定指标为胎盘病理的检查结果。新生儿窒息标准:根据Apgar评分进行判定,生后5min评分低于或等于7分。肺炎诊断标准:婴儿出现呼吸急促、呼吸困难、呻吟以及发绀等,使用X线检查后,胸片呈现两侧肺纹理加粗,有明显的不规则斑片和粗大结节,合并肺不张、阻塞肺。重度脑损害诊断:新生儿产后1个月,身体发硬、发软、吸吮无力、头围形态异常、姿势固定、自发运动减少,以上症状至少持续4个月,或者研究期间不明原因死亡均提示为脑损害(重度)。研究过程应详细记录组间患者符合上述标准的具体例数,并计算发生率。
1.4 统计学方法
研究数据使用SPSS 19.0计算和统计软件,其统计的计数资料采用(%)表示,(χ2)进行数据检测校验;计量资料采用()表示,(t)对其进行数据校验。P<0.05表示差异存在统计学意义。
2 结果
2.1 孕31~33周的患者胎膜早破不同处理方法的对比
经过对比,终止组新生儿发生窒息、脑损的概率更大,产妇感染、发炎概率更低,组间差异均有统计学意义(P<0.05),详见表1。
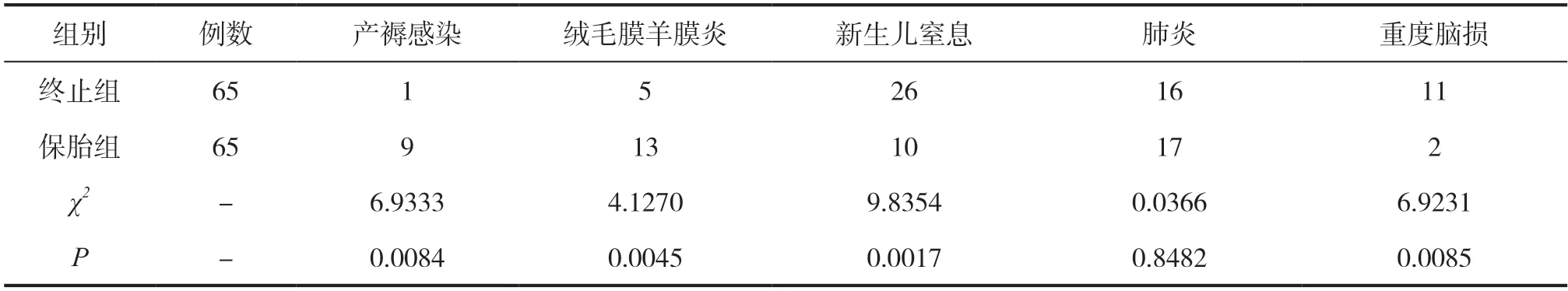
表1 两组患者胎膜早破不同处理方法的比较[n(%)]
2.2 孕33~35周患者胎膜早破不同处理方法的对比
对比后发现,终止组新生儿发生窒息的概率更大,产妇感染、发炎概率更低,组间差异均有统计学意义(P<0.05);新生儿发生肺炎、脑损的发生率对比无意义(P>0.05),详见表2。
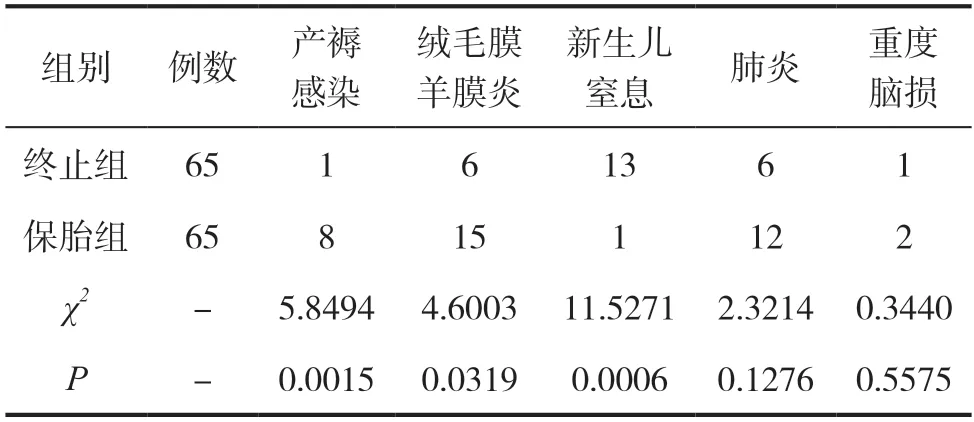
表2 两组患者胎膜早破不同处理方法的比较[n(%)]
3 讨论
据我国流行病学统计显示,未足月胎膜早破率在2.0%~3.5%之间。且产妇实际孕周越小,母婴围产期预后越差。产妇早产、母婴感染、婴儿脐带脱垂、胎盘早剥、胎膜早破等现象均是由未足月破膜导致的。分娩的孕周期越小,早产胎儿器官缺陷的预后越差。在综合性三甲医院产科中,未足月胎膜早破较为常见,其作为多发围生期疾病,疾病不可逆,诱发产妇早产[5]。早产儿胎龄较小,婴儿体内各项器官尚未发育成熟,生存能力较低下。因此,临床上针对该类型的产妇,应早期积极开展宫内感染疾病预防,尽可能延长产妇孕周[6]。此外,胎膜早破作为妊娠后期常见的不良并发症,伴随临床研究的不断深入,医学研究者发现疾病与产妇孕期发生的羊膜腔感染联系紧密。发生胎膜早破后,产妇胎膜将失去既有的保护屏障作用,病原菌可直接经宫颈口进入产妇阴道,最终到达羊膜腔,导诱发宫腔感染[7]。基于此,临床上应加强妊娠后期产妇体征和宫腔情况的监测,在患者胎膜相对完整时,及时采取保护措施,阻止羊膜腔感染。近年来,临床研究发现除了羊膜腔感染因素,胎膜早破还与其他因素有关,即感染因素[8]。细菌在阴道内持续存活,上行感染也会诱发胎膜早破,而这一现象在临床上并不罕见,产妇妊娠过程中受微生物影响,会产生大量的蛋白水解酶,降低胎膜抵抗力,增加胎膜早破风险[9]。
现阶段,胎膜早破临床治疗争议较少,普遍认为妊娠超33周,产妇发生胎膜早破,应主动终止妊娠;即使在低于33周的妊娠周期,羊膜腔感染,胎儿窘迫,脐带脱垂也明显存在,建议在终止妊娠的基础上尽量完成注射地塞米松(6mg/12h,总共4次),以促进胎儿肺成熟。然而,对于没有明显宫内感染迹象的胎膜早破、胎盘早剥、孕周小于34的胎儿窘迫处理仍有争议[10]。国内研究文献建议小于34周,可延长胎龄。建议观察母体内胎儿肺成熟,及时终止妊娠,其中,保胎药的使用只对肺成熟起促进作用[11-12]。
本次研究表明:产妇孕周为31~33周的,产妇各项数据经过对比,终止组新生儿发生窒息、脑损的概率更大,产妇感染、发炎概率更低,组间差异均存在统计学意义(P<0.05);对比后发现,产妇孕周33~35周的,终止组新生儿发生窒息的概率更大,产妇感染、发炎概率更低,组间差异存在统计学意义(P<0.05);新生儿发生肺炎、脑损的发生率对比无意义(P>0.05)。
综上所述,产妇指征为孕周≤31周,此时发生胎膜早破,应尽可能延长孕周,预防新生儿生后并发症,产妇指征为孕31~33周,应先予胎肺成熟促进治疗,后续治疗可顺其自然。

