植物根际土壤真菌Trichoderma velutinum的化学成分研究
旷敏,彭伟伟,许立,郑雨婷,桑子焕,秦思雨,邹振兴*(1.中南大学湘雅药学院,长沙 410013;2.慢病诊疗小分子药物发现与转化湖南省重点实验室,长沙 410013)
微生物代谢是发现天然活性产物的一大重要途径,目前为止,从微生物天然产物中分离出的具有生物活性的化合物有1 万多种[1-2]。其中,植物根际土壤真菌因其强大的次生代谢能力、潜在的物种多样性及便于发酵和遗传等优势,逐渐成为继植物内生真菌之后研究者们关注的焦点。植物根际土壤真菌是指生存于植物根系活动区域的真菌,它们同植物根系紧密联系,又广泛参与土壤生态中营养物质的循环,其代谢途径独特,能够产生结构新颖、生物活性显著的次生代谢产物[3]。据统计,植物根际土壤真菌目前研究偏重于农业应用,其化学成分研究存在较大的探索空间[4-5]。
木霉属真菌是普遍存在于土壤中的一种常见植物根际微生物。在自然界中,木霉属真菌多通过化学途径帮助植物抵抗虫害,具有强大的代谢能力。目前,木霉属真菌已被发现数百种次生代谢产物,主要包括萜类、环肽类、二酮哌嗪类、生物碱类及聚酮类化合物,且大多具有较好的抗肿瘤、抗菌等药理活性[6-7]。现有研究表明,木霉属真菌能产生众多结构独特的活性分子,具有极大的挖掘价值。本研究前期从药用植物根际土壤样本中分离筛选出一株木霉属真菌Trichoderma velutinum,化学丰度筛选显示其代谢产物丰富,且经文献调研发现Trichoderma velutinum的次级代谢产物成分研究稀少,因此,有必要对其化学成分进行深入探索。将其进行大规模固体发酵并用乙酸乙酯冷浸提取发酵产物,利用各色谱层析手段进一步分离纯化获得13 个化合物,其中包括4 个细胞松弛素、6 个二酮哌嗪、1 个N-acetyltryptamine 和2 个腺苷类化合物。化学结构如图1 所示。
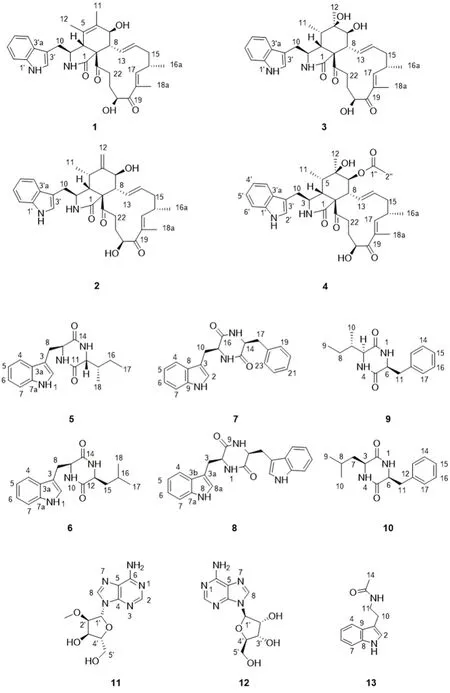
图1 化合物1 ~13 的结构Fig 1 Structures of compounds 1 ~13
1 材料
Agilent 1290 型高效液相色谱-Agilent 6500 series Q-TOF 质谱联用仪(美国安捷伦公司);Bruker AV-400/AV-500/AV-600 型核磁共振仪(德国Bruker 公司);Autopol IV-T 全自动旋光仪(美国鲁道夫公司);X-6 熔点测定仪(北京泰克仪器有限公司),安捷伦1100 半制备型液相色谱仪(美国安捷伦科技有限公司);高压灭菌锅(上海博迅实业有限公司医疗设备厂);ODS 反相C18填料(日本YMC 公司);Sephadex LH-20 葡聚糖凝胶(美国GE 公司);柱色谱硅胶(80 ~100 目、200 ~300 目、300 ~400 目,青岛海洋化工有限公司);大孔树脂(HPD-100 型大孔吸附树脂,沧州宝恩吸附材料科技有限公司);Innoval ODS-2半制备色谱柱(10 μm,10 mm×250 mm);旋转蒸发仪(上海亚荣生化仪器厂);二甲基亚砜(DMSO)、无水乙醇、甲醇、乙酸乙酯、石油醚、二氯甲烷试剂均为市售分析纯,乙腈为色谱纯。万古霉素(批号:V871983,规格:250 mg)、硫酸阿米卡星(批号:A837351,规格:1 g)(上海麦克林生化科技有限公司)。
本实验的真菌于2019年7月从湖南省江华县大玗镇长山村海拔520 m 的深绿卷柏根际土壤中分离得到,通过ITS 序列比对鉴定为Trichoderma velutinum,目前该菌株保存于中南大学湘雅药学院天然药物化学实验室。抗菌活性测试菌株来自于中南大学湘雅二医院,分别为大肠埃希菌ATCC25922、铜绿假单胞菌ATCC27853、金黄色葡萄球菌ATCC29213、粪肠球菌 ATCC29212。
2 方法与结果
2.1 菌株发酵
将菌株从-80℃冰箱的30%甘油水溶液中接种到PDA 培养基上复苏,再接种到4 L 灭菌液体培养基中,于28℃恒温摇床中以150 r·min-1震荡培养7 d,将此种子液倒入40 L 灭菌大米固体培养基中于室温下培养28 d。
2.2 发酵产物的分离纯化
采用乙酸乙酯将固体培养基浸泡提取3 次,减压浓缩得到浸膏78 g。首先通过大孔树脂层析将粗提物划分为20%乙醇、80%乙醇、100%乙醇3 个部位。选取80%馏分(30 g)通过硅胶柱层析(以石油醚-二氯甲烷-甲醇三相体系梯度洗脱)划分为5 个组分(Fr.1 ~Fr.5)。Fr.2 经过ODS 柱层析(以水-甲醇体系梯度洗脱),得到Fr.2.1 ~Fr.2.8,Fr.2.3 和Fr.2.4 经过Sephadex LH-20 柱色谱(以甲醇等度洗脱)得到化合物1(20.1 mg)、2(4.0 mg)、3(3.2 mg)和4(3.1 mg)。Fr.3 经过ODS 柱层析(以水-甲醇体系梯度洗脱),得到Fr.3.1 ~Fr.3.5。Fr.3.2 再通过小体积硅胶柱梯度洗脱得到Fr.3.2.2,再利用半制备型高效液相色谱(以纯水-乙腈为流动相)得到化合物5(2.1 mg)和6(3.0 mg)。Fr.3.3 经过Sephadex LH-20柱色谱[以二氯甲烷-甲醇(1∶9)等度洗脱]得到Fr.3.3.2,经过半制备型高效液相色谱(以纯水-乙腈为流动相)得到化合物7(2.2 mg)、8(2.0 mg)和13(5.7 mg)。Fr.3.4 经过Sephadex LH-20 柱色谱(以甲醇等度洗脱)得到Fr.3.4.3 和Fr.3.4.4,通过重结晶得到化合物9(1.4 mg)和10(1.5 mg)。Fr.4 经过反相硅胶柱层析,得到两个白色沉淀为化合物11(6.5 mg)和12(2.4 mg)。
2.3 结构鉴定
化合物1:白色粉末,易溶于DMSO,+150°(c0.10,MeOH),HR-ESI-MS 显示:m/z531.2857 [M +H]+,结合1H-NMR 和13C-NMR谱推测该化合物的分子式为C32H38N2O5;1H-NMR(600 MHz,DMSO-d6)δH:8.10(1H,s,NH-2),3.32(1H,m,H-3),2.79(1H,s,H-4),3.64(1H,m,H-7),4.50(1H,d,J=11.4 Hz,OH-7),1.97(1H,m,H-8),2.34(1H,m,H-10α),2.70(1H,m,H-10β),1.51(3H,s,H-11),1.10(3H,s,H-12),6.22(1H,dd,J=19.8,13.2 Hz,H-13),5.06(1H,m,H-14),2.36(1H,m,H-15α),1.97(1H,m,H-15β),2.70(1H,m,H-16),1.01(3H,d,J=9.6 Hz,C-16a),6.27(1H,d,J=14.4 Hz,H-17),1.71(3H,s,C-18a),4.76(1H,m,H-20),4.89(1H,d,J=9.6 Hz,OH-20),1.76(2H,m,H-21),2.70(1H,m,H-22α),2.93(1H,m,H-22β),10.92(1H,s,NH-1'),7.05(1H,s,H-2'),7.40(1H,d,J=12.0 Hz,H-4'),6.98(1H,t,J=11.4,10.8 Hz,H-5'),7.06(1H,t,J=10.2,8.4 Hz,H-6'),7.34(1H,d,J=12.6 Hz,H-7');13C-NMR(150 MHz,DMSO-d6)δC:173.9(C-1),57.1(C-3),49.3(C-4),125.5(C-5),133.5(C-6),67.7(C-7),50.9(C-8),61.6(C-9),31.9(C-10),14.7(C-11),16.2(C-12),128.5(C-13),133.4(C-14),40.7(C-15),32.9(C-16),19.8(C-16a),148.3(C-17),135.1(C-18),12.0(CH3-18a),204.1(C-19),70.1(C-20),30.5(C-21),36.5(C-22),210.3(C-23),136.2(C-1'),123.6(C-2'),109.9(C-3'),117.9(C-4'),118.5(C-5'),121.1(C-6'),111.6(C-7'),127.1(C-3'a)。 以上核磁及旋光数据与文献报道[8]基本一致,故鉴定化合物1 为chaetoglobosin E。
化合物2:白色粉末,易溶于甲醇,+60°(c0.10,MeOH),HR-ESI-MS 显 示:m/z531.2864 [M +H]+,结合1H-NMR 和13C-NMR谱推测该化合物的分子式为C32H38N2O5;1H-NMR(600 MHz,CD3OD)δH:3.45(1H,m,H-3),2.58(1H,m,H-4),2.54(1H,m,H-5),3.79(1H,d,J=10.8 Hz,H-7),1.85(1H,m,H-8),2.56(1H,m,H-10α),2.83(1H,m,H-10β),1.02(3H,d,J=6.6 Hz,H-11),5.06(1H,s,H-12α),5.24(1H,s,H-12β),6.05(1H,dd,J=17.4,9.6 Hz,H-13),5.18(1H,m,H-14),2.41(1H,m,H-15α),1.98(H,m,H-15β),2.84(1H,m,H-16),0.91(3H,d,J=4.8 Hz,H-16a),6.15(1H,d,J=9.6 Hz,H-17),1.78(3H,s,H-18a),4.63(1H,m,H-20),1.41(1H,m,H-21α),1.58(1H,m,H-21β),2.76(2H,m,H-22),6.99(1H,s,H-2'),7.48(1H,d,J=7.8 Hz,H-4'),7.02(1H,t,J=6.6 Hz,H-5'),7.08(1H,t,J=6.6 Hz,H-6'),7.33(1H,d,J=7.8 Hz,H-7');13C-NMR(150 MHz,CD3OD)δC:176.8(C-1),54.2(C-3),48.2(C-4),34.7(C-5),150.2(C-6),71.9(C-7),50.5(C-8),64.3(C-9),32.8(C-10),13.9(C-11),114.4(C-12),129.3(C-13),136.8(C-14),42.2(C-15),33.3(C-16),12.5(C-16a),151.2(C-17),135.8(C-18),20.3(C-18a),205.8(C-19),72.3(C-20),31.6(C-21),38.2(C-22),210.6(C-23),138.0(C-1'),125.6(C-2'),110.4(C-3'),119.4(C-4'),120.3(C-5'),122.6(C-6'),112.7(C-7'),129.3(C-3'a)。以上核磁及旋光数据与文献报道[9]基本一致,故鉴定化合物2 为chaetoglobosin Fex。
化合物3:白色粉末,易溶于甲醇,-15.0° (c0.53,MeOH),HR-ESI-MS 显示:m/z549.2967 [M+H]+,结合1H-NMR 和13C-NMR 谱推测该化合物的分子式为C32H40N2O6;1H-NMR(600 MHz,CD3OD)δH:3.81(1H,dd,J=9.0,4.8 Hz,H-3),2.50(1H,m,H-4),2.03(1H,m,H-5),3.16(1H,d,J=12.0 Hz,H-7),2.63(1H,dd,J=12.0,10.2 Hz,H-8),2.80(1H,dd,J=14.4,4.8 Hz,H-10α),2.97(1H,dd,J=14.4,4.8 Hz,H-10β),1.03(3H,d,J=7.2 Hz,H-11),1.22(3H,s,H-12),5.95(1H,dd,J=16.2,10.2 Hz,H-13),5.12(1H,dt,J=15.6,10.8,2.4 Hz,H-14),2.41(1H,m,H-15α),1.99(1H,m,H-15β),2.75(1H,m,H-16),1.02(3H,d,J=7.2 Hz,H-16a),6.19(1H,d,J=9.6 Hz,H-17),1.77(3H,s,H-18a),4.66(1H,dd,J=6.6 Hz,4.8 Hz,H-20),1.89(1H,s,OH-20),1.36(1H,m,H-21α),1.60(1H,m,H-21β),1.83(1H,m,H-22α),2.50(1H,m,H-22β),7.03(1H,s,H-2'),7.50(1H,d,J=7.8 Hz,H-4'),7.03(1H,t,J=7.2 Hz,H-5'),7.08(1H,t,J=7.8 Hz,H-6'),7.33(1H,d,J=7.2 Hz,H-7');13C-NMR(150 MHz,CD3OD)δC:176.9(C-1),54.5(C-3),45.9(C-4),40.2(C-5),74.2(C-6),73.7(C-7),47.4(C-8),65.8(C-9),33.5(C-10),13.6(C-11),24.9(C-12),129.4(C-13),135.1(C-14),42.1(C-15),34.7(C-16),20.3(C-16a),150.1(C-17),136.5(C-18),12.5(C-18a),205.8(C-19),72.6(C-20),31.9(C-21),38.7(C-22),210.1(C-23),138.1(C-1'),125.8(C-2'),110.0(C-3'),119.4(C-4'),120.3(C-5'),122.7(C-6'),112.7(C-7'),129.6(C-3'a)。以上核磁及旋光数据与文献报道[10]基本一致,故鉴定化合物3 为armochaetoglobin S。
化合物4:白色粉末,易溶于甲醇,+14.5° (c0.34,MeOH),HR-ESI-MS 显示:m/z591.3073 [M +H]+,结合1H-NMR 和13C-NMR 谱推测该化合物的分子式为C34H42N2O7;1H-NMR(600 MHz,CD3OD)δH:3.78(1H,m,H-3),2.76(1H,m,H-4),1.98(1H,m,H-5),4.74(1H,d,J=12.0 Hz,H-7),2.91(1H,m,H-8),2.83(1H,dd,J=14.4,5.4 Hz,H-10α),2.86(1H,dd,J=14.4,4.8 Hz,H-10β),1.03(3H,d,J=7.8 Hz,H-11),1.15(3H,s,H-12),5.98(1H,m,H-13),5.16(1H,dt,J=15.6,10.8,3.0 Hz,H-14),2.34(1H,m,H-15α),1.97(1H,m,H-15β),2.76(1H,m,H-16),1.02(3H,d,J=7.2 Hz,H-16a),6.21(1H,d,J=9.0 Hz,H-17),1.77(3H,s,H-18a),4.71(1H,t,J=5.4 Hz,H-20),1.46(1H,m,H-21α),1.68(1H,m,H-21β),2.64(1H,m,H-22α),2.92(1H,m,H-22β),7.06(1H,s,H-2'),7.51(1H,d,J=7.8 Hz,H-4'),7.02(1H,t,J=7.2 Hz,H-5'),7.09(1H,t,J=7.2 Hz,H-6'),7.33(1H,d,J=7.8 Hz,H-7'),1.98(3H,s,H-2'');13C-NMR(150 MHz,CD3OD)δC:176.4(C-1),55.3(C-3),44.9(C-4),41.9(C-5),73.9(C-6),75.0(C-7),46.2(C-8),65.2(C-9),33.0(C-10),13.4(C-11),24.9(C-12),128.6(C-13),135.5(C-14),41.9(C-15),34.6(C-16),20.2(C-16a),150.0(C-17),136.4(C-18),12.4(C-18a),205.6(C-19),72.7(C-20),32.3(C-21),38.9(C-22),210.3(C-23),138.1(C-1'),125.5(C-2'),110.5(C-3'),119.4(C-4'),120.2(C-5'),122.3(C-6'),112.6(C-7'),129.2(C-3'a),172.5(C-1''),21.0(C-2'')。 以上核磁及旋光数据与文献报道[10]基本一致,故鉴定化合物4 为7-O-acetylarmochaetoglobin S。
化合物5:白色粉末,易溶于甲醇,+77.3° (c0.50,EtOH),HR-ESI-MS 显示:m/z300.1717 [M +H]+,结合1H-NMR 和13C-NMR 谱推测该化合物的分子式为C17H21N3O2;1H-NMR(600 MHz,CD3OD)δH:7.07(1H,s,H-2),7.31(1H,d,J=10.2 Hz,H-4),6.99(1H,t,J=8.4 Hz,H-5),7.06(1H,t,J=8.4 Hz,H-6),7.61(1H,d,J=9.6 Hz,H-7),3.21(1H,dd,J=17.4,4.8 Hz,H-8α),3.42(1H,dd,J=18.0,6.0 Hz,H-8β),4.31(1H,dd,J=5.4,1.8 Hz,H-9),3.63(1H,dd,J=5.4,2.4 Hz,H-12),1.22(1H,m,H-15),0.38(1H,m,H-16α),0.55(1H,m,H-16β),0.52(3H,t,J=7.8 Hz,H-17),0.60(3H,d,J=8.4 Hz,H-18);13C-NMR(150 MHz,CD3OD)δC:125.9(C-2),109.9(C-3),129.6(C-3a),120.1(C-4),120.2(C-5),122.6(C-6),138.2(C-7),112.6(C-7a),40.1(C-8),57.5(C-9),169.3(C-11),61.1(C-12),170.2(C-14),30.4(C-15),24.5(C-16),11.9(C-17),15.3(C-18)。以上核磁与旋光数据与文献报道[11]基本一致,故鉴定化合物5 为cyclo-(L-Trp-D-Ile)。
化合物6:白色粉末,易溶于甲醇,-10.6° (c0.14,MeOH),HR-ESI-MS 显示:m/z300.1716 [M +H]+,结合1H-NMR 和13C-NMR 谱推测该化合物的分子式为C17H21N3O2;1H-NMR(600 MHz,CD3OD)δH:7.06(1H,s,H-2),7.31(1H,d,J=7.8 Hz,H-4),6.99(1H,t,J=16.8 Hz,7.2Hz,H-5),7.07(1H,t,J=16.8,7.2 Hz,H-6),7.59(1H,d,J=7.8 Hz,H-7),3.11(1H,dd,J=14.4,4.2 Hz,H-8α),3.48(1H,dd,J=14.4,3.6 Hz,H-8β),4.27(1H,dd,J=4.2,3.6 Hz,H-9),3.57(1H,dd,J=10.2,4.8 Hz,H-12),0.17(1H,ddd,J=13.8,10.2,4.8 Hz,H-15α),0.66(1H,ddd,J=13.8,9.6,4.2 Hz,H-15β),1.14(1H,m,H-16),0.46(3H,d,J=6.6 Hz,H-17),0.60(3H,d,J=6.6 Hz,H-18);13C-NMR(150 MHz,CD3OD)δC:126.0(C-2),109.6(C-3),129.4(C-3a),120.2(C-4),120.3(C-5),122.6(C-6),137.9(C-7),112.6(C-7a),45.2(C-8),54.3(C-9),170.0(C-11),57.6(C-12),170.7(C-14),24.7(C-15),30.8(C-16),21.4(C-17),23.4(C-18)。以上核磁与旋光数据与文献报道[12]基本一致,故鉴定化合物6 为cyclo-(L-Trp-L-Leu)。
化合物7:白色针晶,易溶于DMSO,-249.5°(c1.00,MeOH),mp:281 ℃,HR-ESI-MS显示:m/z334.1560 [M +H]+, 结合1H-NMR和13C-NMR 谱推测该化合物的分子式为C20H19N3O2;1H-NMR(600 MHz,DMSO-d6)δH:10.89(1H,s,H-1),6.96(1H,s,H-2),7.48(1H,d,J=8.4 Hz,H-4),6.98(1H,t,J=7.8 Hz,H-5),7.08(1H,t,J=7.2 Hz,H-6),7.32(1H,d,J=8.4 Hz,H-7),2.52(1H,dd,J=14.4,5.4 Hz,H-10α),2.81(1H,dd,J=14.4,4.2 Hz,H-10β),3.98(1H,m,H-11),7.92(1H,s,H-12),3.89(1H,m,H-14),7.70(1H,s,H-15),2.45(1H,dd,J=13.2,4.8 Hz,H-17α),1.83(1H,dd,J=13.2,7.2 Hz,H-17β),7.16(1H,m,H-19),6.70(1H,m,H-20),7.17(1H,m,H-21),6.70(1H,m,H-22),7.16(1H,m,H-23);13C-NMR(150 MHz,DMSO-d6)δC:120.9(C-2),108.8(C-3),118.5(C-4),118.8(C-5),124.5(C-6),111.4(C-7),127.6(C-8),136.1(C-9),29.7(C-10),55.3(C-11),166.3(C-13),55.7(C-14),170.0(C-15),166.9(C-16),39.9(C-17),136.5(C-18),128.1(C-19),129.8(C-20),126.5(C-21),129.8(C-22),128.1(C-23)。以上核磁与旋光数据与文献报道[13]基本一致,故鉴定化合物7 为cyclo-(L-Trp-L-Phe)。
化合物8:白色簇晶,易溶于甲醇,-108° (c0.30,MeOH),mp:242 ℃,HR-ESI-MS 显示:m/z373.1669 [M +H]+,结合1H-NMR 和13C-NMR谱推测该化合物的分子式为C22H20N4O2;1H-NMR(600 MHz,CD3OD)δH:4.06(1H,dd,J=7.2,4.2 Hz,H-2),2.18(1H,dd,J=14.4,7.2 Hz,H-3α),2.92(1H,dd,J=14.4,4.2 Hz,H-3β),7.44(1H,d,J=7.8 Hz,H-4),7.02(1H,t,J=7.2 Hz,H-5),7.10(1H,t,J=7.2 Hz,H-6),7.31(1H,d,J=8.4 Hz,H-7),6.48(1H,s,H-8a);13C-NMR(150 MHz,CD3OD)δC:57.0(C-2),31.5(C-3),109.5(C-3a),128.7(C-3b),119.8(C-4),120.2(C-5),122.7(C-6),112.6(C-7),138.2(C-7a),126.1(C-8a),169.9(C-9)。以上核磁与旋光数据与文献报道[14]基本一致,故鉴定化合物8 为cyclo-(L-Trp-L-Trp)。
化合物9:白色针晶,易溶于DMSO,HRESI-MS 显示:m/z261.1611 [M +H]+, 结合1H-NMR 和13C-NMR 谱推测该化合物的分子式为C15H20N2O2;1H-NMR(600 MHz,DMSO-d6)δH:8.10(1H,s,NH-1),3.57(1H,m,H-3),7.88(1H,s,NH-4),4.20(1H,m,H-6),1.39(1H,m,H-7),0.59(1H,m,H-8α),0.56(1H,m,H-8β),0.56(3H,m,H-9),0.54(3H,d,J=7.2 Hz,H-10),2.84(1H,dd,J=13.8,5.4 Hz,H-11α),3.16(1H,dd,J=13.8,4.2 Hz,H-11β),7.17 ~7.23(1H,m,H-13),7.17~7.23(1H,m,H-14),7.17~7.23(1H,m,H-15),7.17 ~7.23(1H,m,H-16),7.17 ~7.23(1H,m,H-17);13C-NMR(150 MHz,DMSO-d6)δC:166.4(C-2),58.7(C-3),166.3(C-5),55.0(C-6),37.8(C-7),23.1(C-8),11.8(C-9),14.4(C-10),37.6(C-11),136.3(C-12),130.4(C-13),127.9(C-14),126.5(C-15),127.9(C-16),130.4(C-17)。以上核磁数据与文献报道[15]基本一致,故鉴定化合物9 为cyclo-(L-Ile-L-Phe)。
化合物10:白色针晶,易溶于DMSO, -29.8°(c0.10,MeOH),mp:284 ℃,HR-ESI-MS 显示:m/z261.1605 [M +H]+, 结合1H-NMR 和13C-NMR 谱推测该化合物的分子式为C15H20N2O2;1H-NMR(600 MHz,DMSO-d6)δH:8.11(1H,s,NH-1),3.46(1H,m,H-3),8.08(1H,s,NH-4),4.17(1H,m,H-6),0.09(1H,m,H-7α),0.73(1H,m,H-7β),1.40(1H,m,H-8),0.62(3H,d,J=6.6 Hz,H-9),0.59(3H,d,J=6.6 Hz,H-10),2.84(1H,dd,J=13.2,4.8 Hz,H-11α),3.13(1H,dd,J=13.2,3.6 Hz,H-11β),7.12 ~7.28(1H,m,H-13),7.12~7.28(1H,m,H-14),7.12~7.28(1H,m,H-15),7.12 ~7.28(1H,m,H-16),7.12 ~7.28(1H,m,H-17);13C-NMR(150 MHz,DMSO-d6)δC:167.6(C-2),55.5(C-3),166.3(C-5),52.3(C-6),43.7(C-7),22.9(C-8),22.8(C-9),21.4(C-10),38.5(C-11),136.3(C-12),130.5(C-13),128.2(C-14),126.8(C-15),128.2(C-16),130.5(C-17)。以上核磁与旋光数据与文献报道[16]基本一致,故鉴定化合物10 为Cyclo-(L-Leu-L-Phe)。
化合物11:白色粉末,易溶于DMSO,HR-ESIMS 显示:m/z282.1209 [M +H]+,结合1H-NMR和13C-NMR 谱推测该化合物的分子式为C11H15N5O4;1H-NMR(600 MHz,DMSO-d6)δH:8.39(1H,s,H-2),8.14(1H,s,H-8),6.00(1H,d,J=5.4 Hz,H-1'),4.34(1H,m,H-2'),4.36(1H,m,H-3'),3.98(1H,m,H-4'),3.66(1H,dd,J=12,3.6 Hz,H-5'α),3.57(1H,dd,J=12,3.6 Hz,H-5'β),3.30(3H,s,O-CH3),7.35(1H,s,NH2-6);13C-NMR(150 MHz,DMSO-d6)δC:139.7(C-2),149.0(C-4),119.3(C-5),156.2(C-6),152.6(C-8),82.5(C-1'),85.8(C-2'),68.8(C-3'),86.5(C-4'),61.5(C-5'),57.5(OCH3)。以上核磁数据与文献报道[17]基本一致,故鉴定化合物11 为2'-O-methyladenosine。
化合物12:白色粉末,易溶于DMSO,HRESI-MS 显示:m/z268.1053 [M +H]+, 结合1H-NMR 和13C-NMR 谱推测该化合物的分子式为C10H13N5O4;1H-NMR(600 MHz,DMSO-d6)δH:8.16(1H,s,H-2),8.37(1H,s,H-8),5.90(1H,d,J=6.0 Hz,H-1'),4.63(1H,m,H-2'),4.17(1H,m,H-3'),3.99(1H,m,H-4'),3.58(1H,m,H-5'α),3.69(1H,m,H-5'β),7.38(2H,s,NH2-6),5.25(1H,s,OH-5'),5.47(1H,s,OH-2'),5.50(1H,s,OH-3');13C-NMR(150 MHz,DMSO-d6)δC:152.5(C-2),149.1(C-4),119.5(C-5),156.2(C-6),139.6(C-8),88.0(C-1'),73.6(C-2'),70.8(C-3'),86.1(C-4'),61.8(C-5')。以上核磁数据与文献报道[18]基本一致,故鉴定化合物12 为β-adenosine。
化合物13:黄色油状物,易溶于甲醇,HRESI-MS 显示:m/z203.1188 [M +H]+, 结合1H-NMR 和13C-NMR 谱推测该化合物的分子式为C12H14N2O;1H-NMR(600 MHz,CD3OD)δH:6.91(1H,s,C-2),7.55(1H,d,J=7.8 Hz,C-4),7.08(1H,t,J=7.2 Hz,C-5),6.99(1H,t,J=7.2 Hz,C-6),7.31(1H,d,J=7.8 Hz,C-7),3.46(2H,t,J=7.2 Hz,C-10),2.93(2H,t,J=6.6 Hz,C-11),1.91(3H,s,C-14);13C-NMR(150 MHz,CD3OD)δC:122.4(C-2),113.4(C-3),119.4(C-4),119.7(C-5),123.5(C-6),112.4(C-7),138.3(C-8),128.9(C-9),26.3(C-10),41.7(C-11),173.4(C-13),22.7(C-14)。以上核磁数据与文献报道[19]基本一致,故鉴定化合物13 为N-acetyltryptamine。
2.4 抗菌活性评价
采用96 孔板倍比稀释法,分别制备金黄色葡萄球菌(Staphylococcus aureus)、粪肠球菌(Enterococcus faecalis)、铜绿假单孢菌(Pseudomonas aeruginosa)和大肠埃希菌(Escherichia coli)的悬浮液并稀释至1×106CFU·mL-1备用。将13 个样品用生物级DMSO 溶解制备成1024 μg·mL-1的母液,取母液置96 孔板第一孔并用肉汤稀释至128 μg·mL-1,倍比稀释后各孔质量浓度分别为128、64、32、16、8、4、2、0 μg·mL-1,再于每孔中加入菌液,使每孔最终质量浓度为64、32、16、8、4、2、1、0 μg·mL-1, 置于30℃恒温培养箱中培养8 h 并观察细菌生长情况。以盐酸万古霉素和硫酸阿卡米星为阳性对照,以同等浓度DMSO 作为阴性对照,目视观察法读取MIC值。结果表明化合物1 ~13 在质量浓度 64 μg·mL-1下对4 个测试菌株均未显示出抑制活性。
3 讨论
植物根际土壤真菌作为一类独特的微生物资源,参与植物体及周围生态的物质循环,植物根际分泌物及根际土壤能够为其提供充足碳源和可利用元素,同时根际土壤真菌大多能通过化学途径为植物体提供生物防治作用,因此其具有强大的产活性代谢产物的潜力。再者,植物根际土壤真菌物种多样,能提供丰富的研究资源,具备极大的研究前景。本研究从植物根际土壤真菌Trichoderma velutinum的代谢产物中分离得到13个化合物,其中化合物1 ~10 为首次从木霉属真菌中分离得到。虽然本研究中化合物1 ~13 对所测4 株致病菌均未表现出抑制作用,但经文献检索发现细胞松弛素类化合物1 ~3 对人前列腺癌细胞和小鼠黑色素瘤细胞具有较好的增殖抑制活性[20-22];二酮哌嗪化合物9 ~10 具有良好的抗炎活性[23]。本研究丰富了木霉属真菌化学成分多样性,可为土壤真菌资源的开发利用提供参考。

