薄叶卷柏内生真菌Clonostachys rogersoniana次生代谢产物研究
彭伟伟,旷敏,许立,郑雨婷,桑子焕,秦思雨,邹振兴*(1.中南大学湘雅药学院,长沙 410013;2.慢病诊疗小分子药物发现与转化湖南省重点实验室,长沙 410013)
内生真菌普遍存在于植物的内部组织中[1]。常见的内生真菌有助于植物克服非生物因素(高温和盐度、干旱、金属毒性和光)以及生物因素(草食动物、昆虫、线虫和病原体)的有害影响以更好地生存[2]。在植物内生真菌和植物宿主的共生环境中,内生真菌一方面从植物宿主吸收自己所需的营养物质,另一方面在代谢过程中产生一系列活性物质促进植物生长发育,使植物宿主抵抗外界不利影响[3]。这些次生代谢产物在医学和农业应用等方面有极大的价值[4]。然而,许多内生真菌种群在这方面仍未被研究,这意味着植物内生真菌仍然是值得我们继续探索,为寻找结构新颖、活性显著的天然产物的资源宝库。
薄叶卷柏(Selaginella delicatula)为卷柏科卷柏属植物,具有活血调血、清热解毒等功效。目前从该属植物中分离得到的化学成分超过300个[5],结构类型涉及双黄酮类[6]、木脂素类、生物碱类以及炔酚类[7]等,部分化合物表现出良好的生物活性,如细胞毒活性[8]、抗炎活性[9]、抗菌活性[10]以及抗氧化作用[11]等。然而目前针对该科属植物内生真菌的研究鲜有报道。课题组前期从薄叶卷柏根部分离筛选得到一株具有较好抗菌活性的内生真菌,经过ITS 鉴定该菌株为Clonostachys rogersoniana,其大米发酵粗提物对Staphylococcus aureus和MRSA(methicillinresistantStaphylococcus aureus)有较好的抑制活性(MIC值均为1 mg·mL-1)。为了挖掘Clonostachys rogersoniana的抗菌活性代谢产物,本研究进一步对其进行放大发酵,运用多种现代色谱和光谱技术,从中分离鉴定得到11 个单体化合物(结构式见图1)。
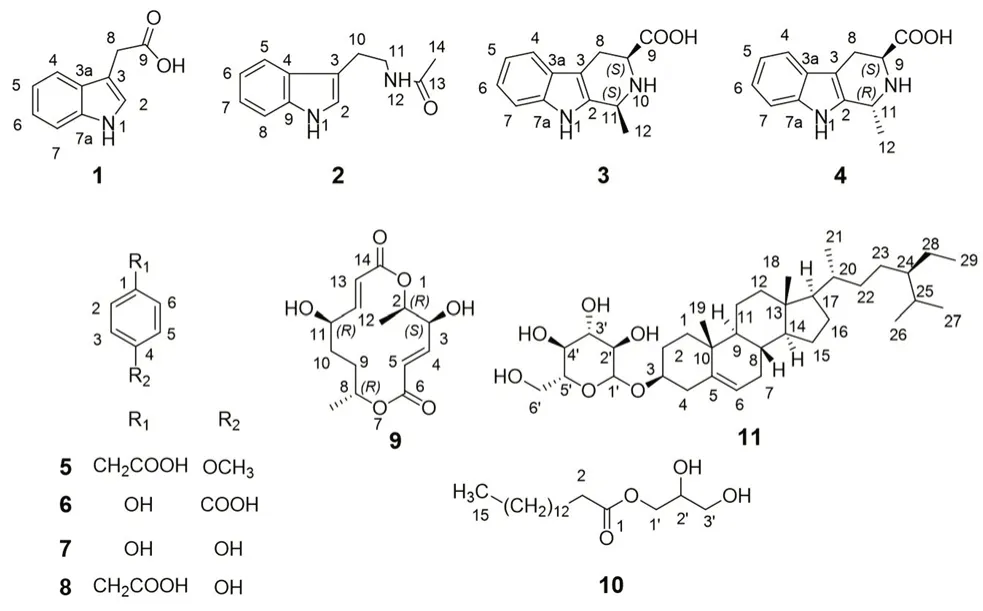
图1 化合物1 ~11 的化学结构Fig 1 Chemical structures of compounds 1 ~11
1 材料
Agilent 1290 型高效液相色谱-Agilent 6500 series Q-TOF 质谱联用仪、Agilent 1100 半制备型液相色谱仪(美国安捷伦公司);Bruker AV-400/AV-500/AV-600 型核磁共振仪(德国Bruker 公司);Agela Innoval ODS-2 半制备色谱柱(10 mm×250 mm,10 μm);安东帕旋光仪MCP 500(奥地利安东帕有限公司);SQP 电子分析天平(北京赛多利斯科学仪器有限公司);Sephadex LH-20 葡聚糖凝胶(美国GE 公司);ODS 反相C18填料(日本YMC 公司);80 ~100 目、200 ~300 目柱层析硅胶(青岛海洋化工有限公司);EYELAN-1100S-W旋转蒸发仪(日本东京理化器械株式会社);所用试剂均为分析纯。抗菌实验所用的细菌材料(Staphylococcus aureusATCC29213,Enterobacter faecalisATCC29212,Pseudomonas aeruginosaATCC27853 和Escherichia coliATCC25922)由中南大学湘雅二医院提供。万古霉素(批号:V871983,规格:250 mg)、硫酸阿米卡星(批号:A837351,规格:1 g)(上海麦克林生化科技有限公司)。
薄叶卷柏植株于2019年采摘自湖南省常德市石门县壶瓶山,由湘雅药学院徐康平副教授鉴定为卷柏属植物薄叶卷柏(Selaginella delicatula)。该实验菌株分离自薄叶卷柏根部,委托擎科生物有限公司进行ITS 测序,鉴定为粉红螺旋聚孢霉(Clonostachys rogersoniana)。目前菌种保存于中南大学湘雅药学院天然药物化学教研室(菌种保存编号为Clonostachys rogersonianaBYJB-1)。
2 方法与结果
2.1 菌株培养与发酵
将目标菌株接种至液体培养基中,置于恒温培养箱内摇床5 d(180 r·min-1,28℃),得到种子液,将种子液接种到500 mL 锥形瓶内(每瓶加入200 g 大米,200 mL 超纯水,于121 ℃高压蒸汽灭菌25 min 并冷却至室温),于28℃恒温条件下静置培养28 d。
2.2 发酵产物的分离纯化
Clonostachys rogersoniana的大米发酵物用乙酸乙酯浸提,提取3 次,每次2 d。合并提取液减压浓缩得到浸膏32 g,浸膏经硅胶柱层析(200 ~300 目),依次用石油醚-乙酸乙酯(1∶0、10∶1、5∶1、2∶1、1∶1、0∶1)、 乙酸乙酯-甲醇(100∶1 ~0∶1)梯度洗脱得到5个组分(Fr.1 ~Fr.5)。Fr.2(6.5 g)经反相柱层析,以甲醇-水(5∶95 ~100∶0)梯度洗脱得到8 个组分(Fr.2-1 ~Fr.2-8)。Fr.2-7 经过反复重结晶纯化得到化合物10(20.7 mg)。Fr.2-8 经过反复重结晶纯化得到化合物11(5.6 mg)。Fr.2-5 经Sephadex LH-20 凝胶柱层析,半制备型高效液相色谱(20%~50%乙腈洗脱30 min,2 mL·min-1)纯化得到化合物9(29.8 mg)。Fr.2-2 经Sephadex LH-20 凝胶柱层析,半制备型高效液相色谱(20%~30%乙腈洗脱40 min,2 mL·min-1)纯化得到化合物5(8.0 mg)、6(12.3 mg)、7(13.2 mg)和8(9.4 mg)。Fr.3(3.5 g)经反相柱层析,以甲醇-水(5∶95 ~100∶0)梯度洗脱得到6 个组分(Fr.3-1 ~Fr.3-6)。Fr.3-2 经Sephadex LH-20凝胶柱层析,半制备型高效液相色谱(15%~25%乙腈洗脱30 min,2 mL·min-1)纯化得到化合物1(4.7 mg)。Fr.3-3经Sephadex LH-20 凝胶柱层析,半制备型高效液相色谱(25%~35%乙腈洗脱30 min,2 mL·min-1)纯化得到化合物2(4.1 mg)、3(4.6 mg)和4(6.2 mg)。
2.3 结构确证
化合物1:白色粉末(甲醇),易溶于甲醇。HR-ESI-MS 显示m/z176.0715 [M +H]+,提示分子式为:C10H9NO2(calcd.for C10H10NO2,176.0712)。1H-NMR(500 MHz,DMSO-d6)δH:10.77(1H,s,-COOH),7.55(1H,d,J=8.0 Hz,H-4),7.31(1H,d,J=8.0 Hz,H-7),7.19(1H,s,H-2),7.02(1H,t,J=7.0 Hz,H-6),6.93(1H,t,J=7.0 Hz,H-5),3.44(2H,s,H-8);13C-NMR(125 MHz,DMSO-d6)δC:118.3(C-2),128.3(C-3),111.3(C-3a),119.6(C-4),120.1(C-5),123.7(C-6),111.5(C-7),136.5(C-7a),34.9(C-8),178.9(C-9)。以上数据与文献[12]报道基本一致,故鉴定为indole-3-acetic acid。
化合物2:黄色油状液体(甲醇),易溶于二氯甲烷和甲醇。HR-ESI-MS 显示m/z203.1176 [M +H]+,提示分子式为:C12H14N2O(calcd.for C12H15N2O,203.1184)。1H-NMR(600 MHz,DMSO-d6)δH:10.80(1H,s,H-1),7.93(1H,s,H-12),7.54(1H,d,J=7.8 Hz,H-4),7.32(1H,d,J=7.8 Hz,H-7),7.14(1H,s,H-2),7.06(1H,t,J=7.2 Hz,H-6),6.97(1H,t,J=7.2 Hz,H-5),3.30(2H,t,J=7.8 Hz,H-11),2.80(2H,t,J=7.8 Hz,H-10),1.80(3H,s,H-14);13C-NMR(150 MHz,DMSO-d6)δC:121.4(C-2),112.3(C-3),118.7(C-4),118.7(C-5),123.0(C-6),111.8(C-7),136.7(C-8),127.7(C-9),25.7(C-10),39.9(C-11),169.5(C-13),23.2(C-14)。以上数据与文献[13]报道基本一致,故鉴定为N-acetyltryptamine。
化合物3:黄色油状液体(甲醇),易溶于二氯甲烷和甲醇。HR-ESI-MS 显示m/z231.1135 [M +H]+,提示分子式为:C13H14N2O2(calcd.for C13H15N2O2,231.1134)。 - 108°(c0.3,MeOH)。1H-NMR(600 MHz,DMSO-d6)δH:11.02(1H,s,-COOH),7.43(1H,d,J=7.8 Hz,H-4),7.32(1H,d,J=7.8 Hz,H-7),7.07(1H,t,J=7.8 Hz,H-6),6.99(1H,t,J=7.8 Hz,H-5),3.54(1H,dd,J=4.8,12 Hz,H-8a),3.11(1H,dd,J=4.8,12 Hz,H-8b),4.45(1H,q,J=6.6 Hz,H-11),2.73(1H,t,J=12 Hz,H-9),1.58(3H,d,J=6.6 Hz,H-12);13C-NMR(150 MHz,DMSO-d6)δC:133.5(C-2),107.4(C-3),126.7(C-3a),118.4(C-4),119.2(C-5),121.7(C-6),111.6(C-7),136.8(C-7a),24.1(C-8),58.3(C-9),49.5(C-11),17.9(C-12),169.5(-COOH)。 以上NMR 及旋光数据与文献[14]报道基本一致,故鉴定为(1S,3S)-1-methyl-2,3,4,9-tetrahydro-1H-pyrido[3,4-b]indole-3-carboxylic acid。
化合物4:黄色油状液体(甲醇),易溶于二氯甲烷和甲醇。HR-ESI-MS 显示m/z231.1139 [M +H]+,提示分子式为:C13H14N2O2(calcd.for C13H15N2O2,231.1134)。 - 75°(c0.3,MeOH)。1H-NMR(600 MHz,DMSO-d6)δH:11.02(1H,s,-COOH),7.43(1H,d,J=7.8 Hz,H-4),7.32(1H,d,J=7.8 Hz,H-7),7.07(1H,t,J=7.8 Hz,H-6),6.99(1H,t,J=7.8 Hz,H-5),3.54(1H,dd,J=4.8,12 Hz,H-8a),3.11(1H,dd,J=4.8,12 Hz,H-8b),4.45(1H,q,J=6.6 Hz,H-11),2.73(1H,t,J=12 Hz,H-9),1.58(3H,d,J=6.6 Hz,H-12);13C-NMR(150 MHz,DMSO-d6)δC:133.5(C-2),107.4(C-3),126.7(C-3a),118.4(C-4),119.2(C-5),121.7(C-6),111.6(C-7),136.8(C-7a),24.1(C-8),53.4(C-9),46.7(C-11),17.9(C-12),170.5(-COOH)。 以上NMR 及旋光数据与文献[15]报道基本一致,故鉴定为(1R,3S)-1-methyl-2,3,4,9-tetrahydro-1H-pyrido[3,4-b]indole-3-carboxylic acid。
化合物5:白色粉末(甲醇),易溶于甲醇。HR-ESI-MS 显示m/z167.0708 [M +H]+,提示分子式为:C9H10O3(calcd.for C9H11O3,167.0708)。1H-NMR(400 MHz,DMSO-d6)δH:9.34(1H,s,-COOH),7.05(2H,d,J=8.4 Hz,H-2,6),6.71(2H,d,J=8.4 Hz,H-3,5),3.60(3H,s,-OCH3),3.53(2H,s,H-7);13C-NMR(150 MHz,DMSO-d6)δC:130.7(C-1),124.9(C-2/6),115.6(C-3/5),156.7(C-4),39.8(C-7),172.5(C-8),52.0(-OCH3)。以上数据与文献[16]报道基本一致,故鉴定为4-methoxyphenylacetic acid。
化合物6:白色粉末(甲醇),易溶于甲醇。HR-ESI-MS 显 示m/z139.0386 [M +H]+,提示分子式为:C7H6O3(calcd.for C7H7O3,139.0395)。1H-NMR(600 MHz,DMSO-d6)δH:7.78(2H,d,J=8.4 Hz,H-3/5),6.79(2H,d,J=7.8 Hz,H-2/6)。通过高分辨质谱分析,和对照品进行TLC 分析,以及和文献[17]氢谱数据对比,判断化合物6 为4-hydroxybenzoic acid。
化合物7:白色粉末(甲醇),易溶于甲醇。HR-ESI-MS 显示m/z111.0442 [M +H]+,提示分子式为:C6H6O2(calcd.for C6H7O2,111.0446)。1H-NMR(600 MHz,DMSO-d6)δH:7.04(2H,d,J=8.0 Hz,H-3/5),6.69(2H,d,J=7.6 Hz,H-2/6)。通过高分辨质谱分析,和对照品进行TLC 分析,以及和文献[18]氢谱数据对比,判断化合物7 为hydroquinone。
化合物8:白色粉末(甲醇),易溶于甲醇。HR-ESI-MS 显示m/z153.0549 [M +H]+,175.0365 [M +Na]+,170.0813 [M +NH4]+, 提示分子式为:C8H8O3(calcd.for C8H9O3,153.0552,C8H8O3Na,175.0371,C8H8O3NH4,170.0812)。1H-NMR(600 MHz,DMSO-d6)δH:7.04(2H,d,J=8.4 Hz,H-3/5),6.77(2H,d,J=8.0 Hz,H-2/6),3.44(2H,s,H-7)。通过高分辨质谱分析、与对照品进行TLC 对比分析以及与文献[19]氢谱数据对比分析,判断化合物8 为4-hydroxyphenylacetic acid。化合物9:白色粉末(甲醇),易溶于甲醇。HRESI-MS 显示m/z285.1349 [M +H]+,提示分子式为:C14H20O6(calcd.for C14H21O6,285.1338)。+103°(c0.1,MeOH)。1H-NMR(600 MHz,DMSO-d6)δH:6.67(1H,dd,J=4.2,15.6 Hz,H-12),6.48(1H,dd,J=8.4,15.6 Hz,H-4),5.92(1H,dd,J=1.2,16.2 Hz,H-5),5.78(1H,dd,J=1.8,16.2 Hz,H-13),5.69(1H,d,J=6.0 Hz,3-OH),5.05(1H,d,J=4.6 Hz,11-OH),5.02(1H,m,H-2),4.72(1H,m,H-11),4.46(1H,m,H-3),3.96(1H,m,H-8),1.82(1H,m,H-10a),1.57(1H,m,H-10b),1.44(2H,m,H-9),1.33(3H,d,J=6.6 Hz,H-15),1.13(3H,d,J=6.6 Hz,H-16);13C-NMR(150 MHz,DMSO-d6)δC:71.2(C-2),74.8(C-3),147.5(C-4),123.4(C-5),164.7(C-6),69.1(C-8),25.6(C-9),28.1(C-10),68.1(C-11),152.8(C-12),119.9(C-13),164.9(C-14),17.5(C-15),17.2(C-16)。以上NMR 及旋光数据与文献[20]报道基本一致,故鉴定为clonostachydiol。
化合物10:白色粉末(甲醇),易溶于甲醇。HR-ESI-MS 显示m/z317.2686 [M +H]+,提示分子式为:C18H36O4(calcd.for C18H37O4,317.2692)。1H-NMR(500 MHz,DMSO-d6)δH:0.86(3H,t,J=7.0 Hz,H-15),1.20~1.27(s,-CH2-),1.51(2H,m,H-3),2.28(2H,t,J=7.5 Hz,H-2),3.36(1H,m,H-3'b),3.62(1H,m,H-3'a),3.90(1H,m,H-1'b),4.03(1H,m,H-1'a),4.61(1H,m,H-2');13C-NMR(125 MHz,DMSO-d6)δC:172.9(C-1),33.5(C-2),24.4(C-3),28.5(C-4),28.7(C-5),28.9(C-6),29.0(C-7),29.0(C-8),29.0(C-9),29.1(C-10),29.3(C-11),32.3(C-12),32.3(C-13),22.1(C-14),13.9(C-15),65.5(C-1'),69.31(C-2'),62.6(C-3')。以上数据与文献[21]报道基本一致,故鉴定为2,3-dihydroxypropyl pentadecanoate。
化合物11:白色粉末(甲醇),易溶于二氯甲烷和甲醇。HR-ESI-MS 显示m/z577.4462 [M +H]+, 提示分子式为:C35H60O6(calcd.for C35H61O6,577.4468)。1H-NMR(500 MHz,DMSO-d6)δH:0.66(3H,s,H-18),0.80(3H,d,J=6.5 Hz,H-26),0.81(3H,d,J=6.5 Hz,H-27),0.83(3H,t,J=8.3 Hz,H-29),0.90(1H,m,H-9),0.92(3H,m,H-21),0.96(1H,m,H-24),1.03(1H,m,H-14),1.06(1H,m,H-22a),1.07(3H,s,H-19),1.04(1H,m,H-15a),1.09(1H,m,H-1a),1.12(1H,m,H-17),1.15(2H,m,H-23),1.19(1H,m,H-12a),1.21(2H,m,H-28),1.24(1H,m,H-16a),1.32(1H,m,H-22b),1.34(1H,m,H-20),1.43(1H,m,H-8),1.45(2H,m,H-11),1.53(1H,m,H-7a),1.57(1H,m,H-15b),1.59(1H,m,H-2a),1.64(1H,m,H-25),1.83(1H,m,H-16b),1.88(1H,m,H-1b),1.90(1H,m,H-2b),1.95(1H,m,H-7b),2.00(1H,m,H-12b),2.24(1H,m,H-4a),2.39(1H,m,H-4b),3.22(1H,t,J=8.3 Hz,H-20),3.27(1H,m,H-50),3.35(1H,m,H-40),3.38(1H,m,H-30),3.57(1H,m,H-3),3.70(1H,dd,J=12.0,5.1 Hz,H-6a),3.81(1H,dd,J=12.0,2.6 Hz,H-6b),4.38(1H,d,J=7.8 Hz,H-10),5.36(1H,m,H-6);13C-NMR(125 MHz,DMSO-d6)δC:36.8(C-1),29.3(C-2),76.8(C-3),38.1(C-4),140.5(C-5),121.2(C-6),31.4(C-7),31.4(C-8),49.6(C-9),36.2(C-10),20.6(C-11),38.3(C-12),41.9(C-13),56.2(C-14),23.9(C-15),27.8(C-16),55.4(C-17),11.7(C-18),19.1(C-19),35.5(C-20),18.6(C-21),33.3(C-22),25.4(C-23),45.1(C-24),28.7(C-25),19.7(C-26),18.9(C-27),22.6(C-28),11.8(C-29),100.8(C-1'),73.51(C-2'),76.8(C-3'),70.1(C-4'),76.8(C-5'),61.1(C-6')。以上数据与文献[22]报道基本一致,故鉴定为daucosterol。
2.4 抗菌活性评价
根据美国临床和实验室标准协会(CLSI)的M07-A9 方案,采用微量肉汤稀释法[23]测定单体化合物对4 种常见的临床致病菌(Staphylococcus aureus、Enterobacter faecalis、Pseudomonas aeruginosa和Escherichia coli)的体外抗菌活性。从新鲜的琼脂平板中选择3 ~5 个形态相同的供试菌菌落,转移到MHB(Mueller-Hinton Broth)培养基中,在225 r·min-1的摇瓶中以37℃的温度培养,使细菌悬浮液 ≥ 0.5 麦克法兰标准的浊度。对所制得的细菌悬浮液用含0.1 mg·mL-1刃天青的MHB 培养液稀释至约1×106CFU·mL-1菌液。用生物级DMSO 溶解单体化合物,配成母液质量浓度为1024 μg·mL-1。第一孔取25 μL 的母液,再取75 μL 肉汤,两者混匀至第一孔质量浓度为256 μg·mL-1;第二至第七孔依次从上一孔取50 μL 混合液和50 μL 肉汤逐级稀释至质量浓度为128、64、32、16、8、4 μg·mL-1,最后一孔加入肉汤50 μL,再向每一孔加入50 μL 菌液;最终每一孔质量浓度依次为128、64、32、16、8、4、2、0 μg·mL-1。同时设置万古霉素和硫酸阿米卡星为阳性对照,以DMSO 为溶剂对照。每组设3 次重复。96 孔培养板放置于37℃培养箱培养18 ~24 h。
抑菌实验结果显示化合物3 和4 对Staphylococcus aureus具有中等抑制活性(MIC值分别为16 和8 μg·mL-1)。化合物1 ~11 在最大质量浓度128 μg·mL-1下对Enterobacter faecalis、Pseudomonas aeruginosa和Escherichia coli均未显示出抑菌活性。
3 讨论
本文对薄叶卷柏内生真菌Clonostachys rogersoniana大米发酵物开展了较为系统的化学成分研究,共分离得到11 个化合物,包括4 个生物碱(1 ~4),4 个酚酸类化合物(5 ~8),1 个大环内酯(9),1 个脂肪酸类化合物(10)以及1 个甾体化合物(11)。对于化合物10,目前我们仅确定其平面结构。抗菌实验结果显示化合物3 和4 对Staphylococcus aureus具有中等抑制活性。本研究结果不仅丰富了菌株Clonostachys rogersoniana的化学成分多样性,亦为薄叶卷柏内生真菌的进一步开发利用提供了一定的实验依据。

