圈套器冷切除术与圈套器热切除术治疗直径4~9 mm无蒂结直肠息肉的疗效比较
季秋南 张继舜 袁志芳 段卓洋 尚占民
作者单位:100043 北京 首都医科大学附属北京朝阳医院西院区消化科
结直肠息肉指突出于结直肠管腔内的隆起性病变,一般来源于肠黏膜上皮,分为腺瘤性与非腺瘤性。大多数结直肠癌由腺瘤性息肉发展而来,因而腺瘤性息肉被认为是结直肠癌癌前病变[1]。结直肠癌是常见的消化道恶性肿瘤,我国结直肠癌发病率、死亡率在恶性肿瘤中均位居前5位[2]。结肠镜能发现并于内镜下切除息肉,已被广泛应用以降低结直肠癌的发生率及死亡率[3]。在临床工作中,内镜医师根据息肉大小、形态、发生部位以及病理组织学类型,选用不同的内镜下息肉切除方法。圈套器热切除术(hot snare polypectomy,HSP)为常用的息肉切除方法之一。近年来,圈套器冷切除术(cold snare polypectomy,CSP)因其操作便捷,出血、穿孔发生率低,同时可避免术后电凝综合征的发生,在日本和西方国家得到逐渐推广。欧洲胃肠内镜学会(European Society of Gastrointestinal Endoscopy,ESGE)指南建议采用CSP作为切除直径≤5 mm息肉的首选方法,同时提出活检钳息肉冷钳除术可用于治疗直径1~3 mm的息肉。同时因CSP操作安全性较高,ESGE还建议采用CSP治疗直径6~9 mm的无蒂结直肠息肉[4]。目前我国对于直径9 mm以下的无蒂结直肠息肉,使用何种切除方法尚无明确定论。因此,本研究拟对采用CSP及HSP治疗的直径4~9 mm无蒂结直肠息肉进行对比研究,以评估两种切除方法的治疗效果。
1 资料与方法
1.1 一般资料
选取2021年6月至2021年11月于首都医科大学附属北京朝阳医院西院区消化科接受CSP或HSP治疗结直肠息肉的患者为研究对象。患者纳入标准:⑴患者年龄18~80岁;⑵内镜检查中发现至少有1个直径4~9 mm无蒂结直肠息肉;⑶未服用抗血小板药物或抗凝药物,或已停用抗血小板药物或抗凝药物≥7 d。患者排除标准:⑴患有炎症性肠病、息肉病、息肉可疑癌变、消化道出血及肠道急性炎症;⑵患有可导致凝血功能异常的疾病,如肝硬化、血液系统疾病等;⑶正在服用抗血小板或抗凝药物或未按上述要求停药者。息肉纳入标准:⑴经CSP或HSP治疗的直径4~9 mm的结直肠息肉;⑵巴黎分型为Ⅰs型、Ⅰsp型、Ⅱa型的息肉。根据纳入和排除标准,本研究最终纳入145例应用CSP治疗的息肉(90例患者)及139例应用HSP治疗的息肉(97例患者)。本研究经本院伦理委员会批准。
1.2 器械及肠镜前准备
主要器械包括结肠镜(Olympus CF-HQ260/290),圈套器(南微医学,直径2.3 mm),注射治疗针(波士顿科学,M00518311),组织夹(南微医学)。患者于结肠镜检查前3 d开始进食少渣饮食,术前1 d 19:00开始服用聚乙二醇电解质散剂2袋(每袋溶于1 000 mL水),2 h内饮用完毕,检查当天6:00服用第3袋聚乙二醇电解质散剂,1 h内饮用完毕,7:00服用2盒二甲硅油散。患者或其家属签署结肠镜检查知情同意书。
1.3 操作方法
采用常规方法进行内镜检查,当内镜检查过程中发现目标息肉时,将活检钳张开以测量息肉的大小,同时以巴黎分型为标准定义息肉形态,经HSP或CSP切除息肉。部分HSP过程为先行黏膜下注射美兰生理盐水隆起息肉后,连接高频电切装置,用圈套器完整套取息肉,逐渐收紧套圈,经高频电切除。部分HSP过程为直接用圈套器完整套取息肉,逐渐收紧套圈,经高频电切除。CSP过程为应用圈套器完整套取息肉及周边部分正常黏膜,不使用黏膜下注射及电切,逐渐收紧圈套器将息肉机械切除。上述两种方法切除的息肉均被吸到吸引管与内镜连接处纱布以回收。
1.4 评价指标
主要终点为息肉完整切除率,完整切除定义为病理标本切缘干净。次要终点为标本回收率、操作时间、治疗费用及住院时间。标本回收定义为切除的息肉被吸入容器中回收;操作时间定义为从圈套器插入内镜到息肉切除结束;治疗费用定义为切除息肉所产生的手术费、药品费及耗材费总和。并发症包括术中出血、迟发出血、术中穿孔、迟发穿孔。术中出血定义为息肉切除过程中发生的出血;迟发出血定义为退镜后出血并需要内镜下止血治疗;术中穿孔定义为息肉切除过程中发生的穿孔;迟发穿孔定义为术后超过6 h发生的穿孔。
1.5 统计学方法
统计学分析使用SPSS 23.0软件。符合正态分布的计量资料组间比较采用独立样本t检验,非正态分布的计量资料组间比较采用Mann-Whitney秩和检验;计数资料组间比较采用χ2检验。采用logistic回归比较两组息肉切除方法的完整切除率,校正性别、年龄、息肉位置、息肉形态、息肉直径、波士顿肠道准备量表(boston bowel preparation scale,BBPS)评分等。以双侧P<0.05差异有统计学意义。
2 结果
2.1 一般资料
本研究纳入了187例患者,共284例息肉,其中145例息肉采用CSP治疗,139例息肉采用HSP治疗。在CSP组中,男性59例,女性31例,平均年龄(56.2±10.6)岁,患者BBPS评分平均(6.7±1.1)分,Ⅰs型息肉104例,Ⅰsp型息肉41例,息肉平均直径(5.57±1.50)mm,息肉位于回盲部3例、升结肠24例、横结肠40例、降结肠32例、乙状结肠34例以及直肠7例;HSP组中,男性51例,女性46例,平均年龄(57.5±11.6)岁,患者BBPS评分平均(6.9±1.3)分,Ⅰs型息肉98例,Ⅰsp型息肉41例,息肉平均直径(5.81±1.53)mm,息肉位于回盲部6例、升结肠22例、横结肠36例、降结肠26例、乙状结肠35例以及直肠14例。两组患者性别、年龄、BBPS评分、息肉类型、息肉直径、息肉位置差异均无统计学意义(均P>0.05),见表1。

表1 两组患者及息肉的一般资料比较Tab.1 Comparison of general clinical data between two groups
2.2 主要研究终点
CSP组完整切除息肉131例,完整切除率为90.34%,HSP组完整切除息肉128例,完整切除率为92.09%。两组的完整切除率差异无统计学意义(P=0.336),见表2。
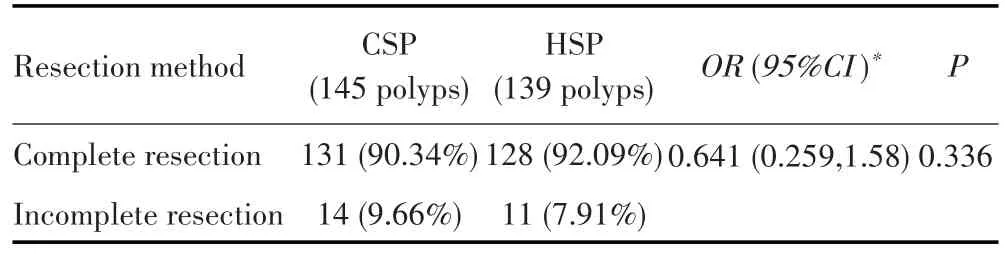
表2 两组息肉切除方法的完整切除率比较Tab.2 Comparison of the complete resection rate between two groups
2.3 次要研究终点
所有息肉切除所获标本均成功收回。CSP组平均操作时间为70.6 s,HSP组平均操作时间为75.2 s,CSP组操作时间明显短于HSP组(P<0.001)。CSP组息肉切除治疗的平均费用为1 371.00元,HSP组息肉切除治疗的平均费用为2 434.90元,CSP组的花费少于HSP组(P<0.001)。CSP组患者平均住院天数为2.9 d,HSP组患者平均住院天数为3.6 d,两者差异有统计学意义(P<0.001)。见表3。
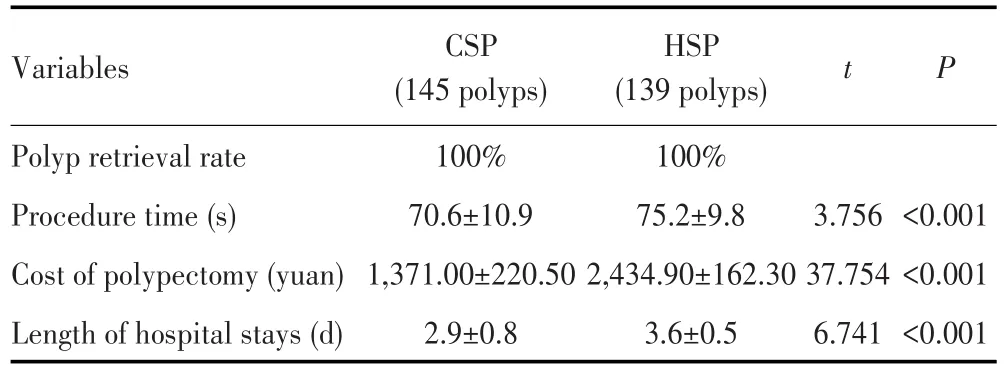
表3 两组息肉切除方法操作时间、标本回收率、治疗费用及住院天数的比较Tab.3 Comparison of the procedure time,polyp retrieval rate,cost of polypectomy and length of hospital stays between two groups
2.4 并发症
CSP组发生7例术中出血,HSP组发生5例术中出血,两者差异无统计学意义(P=0.606)。CSP组出现1例迟发出血,HSP组无迟发出血,两组均未发生穿孔。见表4。
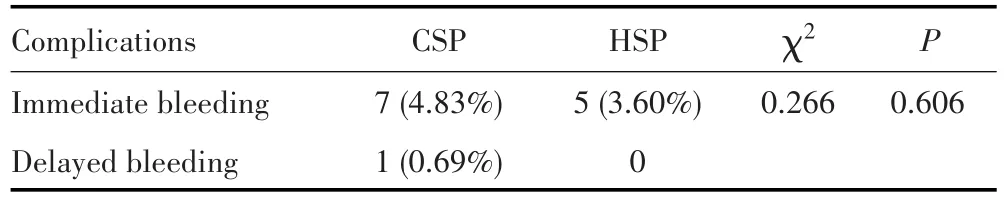
表4 两组息肉切除方法并发症的比较Tab.4 Comparison of complications between two groups
3 讨论
本研究证实,对于直径4~9 mm的无蒂结直肠息肉,CSP的完整切除率及并发症发生率与HSP相当,但CSP操作时间较短,患者住院时间及花费相对更少。因此,CSP在切除直径4~9 mm无蒂结直肠息肉方面较HSP具有更优的治疗效果。
马杰等[5]进行的前瞻性、多中心、随机对照试验的研究结果显示,内镜下切除直径3~9 mm结直肠息肉的完全切除率在CSP组和HSP组间无差异。随后,KAWAMURA等[6]在日本进行的一项非劣性研究亦得出同样结论,对于直径4~9 mm的结直肠息肉,CSP完整切除率不劣于HSP。王妍等[7]的研究得出了与上述一致的结论。同时有学者对两种息肉切除方法的切除宽度及深度进行比较,结果表明对于直径≤10 mm的息肉,CSP可以达到足够的切除宽度及深度以完全切除息肉,且比HSP更安全。本研究结果显示,CSP组完整切除率为90.34%,HSP组完整切除率为92.09%,两者差异无统计学意义。可见,对于直径4~9 mm结直肠息肉,CSP与HSP的完整切除率相当。无论采用何种方法,在使用圈套器闭合时应尽量获取息肉基底部边缘的少量正常黏膜组织,从而保证息肉的完整切除。但CSP切缘无电灼痕迹,更有利于后续病理评估。
虽然两组完整切除率相当,但是本研究发现CSP较HSP具有操作时间短的优点。多项研究[6,8-9]也显示,CSP治疗的平均耗时短于HSP。原因可能在于CSP操作过程避免了反复更换内镜附件,提高了内镜医师的工作效率。本研究同时还比较了两组不同切除方法的治疗费用及患者住院时间,结果发现CSP的治疗费用较HSP明显降低,可能与CSP操作中应用的器械较少有关。同时CSP未进行高频电切,避免了息肉术后电凝综合征的发生,缩短了患者需住院观察的时间。
内镜下息肉切除术常见的并发症为出血、穿孔。其中,出血又可分为术中出血与迟发出血。术中出血可及时进行内镜下止血治疗,因出血部位明确、处理及时,大多能成功止血,对患者预后影响较小。而迟发出血常发生在息肉切除术后,再次进镜后视野不佳,止血难度增加。REPICI等[10]研究纳入了823例患者,CSP切除了共1 015例直径<10 mm的结直肠息肉,无迟发出血的发生。HORIUCHI等[11]在服用华法林的患者中进行了CSP治疗,迟发出血率为0。在本研究中,CSP组发生1例迟发出血,HSP组没有出现迟发出血,两者差异无统计学意义。因此,上述两种息肉切除方式的迟发性出血风险相当。但也有研究认为CSP的迟发出血风险更小,TAKAYANAGI等[12]对比了HSP术后与CSP术后创面组织学上的区别,结果显示HSP的损伤可贯穿固有肌层,从而损伤固有肌层深层的大血管,导致术后出血的发生,而CSP导致的损伤仅累及固有肌层浅层,因而出血风险更小。关于术中出血,KAWAMURA等[6]对直径4~9 mm的结直肠息肉进行的研究显示,CSP组术中出血发生率高于HSP组(7.1%vs3.5%),但两者之间差异无统计学意义。张黎明等[9]的研究亦得出同样结论。本研究结果与上述研究结果一致,CSP组术中出血率虽高于HSP组,但两者差异无统计学意义。
本研究存在以下局限性。⑴本研究为回顾性研究,而且未纳入无蒂锯齿状息肉/腺瘤(sessile serrated polyps/adenoma,SSA/P)。POHL等[13]研究结论显示SSA/P的息肉是息肉切除术不完整切除的相关因素之一。因而,本研究结果还有待前瞻性大样本量的随机对照研究进一步验证。⑵纳入的病例由不同年资的内镜医师完成,息肉的完整切除率及并发症发生率在一定程度上可能受到医师操作经验的影响。
综上,对于直径4~9 mm的无蒂结直肠息肉,CSP与HSP相比完整切除率、并发症发生率无明显差异,而CSP操作时间较HSP缩短,且无电凝损伤,降低了治疗成本的同时缩短了患者住院时间,值得临床推广。

