快速消解-原子荧光光谱法测定大米中总砷
袁野
(南充农产品质量监测检验中心,四川南充 637000)
砷是一种在自然界中广泛存在且毒性很强的元素,于2012 年被世界卫生组织国际癌症研究机构列为Ⅰ类致癌物[1]。砷进入人体后将影响细胞中酶的活性,从而影响人的新陈代谢。砷在人体内大量富集会导致人体中毒,轻者表现为皮肤干燥、角质化严重等皮肤损害,重者表现为肾脏、肝脏、神经系统、消化系统等功能受损[2-6]。砷在大气沉降、微生物代谢等作用下,参与自然环境中内部循环。人们使用农药、矿产开采等生产活动,加剧了砷在自然环境中的循环过程。土壤中的砷元素易被生物(尤其是水稻)富集。水稻根部对砷元素较敏感,在受污染的土壤中极容易吸收砷元素,因此准确测定大米中的砷含量,对评估大米中砷对人体健康的危害和有效防控重金属污染、维护国家食品安全具有十分重要的意义[7-9]。
砷含量测定有多种方法,其中电感耦合-等离子体质谱法[10]和原子荧光光谱法[11]应用较为广泛,而氢化物发生-原子荧光光谱法使用成本更低,普及率更高[12]。GB 5009.11—2014 《食品安全国家标准 食品中总砷及无机砷的测定》中第二法:氢化物发生-原子荧光光谱法包括湿法消解和干法灰化两种样品处理方法,但是在实际测定大米中砷含量时,上述两种样品处理方法操作步骤繁琐,耗酸量大,实验时间长[13],影响检测效率。当采用氢化物发生-原子荧光光谱法测定砷时,消解后残留的有机颗粒和硝酸等会影响检测结果,需要将酸尽可能赶尽[14-15]。
笔者探索了一种快速消解样品的方法,与GB 5009.11—2014 中第二法:氢化物发生-原子荧光光谱法中湿法消解样品方法相比具有以下优点:(1)加酸种类少,国标法需要加入硝酸、硫酸、高氯酸,而该方法只需要加入硝酸;(2)酸消耗量少,国标法需要加入20 mL 硝酸、4 mL 高氯酸、1.25 mL 硫酸,该方法只需10 mL 硝酸,国标法的酸用量比该方法多了一倍多;(3)在实验环境相同的条件下,除去放置时间,用国标法完全消解样品需要10 h,而该方法只需要5 h,消解时间缩短了一半,大幅度提高了消解效率。同时探讨了硼氢化钾溶液、载流酸溶液及还原掩蔽剂溶液的质量浓度等因素对砷含量测定结果的影响,确定了最优测定条件,建立了快速消解-原子荧光光谱法测定大米中总砷的分析方法。
1 实验部分
1.1 主要仪器与试剂
原子荧光光度计:AFS-9230 型,北京吉天仪器有限公司。
自动进样器:AS-90 型。北京吉天仪器有限公司。
砷空心阴极灯:北京有色金属研究院。
全自动样品消解仪:Vulcan84 型,加拿大Qtechcorp 公司。
消解管:50 mL,美国Cole-Parmer 仪器公司。天平:ML204 型,感量为1 mg,梅特勒-托利多仪器(上海)有限公司。
浓盐酸、浓硝酸:优级纯,苏州晶瑞化学股份有限公司。
氢氧化钾:优级纯,成都市科隆化学品有限公司。
硼氢化钾:优级纯,成都市科龙化工试剂厂。
硫脲:优级纯,天津市科密欧化学试剂有限公司。
抗坏血酸:优级纯,成都市科隆化学品有限公司。
大米粉成分分析标准物质:编号为GBW(E)100359,标准值为0.15 mg/kg,扩展不确定度0.02 mg/kg,钢研纳克检测技术股份有限公司。
大米粉成分分析标准物质:编号为GBW(E)100361,标准值为0.12 mg/kg,扩展不确定度0.01 mg/kg,钢研纳克检测技术股份有限公司。
氩气:纯度不小于99.999%(体积分数),四川金瑞气体有限公司。
砷标准溶液:1 000 μg/mL,编号为BWJ 4223-2016,北京北方伟业计量技术研究院。
实验用水为去离子水。
1.2 溶液配制
盐酸溶液(5+95):量取50 mL 浓盐酸,缓缓倒入950 mL 水中,混匀。
硫脲-抗坏血酸-盐酸溶液:硫脲、抗坏血酸的质量浓度均为10 g/L,称取10 g 硫脲,加适量盐酸溶液溶解,再加入10 g 抗坏血酸,用盐酸溶液定容至1 L,摇匀。
氢氧化钾溶液:5 g/L,称取2.5 g 氢氧化钾,溶于500 mL 纯水中。
硼氢化钾溶液:10 g/L,称取5 g 硼氢化钾,溶于500 mL 氢氧化钾溶液中,摇匀。
砷标准中间溶液:10 μg/mL,准确吸取1 mL砷标准溶液于100 mL 容量瓶中,用盐酸溶液稀释至标线,摇匀。
砷标准使用溶液:0.1 μg/mL,准确吸取1 mL砷标准中间溶液于100 mL 容量瓶中,用盐酸溶液稀释至标线,摇匀。
系列砷标准工作溶液:依次吸取0、1.00、2.00、4.00、8.00、10.00 mL 砷标准使用溶液,分别置于6只100 mL 容量瓶中,用硫脲-抗坏血酸-盐酸溶液定容至标线,摇匀,配制成质量浓度分别为0.00、1.00、2.00、4.00、8.00、10.00 μg/L 的系列砷标准工作溶液。
1.3 仪器工作条件
负高压:270 V;灯电流:60 mA;原子化高度:10 mm;载气:氩气,流量为300 mL/min;屏蔽气:氩气,流量为700 mL/min;读数时间:8 s;延迟时间:1.0 s。
1.4 标准曲线绘制
以盐酸溶液为载流,硼氢化钾溶液为还原剂,在1.3 仪器工作条件下,按照质量浓度由低到高的顺序,分别测定系列砷标准工作溶液,以溶液质量浓度(ρ)为横坐标、荧光强度(I)为纵坐标绘制标准工作曲线。同法测定样品溶液,用标准曲线法定量。
1.5 样品处理
称取0.500 0 g 大米样品于50 mL 消解管中,加入10 mL 硝酸,放置12 h,然后置于全自动样品消解仪中,升温至90 ℃保持30 min,揭盖赶酸,温度不能超过120 ℃(该消解管超过120 ℃会有轻微形变),赶酸完成后将溶液转移至25 mL 比色管中,用硫脲-抗坏血酸-盐酸溶液定容至标线,摇匀,静置,充分还原后上机测定。同时做试剂空白试验。
2 结果与讨论
2.1 硫脲、抗坏血酸质量浓度选择
样品经湿法消解处理后,加入硫脲-抗坏血酸-盐酸溶液,将5 价砷预还原为3 价砷,同时硫脲对Cu2+、Co2+、Ni2+等干扰离子有掩蔽作用。表1 为不同硫脲、抗坏血酸质量浓度的硫脲-抗坏血酸-盐酸溶液还原8 μg/L 砷标准工作溶液后测得的荧光值,图1 为对应的趋势图。
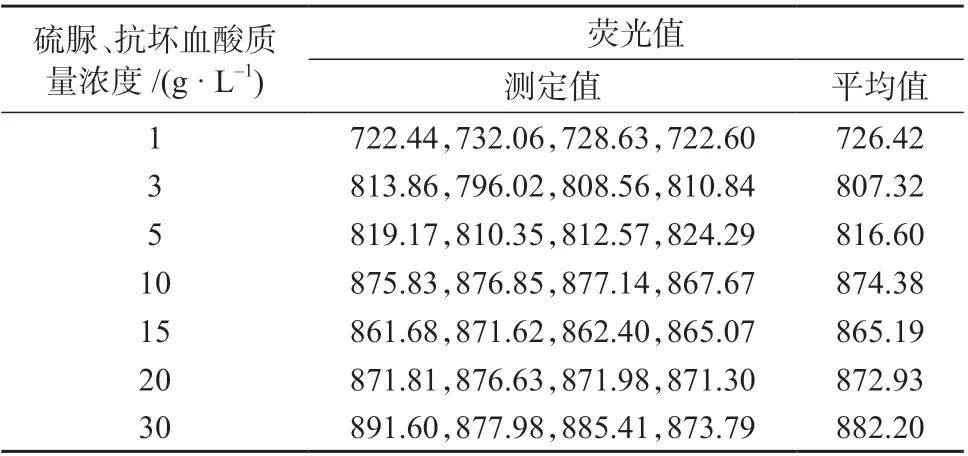
表1 不同硫脲、抗坏血酸质量浓度对应的荧光值

图1 不同硫脲、抗坏血酸质量浓度对应的荧光值
由表1 和图1 可以看出,随着硫脲-抗坏血酸-盐酸溶液中硫脲、抗坏血酸质量浓度的增大,荧光强度有所增加,但当硫脲、抗坏血酸的质量浓度达到10 g/L 后,继续增大硫脲、抗坏血酸的质量浓度,荧光值变化不大,这说明当硫脲、抗坏血酸的质量浓度为10 g/L 时,已经能够将5 价砷全部还原为3 价砷,所以选择硫脲、抗坏血酸的质量浓度均为10 g/L 的硫脲-抗坏血酸-盐酸溶液作为预还原剂。
2.2 硼氢化钾溶液质量浓度选择
硼氢化钾作为还原剂能够将3 价砷进一步还原为砷化氢。硼氢化钾溶液的质量浓度影响测定结果的准确性。在保持其它条件相同的情况下,考察不同质量浓度的硼氢化钾溶液对8 μg/L 砷标准工作溶液荧光值的影响,试验数据见表2,图2 为对应的趋势图。
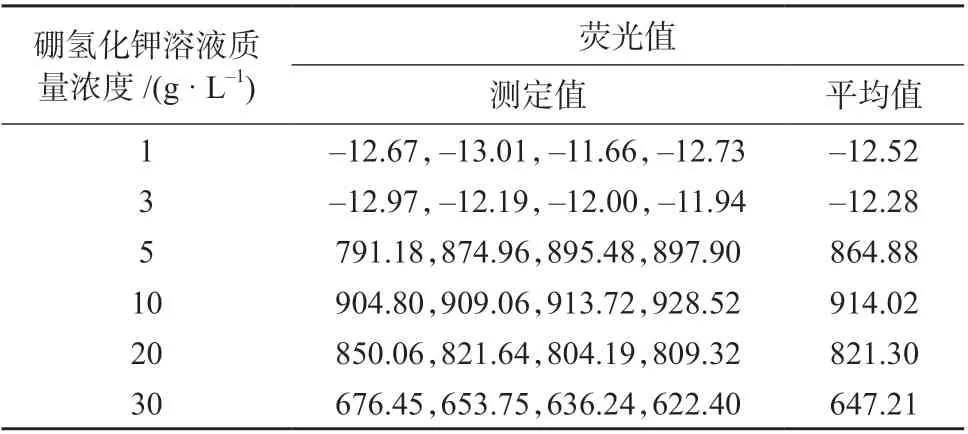
表2 不同硼氢化钾浓度对应的荧光值
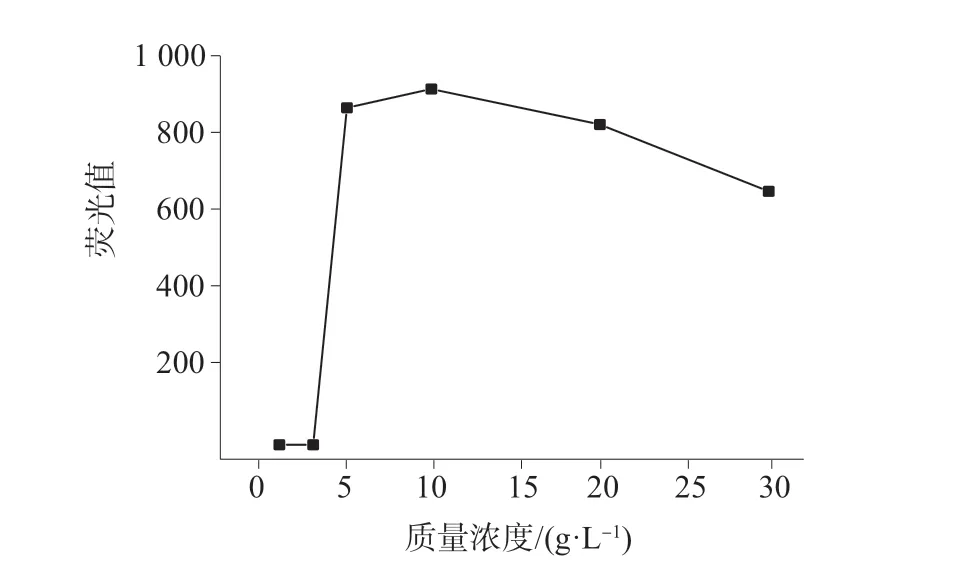
图2 不同硼氢化钾溶液质量浓度对应的荧光值
由表2 和图2 可以看出,在以5 g/L 氢氧化钾溶液作为稳定剂的前提下,当硼氢化钾溶液的质量浓度小于5 g/L 时,荧光值为负数,说明硼氢化钾溶液质量浓度太低时几乎没有砷化氢生成,随着硼氢化钾溶液质量浓度的增大,荧光值逐渐增大,当硼氢化钾溶液质量浓度为10 g/L 时荧光值最大,继续增大硼氢化钾溶液的质量浓度,荧光值反而降低。这说明当硼氢化钾溶液的质量浓度过高时会产生大量氢气,从而稀释砷化氢,使得荧光值降低。综合考虑,选择硼氢化钾溶液的质量浓度为10 g/L。
2.3 载流盐酸溶液浓度选择
盐酸具有还原性,选择盐酸溶液作为载流能有效避免强氧化性对测定结果的影响。选择硫脲、抗坏血酸质量浓度均为10 g/L 的硫脲-抗坏血酸-盐酸溶液预还原样品,10 g/L 硼氢化钾溶液作为还原剂,考察不同浓度的载流盐酸溶液对8 μg/L 砷标准工作溶液荧光值的影响,结果见表3,图3 为对应的趋势图。

表3 不同盐酸浓度对应的荧光值
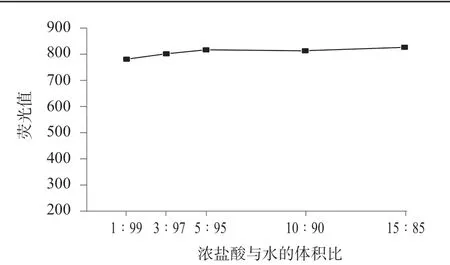
图3 不同盐酸溶液浓度对应的荧光值
由表3 和图3 可以看出,随着盐酸溶液浓度的增加,荧光值有所增大,但趋势不明显。当盐酸溶液中浓盐酸与水的体积比大于5∶95 时,荧光值基本恒定,因此选择盐酸溶液(5+95)作为载流。
2.3 线性方程与检出限
按照1.4 方法测定系列砷标准工作溶液并绘制标准工作曲线,计算线性方程和相关系数。连续测定样品空白11 次,计算测定结果的标准偏差,按照文献[15]计算方法检出限。砷质量浓度线性范围、线性方程、相关系数及检出限见表4。

表4 砷质量浓度线性范围、线性方程、相关系数及检出限
2.4 加标回收与精密度试验
选取3 种大米样品,精确称定,分别加入0.1、0.2、0.4 mg/kg 砷标准溶液,按照1.5 方法各平行处理5 份样品溶液,在1.3 仪器工作条件下分别进行测定,结果见表5。由表5 可知,样品加标回收率为92.1%~104.9%,测定结果的相对标准偏差为0.27%~2.35%。表明该方法精密度、准确度满足测定要求。
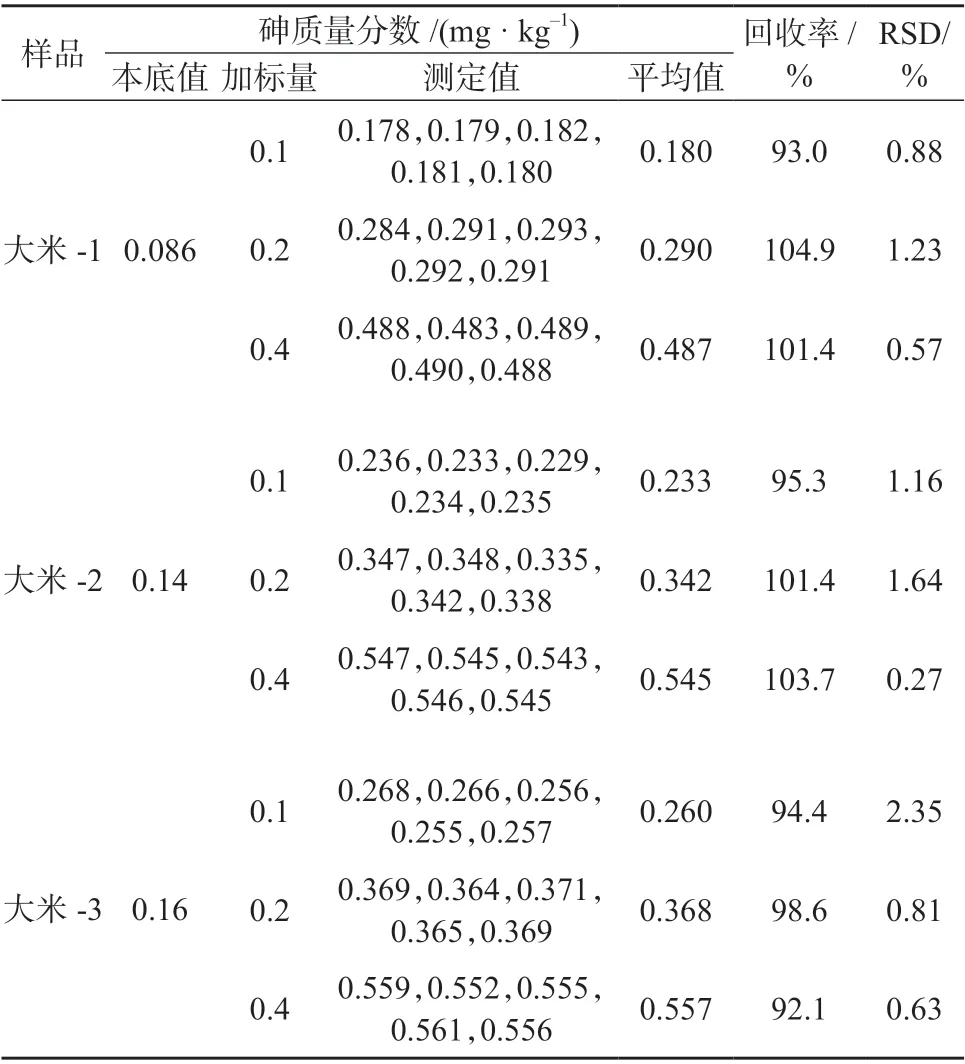
表5 加标回收与精密度试验结果
2.5 标准物质测定
称取有证标准物质样品GBW(E) 100359、GBW(E) 100361 各7 分,按照1.5 方法处理,在1.3仪器工作条件下分别进行测定,结果见表6。由表6可知,两种标准物质测定值均在标准值不确定度范围内,相对误差分别为6.7%和8.3%。表明该方法准确度良好。

表6 标准物质测定结果
3 结语
采用快速消解-原子荧光光谱法测定大米中砷,该方法步骤简单,酸消耗量少,准确度、精密度良好,具有推广应用价值。

