HPVE6/E7mRNA和HPV-DNA检测在宫颈癌筛查中的价值
武振宇
(张家口市妇幼保健院微生物科,河北 张家口 075000)
宫颈癌是全世界高发的严重危害女性身心健康的恶性肿瘤。在全球范围内,每年新发病例和死亡病例分别约为53万和27.5万[1],且全球数据表明,宫颈癌的新发病例呈现越来越年轻化趋势[2]。有研究[3]表明,高危型人乳头瘤病毒(HPV)的持续性或反复性感染是宫颈癌的主要致病原因。宫颈癌可防可治,从宫颈癌癌前病变到宫颈癌确诊需要5~12年,因此,早筛查早治疗对宫颈癌的防治具有重要意义[4]。组织细胞学联合HPV-DNA检测是目前我国筛查宫颈癌的主要方案[5],HPV-DNA检测的敏感性较高,但其特异性和阳性预测值较低[6-7]。研究[8]表明,HPV E6/E7 mRNA 基因在癌基因的转录表达中发挥作用,可作为宫颈癌病变发展的早期标志物,其与HPV-DNA检测相比,具有更高的特异性和相似的敏感性,能弥补HPV-DNA检测的不足,具有较高的宫颈癌筛查价值。本研究通过分析不同组织病理学级别中HPV E6/E7 mRNA 和 HPV DNA检测结果的差异,探讨 HPV E6/E7mRNA和HPV-DNA检测对宫颈癌的筛查价值。
1 资料与方法
1.1 一般资料
选择2021年1月至2021年7月在张家口市妇幼保健院975例进行宫颈癌筛查并获得病理结果者为研究对象,其中年龄20~70岁,平均(41.50±2.00)岁。本研究经医院伦理会员会审核并批准,研究对象均自愿接受宫颈癌各项筛查方法并签署知情同意书。纳入标准:(1)检查前3 d无阴道用药治疗史、无性生活;(2)月经结束后 3~7 d;(3)未进行宫颈锥切术或子宫切除术。排除标准:(1)已经确诊为宫颈癌前病变或宫颈癌者;(2)子宫切除术后或其他宫颈手术者;(3)盆腔放射治疗史者;(4)合并妊娠者;(5)合并其他恶性肿瘤者;(6)有自身免疫性疾病或正在接受免疫抑制治疗者。
1.2 方法
1.2.1 HPVE6/E7mRNA检测 使用郑州Kodia 生物技术公司生产的宫颈稳态检测试剂盒,采用支链DNA杂交捕获技术(操作严格按照试剂盒说明书进行)定量检测14 种高危型 HPV,分别为HPV16、18、31、33、35、39、45、51、52、56、58、59、66 和 68型。其检测探针是针对这14种高危型HPV病毒的E6/E7mRNA,只要任何一种存在即阳性。检测结果由计算机软件根据E6/E7mRNA的拷贝数、产品临床实验阈值等自动计算,结果<1为阴性,≥1为阳性。
1.2.2 HPV-DNA检测 采用杭州德同生物技术有限公司提供的 HPV 核酸检测试剂盒,在 HPV 取样管中加入变性试剂,65 ℃水浴 45 min 后室温保存,将样本吸取至已经加入探针试剂的杂交板孔内,65 ℃孵育 60 min。降至室温后将上述样本转移至对应捕获板中振荡 60 min,然后移除捕获板中液体并拍干,加入检测试剂25 ℃孵育45 min。接着移除液体、使用清洗液洗板并拍干,加入底物试剂,室温避光15 min后于化学发光免疫分析仪上读数。通过杂交捕获-化学发光方法对14种HPV型[2种极度高危型(HPV16、HPV18)、12 种高危型(HPV31、HPV33、HPV35、HPV39、HPV45、HPV51、HPV52、HPV56、HPV58、HPV59、HPV66、HPV68)]进行检测,检测到其中≥1种 HPV型者为阳性,未检测到者为阴性。
1.2.3 组织病理学检查 医师借助深圳市金科威公司生产的光电一体电子阴道镜进行组织活检。对无异常者进行3、6、9、12点取材,对于有异常者进行区域多点取材。病理标本由两名资深的病理医师进行阅片并作出病理诊断。按照病理学诊断标准[9]进行宫颈病变分型:(1)正常或炎症;(2)宫颈上皮细胞内瘤变Ⅰ级(CINⅠ);(3)CINⅡ;(4)CINⅢ或原位癌;(5)宫颈浸润癌。将正常或炎症判定为阴性,其他诊断结果判定为阳性。
1.3 统计学分析

2 结果
2.1 不同组织病理学结果分级中HPV-DNA和HPV E6/E7mRNA检测结果比较
975名研究对象中,HPVE6/E7mRNA检测阳性405例,阳性率41.83%;HPV-DNA检测阳性564例,阳性率57.84%;阴道镜组织病理学检查结果为正常或炎症515例、CINⅠ200例、CINⅡ129例、CINⅢ或原位癌123例、宫颈浸润癌8例。两种检测方法的阳性率随着宫颈组织病理学级别的增高呈逐渐上升的趋势(P<0.05);在正常或炎症中HPV-DNA检测的阳性率高于HPVE6/E7mRNA检测(P<0.05);在CINⅠ级中,HPV-DNA检测的阳性率高于HPVE6/E7mRNA检测(P<0.05);在CINⅡ、CINⅢ或原位癌、宫颈浸润癌中,两种检测方法比较差异无统计学意义(P>0.05)。见表1。
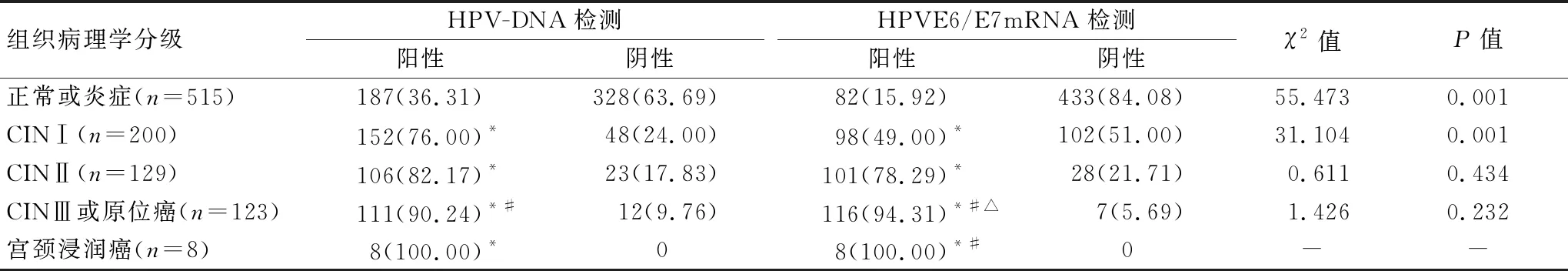
表1 不同组织病理学分级中HPV-DNA检测和HPVE6/E7mRNA检测结果比较[n(%)]
2.2 HPV-DNA、HPV E6/E7mRNA检测及两者联合检测结果比较
病理学检查结果中,将正常或炎症判定为阴性,其他诊断结果判定为阳性。两者联合检测时任一种检测结果阳性即判定结果为阳性,两种检测结果均为阴性则判定结果为阴性。见表2。
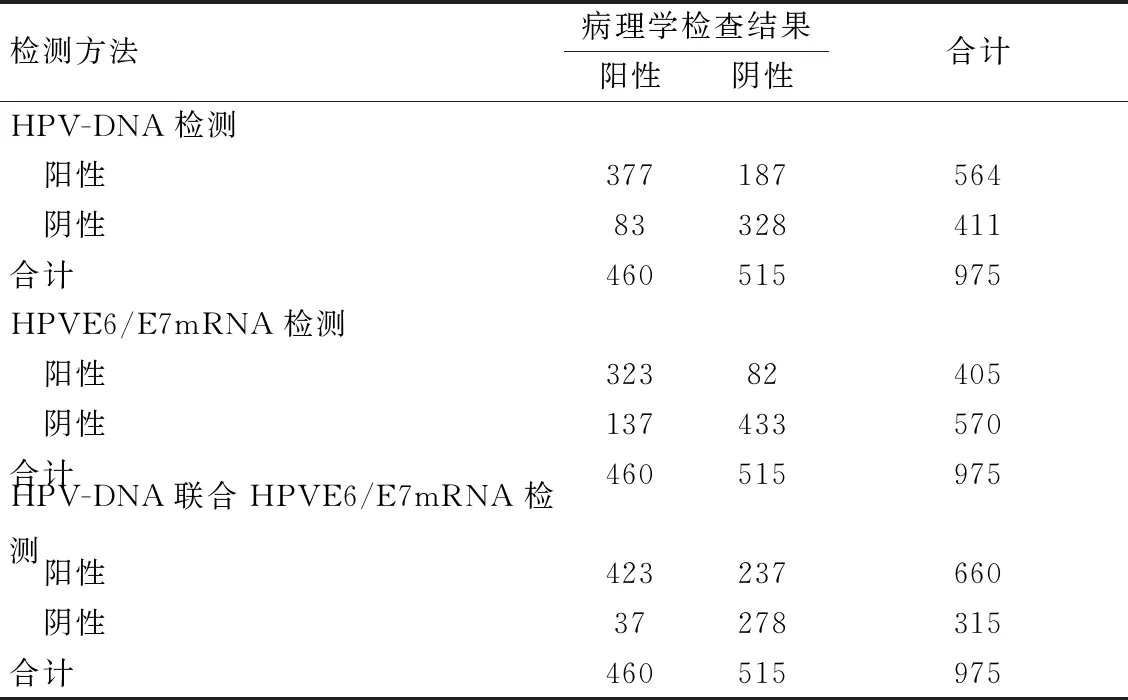
表2 HPV-DNA、HPV E6/E7mRNA检测及两者联合检测结果比较(例)
2.3 HPV-DNA、HPV E6/E7mRNA检测及两者联合检测对宫颈癌的筛查价值
HPV-DNA检测的敏感性高于HPVE6/E7mRNA检测(P<0.05);特异性、阳性预测值及准确性均低于HPVE6/E7mRNA检测(P<0.05);两种检测方法的阴性预测值比较,差异无统计学意义(P>0.05)。两者联合检测的敏感性及阴性预测值高于两者单独检测(P<0.05);特异性低于两者单独检测(P<0.05);两者联合检测的阳性预测值及准确性有所降低,但与HPV-DNA检测比较,差异无统计学意义(P>0.05),与HPVE6/E7mRNA检测比较,差异有统计学意义(P<0.05)。见表3。
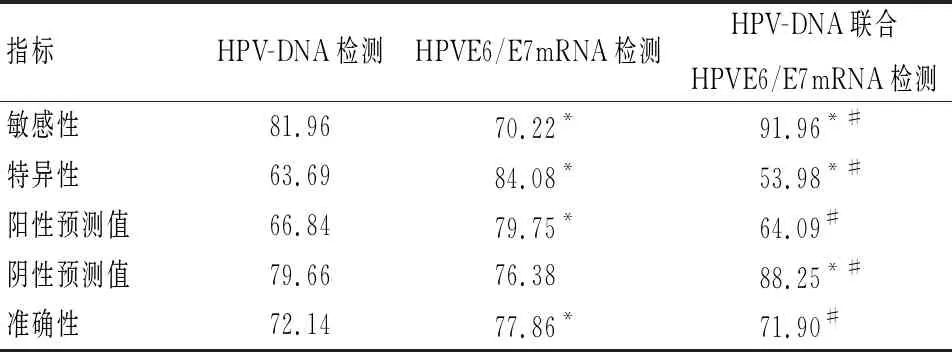
表3 HPV-DNA、HPV E6/E7mRNA检测及两者联合检测对宫颈癌的筛查价值(%)
3 讨论
宫颈癌是严重危害女性健康的恶性肿瘤之一,通过早期发现CIN并采取合适的治疗措施,可使宫颈癌的发病率和死亡率明显降低,且患者预后良好[10]。有研究表明,高危型HPV持续或反复感染是宫颈癌前病变及宫颈癌发生发展的必要条件,因此检测HPV-DNA有助于宫颈癌的筛查和诊断,但HPV感染往往是一过性且无害的,HPV-DNA检测仅能诊断是否出现HPV感染,对病毒的活跃状态及宫颈病变的严重程度并不明确[11]。PVE6/E7mRNA是HPV致癌基因表达的直接标志物,是致癌蛋白合成的模板,是宫颈病变开始和进展的必经之路。有研究[12]指出,HPVE6/E7mRNA是HPV病毒活跃的指标,其表达水平提升提示HPV病毒与机体DNA发生整合,细胞恶化启动。
本研究中,随着宫颈癌组织病理学级别的升高,两种检测方法的检出阳性率随之增加(P<0.05),在宫颈浸润癌,两种检测方法的阳性率均达到100%,说明HPV-DNA及HPVE6/E7mRNA表达水平与病变程度呈正相关,随着宫颈癌级别加重呈上升趋势。有研究[13]证实,绝大多数宫颈癌患者早期均有HPV感染,且多有反复或长期感染。HPV在机体定植后会与体内特异的基因组合并高度表达,促进宫颈癌细胞的增殖,宫颈癌组织病理学级别越高,机体HPV-DNA表达水平越高。在宫颈炎组、CINⅠ组、CINⅡ组、CINⅢ组及宫颈癌组中随着病理学级别的升高,HPV-DNA的检出阳性率随着升高,与谌琼华[14]的研究结果一致。HPVE6/E7是HPV的基因编码的致癌蛋白,是导致宫颈细胞癌变的重要因子,其可使宫颈被感染的细胞无限增殖并恶化[15]。HPVE6/E7mRNA的表达水平是细胞高级别恶变的一个生物学标志,在各级别组织病理学检查结果中,级别越高,HPVE6/E7病毒载量随之升高[16]。也有研究[17]表明,随着宫颈组织病理学级别升高,HPVE6/E7 mRNA检出阳性率随之升高。在正常或炎症及CINⅠ中,HPV-DNA的阳性检出率高于HPVE6/E7 mRNA检测,这是因为在正常或炎症及CINⅠ中,大部分HPV病毒呈游离态,尚未与机体DNA发生整合,即大多数HPV感染者可能是一过性的并未出现持续感染,部分HPV-DNA的阳性者可能出现HPVE6/E7 mRNA检测阴性[18]。因此,HPVE6/E7 mRNA检测的假阳性率相对较低,能减少一过性感染的检出率。在CINⅡ及以上级别中,两种检测方法的阳性率差异无统计学意义(P>0.05),可能是因为随着HPV的持续感染,病毒与机体DNA发生整合,癌基因表达活跃,大量癌蛋白E6E7产生,宫颈癌风险增加。
本研究中,HPV-DNA检测的敏感性高于HPVE6/E7mRNA检测(P<0.05),说明HPV-DNA检测具有较高的敏感性,在宫颈癌筛查中不易发生漏诊,与既往研究[19]相符。HPVE6/E7mRNA检测的特异性、阳性预测值及准确性高于HPV-DNA检测(P<0.05),与雷冬梅等[20]的研究结果一致。HPV-DNA检测仅说明感染了HPV,有些患者的HPV感染是一过性的,可自行消退,仅有小部分高危型HPV持续或反复感染者才发展为宫颈恶性肿瘤。因此,相对来说,HPV-DNA检测对宫颈癌的特异性不高,风险预测过早,易造成某些仅感染HPV但未发展为宫颈癌者的误诊,而HPVE6/E7mRNA检测有较高的特异性,可降低一过性感染者的过度医疗行为[21]。HPVE6/E7mRNA检测能弥补传统HPV-DNA检测特异度和阳性预测值不高的问题,能更精确反映癌变风险。两种检测方法的阴性预测值比较,差异无统计学意义(P>0.05),可能与本研究样本量小有关。赵涌等[1]也指出,HPVE6/E7mRNA检测有较高的敏感性、特异性、阳性预测值和阴性预测值。因此,HPVE6/E7mRNA和HPV-DNA检测均对宫颈癌筛查具有较高的指导价值,当两种检测均为阳性时,应行宫颈癌组织病理学检查及早明确诊断,早期进行干预[22]。本研究结果还显示,两种检测方法联合使用,能提高检测的敏感性及阴性预测值,具有较好的诊断效能(P<0.05)。
综上,HPV-DNA检测用于宫颈癌一线筛查中,可提高筛查的敏感性和阳性检测率。对一线筛查阳性者进行HPVE6/E7mRNA二线筛查,能将一过性感染者及低风险者重新纳入常规筛查管理中,以减少不必要的检查和治疗,两者联合具有良好的筛查价值。

