单分散SiO2-TiO2 微球可控合成及性能研究
陈作雁,任学昌,杨林海,张玉杰,付 宁,安兴才
(1.兰州交通大学环境与市政工程学院,兰州 730070;2.甘肃自然能源研究所,兰州 730046)
悬浮态TiO2光催化-膜分离技术将膜分离技术的高效截留、无相变分离特性与悬浮态光催化技术相结合,不仅实现了光催化剂分离回收和重复使用,同时,光催化技术对有机污染物的有效降解,改善了有机污染物造成的膜污染[1-2].此外,利用膜的分离特性,可以实现反应底物、中间产物和终产物的有效实时在线分离,提高光催化反应对反应底物和有毒、有害中间产物光降解的针对性,进而提高水处理效果和处理工艺的经济性[3].但TiO2粉体颗粒粒径从纳米至微米范围分布,小于膜孔径的TiO2颗粒容易堵塞膜孔道,导致的膜不可逆污染是光催化工艺与压力驱动膜分离耦合工艺的最大问题[4].
单分散TiO2微球具有各向同性的球形结构,同时从几何学角度可以进一步增大比表面积,增强光的吸收,是光化学领域理想的材料结构,可在一定程度上解决上述问题[5].但高比表面积的TiO2机械强度和热稳定性低,在紊流状态下的反应溶液中一次晶粒易解离,造成TiO2不完全分离和膜污染.研究表明,通过表面包覆形成的 SiO2@TiO2或 TiO2@SiO2核壳结构中,SiO2与TiO2间形成的Si-O-Ti键可进一步提高材料的热稳定性和机械强度、增加表面电荷和改善吸附性能,提高光催化反应效率[6-7].但核壳结构的壳层结合力较弱,在酸碱性环境中易溶解或脱落造成结构失效,而实现SiO2均匀掺杂的单分散TiO2微球光催化材料更具优势,目前该方面的研究报道较少.
本文采用溶胶凝胶+水热+煅烧法制备出了单分散SiO2-TiO2微球,通过调节煅烧温度和 Si/Ti比,分析了材料微观形貌、晶体结构以及表面电荷的变化.以MB和苯酚作为目标污染物,在紫外光下,比较了其与TiO2微球吸附和光催化性能的差异.
1 实验部分
1.1 试剂与仪器
试剂:钛酸异丙酯(上海麦克林生化科技有限公司,99.99%);正硅酸乙酯(国药集团化学试剂有限公司,99.5%);无水乙醇(利安隆博华(天津)医药化学有限公司,99.5%);无水乙腈(西陇科学股份有限公司,99.5%);氨水(烟台市双双化工有限公司,25~28%);所有试剂均为分析纯,实验用水为实验室超纯水机制得的超纯水.
仪器:PCX-50B Discover多通道光催化反应系统(北京泊菲莱科技有限公司);冷却循环水机(上海爱朗仪器有限公司;CCA-1111);TGL-6G离心机(上海安亭科学仪器厂);S-90马弗炉(日本KDF);真空冷冻干燥机(宁波新芝生物科技股份有限公司);UV-2550型紫外可见分光光度计(日本岛津);LC-2030高效液相色谱仪(日本岛津);D8 ADVANCE X射线衍射仪(德国布鲁克);ZEISS GeminiSEM 500扫描电子显微镜(德国蔡司);Tecnai G2 F20 S-TWIN场发射透射电子显微镜(美国FEI);VERTEX 70型傅立叶红外分光光度计(德国布鲁克);90Plus Pals Zeta电位及粒度分析仪(德国布鲁克).
1.2 SiO2-TiO2微球制备
以钛酸异丙酯(TTIP)为钛源,正硅酸乙酯(TEOS)为硅源,氨水(NH3·H2O)为结构导向剂,乙醇(EtOH)为溶剂,乙腈(ACN)为共溶剂,采用溶胶凝胶法,通过调节TEOS和TTIP摩尔比(Si/Ti=0~1),制备具有不同SiO2含量的非晶SiO2-TiO2微球.再经过水热+煅烧工艺,调节煅烧温度(500~800℃),得到不同结晶度的SiO2-TiO2介孔微球.典型的合成过程如下:在20℃下,首先将0.38 g NH3·H2O和1.52 g H2O加入到250 mL乙醇和乙腈(体积比为6:4)的混合溶液中.在剧烈搅拌条件下,依次将1.1 mL TEOS和5 mL TTIP加入NH3·H2O(0.38 g)+H2O(1.52 g)+EtOH(150 mL)+ACN(100 mL)的混合溶液中溶解.连续搅拌2 h后静置6 h.将溶液中的产物离心分离,用乙醇和H2O分别洗涤3次,通过真空冷冻干燥得到非晶SiO2-TiO2微球,标记为TS-0.3.将1.5 g非晶SiO2-TiO2微球投加到50 mL H2O中,通过搅拌和超声分散均匀后,在110℃下水热10 h得到部分结晶的SiO2-TiO2微球.抽滤得到的产物用蒸馏水洗涤后60℃干燥,在马弗炉中800℃煅烧,得到结晶的SiO2-TiO2微球,标记为TS-0.3-800.其中,0.3表示 Si/Ti为 0.3:1,800表示煅烧温度为800℃.为了便于比较锐钛矿型TiO2与SiO2-TiO2结构性能的差异,而煅烧温度超过500℃会造成纯TiO2由锐钛矿向金红石晶型转变,根据文献报道TiO2微球(TS-0)水热后煅烧温度设定为450℃[8].
1.3 表征
通过D8 ADVANCE X射线衍射仪测试样品的晶体结构,Cu靶 λKα=0.154 187 nm,扫描范围:20°~90°,扫描速度:5°/min.利用 ZEISS Gemini SEM 500扫描电子显微镜(SEM)观察样品的微观形态和元素分布图像,通过计数100个颗粒,获得微球平均直径.利用Tecnai G2 F20 S-TWIN场发射透射电子显微镜(TEM)微观结构和EDX元素含量.利用ASAP2020比表面积测试仪在液氮温度(76 K)下测量N2的吸附-解析等温线,在进行测量之前,将样品在真空150℃下排气 8 h;使用 Brunauer-Emmett-Teller(BET)方程,相对压力P/P0=0.01~0.30的范围内,根据吸附数据计算表面积.根据等温线的吸附分支,使用Barrett-Joyner-Halenda(BJH)方法估算平均孔径.利用VERTEX 70傅立叶红外-拉曼光谱仪测试样品红外光谱(FT-IR).用去离子水配置0.1 g/L样品悬浊液,用HCl和NaOH调节pH至2~10范围内,通过90Plus Pals Zeta电位及粒度分析仪测试不同pH值悬浊液中的Zeta电位.
1.4 光催化活性评价
采用PCX-50B Discover多通道光催化反应系统在主波长为365 nm的紫外光源(I365=235 mW/cm2)照射下,通过降解20 mg/L亚甲基蓝(MB)和苯酚(Phenol)来评价SiO2-TiO2微球的光催化性能.具体步骤如下:将0.025 g样品分散在50 mL目标污染物溶液中,在避光条件下以250 rpm的转速搅拌30 min,以实现在打开光源前达到吸附-解析平衡.打开光源开始光催化活性测定实验,每隔一定时间取4 mL悬浮液在5 000 rpm下离心分离,获得的上清液用0.22μm醋酸纤维素膜过滤后加入比色皿中,用UV-2550型紫外可见分光光度计于662 nm(MB)或270 nm(苯酚)下测定吸光度.
2 结果与讨论
2.1 SEM 和 TEM
对比TiO2微球和 Si/Ti为0.3的 SiO2-TiO2微球的SEM图发现,TiO2微球煅烧前(见图1(a))和煅烧后(见图1(b))样品均为球形颗粒,平均直径分别为347 nm和271 nm,且存在部分未聚集成球的一次晶粒.SiO2-TiO2微球煅烧前(见图1(c))和煅烧后(见图1(d))样品均为球形颗粒,平均直径分别为341 nm和236 nm,具有良好的单分散性,没有出现未聚集成球的一次晶粒,说明SiO2-TiO2微球具有更好的结构强度.
通过SEM-EDS观测TS-0.3-800的元素分布图像如图 1(e)所示,微球表面形成了 Ti、O、Si元素的均匀分布.如表1所列,通过EDX分析测定的样品中 Si与 Ti的摩尔比(nSi:Ti)均低于 Si/Ti,且随着TEOS投加量增大,两者差值逐渐增大.这是由于TTIP水解速度明显快于TEOS,随着优先水解造成TEOS水解所需的H2O量不足,只有部分Si能够生成 SiO2-TiO2微球[9].

图 1 TiO2微球和 SiO2-TiO2微球(Si/Ti:0.3)SEM 图Fig.1 SEM image of TiO2 m icrospheres and SiO2-TiO2 m icrospheres(Si/Ti:0.3)

利用TEM进一步表征TiO2微球和Si/Ti为0.3的SiO2-TiO2微球的微观结构,如图2所示.TiO2微球(见图2(a))由15~40 nm不规则一次晶粒聚集形成的颗粒,颗粒之间具有明显的孔结构.而Si/Ti为0.3的SiO2-TiO2微球(见图2(b))颗粒均匀致密,未观察到明显的一次晶粒界限.另外,从高分辨HRTEM图像发现,TiO2微球(见图 2(c))和 Si/Ti为0.3的SiO2-TiO2微球(见图2(d))的晶格间距均为0.35 nm,对应于锐钛矿TiO2{101}晶面.
2.2 XRD
为了研究 Si/Ti对 SiO2-TiO2微球晶相转变温度的影响,对不同温度煅烧得到的TiO2微球和SiO2-TiO2微球的XRD图谱进行比较,如图3(a)所示.其中,TS-0.30-500仅在25.3°出现了微弱的吸收峰,TS-0.30-600、TS-0.30-700、TS-0.30-800、TS-0-450均在 25.3°,37.84°,48.12°,53.97°,55.13°,62.79°处出现了锐钛矿型TiO2的吸收峰(JCPDS,NO.21-1272),且随Si/Ti减小吸收峰强度逐渐增强,这与前述TEM观察到的锐钛矿晶格条纹相印证.根据Scherrer公式[10]基于(101)半峰宽估算 TS-0.30-500、TS-0.30-600、TS-0.30-700、TS-0.30-800和TS-0-450的晶粒尺寸分别为:8.02 nm、8.42 nm、8.88 nm、10.70 nm和24.88 nm.即随着煅烧温度从500℃升至800℃,SiO2-TiO2微球晶粒尺寸逐渐增大,但仍明显小于TiO2微球.
经过800℃煅烧的不同Si/Ti比SiO2-TiO2微球的 XRD图谱如图3(b)所示,TS-0.12-800、TS-0.24-800、TS-0.30-800、TS-0.50-800、TS-0.80-800、TS-1.0-800均具有锐钛矿型TiO2的吸收峰,且随着Si/Ti比的增加,吸收峰强度逐渐减弱,晶粒尺寸分别为:13.61 nm、12.13 nm、10.70 nm、8.99 nm、6.90 nm和6.60 nm.同时,所有样品中均未检测到SiO2的衍射峰,说明微球中的SiO2均为无定形态.已有研究发现[11-12],SiO2的均匀掺杂并形成 Ti-O-Si键,会抑制TiO2晶粒生长和晶相转变温度的升高.对比前述数据表明,SiO2-TiO2微球均实现了SiO2在TiO2微球中的均匀掺杂,无定形态SiO2对微球中TiO2的晶粒尺寸和晶相转变温度具有明显的影响,且Si/Ti比越大晶粒尺寸越小.
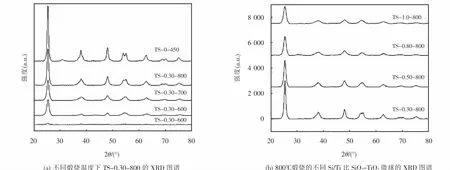
图3 不同煅烧温度和不同Si/Ti比的SiO2-TiO2微球的XRD图谱Fig.3 XRD patterns of SiO2-TiO2 m icrospheres w ith different calcination temperatureand different Si/Ti ratio
2.3 FT-IR分析
图4为TiO2微球和不同Si/Ti比SiO2-TiO2微球的FT-IR图谱.如图4所示,在600 cm-1、930 cm-1、1 100 cm-1和1 600 cm-1处出现的吸收峰分别是由Ti-O-Ti键、Ti-O-Si键、Si-O-Si键和-OH的拉伸震动引起的,TS-0-450仅出现了Ti-O-Ti键和-OH的明显吸收峰,而SiO2-TiO2微球还出现了Ti-O-Si键、Si-O-Si键,且吸收峰强度与 Si/Ti比正相关[13-15].以上数据表明,不同Si/Ti比的SiO2-TiO2微球中Si主要以SiO2和部分Ti-O-Si键形式存在,提高Si/Ti比可以形成更多 Ti-O-Si键.有研究表明[16],Si-O-Si和Ti-O-Si键的相对丰度与催化剂表面酸度有正相关性,而表面酸度的变化会影响金属氧化物对阴阳离子的吸附作用,进而影响光催化反应过程中的降解行为.通过接下来的Zeta电位和光催化降解实验进一步分析上述影响.
2.4 比表面积和孔径分析
为了进一步阐明TiO2微球和SiO2-TiO2微球微观结构的差异,测量了两种样品的N2吸/脱附等温线.如图5所示,TS-0-450和TS-0.30-800的N2-吸/脱附曲线属于具有不同毛细凝聚步骤的IV型吸/脱附等温线,两种样品中均存在介孔,比表面积分别为88.81 m2/g和12.49 m2/g.TS-0-450的吸附等温线表现出分别在P/P0=0.4~0.75(H2型)和P/P0=0.8~1.0时(H4型)观察到两个回滞环,对应于孔径72 nm宽分布的大孔和孔径31 nm窄分布的介孔区域,孔容为0.18 cm3/g.相比之下,在TS-0.30-800微球中仅观察到P/P0=0.8~1.0时的H3型回滞环,对应于孔径分布集中在20 nm的介孔区域,且孔容下降至0.048 cm3/g.如表1所列,其他 Si/Ti比的 SiO2-TiO2微球的比表面积和孔容较TS-0-450均大幅降低,且随着Si/Ti比的增大逐渐减小.而孔径均集中分布于18~20 nm的介孔区域.上述数据说明,非晶态SiO2的加入明显抑制了微球晶体生长过程中颗粒的不均匀收缩和孔的形成,形成了更为致密而均匀的介孔微球[10],这与SEM观测到的图像相印证.
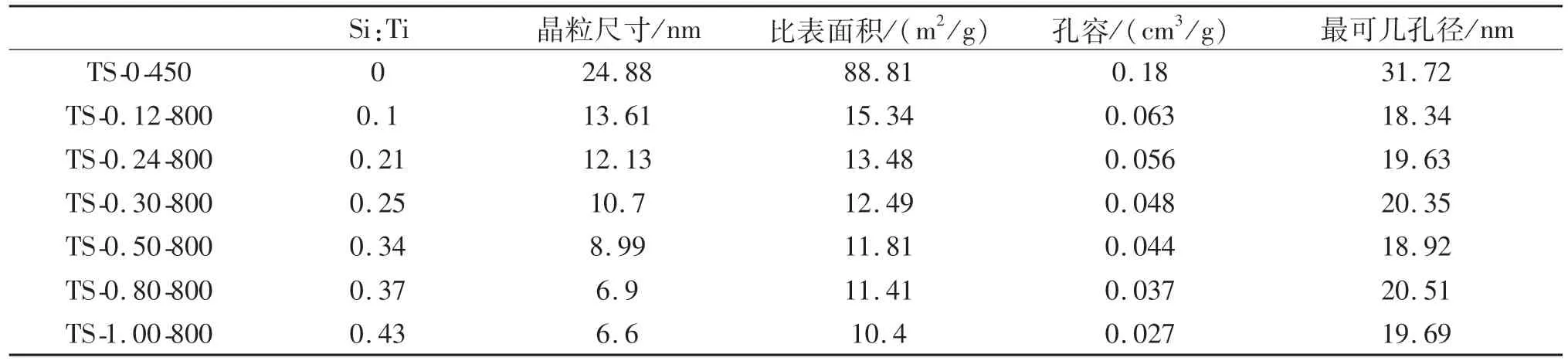
表1 不同样品的Si/Ti值、晶粒尺寸、比表面积、孔体积和最可几孔径Tab.1 Si/Ti value,grain size,specific surface area,pore volume and the most probable pore diameter of different samples
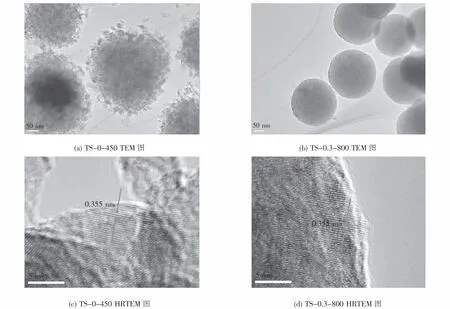
图 2 TiO2微球和 SiO2-TiO 2微球(Si/Ti:0.3)TEM 图Fig.2 TEM and HRTEM image of TiO2 m icrospheres and SiO2-TiO2 m icrospheres(Si/Ti:0.3)
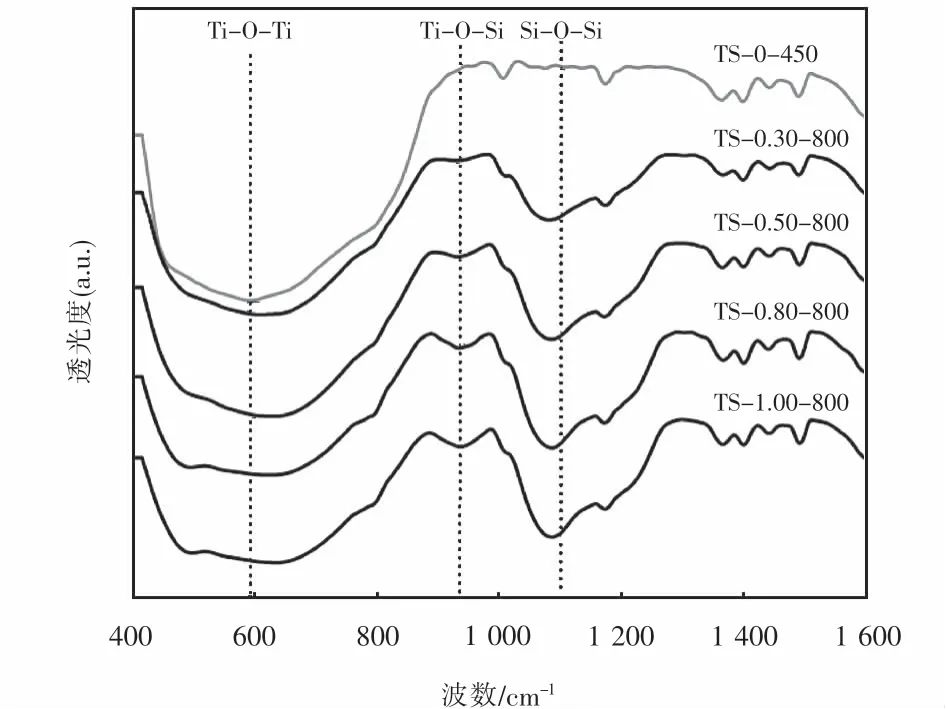
图 4 TiO2微球和 SiO2-TiO2微球(Si/Ti:0.3、0.5、0.8、1.0)的 FT-IR图谱Fig.4 FT-IR spectra of TiO2 m icrospheres and SiO2-TiO2 m icrospheres(Si/Ti:0.3,0.5,0.8,1.0)
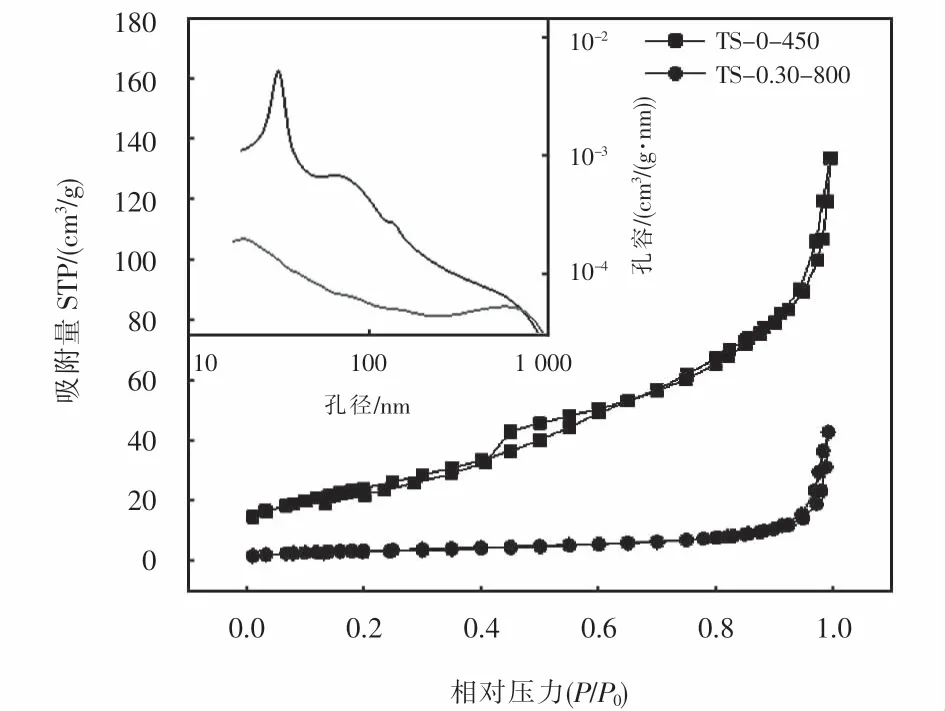
图5 TS-0-450和TS-0.30-800的N2-吸/脱附等温线和孔径分布(插图)Fig.5 N2 adsorption/desorption isotherms and pore size distribution of Ts-0-450 and Ts-0.30-800(illustration)
2.5 Zeta电位
TiO2微球和不同 Si/Ti比的 SiO2-TiO2微球(Si/Ti:0.3、0.5、0.8、1.0)在 pH:2~10范围内的Zeta电位测定结果如图6所示.TS-0-450、TS-0.12-800、TS-0.24-800、TS-0.30-800、TS-0.50-800、TS-0.80-800和TS-1.0-800的等电点分别为:5.23、3.19、2.90、2.66、2.50、2.19和1.22,SiO2-TiO2微球的等电位点随着Si/Ti比的增大而降低.同时,在pH大于等电位点的溶液中,随着Si/Ti比地提高微球表面带负电荷量逐渐增加.如前所述,Si-O-Si和Ti-O-Si可以提高表面酸度,因此在水溶液中的催化剂表面生成更多的带负电的酸性·OH基团,这将导致更负的Zeta电位[16].
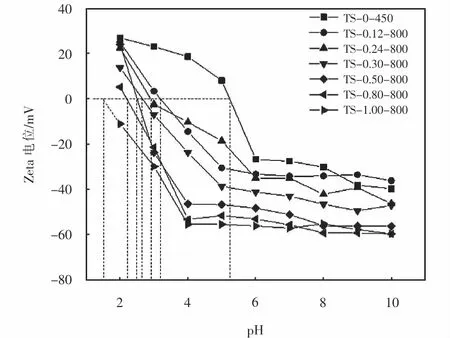
图6 不同pH值下SiO2-TiO2微球的Zeta电位Fig.6 Zeta potential of SiO2-TiO2 m icrospheres at different pH values
2.6 光催化活性
分别以亚甲基蓝(MB)和苯酚(Phenol)为目标降解物,不同Si/Ti比的SiO2-TiO2微球光催化活性如图7所示,由于实验所采用光源的紫外辐射量较小,对目标污染物的光解与光催化降解相比较小,不影响光催化性能的比较.在暗吸附阶段,TS-0-450对MB和苯酚的吸附量均较低(3.83%和0.7%),而SiO2-TiO2微球表现出对两种目标污染物更好的吸附性能(33±1%,1.89% ~8.75%).在光催化反应阶段,TS-0-450对MB和苯酚的降解率分别为88.52%和51.72%,而TS-0.30-800表现出了最优的光催化性能,降解率分别为92.34%和59.49%.
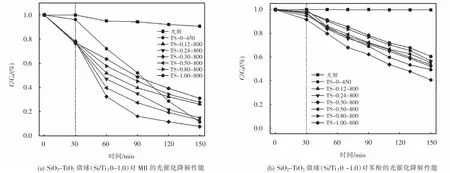
图 7 SiO2-TiO2微球(Si/Ti:0~1.0)对 MB和苯酚的光催化降解性能Fig.7 Photocatalytic degradation of MB and Phenol by SiO2-TiO2 m icrospheres(Si/Ti:0~1.0)
在上述反应过程中,光催化性能受到吸附和降解两方面因素的影响[16-18].如前所述,SiO2-TiO2微球中的Si-O-Si和Ti-O-Si键,导致微球表面产生更多的带负电的酸性·OH基团,对阳离子染料MB和电中性的苯酚的吸附作用更强,从而有效促进了光催化反应效率[19-20].尽管TS-0-450的比表面积是TS-0.30-800的7.5倍,但最佳Si/Ti比的TS-0.30-800却表现出了对MB和苯酚更高的降解率.
3 结论
1)以钛酸异丙酯(TTIP)为钛源,正硅酸乙酯(TEOS)为硅源,氨水为结构导向剂,乙醇为溶剂,乙腈为共溶剂,采用sol-gel+水热+煅烧工艺制备出的SiO2-TiO2微球实现了Ti、O、Si元素的均匀分布,具有良好的单分散性和结构稳定性.为悬浮态TiO2光催化的高效膜分离研究提供了材料基础,有望进一步扩展光催化环境净化技术的应用范围.
2)单分散SiO2-TiO2微球中,以Si-O-Si和Si-OTi形式存在的Si元素有效抑制了晶粒的长大,形成了更为致密的介孔结构,导致其比表面积较TiO2微球大幅度降低.
3)随着Si/Ti比的降低,SiO2-TiO2微球的表面Zeta电位和等电位点也随之降低,对阳离子染料MB和电中性的苯酚的吸附更强.当Si/Ti比为0.3时,对MB和苯酚具有最高吸附和光催化降解速率,光催化反应120 min对MB和苯酚降解率分别为92.34%和59.49%,优于纯TiO2微球.

