加热处理对4种植物油的脂肪酸组成的影响
魏宁果,范芳芳,贾亦森,樊 成,张敏娟
陕西省产品质量监督检验研究院 (西安 710048)
食用植物油是以食用植物油料或植物原油为原料制成的食用油脂。它是人们日常膳食的重要组成部分,为人体提供能量、必需脂肪酸及多种微量营养成分。植物油主要由甘油三酯组成,含有丰富的脂肪酸。市面上的植物油种类繁多,常见的食用植物油包括:菜籽油、花生油、大豆油、玉米油、葵花籽油、棕榈油等。
脂肪酸根据饱和程度(双键的多少)分为饱和脂肪酸(SFA)、单不饱和脂肪酸(MUFA)和多不饱和脂肪酸(PUFA)。不同的脂肪酸功能有所不同,单不饱和脂肪酸酸具有降低血清总胆固醇、甘油三酯等作用,油酸具有抗炎和抗癌的作用,n-3脂肪酸能够预防心血管疾病、冠心病等的发生[1-3]。我国常用的烹饪方式是高温烹调,油脂在高温加热的过程中会发生一系列的化学反应,如水解、氧化(自动氧化、光氧化和酶催化氧化)、聚合、断裂和热致异构化等[4-5]。这些反应受到植物油的品种、温度、时间等多种因素的作用和影响。脂肪酸构成(种类、含量和比例等)是高温加热过程中油脂品质的评价的一个重要参数,很大程度上决定了食用油的营养价值。
本文选用常见的菜籽油、花生油、大豆油、玉米油为实验原料,研究不同加热时间和加热温度对植物油中脂肪酸比例变化的影响。为食用油加热过程品质变化积累数据,指导人们科学合理选择食用油和烹调方式,为科学合理的开发利用食用油提供技术依据和理论参考。
1 材料与方法
1.1 材料与试剂
市售的16个植物油:菜籽油(4个)、大豆油(4个)、花生油(4个)、玉米油(4个)由金龙鱼嘉里粮油有限公司、山东龙大植物油有限公司、渭南石羊长安花粮油有限公司、莱阳鲁花高端食用油有限公司等生产。
37种脂肪酸甲酯混和标准溶液(证书编号:CRM47885),美国sigma公司;异辛烷(色谱纯)和甲醇(色谱纯),格雷斯Grace;硫酸氢钠(分析纯)和无水硫酸钠(分析纯),国药集团化学试剂有限公司;氢氧化钾(分析纯),天津市红岩化学试剂厂;超纯水,电阻率18.2 mΩ·cm2。
1.2 仪器与设备
Agilent 7890A型气相色谱仪(配置FID检测器),安捷伦科技有限公司;BSA224S型电子天平,Sartorius科学仪器有限公司;XK80-A型快速混匀器,江苏新康医疗器械有限公司;UPH-Ⅲ-20T型优普系列超纯水机,成都超纯科技有限公司。
1.3 方法
1.3.1样品加热试验
本实验采用恒温干燥箱对4种食用植物油进行加热实验,分别取油样于玻璃试管中,加热温度为180 ℃和210 ℃,加热时间为 0.5 h、1 h、3 h、5 h,加热后冷却至室温,密封,置于冰箱冷冻备用。
1.3.2脂肪酸甲酯化
参照GB 5009.168—2016《食品安全国家标准 食品中脂肪酸的测定》[6]酯交换法:称取60.0 mg样品于离心管中,加入4 mL异辛烷溶解(必要时可微热溶解),加入200 μL,2mol/ L氢氧化钾甲醇溶液,振摇30 s后静置至澄清。加入约1 g硫酸氢钠,中和氢氧化钾。待盐沉淀后,过滤膜待测。
1.3.3仪器条件
色谱柱,SP-2560(100 m×0.25 mm×0.20 μm)毛细管柱;载气,高纯氮气;分流比30∶1;流速1 mL/min;进样口温度260 ℃;检测器温度280 ℃;升温程序,初始温度140 ℃,保持5 min;以4 ℃/min升至240 ℃,保持15 min;空气流量300 mL/min;氢气流量40 mL/min;尾吹气流量25 mL/min;进样量1 μL。
1.3.4数据分析
采用安捷伦化学工作站(Agilent Chemstation)的数据分析软件进行分析,保留时间定性,面积归一化法定量测定脂肪酸百分含量。实验数据采用Excel 2019和Origin 2019软件进行计算分析和作图。油脂氧化能力的计算参照下式计算:
COS=(1×油酸含量+10.3×亚油酸含量+21.6×亚麻酸含量)/100
2 结果与讨论
2.1 试验条件的优化
气相色谱测定脂肪酸需要对其进行衍生化处理,目前脂肪酸的衍生化技术包括氢氧化钾-甲醇法、三氟化硼-甲醇法和硫酸-甲醇法。酸催化法适于酯化游离脂肪酸,而碱催化法更适合甘油三酯的甲酯化[7-8]。结合植物油脂肪酸的存在形式和酯化效率等因素,选择碱催化法,三氟化硼具有较强的毒性,而氢氧化钾-甲醇法无需冷凝回流装置、操作简便,重现性好。故选用氢氧化钾甲醇法作为甲酯化方法。
鉴于脂肪酸种类较多(37种)、碳链分布范围宽、存在双键的顺反异构和化学性质相似等,分离较为复杂,实验选用100 m的极性色谱柱(固定相:强极性氰丙基硅氧烷类)、优化升温程序、流速、进样口温度、检测器温度等色谱条件,得到了较好的分离效果,且峰型较好,分离度、检出限及精密度等指标均能满足定性、定量分析要求。
2.2 不同植物油的脂肪酸组成
按照本试验的最佳参数条件对选取的4种植物油(共16个样品)的脂肪酸组成进行分析,主要脂肪酸组成及相对含量见表1所示。由表1可以看出,16个植物油的主要脂肪酸组成均符合相关的国家食品安全标准的特征指标要求,主要由棕榈酸、硬脂酸、油酸、亚油酸、亚麻酸、花生酸、花生一烯酸等长链脂肪酸组成,以C18和C16脂肪酸为主要脂肪酸,饱和脂肪酸主要以棕榈酸和硬脂酸为主。其中玉米油和大豆油中以多不饱和脂肪酸为主(含量57.97%~63.17%),尤其是亚油酸含量最高;菜籽油中以单不饱和脂肪酸的含量最高(含量55.84%~62.76%),主要以油酸为主,饱和脂肪酸的含量最低,试验选取的4个菜籽油的芥酸含量均<3%,属于低芥酸菜籽油[9];花生油中单不饱和脂肪酸和多不饱和脂肪酸的含量相当,饱和脂肪酸含量最高。该结果与廖静[10]等的研究结果一致。不同脂肪酸比例的植物油的氧化能力不同,较难用一种脂肪酸含量来评价其氧化能力。有学者用油脂氧化能力计算值(COX)来评价油脂的氧化稳定性[11-12],结合各植物油脂肪酸含量,经计算后,大豆油、玉米油、菜籽油、花生油的COX值范围分别为7.12~7.51、6.34~6.57、4.75~5.39、3.82~4.39。
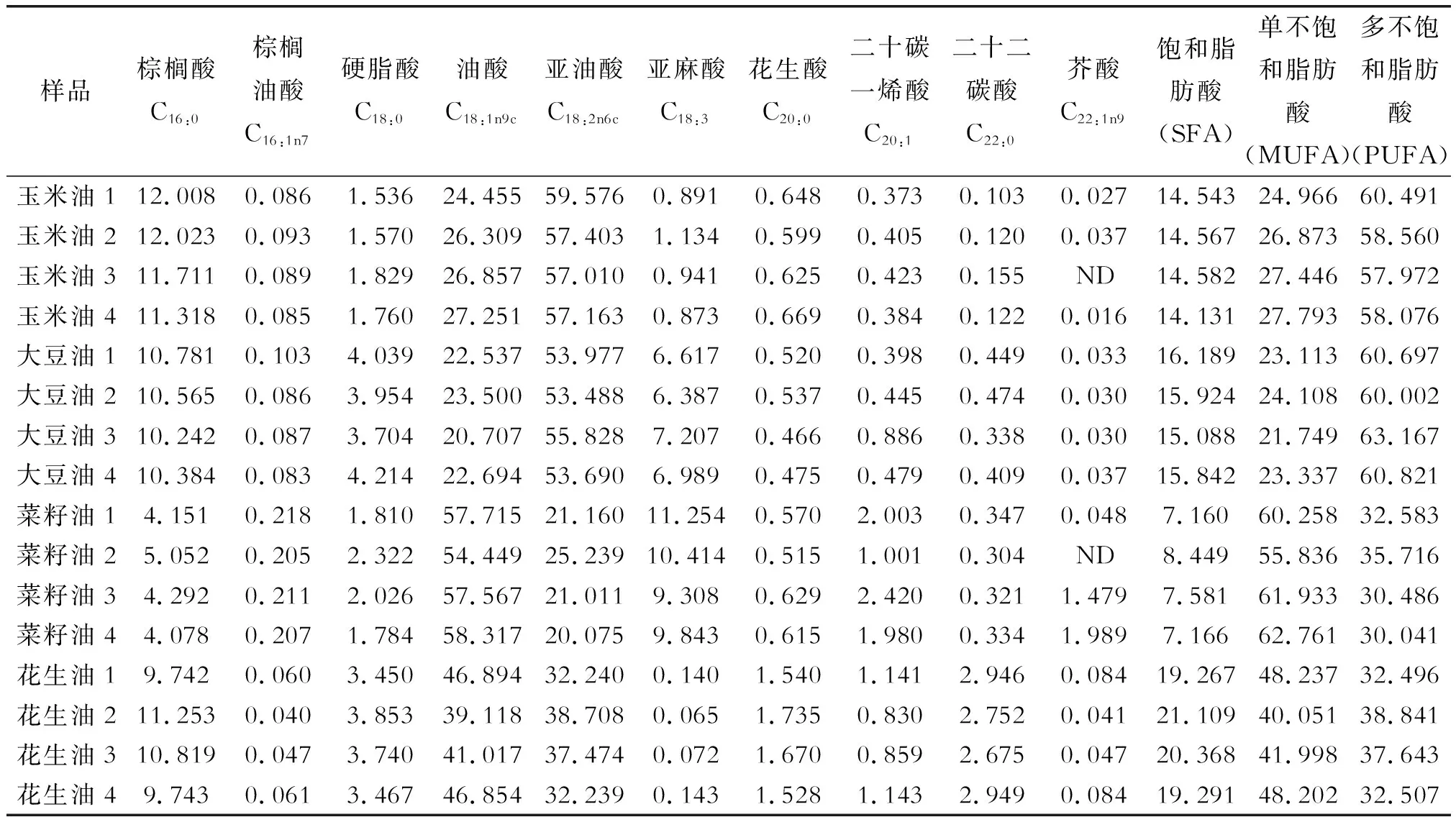
表1 不同植物油的脂肪酸组成及相对含量 %
2.3 加热处理对脂肪酸组成的影响
同种植物油加热处理后脂肪酸的变化规律是一致的,故每种植物油选择一个进行分析。4种植物油在180 ℃和210 ℃下不同加热时间的主要脂肪酸含量变化,如表2和表3所示。由表中可以看出随着温度的增加和时间的延长,4种植物油的脂肪酸组成都发生了变化,棕榈酸、硬脂酸、油酸含量与加热时间呈正相关,亚油酸和亚麻酸含量与加热时间呈负相关,这与文献报道的结果是一致的[13-14]。4种植物油之间没有显著性差异,可能是油脂加热过程中发生的水解、氧化、聚合、热致异构化等反应是一致的。
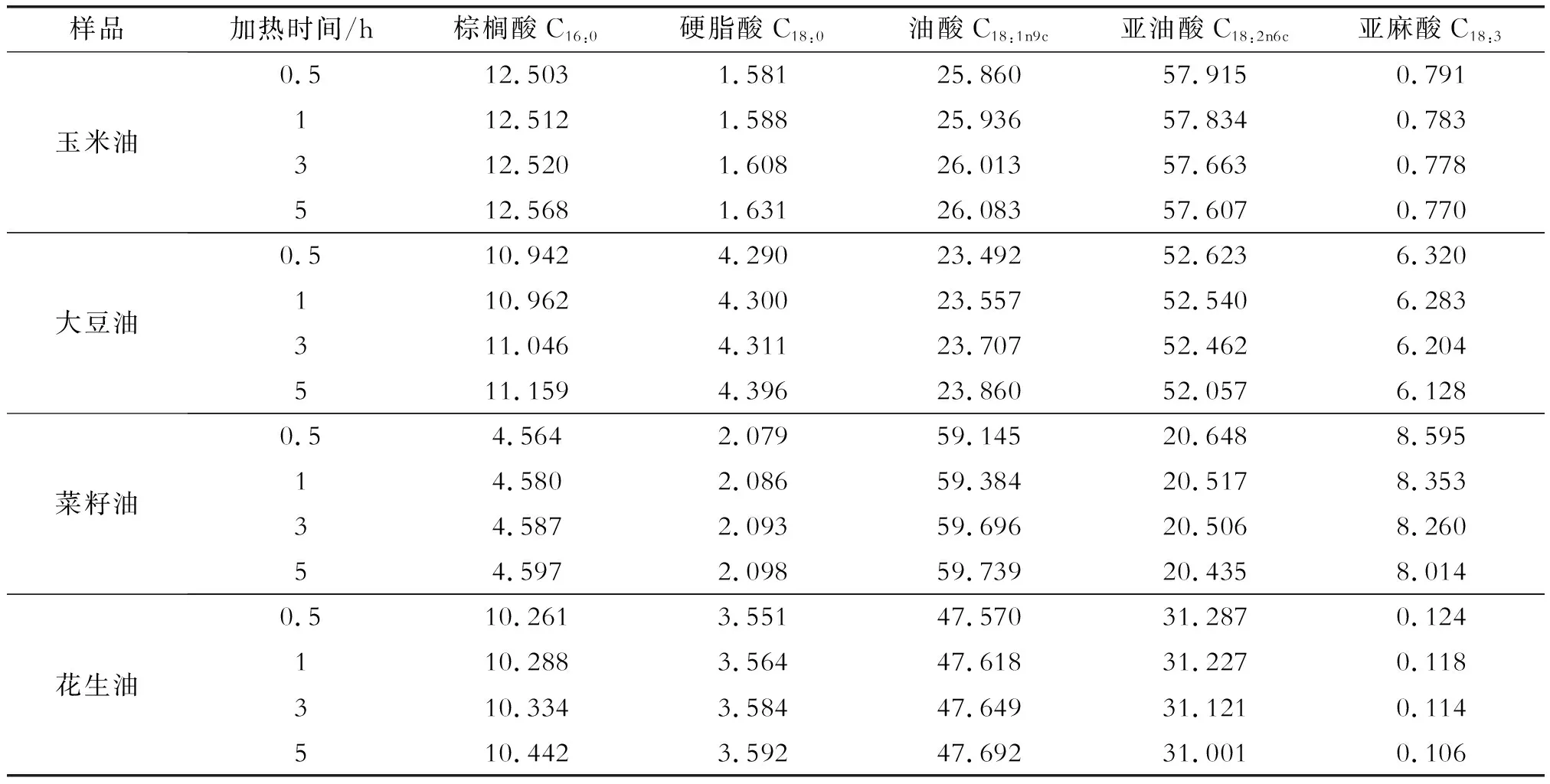
表2 植物油180 ℃加热处理后的脂肪酸含量 %
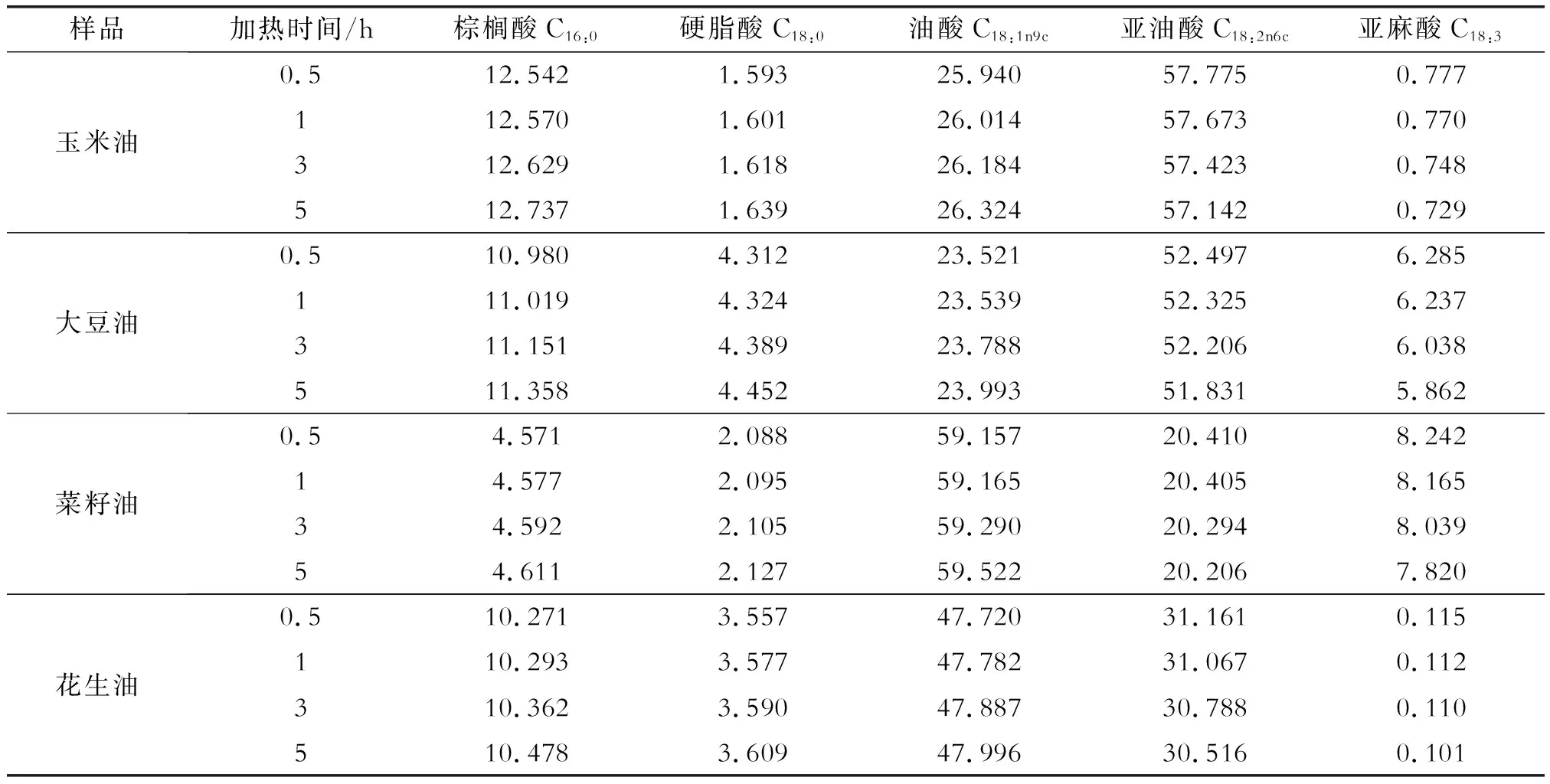
表3 植物油210 ℃加热处理后的脂肪酸含量 %
4种植物油在180 ℃和210 ℃下不同加热时间的饱和脂肪酸、单不饱和脂肪酸、多不饱和脂肪酸变化如图1所示。由图1可以看出,4种植物油变化趋势是一致的,饱和脂肪酸和单不饱和脂肪酸在180 ℃和210 ℃下随着加热时间的延长而增加,多不饱和脂肪酸随着加热时间的延长而减少,并且210 ℃的变化幅度更大,这与文献报道的研究结果一致[13, 15]。这可能由于在高温加热条件下,植物油中不饱和脂肪酸不稳定,容易发生降解和氧化,分解成单不饱和脂肪酸、饱和脂肪酸、甘油二酯、单酰基甘油、游离脂肪酸、甘油等并形成挥发性化合物包括醛、醇、酮等小分子物质[16]。加热时间与食用油中多不饱和脂肪酸含量有负相关性,时间越长,含量越少。210 ℃下加热5 h,4种植物油多不饱和脂肪酸分别降低了2.58%(玉米油)、2.91%(大豆油)、2.43%(菜籽油)、1.79%(花生油),该结果与植物油的油脂氧化能力值(COX)结果一致,因此利用COX值来评价油脂的氧化稳定性是可行的,同时也说明多不饱和脂肪酸含量高的油脂的氧化稳定性较差。
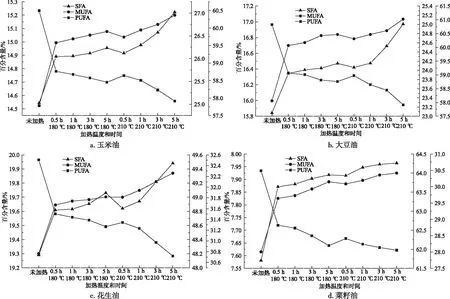
图1 加热处理对4种植物油脂肪酸的影响
3 结论
本文采用气相色谱法对4种植物油(玉米油、大豆油、菜籽油、花生油)的脂肪酸组成进行分析,利用峰面积归一化法进行定量,并研究了在180 ℃和210 ℃下加热不同时间(0.5 h,1 h,3 h,5 h)后脂肪酸组成的变化。结果表明:加热处理后4种植物油的脂肪酸组成都发生了变化,饱和脂肪酸(棕榈酸、硬脂酸)和单不饱和脂肪酸(油酸)的含量与加热时间呈正相关,多不饱和脂肪酸(亚油酸、亚麻酸)的含量与加热时间呈负相关,并且210 ℃的变化幅度更大。本文研究成果为食用油烹调安全提供理论参考,指导人们科学合理选择食用油,降低应用成本,具有十分重要实际应用价值。

