接受围手术期标准加速康复管理的颅内动脉瘤患者营养状态与显微外科夹闭术后并发症关系研究
王李,李振水,吴俊,许英霞,郝春满
颅内动脉瘤是发病率较高的脑血管疾病,破裂后致残率和致死率极高[1]。显微外科夹闭手术为颅内动脉瘤的有效治疗方式,有研究显示改善患者围手术期的营养状态可减少术后并发症,从而提高患者的预后[2]。目前针对颅内动脉瘤手术患者围手术期营养状态的研究较少,围手术期营养干预措施也缺乏循证医学的证据支持[3]。在此背景下,本研究对颅内动脉瘤显微夹闭手术患者进行了标准加速康复管理,并对其围手术期的营养状态进行了调查,分析营养状态与术后并发症的关系,为改进颅内动脉瘤患者围手术期管理提供依据。
1 对象与方法
1.1 研究对象 前瞻性连续入组2018年1月- 2019年3月在首都医科大学附属北京天坛医院神经外科进行显微外科夹闭手术的颅内动脉瘤患者。纳入标准:①年龄18~75岁;②颅内前循环(包括颈内动脉颅内段、大脑前动脉、大脑中动脉及其分支、前交通动脉和后交通动脉)动脉瘤;③动脉瘤未破裂或动脉瘤破裂但Hunt-Hess分级≤4级;④进行了动脉瘤显微外科夹闭手术;⑤术前美国麻醉协会病情分级1~4级;⑥患者及家属同意参与研究并签署知情同意书。排除标准:①术前手术区域存在感染或炎症;②精神疾病或严重心理疾病;③妊娠期、哺乳期女性;④参与其他临床研究;⑤晚期肿瘤或预期寿命<1年。
本研究获得首都医科大学附属北京天坛医院伦理委员会的批准(批准号:KY2018-059-02)。
1.2 数据收集和分析 收集患者的临床资料,包括人口学信息(年龄、性别);既往病史(高血压、糖尿病);动脉瘤的特点(部位、直径、是否破裂);术前营养相关指标(血红蛋白、白蛋白、空腹血糖水平,白细胞、血小板计数及纤维蛋白原水平);术后至出院前的感染性和非感染性并发症情况。
感染并发症包括颅内感染和肺部感染。颅内感染诊断标准[4]:①患者出现发热、颅内高压,脑脊液浑浊或脓性、白细胞增多、葡萄糖含量<2.2 mmol/L及脑脊液葡萄糖含量/血清葡萄糖含量≤0.4 mmol/L,颅内感染临床诊断成立。②在临床诊断基础上,出现标本涂片、引流管头、植入物及脑脊液微生物培养阳性(排除污染和定植),病原学诊断成立。肺部感染依据《医院获得性肺炎诊断和治疗指南(草案)》诊断[5]。非感染并发症包括下肢深静脉血栓形成和卒中。下肢深静脉血栓形成由下肢彩色多普勒超声检查明确诊断。卒中包括缺血性卒中和颅内出血,出现相应症状后经头颅CT确诊。
根据术后是否发生上述1个及以上并发症,将患者分为并发症组和无并发症组。比较2组的基线资料和营养学指标的差异。
1.3 围手术期营养干预方法和营养指标的检测所有患者住院期间均接受标准加速康复管理,其中营养管理流程包括术前营养风险筛查、营养评定及干预,术后动态营养检测和干预。围手术期营养干预方案和流程由神经外科、营养科、麻醉科医师和责任护士共同讨论制订。
1.3.1 术前营养风险筛查、营养评定及干预患者入院24~48 h内采用营养风险筛查2002(nutritional risk screening 2002,NRS 2002)评分进行营养风险筛查,NRS2002评分≥3分为存在营养风险。营养相关的人体测量指标包括①身高:患者赤足,测试人员读数时双眼应与压板平面等高;②体质量:患者清晨空腹,排空大小便,穿单衣裤立于体重计中心测量;③BMI;④上臂围:测量时左臂自然下垂,用软皮尺先测出上臂中点位置(鹰嘴和尖峰连线中点),然后测中点位置的上臂周长;⑤三头肌皮褶厚度(triceps skinfold thickness,TSF):被测者上肢自然下垂,测定者以左手拇指将上臂背侧中点皮肤连同皮下组织捏起,从拇指下测量1 cm左右处皮褶厚度,应注意皮褶厚度计与上臂垂直。如患者为卧床,则将前臂舒适地横置在胸部进行测量;⑥小腿围:用皮尺测量小腿最宽处周径;⑦握力:用电子握力计测量优势手的握力,测量3次,取平均值。经营养评定后,由营养科医师依据《营养风险及营养风险筛查工具营养风险筛查2002临床应用专家共识(2018版)》诊断患者是否存在营养不良[6]。
术前营养干预:对NRS2002评分<3分的患者术前给予饮食宣教,强调蛋白质类食物摄入;对NRS2002评分≥3分的患者制订对应的营养支持方案,计算患者住院期间的每日目标能量摄入(25~30 kcal/kg,1 kcal=4.18 kJ)[7],由营养科医师决定进一步营养支持方案,如口服营养补充(oral nutritional supplements,ONS)或启动肠内营养(enteral nutrition, EN);若72 h仍未达到目标能量摄入的60%,可考虑联合肠外营养(parenteral nutrition, PN)支持。
术前措施:术前6 h停止进固体食物,术前2~3 h可口服5%葡萄糖溶液200 mL(除既往有胃食管反流病患者);术前2 h内禁水。
1.3.2 术后营养支持措施和营养评定 ①无吞咽障碍的清醒患者术后早期恢复经口进食:术后4 h鼓励进水;术后6~12 h给予肠内营养粉250 mL;术后12~24 h开始进食流食,联合肠内营养粉250 mL;24~48 h进食半流食;术后48 h进普食。②术前无营养风险的患者常规不加用ONS,术后3 d经口进食无法达到目标能量摄入量的60%考虑加用ONS(根据需要量调整剂量)。③术后管饲的患者:对出现吞咽困难或意识障碍的患者,术中留置鼻胃管/鼻肠管给予管饲喂养。术后6~12 h给予5%葡萄糖/米汤试餐,无胃肠道并发症者术后12~24 h过渡至短肽型肠内营养制剂;术后24~48 h过渡至整蛋白型肠内营养制剂;术后48 h逐渐增加至目标能量摄入。④PN:对于术后72 h给予ONS或鼻饲肠内营养制剂后,仍无法达到目标能量摄入60%的患者,考虑补充性PN支持,对于不耐受肠内营养的患者,给予PN。⑤对住院期间存在营养不良的患者,出院前给予个体化营养指导。
术后营养评定指标包括术后1 d和出院时的血红蛋白、白蛋白和血糖水平,术后恢复普食时间,非自主体重下降(入院时空腹体重-出院时空腹体重)及出院时是否存在营养不良。
1.4 统计学方法 使用SPSS 18.0统计软件。计量资料符合正态分布,采用表示,不符合正态分布的用M(P25~P75)表示,组间比较采用独立样本t检验或非参数检验。计数资料采用频数和率(%)描述,组间比较采用χ2检验。利用logistic回归进行多因素分析,将单因素分析中P<0.05的变量以及根据临床经验判断可能对结局指标有影响的变量作为自变量,将手术并发症作为因变量(有并发症=1,无并发症=0),筛选出可能影响颅内动脉瘤术后并发症的因素。以P<0.05为差异有统计学意义。
2 结果
2.1 并发症组和无并发症组基线资料比较结果 共纳入患者97例,年龄28~71岁,平均55.6±8.8岁,其中男性46例(47.4%),女性51例(52.6%)。64例术后无并发症,33例发生术后并发症,其中有6例出现2种及以上并发症,发生肺部感染7例(21.2%),颅内感染8例(24.2%),下肢深静脉血栓13例(39.4%),卒中11例(33.3%)。并发症组既往高血压、糖尿病史比例,动脉瘤破裂比例高于无并发症组,差异有统计学意义;2组年龄、性别、动脉瘤部位和直径等指标的差异无统计学意义(表1)。
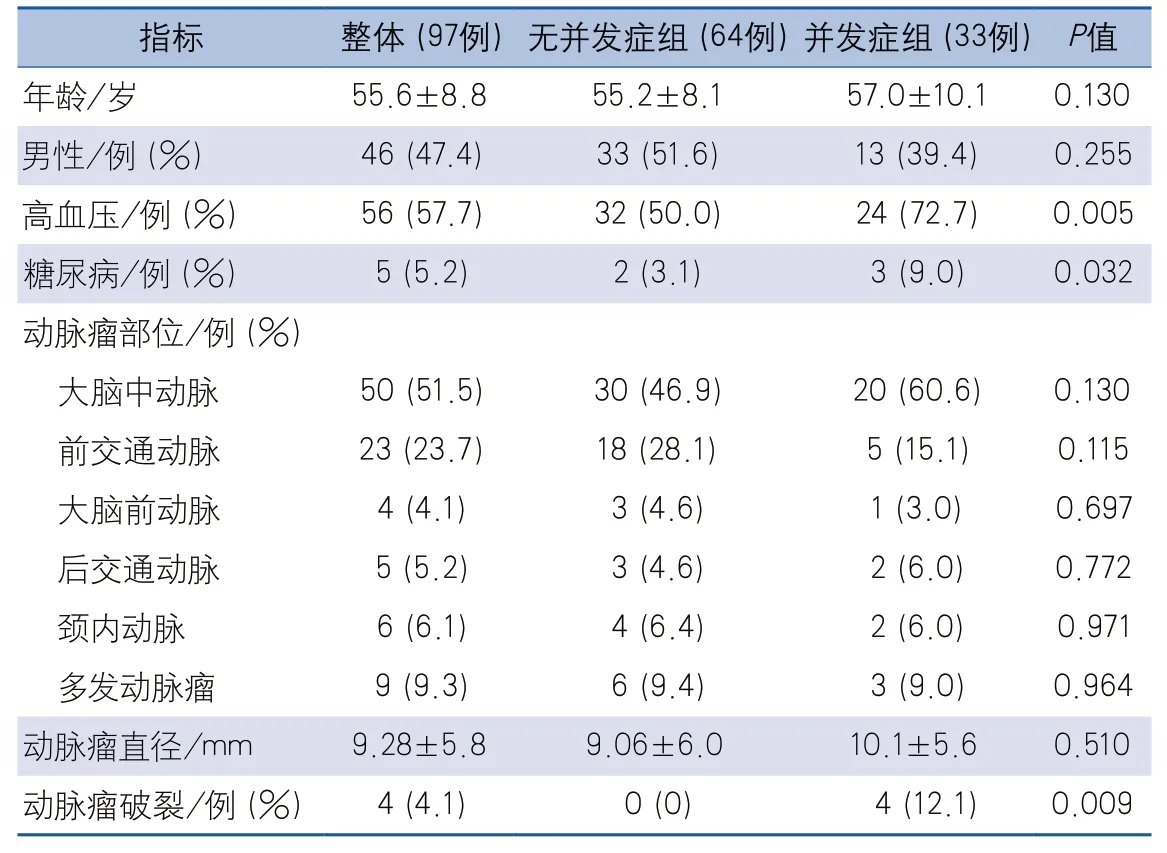
表1 并发症组和无并发症组基线资料比较
2.2 并发症组和无并发症组营养相关指标比较结果 单因素分析显示并发症组术前BMI、TSF、小腿围均高于无并发症组,血红蛋白水平低于无并发症组,差异有统计学意义;并发症组术后营养干预以及不同营养方式(ONS、EN、PN)支持的比例均高于无并发症组,PN持续时间长于无并发症组,差异有统计学意义;其余指标2组间差异无统计学意义(表2)。
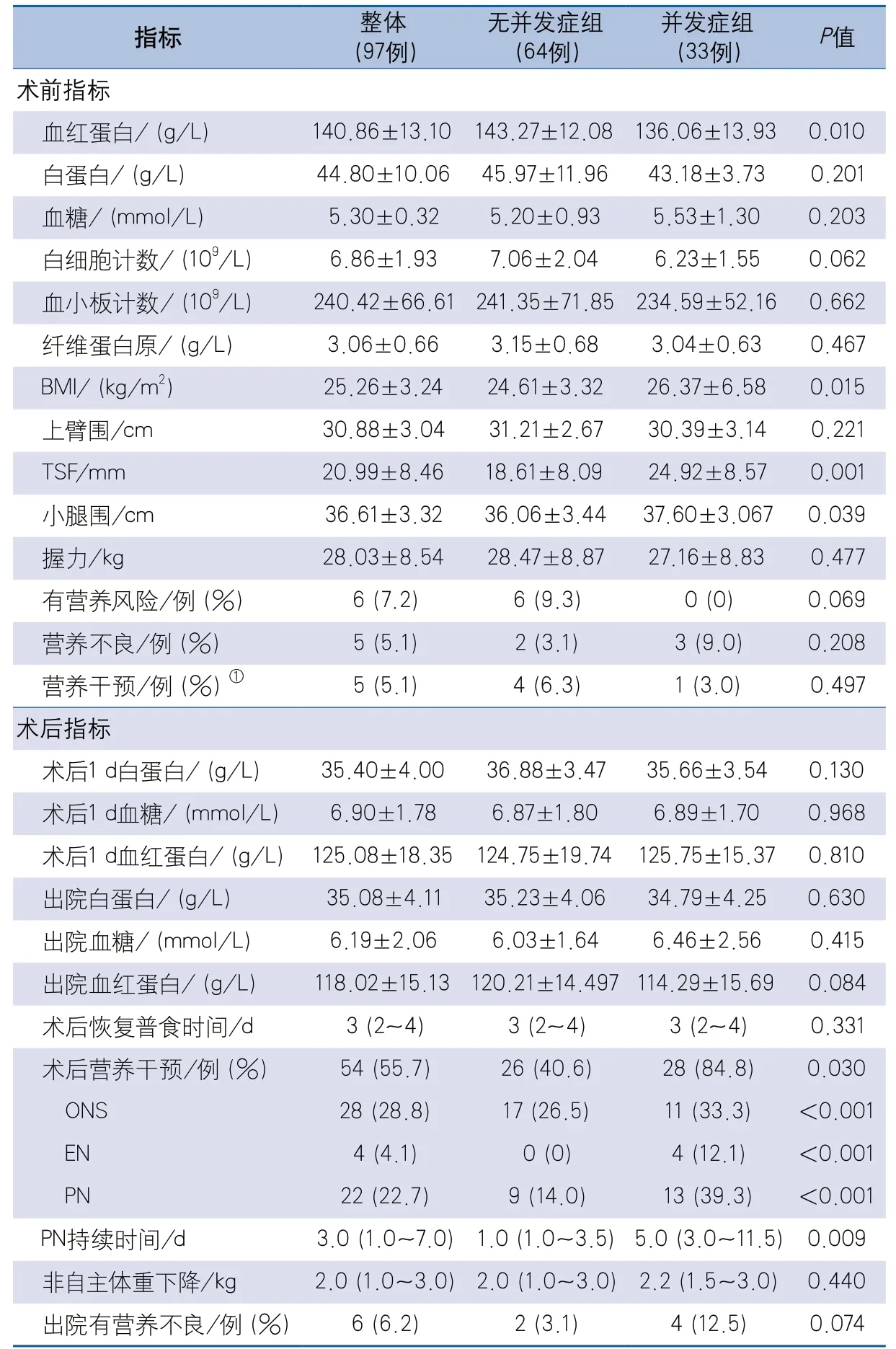
表2 并发症组和无并发症组营养相关指标比较
2.3 营养相关指标对并发症影响的多因素分析结果 多因素分析显示,患者术前高TSF是术后并发症的独立危险因素,术后1 d白蛋白水平高是术后并发症的独立保护因素(表3)。
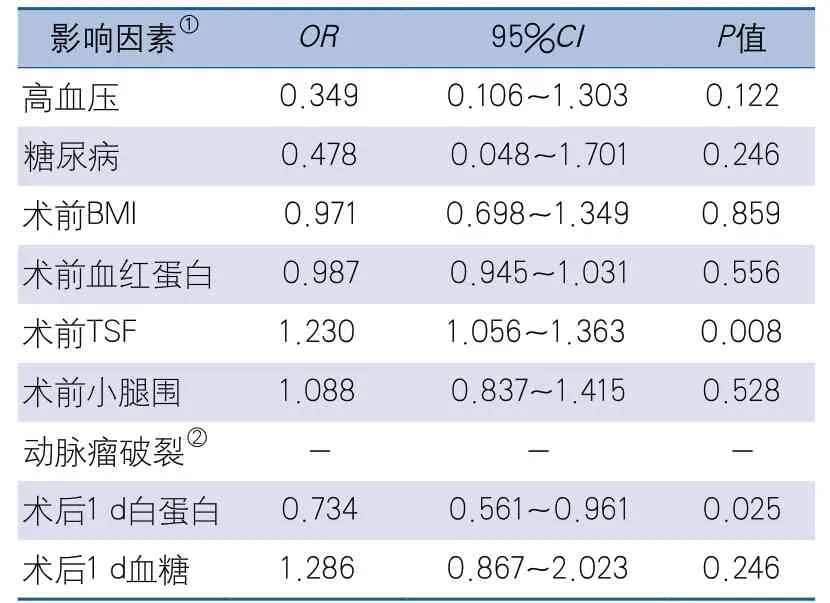
表3 颅内前循环动脉瘤并发症独立影响因素分析结果
3 讨论
本研究通过多因素logistic回归分析发现,术前TSF和术后1 d白蛋白水平与前循环动脉瘤患者显微外科夹闭术后并发症相关。TSF是判断皮下脂肪情况的一项重要指标。有报道显示外科手术患者的皮下脂肪厚度与术后伤口感染有关[8]。本研究结果显示对于颅内前循环动脉瘤患者,术前的TSF较高则术后感染等并发症风险升高。白蛋白是临床常用的营养学指标,但除营养状态外,其他因素也可能影响白蛋白水平,如炎症状态下患者体内毛细血管通透性增加、体液重新分布等因素也可引起白蛋白降低[9-10]。本研究中发现颅内前循环动脉瘤患者术后1 d白蛋白水平为术后并发症的保护性因素,即术后白蛋白水平越高,患者术后并发症风险越低。既往有研究者认为,较高的白蛋白水平利于颅内动脉瘤患者术后脑灌注的维持,而白蛋白水平降低与患者术后应激状态和炎症程度有关[11]。另一项多中心观察性研究也发现入院72 h内白蛋白水平降低与动脉瘤性蛛网膜下腔出血患者住院期间感染并发症增加有关[12]。
目前有研究者认为传统的术前禁食方式可增加患者的术后应激,不利于术后恢复[13]。加速康复外科管理下术前给予患者口服碳水化合物,让患者从“禁食”状态转变为“进食”状态,从而减少术后胰岛素抵抗和蛋白质丢失的风险,保护肌肉组织[14-15]。患者术后早日恢复经口进食,摄入充足的蛋白质,为合成代谢提供充足的营养底物,利于骨骼肌的保留和减少应激因素。上述干预措施均是减轻手术应激的可行措施。本研究对患者围手术期进行了标准加速康复管理,管理方案由神经外科、营养科、麻醉科医师和责任护士共同讨论制订,具体措施包括术前营养风险筛查、营养评定及干预,术后动态营养检测和干预。在此干预背景下,未发现颅内动脉瘤患者术前营养风险和营养不良与术后并发症增加有关。研究中颅内动脉瘤患者术前存在营养风险比例为7.2%,术前存在营养不良的比例为5.1%,低于既往报道中其他外科如普外科、胸外科患者术前营养风险比例和营养不良的比例[16]。可能由于本研究入组的颅内动脉瘤患者术前营养状态较好,平均BMI在25 kg/m2以上有关。另外,本研究中患者出院时营养不良发生率为6.2%,也相对较低,提示标准加速康复管理可能有利于患者术后营养支持,改善术后营养不良的发生。但本研究并没有针对标准加速康复管理干预措施设立对照研究,因此不能得出确切的结论,后续可针对标准加速康复管理进行随机对照研究以进一步探索更优良的动脉瘤夹闭手术围手术期营养管理措施。
本研究未能对出院患者进一步随访,无法对患者远期并发症、营养状态进行监测。样本量较小,有待更大样本的关于颅内动脉瘤患者围手术期营养的临床研究。
【点睛】本研究对前循环颅内动脉手术患者围手术期营养状态和营养支持进行了标准加速康复管理,并进行了前瞻性调查,发现TSF和术后1 d白蛋白水平是术后并发症的独立影响因素。

