万古霉素对颅脑损伤患者术后颅内感染预防效果分析
骆苗虹,张瑜君,康丽珊
(中国人民解放军联勤保障部队第九一〇医院神经外科,福建 泉州 362000)
颅脑术后患者继发颅内感染的可能性较大,主要由于病原菌侵入大脑引发,术中颅内物质与外界异物接触,容易造成多种病原菌或者细菌进入至颅内并导致颅内感染风险升高[1,2]。此外,颅内失活脑组织可促进细菌及病原菌繁殖,若治疗不当,可造成患者出现发热、呕吐等症状,甚至会对患者正常脑组织造成损伤,对其预后改善会产生不良影响,若干预措施不当或者不及时,不但会对手术治疗效果造成影响,甚至会对患者生命安全产生威胁[3,4]。因此,早期应用抗生素对于降低颅脑术后感染风险至关重要。此次研究对象为74例纳入颅脑损伤患者,患者在本院接受颅脑手术时间为2019年1月-2022年4月,分析万古霉素联合综合性干预措施在术后颅内感染中的防控效果,研究结果汇报如下:
1 资料与方法
1.1 临床资料
随机选取74例颅脑损伤患者,依照患者采用干预方式将其分成对照组与观察组,两组均有样本量37例。对照组:男性21例、女性16例,年龄范围为27~79岁,年龄平均值为(44.38±3.09)岁,颅脑损伤原因如下:脑出血7例、跌伤8例、车祸伤12例、高空坠落受伤5例、其他原因5例。观察组:男性22例、女性15例,年龄范围为25~76岁,年龄平均值为(45.14±3.12)岁,颅脑损伤原因如下:脑出血6例、跌伤9例、车祸伤11例、高空坠落受伤5例、其他原因6例。对比患者受伤原因、性别及年龄无显著差异(P>0.05),存在可比性。伦理委员会对研究方案进行审核后批准。
纳入标准:①符合《中国神经外科重症患者感染诊治专家共识(2017年版)》[5]中的颅内感染相关诊断标准符合且结合患者临床表现、影像学检查结果与实验室检查结果等确诊;②均首次接受颅脑手术;③对此次研究药物能够耐受且无过敏反应;④患者家属对本次研究方案及风险知情并在研究同意书上签字;⑤患者能够积极配合用药并进行调查研究。
排除标准:①合并恶性病变者;②合并肝肾功能障碍者;③存在腰椎穿刺禁忌症者;④合并部位感染者;⑤有未得到有效控制感染者;⑥肝肾心等重要脏器功能异常者;⑦由于病情恶化或者转院等自本研究脱落者。
1.2 方法
对有感染征象者进行药敏试验并依据试验结果为患者选择抗生素,对照组患者采用利奈唑胺静脉滴注及常规护理,观察组患者万古霉素鞘内注射及综合护理。
对照组患者实施利奈唑胺600mg静脉滴注治疗,每日滴注2次。
观察组患者行常规腰椎穿刺并使穿刺针位于蛛网膜下腔,穿刺成功后连接测压表并对脑脊液压力进行准确记录,然后将脑脊液缓慢放出,将脑脊液标本2~4mL置于无菌试管中并实施脑脊液常规检验、生化指标检验以及细菌培养与药敏试验,待脑脊液放出一定量时以0.9% 氯化钠注射液反复冲洗,每次注入置换液5~10mL,待脓性脑脊液呈清亮状且脑脊液压力降至约100 mmH2O时向椎管后缓慢注入万古霉素5mg及地塞米松2~3mg,然后将穿刺针拔出。通常情况下,置换液总量需少于引流液总量,若置换液量为50~200mL,进行脑脊液置换时需要将脑脊液缓慢放出。操作完成后将穿刺针芯插入并将穿刺套管针拔出,通过碘伏对穿刺点周围部位皮肤实施消毒,应用无菌纱布对穿刺部位进行覆盖,每日用药1次。
1.3 观察指标
(1)统计并对比两组术后颅内感染率,颅内感染率=颅内感染例数/总例数*100%。
(2)对比干预前后患者脑脊液检测指标水平,包括晚期糖基化终末产物受体[晚期糖基化终产物受体(RAGE)、高迁移率族蛋白-1(HMGB-1)],干预前后通过腰椎穿刺留取脑脊液标本并离心5min,速度为3000r/min,通过酶联免疫吸附法测定RAGE及HMGB-1。
(3)对比干预前后患者炎性因子水平,包括降钙素原(PCT)、肿瘤坏死因子-α(TNF-α)、白细胞介素-(IL-6),治疗前后抽取患者脑脊液并离心,以酶联免疫吸附试验进行TNF-α及IL-6检测,采用全自动血液分析仪测定患者血清降钙素原(PCT)水平。
(4)统计两组术后脑水肿、消化道出血、癫痫发生情况,(脑水肿例数+消化道出血例数+癫痫例数)/总例数*100%即为并发症总发生率。
1.4 统计学方法
2 结果
2.1 颅内感染率对比
对照组术后颅内感染患者7例,颅内感染率达18.92%,观察组术后颅内感染患者1例,颅内感染率达2.70%,观察组术后颅内感染率显著低于对照组,两组感染率差异有统计学意义(χ2=5.046,P=0.025)。
2.2 干预前后患者脑脊液检测指标水平对比
干预前患者脑脊液检测指标水平无明显差异(P>0.05),干预后观察组RAGE及HMGB-1水平均更低(P<0.05)。见表1。
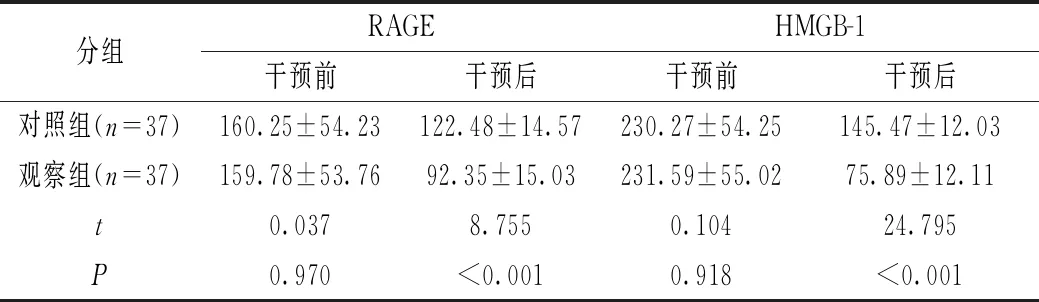
表1 比较干预前后患者脑脊液检测指标水平(ng/mL)
2.3 干预前后患者炎性因子水平对比
干预前患者炎性因子水平组间对比差异不显著(P>0.05),干预后观察组PCT、TNF-α及IL-6水平均较对照组低(P<0.05)。见表2。

表2 比较干预前后患者炎性因子水平
2.4 并发症情况对比
患者并发症总发生率组间对比可知,观察组显著更低且差异有统计学意义(P<0.05)。见表3。

表3 比较术后两组并发症[n(%)]
3 讨论
患者颅脑手术颅骨结构受损,脑内组织液与外界联通,在人为因素及外界环境因素等的影响下患者发生颅内感染的风险较高,一旦出现颅内感染可导致患者残疾风险及死亡风险显著增加,严重影响其预后,因此,必须科学、合理且及时的应用抗菌药物以使患者生存质量获得提高,同时减轻其心理压力与经济负担[6-7]。
颅脑手术具有手术难度大、创伤大以及风险高等特点,脑组织与外界间接或者直接相通,可导致感染风险增加,此外颅脑损伤患者机体免疫力较差,使得感染几率进一步增加。针对头颈部手术患者需要为其提供针对金黄色葡萄球菌的抗菌药物以降低金黄色葡萄球菌感染风险。利奈唑胺具有非浓度依赖性以及口服吸收迅速等特点,用药后1~2h即可达到血浆浓度,生物利用度极高,可达到100%,口服与静脉滴注序贯治疗均可,无需对用药剂量进行调整,用药后药物迅速在灌注良好的组织中分布,具有较强的组织穿透力,可迅速穿透血脑屏障。利奈唑胺与5-羟色胺类药物或者类肾上腺素能等药物可相互作用,在感染预防中效果确切。该药物在肺泡中有着较高的浓度,在临床上被广泛应用于肺部感染与皮肤软组织感染等病症的治疗,在神经外科术后颅内感染中也能够取得一定的效果,本次研究结果证实该药物对于控制颅脑损伤术后颅内感染也可取得一定的效果。
万古霉素在临床上应用广泛,能够使金黄色葡萄球菌、肺炎球菌、溶血性链球菌、表皮葡萄球菌及革兰阴性菌等病原菌得到有效杀灭,还可与细菌细胞壁前体肽聚末端丙氨酰丙氨酸有效结合,对肽聚糖合成可发挥阻断作用并能够破坏细胞壁,而且与其他抗生素联用不会产生交叉耐药性,极少生成耐药菌株[8-9]。除此之外,万古霉素还能够改善细胞膜渗透性,对细菌RNA合成产生抑制作用,从而取得杀灭细菌的效果[10]。万古霉素鞘内给药的方式药物不经过血脑屏障,而是经腰椎穿刺后直接进入至蛛网膜下腔,能够保证脑脊液与蛛网膜下腔等局部药物浓度,可直接产生杀菌效果,有助于提高用药效果并有效减轻患者炎性反应及脑损伤,进而可减少癫痫、脑水肿等并发症,可显著降低术后颅内感染等发病风险。对蛛网膜下腔反复冲洗可使黏稠脑脊液得到稀释,有助于促进引流,使脑脊液细菌与坏死组织获得清除,促进患者健康恢复。
此次研究中,两组干预效果对比,观察组术后颅内感染率显著更低,RAGE、HMGB-1水平、PCT、TNF-α、IL-6水平及并发症总发生率均更低(P<0.05)。作为水溶性药物,万古霉素对血脑屏障的穿透力相对较差,即便药物能够进入脑脊液,其浓度也无法达到最低抑菌浓度,因此,静脉滴注用药方式难以提高体内有效抑菌浓度,而且起效慢,抗菌作用相对较差。鞘内注射则能够对局部发挥针对性作用,能够使脑脊液中血药浓度迅速得到提高,可更加高效地对病灶发挥作用,局部抗感染及抗炎等效果更加显著[11-12]。
综上所述,予以颅脑损伤患者万古霉素鞘内注射治疗及综合护理干预有能够取得理想的颅内感染防控效果,对于改善患者脑脊液指标及炎性因子水平、减少并发症等也可发挥积极作用,可推动患者康复进程顺利进行,能够减轻病情对患者身心产生的不适感。此次研究存在一定的局限性,纳入样本量少无法使病例的特点得到充分显示,研究时间短难以充分验证万古霉素的用药效果以及用药安全性,故而可通过扩大样本量与延长研究时间的方式进一步验证万古霉素的应用价值以为临床应用提供借鉴。

