HPLC法对不同厂家博落回注射液质量评价的研究
朱丽飞,陈 盼,赵玉丛,王笃学,李利红
(河南牧业经济学院 动物医药学院,河南 郑州 450046)
博落回注射液是《兽药质量标准(2017年版)》中药卷中收录的制剂,为罂粟科植物博落回Macleayacordata(Willd.) R. Br.的果实经提取分离制成的生物碱硫酸盐灭菌水溶液[1]。博落回注射液含有多种异喹啉类生物碱[2],具有抗菌消炎等功能,主要用于治疗仔猪白痢、黄痢等疾病[3-5]。目前,《兽药质量标准(2017年版)》主要采用薄层色谱法对博落回注射液中博落回总碱进行定性鉴别,采用紫外-可见分光光度法检查吸光度,要求吸光度不得低于0.55[1],但是由于缺少含量测定项导致市售博落回注射液质量不一。血根碱和白屈菜红碱是博落回提取物中最主要的生物碱,也是博落回注射液中的主要有效成分。因此,本论文旨在以血根碱和白屈菜红碱为有效成分指标,建立HPLC同时测定博落回注射液中血根碱和白屈菜红碱的含量测定方法,以评价不同厂家博落回注射液的质量差异。
1 材料与方法
1.1 药品与试剂
甲醇购自天津市四友精细化学品有限公司;乙腈购自安徽天地高纯溶剂有限公司;磷酸、浓盐酸等购自天津市风船化学试剂有限公司;血根碱及白屈菜红碱对照品购自上海源叶生物科技有限公司;博落回注射液四批(规格5 mL),分别购自吉林省华牧动物保健品有限公司(厂家A,批号20201104)、四川积善之家药业有限公司(厂家B,批号20201101)、山东圣旺药业有限公司(厂家C,批号20201101)、合肥强力动物药品有限责任公司(厂家D,批号20200902)。
1.2 主要仪器
E2695-Waters高效液相色谱仪购自沃特世科技上海有限公司;KQ-200KDE 超声波清洗机购自昆山市超声仪器有限公司;ESJ-S分析天平购自沈阳龙腾电子有限公司;SHZ-95B循环水多用真空泵购自巩义市予华仪器有限公司。
1.3 色谱条件
色谱柱为Waters-symmetry C18(5 μm, 4.6×250 mm);检测器为2489 UV-Vis,检测波长为270 nm;流动相:乙腈(A)-0.1%磷酸(B),梯度洗脱(0~5 min,A∶B=25∶75;5~12 min,A∶B=60∶40;12~15 min,A∶B=25∶75;15~20 min,A∶B=25∶75);流速为1.0 mL/min,进样量为5 μL,柱温为30 ℃。
1.4 溶液的制备
1.4.1 对照品溶液的制备
分别精密称量血根碱对照品9.90 mg、白屈菜红碱对照品11.70 mg于10 mL容量瓶中,加入1%盐酸-甲醇溶液(50∶50)4 mL,超声溶解,自然冷却后加上述溶液定容至10 mL,摇匀,分别制成每1 mL含血根碱0.99 mg的溶液和每1 mL含白屈菜红碱1.17 mg 的溶液作为对照品储备液。分别精密量取血根碱储备液0.5 mL、白屈菜红碱储备液1.0 mL置于10 mL容量瓶中,用1%盐酸-甲醇(50∶50)定容,作为混合对照品溶液(1 mL含血根碱49.5 μg、白屈菜红碱117 μg)。
1.4.2 供试品溶液的制备
分别精密量取不同厂家的博落回注射液0.1 mL于10 mL容量瓶中,用1%盐酸-甲醇(50∶50)稀释至刻度,摇匀,即得供试品溶液。
2 结果
2.1 系统适用性实验
分别精密吸取血根碱对照品溶液、白屈菜红碱对照品溶液、混合对照品溶液各5 μL,按照1.3所述的色谱条件进样测定,色谱图见图1~2,系统适用性结果如表1所示。结果表明血根碱保留时间约4.8 min,白屈菜红碱保留时间约7.3 min,供试品溶液中血根碱和白屈菜红碱的保留时间与对照品基本一致,且与相邻成分色谱峰完全分离(分离度>1.5),理论塔板数以血根碱峰计算大于5 000。

表1 系统适用性实验结果

图1 混合对照品色谱图
2.2 线性关系考察
精密量取血根碱对照品储备液适量,通过逐步稀释配制成99.0、49.5、19.8、9.90、4.95、1.98 μg/mL的一系列血根碱对照品溶液。另精密量取白屈菜红碱对照品储备液适量,通过逐步稀释配制成117、58.5、23.4、11.7、5.85、2.34 μg/mL一系列白屈菜红碱对照品溶液。精密吸取各对照品溶液5 μL,在1.3色谱条件下进样测定,以峰面积A为纵坐标,分别以血根碱对照品浓度、白屈菜红碱对照品浓度c(μg/mL)为横坐标建立标准曲线。血根碱的回归方程为y=14258x-4574.6(R2=0.9978),在1.98~99.0 μg/mL范围内线性关系良好;白屈菜红碱的回归方程为y=25895x-951.09(R2=0.9978),在2.34~117 μg/mL范围内线性关系良好。
2.3 精密度实验
通过检测日内精密度和日间精密度评价仪器的精密度。取1.4.1混合对照品溶液,按照1.3色谱条件进行测定,日内精密度同一天连续进样6次,日间精密度连续3天每天连续进样3次,分别计算血根碱和白屈菜红碱峰面积的相对标准偏差(RSD),结果如表2~3所示。血根碱和白屈菜红碱的日内精密度RSD分别为0.18%、0.15%,血根碱和白屈菜红碱的日间精密度RSD分别为0.72%、0.32%,表明仪器精密度良好。

表2 日内精密度实验结果

表3 日间精密度实验结果
2.4 稳定性实验
取1.4.1混合对照品溶液,按1.3项色谱条件分别在1、2、4、12、24 h进样,记录不同时间血根碱和白屈菜红碱的峰面积,计算RSD,结果如表4所示,其中血根碱的RSD为0.44%(n=5),白屈菜红碱的RSD为0.20%(n=5),表明样品溶液在24 h内稳定性良好。

表4 稳定性实验结果
2.5 加样回收实验
精密量取厂家A博落回注射液9份,每份0.1 mL,置于10 mL容量瓶中,分别按高(约150%)、中(约100%)、低(约50%)3个梯度加入血根碱对照品储备液(0.99 mg/mL)和白屈菜红碱对照品溶液(58.5 μg/mL)适量,每个梯度3份,用1%盐酸-甲醇(50∶50)稀释至刻度,摇匀,制备加样回收样品溶液,在使用1.3色谱条件进样测定,计算血根碱和白屈菜红碱的平均回收率和RSD值,结果如表5所示。血根碱的平均回收率(高、中、低)分别为103.01%、99.07%、100.82%,RSD值(高、中、低)分别为0.63%、1.80、1.15%;白屈菜红碱的平均回收率(高、低、中)分别为102.45%、99.09%、99.57%,RSD值(高、中、低)分别为0.59%、1.61%、2.21%,结果表明该方法准确度良好。
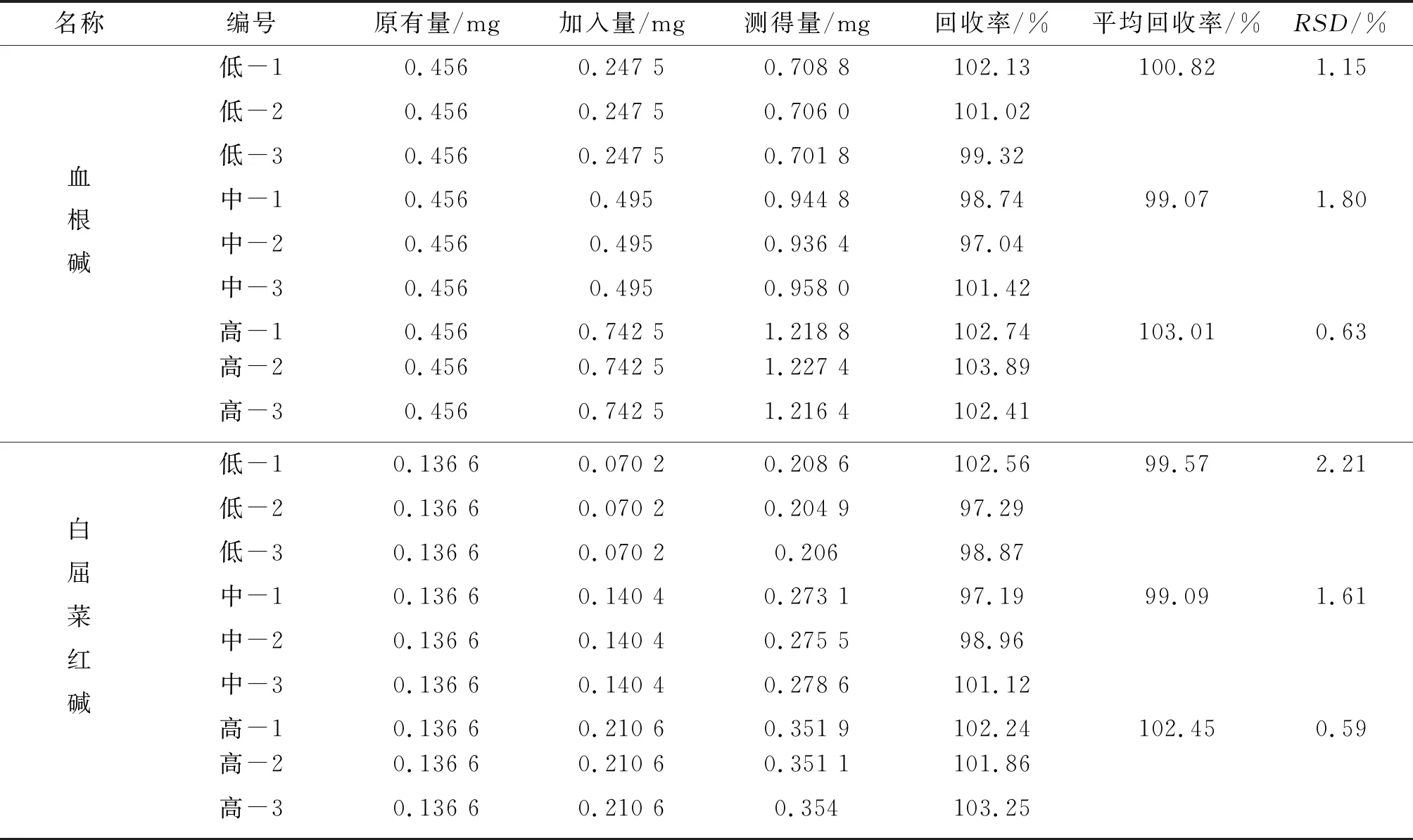
表5 加样回收实验结果
2.6 样品含量测定
将1.4.2配制的供试品溶液1.3项色谱条件进行测定,每个样品平行测定2次,记录峰面积,计算供试品溶液中血根碱和白屈菜红碱的浓度,结果如表6和图2~5所示。结果表明,厂家A博落回注射液中血根碱和白屈菜红碱的浓度分别为4.560、1.266 mg/mL,每支(5 mL)博落回注射液中血根碱和白屈菜红碱的含量分别为22.80、6.831 mg;厂家B博落回注射液中血根碱和白屈菜红碱的浓度分别为3.960、1.290 mg/mL,每支(5 mL)博落回注射液中血根碱和白屈菜红碱的含量分别为19.80、6.449 mg;而厂家C、D均未检出血根碱和白屈菜红碱。
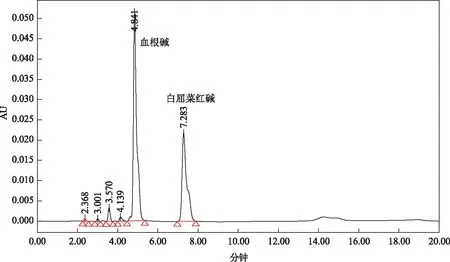
图2 供试品溶液色谱图(厂家A)
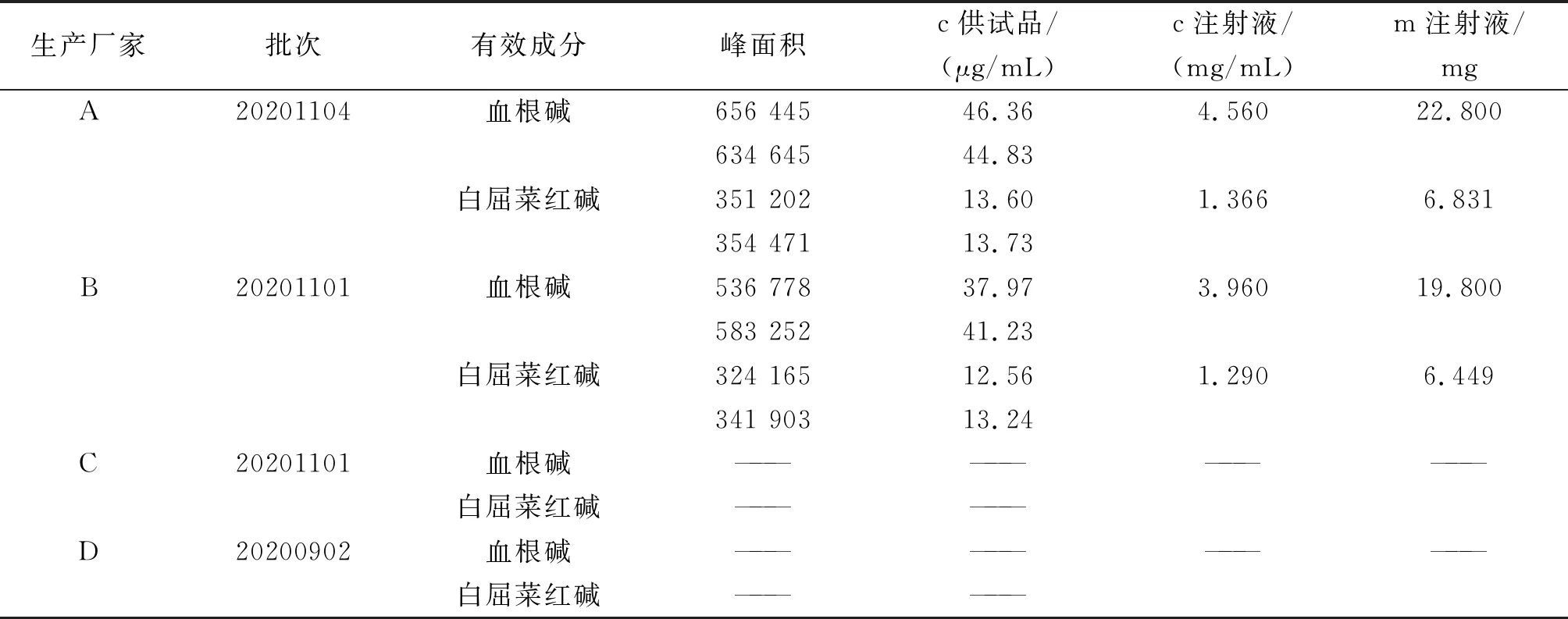
表6 博落回注射液中血根碱和白屈菜红碱含量测定结果
3 讨论
3.1 色谱条件的确立
3.1.1 流动相和洗脱方式的选择
按照农村农业部第246号公告中博落回散质量标准的色谱条件[6],以乙腈为流动相A、以0.2%三乙胺溶液(磷酸调节pH值至2.5)为流动相B进行梯度洗脱,结果血根碱和白屈菜红碱色谱峰均出现分叉。因此结合参考文献[7-9],以乙腈为流动相A、0.1%磷酸溶液为流动相B,同时调节进样体积至5 μL,比较等度洗脱(A∶B=25∶75)和梯度洗脱(见1.3)的差异,发现等度洗脱时血根碱和白屈菜红碱峰峰形较宽,且白屈菜红碱出现分叉,而梯度洗脱时分叉现象消失,拖尾现象有所改善,但白屈菜红碱拖尾现象仍存在,且加入扫尾剂三乙胺拖尾现象并未改善。因此最终选择流动相和洗脱方式为乙腈(A)-0.1%磷酸(B),梯度洗脱(0~5 min,A∶B=25∶75;5~12 min,A∶B=60∶40;12~15 min,A∶B=25∶75;15~20 min,A∶B=25∶75)。
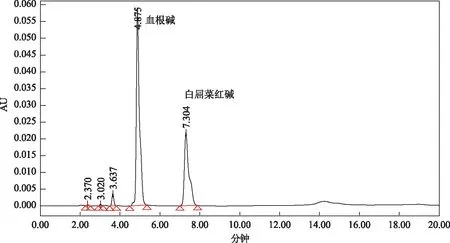
图3 供试品溶液色谱图(厂家B)

图4 供试品溶液色谱图(厂家C)
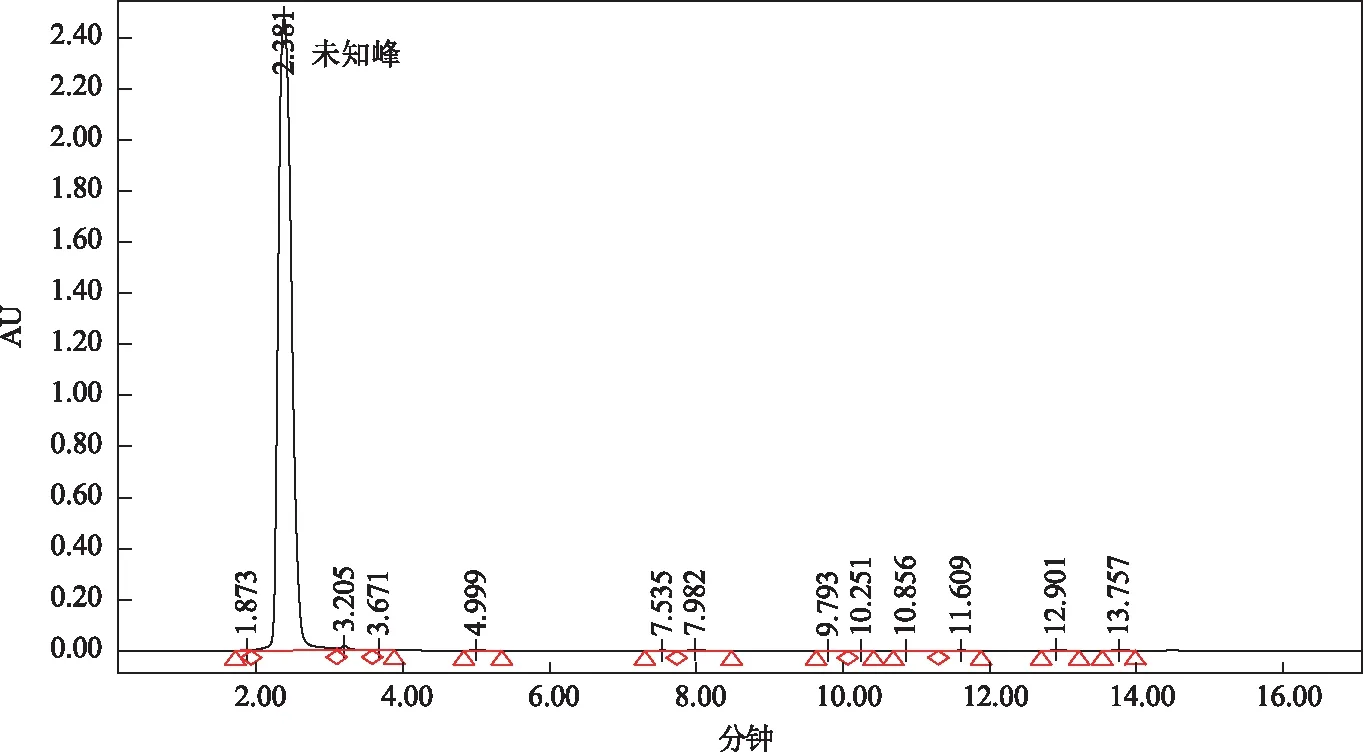
图5 供试品溶液色谱图(厂家D)
3.1.2 波长的选择
根据参考文献[7, 9, 10],HPLC法测定血根碱和白屈菜红碱的常用波长有270 nm和284 nm,经比较发现,血根碱和白屈菜红碱在270 nm的吸收值均比284 nm吸收值大,因此选择270 nm为检测波长。
3.2 博落回注射液质量差异分析
厂家A、B的博落回注射液中均能有效检出血根碱和白屈菜红碱,每支(5 mL)博落回注射液中两种有效成分总含量分别为29.63、26.25 mg,大于25 mg,满足说明书规格要求(5 mL∶25 mg);而厂家C、D的博落回注射液中均不含血根碱和白屈菜红碱两种有效成分,且均检测出未知色谱峰(厂家C∶tR=5.558 min;厂家D∶tR=2.381 min);表明厂家A、B的博落回注射液成分含量接近,而厂家C、D与厂家A、B的成分差异较大,说明目前市售博落回注射液质量差异较大。
目前《兽药质量标准》博落回注射液缺少含量测定项,无法统一进行评价,导致目前市售博落回注射液质量不一,存在以次充好的现象。本论文结合参考文献,通过反复优化色谱条件,建立了简单、稳定、准确的测定博落回注射液中血根碱和白屈菜红碱含量的HPLC法,并且评价了四个厂家博落回注射液的质量,为博落回注射液质量标准的建立提供参考。

