高效液相色谱法测定巴氏杀菌乳中糠氨酸含量的不确定度评定
何 瑛,曹学思,纪坤发,杨爱君,陈 欣,陈春裕
广东燕塘乳业股份有限公司品控中心,广东广州510507
0 引言
糠氨酸(ε-N-2-呋喃甲基-L-赖氨酸)是美拉德反应初期产生的Amadori化合物酸水解产生的稳定产物[1],其在牛奶中的含量很大程度取决于牛奶的热处理强度和储存条件,可以很好地体现牛奶美拉德反应的程度[2]。早在1992年,欧盟各国政府便将糠氨酸质量分数作为评价液态乳品质的一个重要的指标。我国原农业部也在2005年发布行业标准将巴氏奶、超高温灭菌乳中的糠氨酸含量作为鉴定是否为复原乳的判定因素之一[3]。
测量不确定度是根据所用到的信息,表征赋予被测量的量值分散性的非负参数[4]。它是测量结果质量水平的表现,表明测量结果的可信程度[5]。实验室在使用《NY/T939—2016 巴氏杀菌乳和UHT灭菌乳中复原乳的鉴定》[3]检测牛奶中糠氨酸含量的过程中,由于实验仪器设备、方法和人员等多种因素的影响,在检测过程中难免会出现误差,进而影响检测结果的准确性。本文依据《CNAS-GL006:2019化学分析中不确定度的评估指南》[6]和《JJF 1059.1—2012测量不确定度评定与表示》[4],对高效液相色谱法测定牛奶中糠氨酸含量的不确定度进行评定,了解该方法在检测牛奶中糠氨酸过程中影响结果可靠性的主要因素,以便在检测过程中予以重视,为牛奶中糠氨酸含量的准确测定提供科学依据。
1 材料与方法
1.1 主要仪器设备及试剂
高效液相色谱仪(Agilent 1200),美国Agilent公司;凯氏定氮仪(FOSS KJELTEC 8100),丹麦FOSS公司;十万分之一天平(Mettler Tledo XSR205DU),瑞士Mettler Tledo公司;超纯水系统(Milli-Q Reference A+),默克化工;精密干燥箱(FD115型),德国爱安姆公司;可调移液器,德国Brand公司。
甲醇、三氟乙酸(色谱纯),德国Merck公司;浓盐酸(优级纯),广州化学试剂厂;糠氨酸(肽纯度系数69%),德国皇家生物科技公司;浓硫酸、氢氧化钠、硼酸(分析纯),广州化学试剂厂;甲基红、溴甲酚绿(分析纯),上海安谱;凯氏定氮催化剂,丹麦福斯公司。本试验中用水符合为GB/T6682—2008中一级水的规定。
1.2 试验方法
1.2.1 样品前处理
吸取2.00 mL样品,置于密闭耐热试管中,加入6.00 mL 10.6 mol/L盐酸溶液(水∶盐酸=88∶12,V∶V),混匀,密闭试管,将其置于干燥箱中,在110 ℃下加热水解20~23 h。加热约1 h后,轻轻摇动试管。加热结束后,将试管从干燥箱中取出,冷却后混匀,用滤纸干过滤,保留滤液待测。试样水解液中蛋白质含量的测定:吸取2.00 mL样品水解液,按《GB 5009.5—2016 食品安全国家标准 食品中蛋白质的测定》[7]的规定测定样品水解液中的蛋白质含量。样品水解液中糠氨酸含量的测定:吸取0.50 mL样品水解液,加入2.50 mL超纯水,混匀,过0.22 μmPVDF针式滤膜,滤液进行HPLC检测。
1.2.2 色谱条件
色谱柱:Waters HSS T3 150 mm×4.6 mm,5.0 μm粒径;进样量:10 μL;柱温:28 ℃;流速1.0 mL/min;检测波长:280 nm;流动相A为含0.1%三氟乙酸的5%甲醇水溶液、流动相B为含0.085%三氟乙酸的95%甲醇水溶液。检测前利用流动相A和流动相B的混合液(50∶50)以1 mL/min的流速平衡色谱系统。然后,用初始流动相平衡系统直至基线稳定。注入10 μL 3 mol/L盐酸溶液,以检测溶剂的纯度。洗脱条件:按NY/T939—2016要求进行梯度洗脱。
1.2.3 标准工作曲线的制作
(1)糠氨酸标准储备液的配制(250 mg/L):将糠氨酸标准品按标准品证书提供的肽纯度系数(0.69)换算后,用3 mol/L盐酸溶液配制成标准储备液。
(2)糠氨酸标准工作液的配制:将糠氨酸标准储备液放至室温,准确吸取糠氨酸标准储备液6 μL、10 μL、20 μL、100 μL、400 μL,用3 mol/L的盐酸溶液定容至25 mL,配制成浓度为0.06 mg/L、0.10 mg/L、0.20 mg/L、1.00 mg/L、4.00 mg/L的标准工作液,4 ℃下可储存21 天[8]。
1.3 检测结果的计算
1.3.1 糠氨酸含量
根据NY/T 939—2016,该方法的计算数学模型为:

式中:F表示试样中糠氨酸含量,mg/100g蛋白质;At表示测试样品中糠氨酸峰面积的数值;Astd表示糠氨酸标准溶液中糠氨酸峰面积的数值;Cstd表示糠氨酸标准溶液的浓度,mg/L;D表示测定时稀释倍数,D=6;m表示样品水解液中蛋白质浓度,g/L。
1.3.2 样品水解液中蛋白质浓度
根据GB 5009.5—2016,该方法中样品水解液蛋白质浓度计算数学模型为:
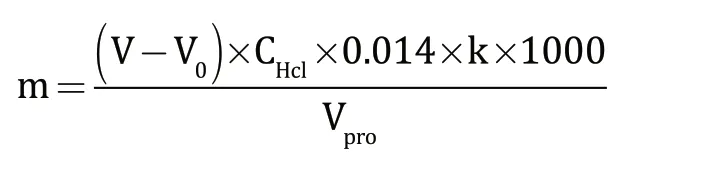
式中:m表示样品水解液中蛋白质浓度,g/L;V表示样品消耗酸体积,mL;V0表示空白消耗酸体积,mL;CHCl表示盐酸标准滴定溶液的浓度,mol/L;Vpro表示样液的体积,mL;0.0140为1.0 mL盐酸标准滴定溶液相当的氮的质量,g;k表示氮换算成粗蛋白的系数,k=6.38。
1.3.3 盐酸标准滴定溶液的浓度
根据《GB/T 601—2016化学试剂 标准滴定溶液的制备》[9],该方法中盐酸标准滴定液的浓度计算数学模型为:

式中:CHCl表示盐酸标准滴定溶液的浓度,mol/L;mNaOH表示无水碳酸钠质量,g;PNaOH表示无水碳酸钠纯度,以质量分数表示;V1表示无水碳酸钠消耗盐酸溶液体积,mL;V2表示空白试验消耗盐酸溶液体积,mL;a表示体积补正值,mL;M表示1/2NaCO3的摩尔质量,g/mol。
2 结果与分析
2.1 测量不确定度来源分析
根据检测过程和数学模型分析,本方法测定牛奶中的糠氨酸含量的测量不确定度来源主要有以下6 个方面:(1)样品重复性测定引入的不确定度(A类);
(2)糠氨酸标准物质引入的不确定度(B类);(3)高效液相色谱仪引入的不确定度(B类);(4)样品水解液中蛋白质含量测定引入的不确定度(A类+B类);
(5)加标回收实验引入的不确定度(A类);(6)结果计算引入的不确定度(B类)。
为清晰地表示检测过程中可能影响检测结果的诸多因素的关联性,将检测过程的测量不确定度用鱼骨图表示,详见图1。
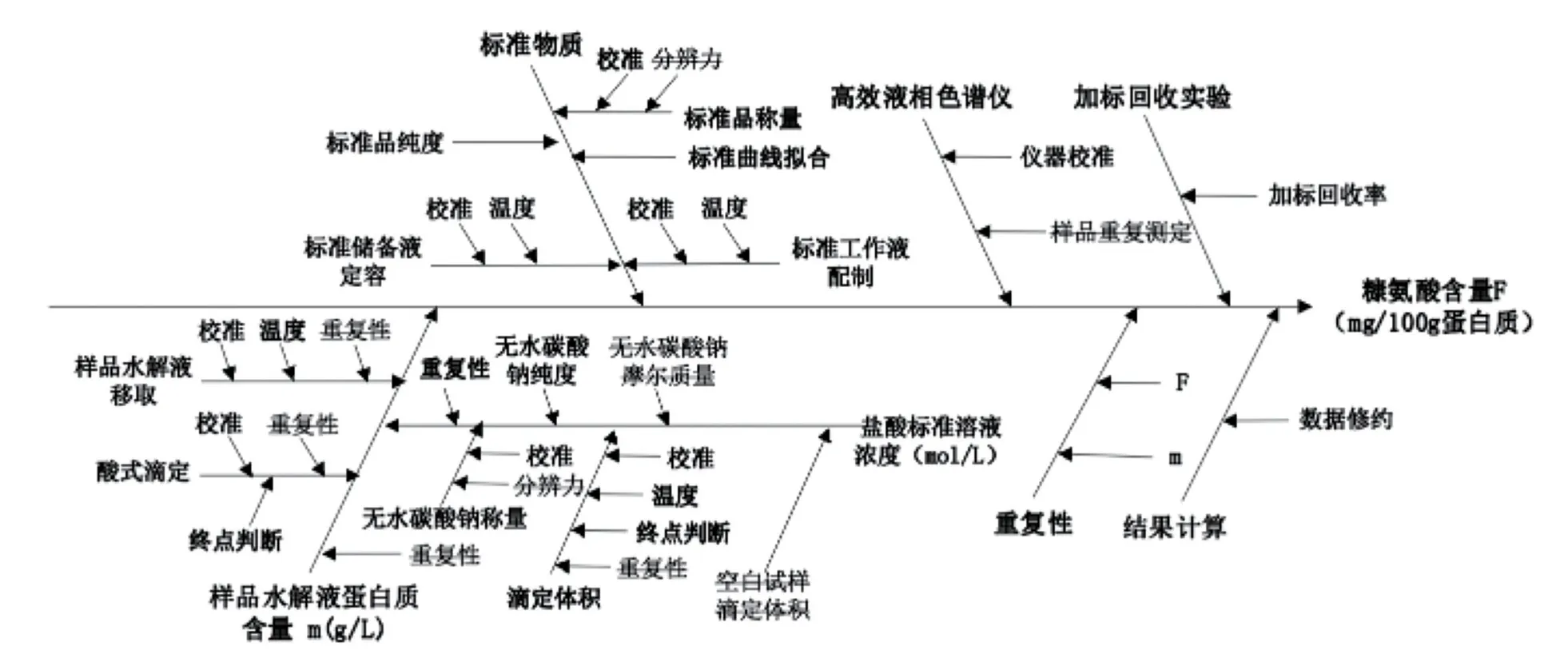
图1 检测过程的测量不确定度来源
2.2 不确定度分量的量化评定
2.2.1 样品重复性测定引入的不确定度
取某品牌巴氏杀菌乳样品,按1.2试验方法进行检测,每个样品平行测定6 次,结果见表1。

表1 样品重复性测定结果
即样品重复性测定引入的相对标准不确定度分别为:
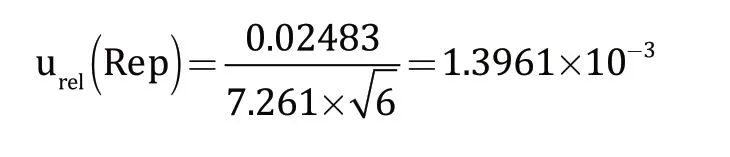
2.2.2 糠氨酸标准物质引入的不确定度
糠氨酸标准曲线的建立分为三步:①标准储备液的配制,称取糠氨酸标准品0.00 908 g于烧杯中,用3 mol/L盐酸溶解,定容至25 mL容量瓶中;②标准工作液的配制,吸取标准储备液6 μL、10 μL、20 μL、100 μL、400 μL,用3 mol/L的盐酸溶液定容至25 mL;③上机测定。此过程的不确定度主要由以下5 个方面构成。
(1)标准品纯度引入的不确定度
试验中使用的糠氨酸标准品,标准物质证书(批次号2051016)给出其纯度为99.7%,考虑矩形分布,则糠氨酸标准品纯度引入的标准不确定度分量为,相对标准不确定度为[10]:
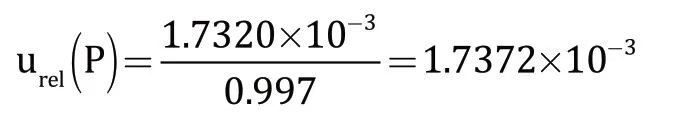
(2)标准品称量引入的不确定度
实验中使用十万分之一天平称取糠氨酸标准品,此过程中的不确定度主要由天平校准的不确定度和天平的分辨力构成,由于实验使用十万分之一天平,天平的分辨力带来的影响很小,可忽略不计。
天平的检定证书(证书编号LE202118637)给出其测量结果扩展不确定度为0.08 mg(K=2),则天平校准引入的标准不确定度分量为0.08 mg/2=0.04 mg[11],相对标准不确定度为:
(3)标准储备液定容引入的不确定度
实验中使用25 mL(V1)容量瓶对标准储备液进行定容,此过程中的不确定度主要容量瓶的相对扩展不确定度和温度构成。
①25 mL容量瓶校准证书(证书编号BEHCL-2020070020-3)给出其在20 ℃时的扩展不确定度为0.02 mL(K=2),则其标准不确定度分量为,0.02mL/2=0.01mL,相对标准不确定度:

②温度对25 mL容量瓶体积的影响引入的不确定度,由于实验室的温度在±4 ℃之间变动,该影响引起的不确定度可通过估算该温度范围和体积膨胀系数来进行计算,J J G 1 9 6—2 0 1 6规定[12],水的体积膨胀系数为2.1×10-4℃, 体积产生的变化为25 mL×4 ℃×2.1×10-4℃=0.021 mL,考虑矩形分布将温度变化分量转化为标准不确定度,相对标准不确定度为:

则标准储备液定容引入的相对标准不确定度为:
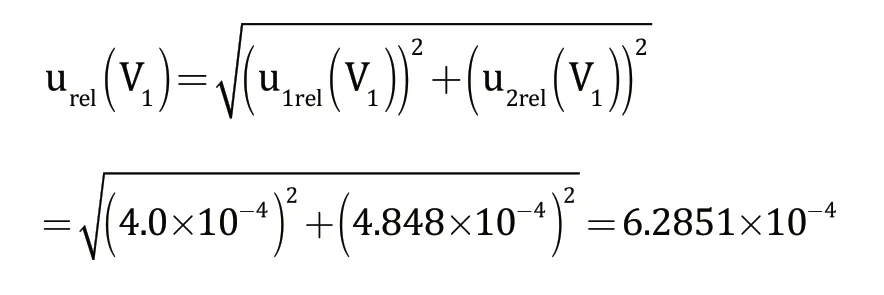
(4)标准工作液的配制引入的不确定度
实验中使用10 μL可调移液器吸取标准储备液6 μL(V2)、10 μL(V3),使用100 μL可调移液器吸取标准储备液20 μL(V4)、100 μL(V5),使用1mL可调移液器吸取标准储备液400 μL(V6),最后用25 mL(V7)容量瓶对标准工作液进行定容,此过程中的不确定度主要由移液器的相对扩展不确定度和温度、容量瓶的相对扩展不确定度和温度构成。
移液器的相对扩展不确定度引入的标准不确定度分量由移液器校准证书给出的扩展不确定度除以2(K=2)再除以移液量得到,温度对移液器体积的影响、容量瓶的相对扩展不确定度和温度引入的标准不确定度分量的计算方式如2.2.2(3)所示,具体计算结果见表2。
由表2可得,标准工作液的配制各步骤引入的相对标准不确定度分别为:

表2 标准工作液配制过程的不确定度评定

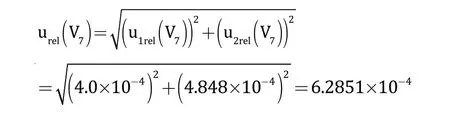
即标准工作液的配制引入的总相对标准不确定度为:
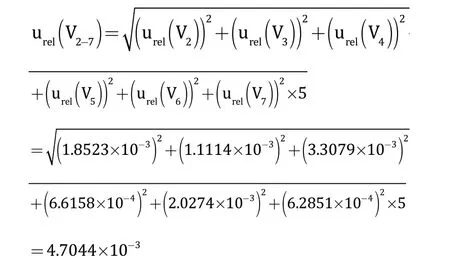
(5)标准曲线拟合引入的不确定度
使用高效液相色谱仪对标准工作液每个浓度上机测定6 次,得到糠氨酸色谱峰面积,使用最小二乘法进行标准曲线拟合,得到标准曲线的线性回归方程,具体结果见表3。根据得到的标准曲线,对4 个不同热处理强度的牛奶样品,按1.2试验方法进行检测,每个样品平行测定6 次,结果见表1。标准曲线拟合的标准不确定度可按下列公式计算:
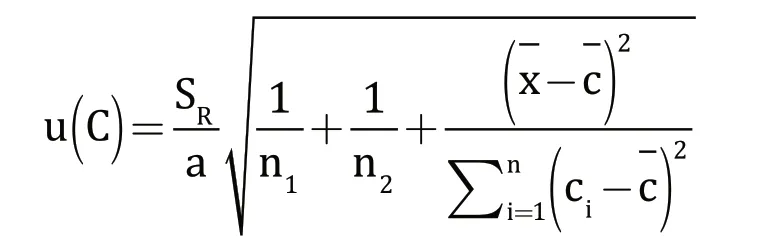
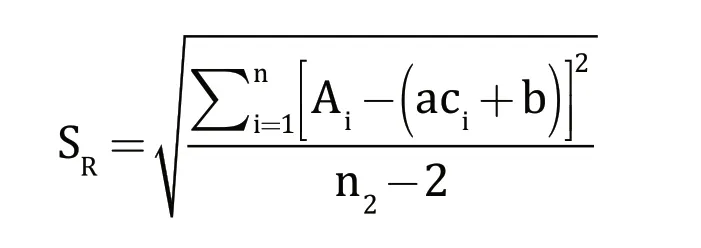
式中:a表示标准曲线的斜率,a=37.9963604;b表示标准曲线的截距,b=0.4413247;n2表示样品的测量次数,n1=6;n2表示标准工作液总共测量次数,n2=30;表示样品中糠氨酸的平均浓度值,=0.1557 mg/L;表示标准工作液中糠氨酸的平均浓度,mg/L;ci表示标准工作液中糠氨酸各点的浓度值,mg/L;Ai表示标准溶液各点的峰面积测定值;SR表示标准溶液峰面积残差的标准差[13]。
根据表1和表3的数据计算得到:
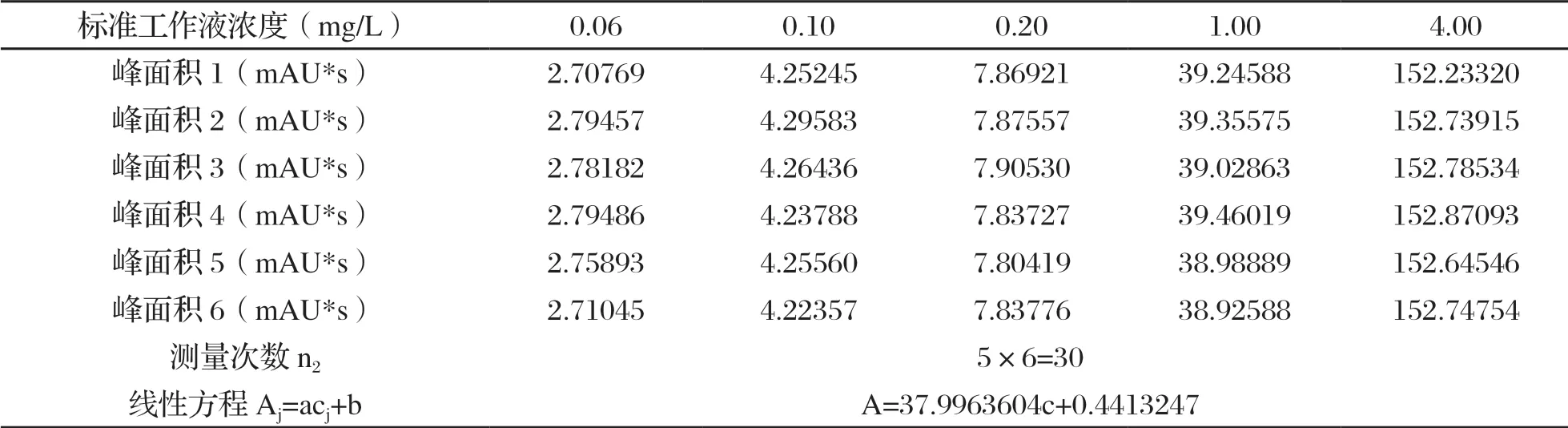
表3 标准曲线线性参数表
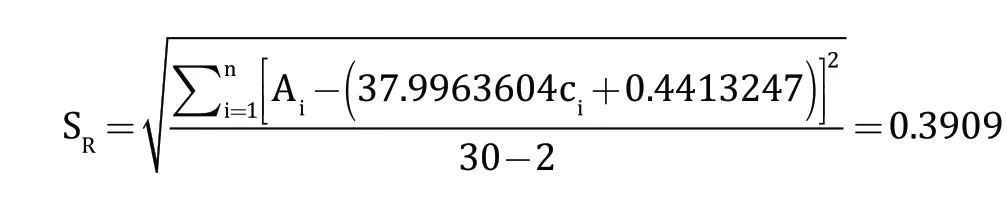
即标准曲线拟合的相对标准不确定度为:

即糠氨酸标准物质引入的总相对标准不确定度为:
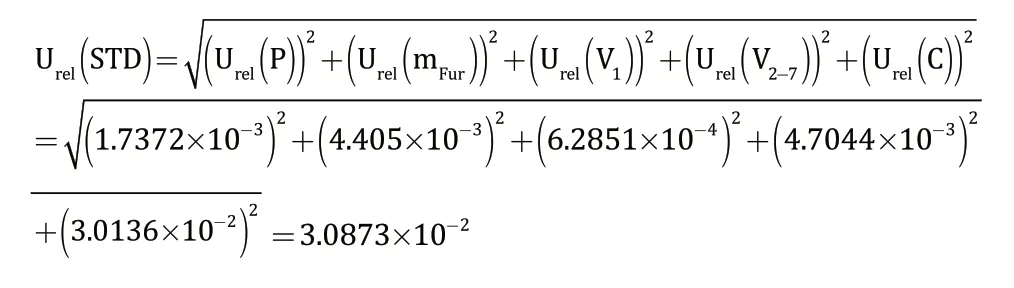
2.2.3 高效液相色谱仪测定引入的不确定度
高效液相色谱仪测定色谱峰面积引入的不确定度主要由仪器的校准和样品的重复测量引入的不确定度2部分组成。其中样品的重复性测量引入的不确定度包含在平行样品的重复性测定带来的误差中,不再单独评定[14,15]。
仪器的检定证书(证书编号NG202101841)显示二级管阵列检测器的定量重复性误差为0.4%,考虑矩形分布[16],液相色谱仪峰面积测量引入的相对标准不确定度为:

2.2.4 样品水解液中蛋白质含量测定引入的不确定度
样品水解液中蛋白质含量测定过程为:吸取2.00 mL样品水解液,按GB 5009.5—2016的规定测定,根据0.1 mol/L盐酸标准滴定溶液的消耗量来计算样品水解液中的蛋白质含量。此过程中的不确定度来源主要由样品水解液的移取、0.1 mol/L盐酸标准滴定溶液的浓度、酸式滴定和重复性测定构成。其中样品水解液重复性测量引入的不确定度包含在平行样品的重复性测定带来的误差中,不再单独评定。
(1)样品水解液的移取
样品水解液的移取过程为:使用5 mL可调移液器吸取2.00 mL(V8)样品水解液。此过程的不确定度主要由移液器的相对扩展不确定度和温度构成,移取体积的变动性包括在重复性测定带来的误差中,不再单独评定。
①5 mL可调移液器的校准证书(证书编号BSHCL-2020080029-4)指出该移液器的扩展不确定度为4.3 μL(K=2),即5mL可调移液器的不确定度分量为4.3μL/2=2.15μL,相对标准不确定度为:

②温度对5 mL可调移液器体积的影响引入的标准不确定度分量,按照2.2.2(3)所示进行计算,为相对标准不确定度为:
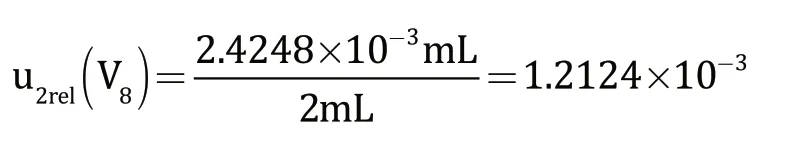
即样品水解液移取引入的相对标准不确定度为:

(2)盐酸标准滴定溶液的浓度测定
盐酸标准滴定溶液的浓度测定过程为:使用万分之一天平称取约0.2 g无水碳酸钠,定容到50 mL,用酸碱滴定管装入配制的盐酸溶液滴定至终点。此过程的不确定度来源主要由无水碳酸钠的摩尔质量、纯度和质量、滴定体积和重复性测定构成。其中无水碳酸钠的摩尔质量引入不不确定度很小,可忽略不计。
a 重复性测定引入的不确定度
对同一个盐酸标准滴定溶液按GB/T 601—2016的方法进行双人八平行测定,结果见表4。
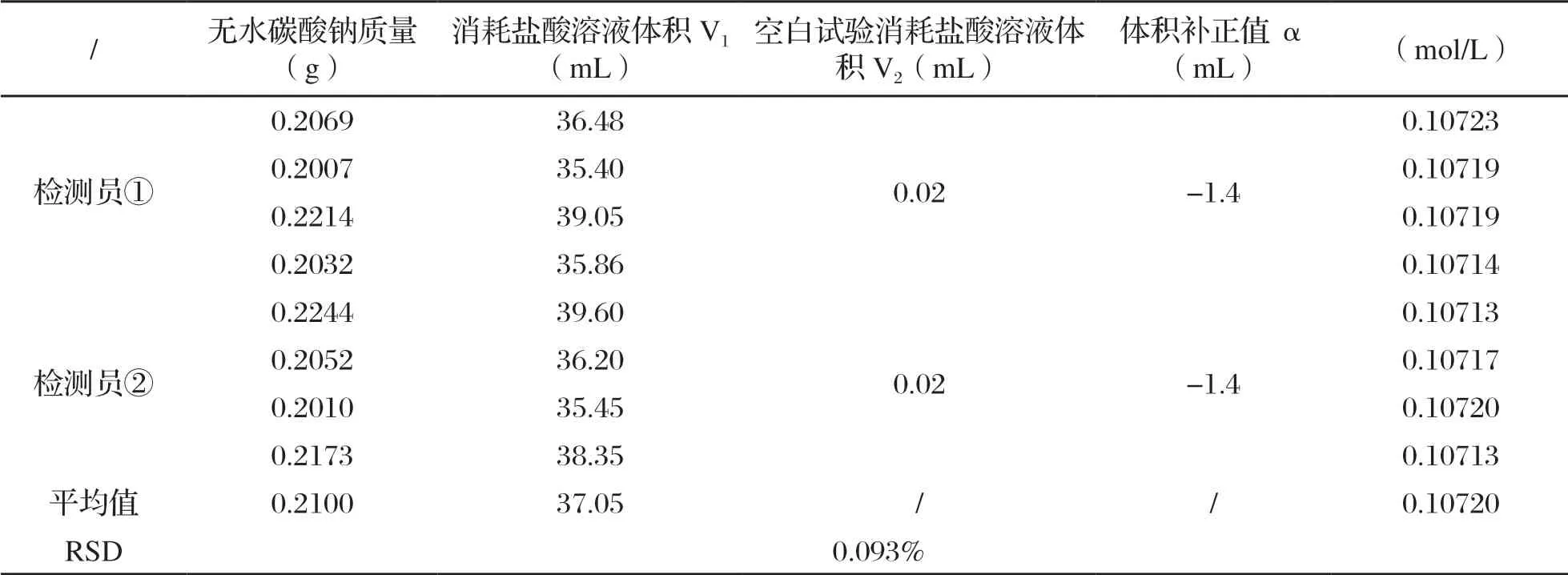
表4 盐酸标准滴定溶液的标定结果
即盐酸标准滴定溶液重复性测定引入的相对标准不确定度为:

b 无水碳酸钠纯度引入的不确定度
无水碳酸钠的标准物质证书(批次号201711)给出其纯度为99.98%,扩展不确定度为0.05%(K=2),则无水碳酸钠准品纯度引入的标准不确定度分量为相对标准不确定度为:
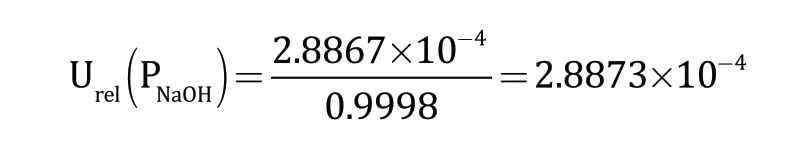
c 无水碳酸钠称量引入的不确定度
实验中使用万分之一天平称取无水碳酸钠标准品,需进行2 次测量,一次为空瓶,一次为总重,此过程中的不确定度主要由和天平的分辨力构成,由于实验使用万分之一天平,天平的分辨力带来的影响很小,可忽略不计。
天平的检定证书(证书编号LE202134727)给出其测量结果扩展不确定度为0.5 mg(K=2),则天平校准引入的标准不确定度分量为0.5mg/2=0.25mg,相对标准不确定度为:

d 滴定体积引入的不确定度
盐酸标准滴定溶液滴定过程使用酸碱滴定管分别对样品和空白进行滴定,空白试验消耗体积数值很小,可忽略不计。此过程中的不确定度主要由具塞滴定管校准和温度、滴定终点判断和重复性测定构成。滴定体积的重复性误差包括在重复性测定带来的误差中,不再单独评定。
①5 0 m L具塞滴定管校准证书(证书编号LE202118637)给出其扩展不确定度为0.030 mL(K=2),则滴定管校准引入的标准不确定度分量为0.030 mL/2=0.015 mL,相对标准不确定度为:
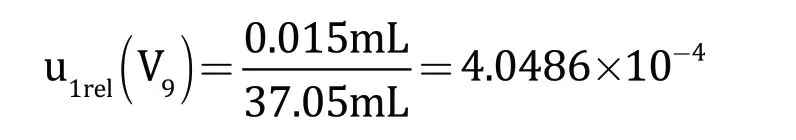
②不考虑指示剂消耗滴定液的因素及滴定终点与等当点之间可能存在的系统误差。通过反复试验,终点判断的最大体积误差为1 滴即±0.03 mL[17],考虑两点分布(K=1)[18],滴定终点判断引入的不确定度分量为0.03 mL/1=0.03 mL,相对标准不确定度为:
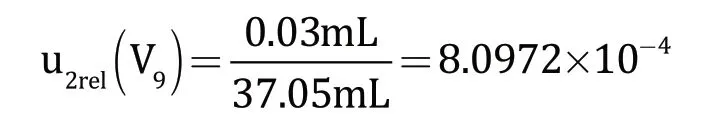
③温度对滴定管体积的影响引入的不确定度,按照2.2.2(3)计算,为相对标准不确定度为:

即滴定体积引入的相对标准不确定度为:
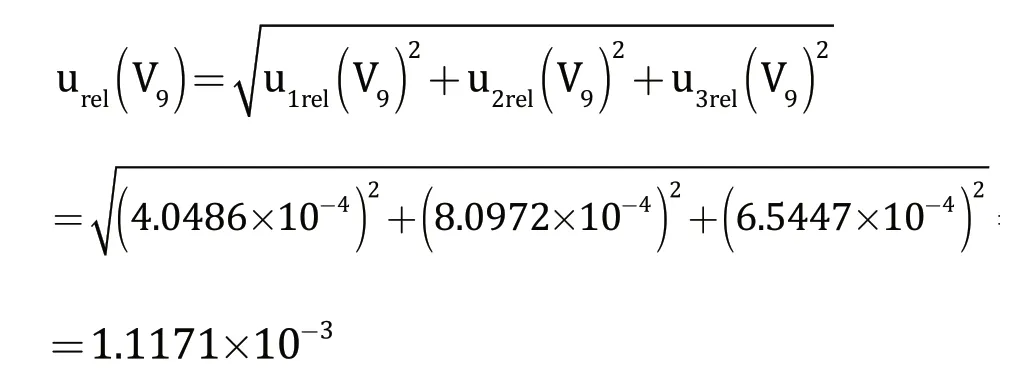
盐酸标准滴定溶液的浓度测定过程引入的总相对标准不确定度为:
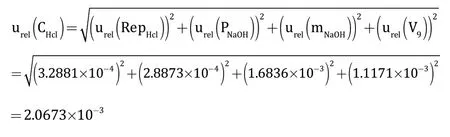
(3)酸式滴定
样品水解液酸式滴定过程:使用数字滴定器分别对样品和空白进行滴定。此过程中的不确定度主要由数字滴定器校准、滴定终点判断和重复性测定构成。滴定体积的重复性误差包括在重复性测定带来的误差中,不再单独评定。
①50mL数字滴定器的校准证书(证书编号LE202106970)给出其测量结果相对扩展不确定度为0.2%(K=2),则数字滴定器校准引入的标准不确定度分量为0.002mL/2=0.001mL,相对标准不确定度为:
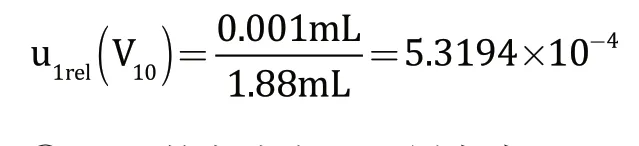
②50mL数字滴定器的刻度为0.01mL,通过反复试验,终点判断的最大体积误差为1滴即±0.01mL,考虑两点分布(K=1),滴定终点判断引入的标准不确定度分量为0.01mL/1=0.01mL,相对标准不确定度为:

即酸式滴定过程引入的相对标准不确定度为:
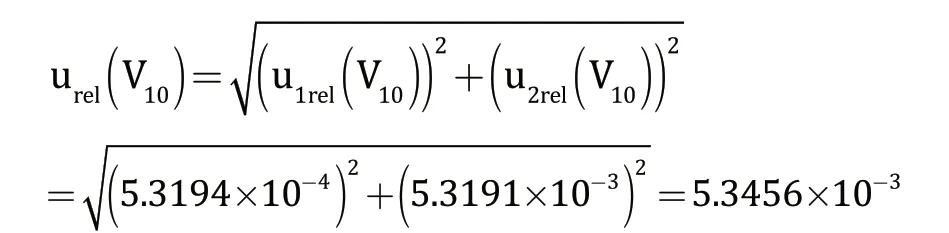
样品水解液中蛋白质含量测定过程总相对标准不确定度为:
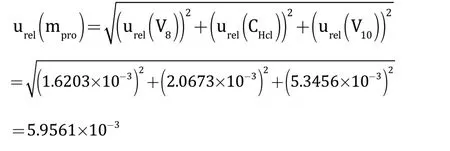
2.2.5 加标回收试验引入的不确定度
分别吸取一定量的糠氨酸标准储备液,配制成加标浓度5 mg/L、10 mg/L、15 mg/L、30 mg/L的加标样品,充分混匀后按1.2的试验方法进行检测,每个样品平行测定6 次,取平均值计算回收率,实验结果见表5。

表5 糠氨酸加标回收试验结果
用t检验来确定平均回收率是否与1.0有显著性差异。检验统计量t为:

该值与95%置信度,n-1=23自由度下的双侧临界值tcrit比较,t>tcrit=2.069,说明平均回收率与1有显著性差异,平均回收率应被明确地包含在结果的计算中。
即回收率引入的相对标准不确定度为:

2.2.6 结果计算引入的不确定度
NY/T939—2016规定,计算结果保留至小数点后一位,采用四舍五入法进行修约时,糠数值修约的半宽为0.05 mg/100g蛋白质,考虑矩形分布[19],结果修约引入的标准不确定度分量为相对标准不确定度为:

综上所述,高效液相色谱法测定牛奶中糠氨酸含量的试验过程中不确定度来源详见表6。
2.3 合成标准不确定度评定
根据表6列出的各不确定度来源及其相对标准不确定度,合成标准不确定度为:

表6 相对不确定度分量一览表


2.4 扩展不确定度计算和结果表示
取置信水平为95%,包含因子k=2,则扩展不确定度:

因此,高效液相色谱法测定巴氏杀菌乳中糠氨酸的检测结果为:
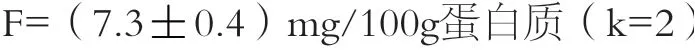
3 结论
本文使用高效液相色谱法测定巴氏杀菌乳中糠氨酸的含量,并对方法的不确定度进行评定。根据评定结果可知,方法中测量不确定度的主要来源包括糠氨酸标准物质(标准品称量、标准工作液的配制、标准曲线的拟合等)和样品水解液中蛋白质含量测定(酸式滴定终点判定)。因此,在实际检测过程中,为确保检测结果的准确性,可通过使用精度较高的称量设备、玻璃量具和滴定设备,做好仪器设备的定期校准和维护保养,减少标准溶液稀释步骤等来降低测量过程的不确定度;在蛋白质滴定时可以选择 pH计进行终点颜色判定[14],避免肉眼判定的误差;此外,在确保样品定量准确度的情况下,可适量减少标准工作液的浓度梯度并增加标准工作液平行测定次数以降低不确定度,一般选择3~5 个浓度梯度的标准溶液进行标准曲线拟合[10]。

