LC引起的医源性右肝管、副肝管损伤的诊治
石毅,白剑峰,高骥,赵翰林,张峰,李相成,吴晓峰,王学浩
(南京医科大学第一附属医院 肝胆中心,江苏 南京 210000)
医源性胆管损伤(iatrogenic bile duct injury,IBDI)发生率为0.3%~1.5%[1-3],由于腹腔镜胆囊切除术(LC)庞大的基数,右肝管/副肝管损伤远比报道的多,又因为缺乏经验和共识,其处理方法高度多样化[4],有时相较单纯胆总管损伤更为困难,文献中含长期随访的研究极少。据报道19%~50%的病例合并胆道变异[1,5-6],且与副肝管变异有关[7]。约91%的副肝管出现在胆囊三角内[8],其中86.7%~100.0%的副肝管引流右后胆管[9]。LC中发生右肝管、副肝管损伤并非少见,部分保守治疗成功的病例并未及时在文献中分享[6,8],这部分患者也因症状、损伤程度、治疗高度个体化而难以精确统计。此类损伤还因纳入标准、诊治规范、随访质量的差异难以确定导致临床决策的多样性。术中胆道造影(intraoperative cholangiography,IOC)对于明确损伤类型有重要作用。很多术者不会借助IOC及时发现损伤或判断损伤类型,不能正确处理,术后也缺乏科学的随访标准[10],导致不良转归,值得临床上重视。本研究对本中心采用新的胆道损伤预后标准,就近7年的20例右肝管/副肝管损伤患者纳入研究,期望进一步提高这种特殊类型胆管损伤的诊疗水平。
1 资料和方法
1.1 一般资料
回顾性分析南京医科大学第一附属医院肝胆中心自2014 年5 月至2021 年11 月收治的LC合并右肝管及副肝管损伤患者20 例,其中男8 例,女12 例,年龄22~79 岁,平均(58.7±15.8)岁。纳入标准:全部病例均依据IOC、MRCP、PTC、胆道镜及手术探查结果,经术者、放射科会诊证实诊断。明确损伤类型后均由同一手术团队处理,其中2 例由外院转入(见表1)我院行确定性手术。排除标准:合并肝总管、胆总管损伤及肝右动脉损伤的病例均排除在本组研究之外。随访指标及依据采用临床推荐的胆管损伤预后标准[11]。术前行MRCP 14 例,术中行IOC 9 例。结合手术辨识和影像学检查(见表1)明确损伤类型。其中右肝管(right hepatic duct,RHD)损伤16 例,其中右肝管裂伤12 例(胆囊结石合并胆总管结石7例、胆囊结石5例),右肝管离断4例(均为胆囊结石);副肝管(accessory hepatic duct,AHD)损伤4例(均为胆囊结石)。截止2021年11月,随访6~133个月,平均42.9个月。患者一般资料详见表1。
1.2 手术方法
12例右肝管裂伤中,术中I期修补置管支撑引流8例(表1)。胆总管结石7例中,5例(病例1至5)术中误损伤右肝管,在胆总管T管置入后另在右肝管破损处置入12#~14#T管(双T管置入),术后3个月行T管造影并拔除胆总管内T管,术后半年至1年拔除右肝管内T管同时经窦道行超细胆道镜检查;1例中转开腹手术,T管右短臂内置细管支撑于损伤右肝管处(夹心T管),术后半年拔除;1例单纯修补。2例Mirizzi综合征于损伤处放置12#T管,术后半年拔除并行超细胆道镜检查。2例右肝管裂伤直接用5-0薇乔线缝合修补。
4例右肝管离断伤:1例LC术后9个月行PTC证实右肝管离断,改行胆肠吻合术;1例误判为副肝管损伤直接缝扎并在损伤处留置腹腔引流,术后3 个月行胆肠Roux-en-Y吻合;1例行IOC后仍直接夹闭,后改行胆肠吻合术;1例术中误缝扎右肝管(术后CT及MRCP证实),远期行胆肠Roux-en-Y吻合术未成功,改行PTCD。
4 例副肝管损伤患者中:1 例以5-0 PDS修补并置管支撑引流;1例术中发现胆瘘直接结扎,术后大量胆瘘,PTC证实副肝管损伤,二期行胆肠吻合术;2例行单纯结扎。
全部病例诊断、治疗策略、所属损伤类型(分型采用中华医学会胆道外科学组推荐的3型4类分型系统[12])及相关临床资料见表1。

表1 患者一般资料、损伤类型、主要外科策略及随访(分型采用中华医学会3型4类分型系统)
IOC方法:(1)右肝管损伤:如破口较小拟行单纯修补者,用造影钳经胆囊管插入硬膜外导管,将导管引出体外,注入碘海醇,行X线透视,明确右肝管裂伤程度及损伤处与胆总管的解剖关系;如破口较大拟置管支撑引流者,裁剪相应型号的T管插入右肝管,4-0薇乔线缝合后将T管引出体外同法造影,可了解修补处有无胆瘘及明确与胆总管的关系(胆总管内同时放置T管者双T管均分别造影,确保损伤处修补、支撑引流效果,见图1A);疑有RHD离断时经胆囊管常规造影也能协助诊断(图1F)。(2)副肝管损伤:经可疑副肝管破口插入相应直径的硬膜外导管或硅胶导尿管,用钛夹以适度力量固定,导管经辅助Trocar直接引出体外同法造影(图2H),可判断副肝管引流范围及是否与主干道交通。
1.3 胆道损伤术后胆道通畅度评级标准
根据圣路易斯华盛顿大学胆道损伤预后标准[11]进行评级。A级:3 个月内即获得并长期维持通畅,不需要支架置入,无需后期有创治疗;B级:需再次有创干预,支架置入<18个月,ERCP/介入<12个月;C级:支架置入18~24个月,ERCP/介入>12个月,胆管炎、肝脓肿,需再次外科重建胆道;D级:支架置入>24个月,肝萎缩或肝硬变。
1.4 统计学分析
2 结果
2.1 右肝管/副肝管损伤治疗结果
12例右肝管裂伤治疗结果:(1)胆总管结石7例:5 例合并胆总管结石的患者于右肝管裂伤处另行单独留置T管(双T管,图1A、2A),其中4例右肝管内T管支撑留置半年造影、拔除(图1B);1例术后合并胆瘘,胆汁日引流量30~120 mL,胆瘘2周内自愈,右肝管内留置T管支撑1年,超细胆道镜检查见短臂内少许胆泥,取石冲洗后拔除,随访77个月无结石复发。1例胆总管结石手术时右肝管裂伤,中转开腹手术后修补右肝管破损,右肝管内置入夹心T管,自胆总管切开处引出,术后半年拔除,拔除时T管内导管尖端明显胆泥,右肝管腔内轻度狭窄,取石、冲洗2次后拔除T管。(2)2例胆囊结石为Mirizzi综合征,右肝管修补并在右肝管内留置T管(图2B)半年,除术后ALP及GGT持续轻度异常外,分别随访34、33个月,远期无狭窄、胆瘘等并发症。(3)4例右肝管裂伤行单纯修补(图2C),其中1 例胆总管结石合并右肝管较大范围裂伤(图2D、2E),修补后持续胆瘘,日引流量<150 mL,3周后自愈)。
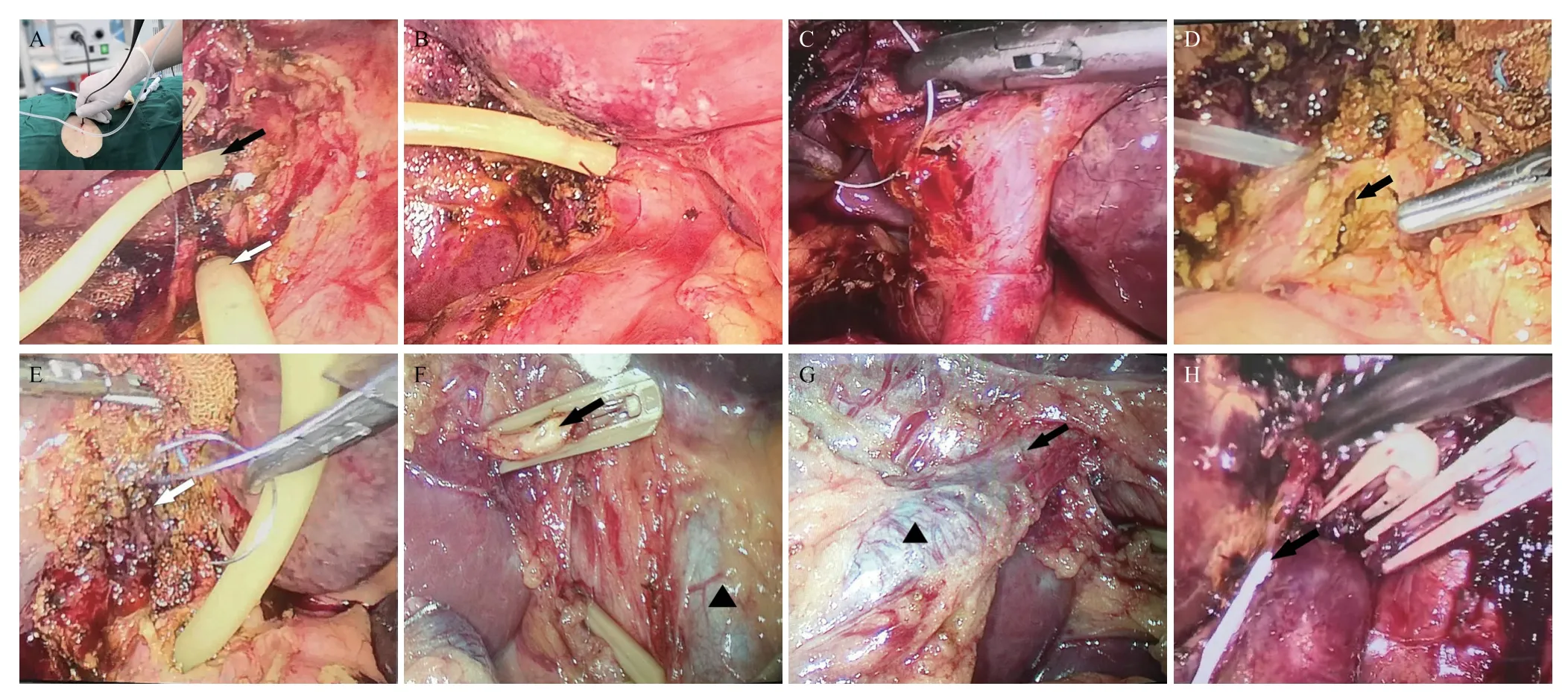
图2 右肝管/副肝管损伤时主要技术操作:双T管或右肝管T管置入、修补、副肝管辨识、IOC。
4例右肝管离断伤,其中1例于LC术时“手术顺利”,未行IOC,术后短暂失访,后ALP、GGT持续异常,9个月后复诊因胆红素持续异常行MRCP显示肝外胆管正常显影,PTC提示右肝管横断(图1D),未见胆瘘,改行胆肠Roux-en-Y吻合术,术后偶有肝功能轻度异常。1例LC术中发现异常胆瘘未行IOC,中转开腹手术后予以缝扎,放置腹腔引流,术后持续胆瘘,日引流量200~450 mL,术后经引流管造影及MRCP提示右肝管横断(图1E),术后3 个月再次探查,证实诊断,行胆肠Roux-en-Y吻合术,术后少量胆瘘(2周后自愈),ALP、GGT仍间断异常,时有胆道感染,MRCP显示吻合口局部轻度狭窄。1例外院行LC时术中发现异常胆管开口合并胆瘘,经IOC判断为右肝管离断可能,因不具备手术条件暂直接夹闭(图1F),患者术后持续肝功能异常合并轻度黄疸,术后2个月在我院手术探查证实副肝管夹闭,行胆肠Roux-en-Y吻合术,术后肝功能逐渐恢复,偶有GGT轻度异常。1 例9 年前于外院行LC时因“考虑副肝管损伤”行瘘口缝扎(未行IOC),术后患者无胆瘘或频发胆管炎。我院查CT及MRCP提示右肝完全萎缩(图1G),左肝内胆管扩张,考虑LC时实为右肝管离断,术中致密粘连及出血,内引流失败,改行PTCD后症状缓解。
4例副肝管损伤中,其中1例LC时IOC证实副肝管裂伤(图1H)予以修补并置管支撑,术后6个月拔除引流管,随访61 个月肝功能无明显异常;1 例LC时发现异常胆道瘘口未行IOC而直接结扎,后短期出现大量胆瘘(日引流量200~400 mL)及发热,行B超引导下腹腔穿刺引流,一月后行胆肠Roux-en-Y吻合术,随访43个月时有胆管炎发作但影像学检查无明显狭窄证据;另2例行IOC进一步确诊、判断副肝管引流范围小(图1C,2F~2H),直接夹闭,术后1~2周ALP、GGT轻度异常,远期随访16~17个月无胆管炎或肝功能异常。
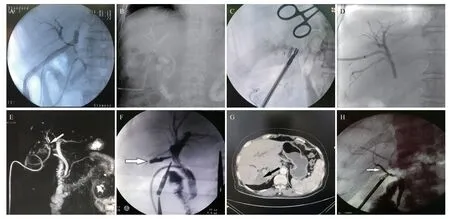
图1 明确右肝管/副肝管损伤类型的关键影像学资料
2.2 IOC与非IOC组术后GP对比
全部病例中9例实施IOC(45%),11例未行IOC(55%),损伤类型构成比无统计学差异(P>0.05)。采用圣路易斯华盛顿大学胆道损伤预后标准[11],显示IOC组术后胆道通畅度评级及预后优于非IOC组(P=0.025),详见表2。
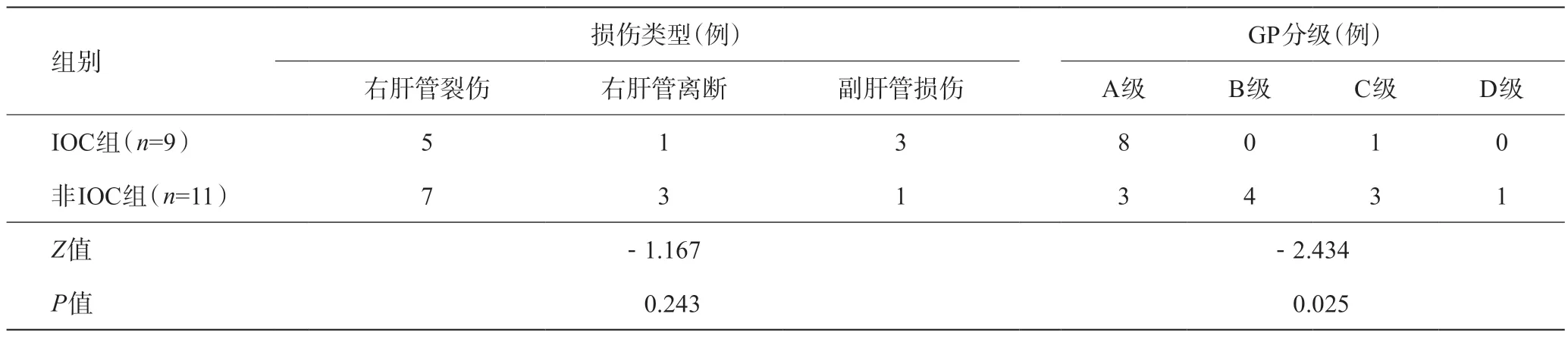
表2 IOC组与非IOC组术后胆道通畅度评级
3 讨论
在IBDI的研究中,肝总管/胆总管损伤已报道较多,处理方法也相对成熟,而单纯右肝管和副肝管损伤的报道很少,且术中发现损伤的同时要明确是右肝管损伤还是副肝管损伤有时并不容易,而及时的正确诊断又直接决定了术后转归。特别是右肝管损伤多为裂伤,横断伤少见,术者因经验及认知差异,在修补、置管、吻合等抉择上多有不同,临床上也缺乏足够的病例随访。充分应用IOC等技术手段,准确判断损伤类型,临床上才可能减少误判并制定出最佳处理方案。
本组12 例为右肝管裂伤,其中5 例胆囊与右肝管致密粘连,分离时误伤右肝管,均为电凝所致右肝管外侧壁裂伤(裂口不规则,缺损0.4~1.0 cm,<1/2 周径),打开胆总管后胆道镜进一步证实,除常规胆总管内置T管外,为防止术后狭窄,修补右肝管后在损伤处腔内留置12#~14#T管(双T管),留置半年到1年(因胆瘘延长置管时间)后拔除。远期随访34~77 个月,远期均无胆管炎或肝功能异常,MRCP显示无胆管狭窄。双T管置入增加了术后不便及护理量,但由于系电凝伤、裂口较大且不规则,为策安全,修补后腔内置入支架管支撑是值得的。实际上此类损伤临床远较报道多见,值得推广。1例因术中胆管裂口近1 cm且缺损达周径1/2,术后短期内胆瘘,故留置右肝管T管达1年,拔除时短臂见少许胆泥,但随访77个月未见狭窄。说明支撑管并非留置时间越久越好,建议不超过1年。对于右肝管小而规则的裂伤,可直接吸收线缝合修补,无需置管支撑,但术后应留置腹腔引流,如有少许胆瘘大多可自愈。
右肝管离断伤罕见,甚至术中未能正确诊断。本组4 例右肝管离断伤中,有2 例损伤时临时行缝扎、引流(未行IOC),术后患者仅表现为胆瘘或无明显不适,但终因不同程度黄疸及肝功能损伤经进一步检查获得右肝管离断伤的诊断,而被迫延期另行胆肠Roux-en-Y吻合,其中1例(未行IOC)合并胆瘘,二期行胆肠Roux-en-Y吻合时因瘘口回缩及组织水肿,手术难度很大,无法完成黏膜对黏膜吻合,仅能将肠袢扣入引流,术后半年ALP、GGT难以恢复正常且时有胆管炎发作,复查MRCP提示吻合口轻度狭窄,值得注意。仅1例行IOC判断为右肝管离断,因技术限制,临时夹闭损伤处,及时转我院行确定性手术(胆肠Roux-en-Y吻合),术后获得良好预后。对3例未行IOC的患者,术中均判断为右肝管裂伤或不重要的副肝管瘘口予以缝扎,事实上,右肝管离断伤后症状不一[13],如不能一期处理,绝大部分需再次被动手术,产生医疗纠纷,极少数可无胆瘘,表现为复发性胆管炎、脓肿、远期肝萎缩(图2G)。该组无一例为术中确诊并行一期确定性修复手术(胆管吻合或胆肠吻合),说明右肝管离断同胆总管损伤一样,有相当病例未能在术中及时发现而失去最佳手术时机。怀疑胆道损伤时不能仅凭经验,应尽可能创造条件行IOC,仔细阅片,高度怀疑右肝管离断时不可心存侥幸,应根据损伤程度果断行胆管吻合或胆肠吻合。是否能结合IOC资料明确损伤类型、保证组织活力并及时行一期修复或重建手术,将直接决定预后。
副肝管损伤远较报道多见,直径在0.3 cm以上的副肝管损伤必须明确引流范围并排除右肝管损伤。本组4例副肝管损伤有3例均经IOC证实,其中1例为副肝管低位汇合,胆管直径0.4 cm,胆管不规则电凝伤但连续性仍存在,5-0 PDS修补并置管支撑引流,术后随访61 个月无胆管炎或肝功能异常;另外2 例胆管外径0.2~0.3 cm,均行IOC,证实引流范围较小,结扎后无胆瘘或肝功能异常;1 例外院行LC,术中未行IOC而直接结扎后大量胆瘘,术后PTC见肝右后叶胆管扩张,考虑为独立引流右后叶的胆管损伤且引流范围较大,因胆道内高压冲脱闭合口而致术后大量胆瘘,故延期行胆肠Roux-en-Y吻合术,术后出现较频繁胆管炎与长期胆瘘、组织水肿、吻合条件差有关。郑和鸣等[14]认为,副肝管直径<0.3 cm,或胆汁日引流量<100 mL可夹闭,直径≥0.3 cm应修复或重建,效果与缝合技术密切相关。但我们认为同时还应尽量行IOC以判断引流范围,及是否与主干道交通,若引流范围大、无交通最好行胆肠吻合。
结合本组资料,右肝管/副肝管损伤绝大部分发生在胆囊壶腹与右肝管炎性致密粘连、或副肝管低位汇合误将副肝管当做胆囊管分离时,此时仅仅明确三管关系是无法预防损伤的。应在核实三管关系的基础上充分显露胆囊后三角,即胆囊管-胆囊颈部后方的区域,才能最大限度预防损伤,如有可疑损伤应尽可能行IOC明确损伤类型以获得正确处理。IOC对安全实施LC的临床价值日益受到肯定[15],必须强调右/副肝管损伤时IOC的重要性,本研究采用胆道损伤预后新标准,以术后远期胆道通畅度评级为指标,对IOC组和非IOC组右/副肝管损伤患者行预后分析,发现IOC组术后胆道通畅度评估及预后明显优于对照组,说明尽可能创造条件行IOC并正确判断结果有助于提高疗效。
总之,右肝管/副肝管损伤是医源性胆管损伤的特殊类型,其诊断和治疗是当前胆道外科的难题之一,在临床工作中需要足够重视并长期关注。及时发现、并根据全面的临床信息(包括损伤类型、IOC资料)灵活制定出最适合的治疗方案是减少远期并发症、改善预后的关键。
利益冲突:所有作者均申明不存在利益冲突。